2026年4月上半月国内市场研究报告
【IVD 思享汇】
2026年第11期

研究报告目录:
一、国内医疗政策
二、行业要闻
三、资本动态
国内医疗政策
1.1 4月9日,国务院办公厅印发《关于加快建设分级诊疗体系的若干措施》
《若干措施》从4个方面提出13条具体措施:
(1)以紧密型医联体为抓手完善分级诊疗协同机制。一是优化医疗卫生机构功能定位和结构布局。动态消除基层医疗卫生服务空白,发挥二级医院在三级医院和基层医疗卫生机构之间的桥梁纽带作用,引导三级医院聚焦急危重症和疑难复杂疾病加强转诊会诊和住院服务。二是推动紧密型医联体提质扩面。全面推开紧密型县域医共体、紧密型城市医疗集团。三是加强紧密型医联体内医疗资源共享。推动形成医联体内医疗、运营、信息管理一体化,促进医疗卫生服务系统连续。
(2)以常见病、慢性病为重点引导群众基层首诊。一是加强基层常见病诊疗和慢性病管理。通过医联体牵头医院在基层医疗卫生机构开设常见病、慢性病门诊,专家团队的普通门诊向基层延伸。二是强化上级医院帮扶机制。通过上级医疗机构持续帮扶,提高基层医疗机构承接能力。三是提升家庭医生签约服务质效。
(3)以提升就医连续性为导向加强转诊服务管理。一是明确转诊规则。以便利群众转诊为导向,完善各级转诊规则,强调发挥医疗机构和临床医师评估作用。二是畅通首诊后患者转诊渠道。三是强化医保政策引导。
(4)完善分级诊疗多元保障措施。一是加快完善紧密型医联体发展保障机制。二是完善基本医保差异性支付政策。因地制宜拉开各层级医疗机构报销比例。三是完善医疗卫生服务相关价格政策。四是加强宣传引导。
1.2 4月13日,国新办举行国务院政策例行吹风会介绍《关于加快建设分级诊疗体系的若干措施》有关情况
按照监测,2025年,在紧密型县域医共体内,基层诊疗人次占比超过了63%,这个比例高于全国基层诊疗人次占比平均水平。几年来,我们主要取得了以下几个方面的进展:
一是紧密型县域医共体建设实现了全覆盖。全国现在有2199个县、县级市和城市的区,正在加紧建设运行紧密型县域医共体。在已经建设的近3000个紧密型县域医共体中,有2300多个由县医院牵头,有600多个由县中医院牵头,覆盖基层医疗卫生机构3.3万个,有超过1100个县疾控中心和超过1600个县级妇幼保健机构加入了紧密型县域医共体。
二是促进县域内资源的协同和下沉。2025年,全国超过90%的县域医共体内,基层成员单位都有上级医院的医务人员下沉派驻,总人数超过了7万人,超过80%的县建设了影像、心电、检验等资源共享中心,服务群众超过3.3亿人次。
三是促进服务的协同和联动。一方面,我们加强县医院重点专科建设,加强乡镇卫生院特色科室建设,建立学科帮扶机制。同时,我们还推动全国1800多个县成立转诊会诊中心,为跨机构转诊的群众提供连续服务。
四是加强基层用药衔接。推进县域医共体药品配备,2025年,全国超过70%的县建立了县级中心药房。
【提示】:当前全国各地正加快推进紧密型医联体建设,部分地区虽存在联而不紧、资源不通、协同不畅等现实问题,但构建分级诊疗体系、推动医疗资源整合共享已是行业发展大势所趋。
1.3 4月2日,国家药监局发布《关于“人工智能+药品监管”的实施意见》
《意见》包括总体要求、数智赋能重点监管场景、“人工智能+药品监管”基础支撑、组织实施四个部分。聚焦药品监管改革的重点任务,以药品监管现代化为目标,提出下一阶段监管数智化的七大重点方向。结合人工智能技术发展新趋势,提出筑牢“人工智能+药品监管”基础支撑的五项重点任务。
《意见》提出,到2030年,初步构建药品监管与人工智能融合创新体系,“人工智能+药品监管”运行管理机制基本形成,算力支撑底座更加集约高效,形成满足监管智能化需要的高质量数据集、垂直大模型和智能体,人工智能在审评审批、监督检查、检验监测、政务服务等场景中有效应用,人机协同效率显著提升,全生命周期数智化监管能力迈上新台阶。到2035年,基本形成数智驱动、智能敏捷、自主可控、生态协同的智慧化药品安全治理新格局。
【提示】:未曾预料,AI 技术率先在监管领域落地应用,通过智能化手段强化产品全流程监督管理,彰显出公平优先、兼顾效率的监管导向。
1.4 4月8日,国家药监局《关于印发2026年国家医疗器械抽检产品检验方案的通知》
(1)检验工作要求
检验机构应当加强对未能依照检验方案完成全部适用项目检验情况的收集。对于注册人、备案人或者进口产品代理人未能提供完成检验所需全部资料和配套必需品的,以及产品技术要求不完善导致无法完成检验的,应当向注册人、备案人或者进口产品代理人所在地省级药品监督管理部门出具国家医疗器械抽检缺项检验提示函,该提示将通过国家医疗器械抽检信息系统传递,省级药品监督管理部门应当对相关情况及时调查处理。对于产品技术要求不完善的,应当监督企业尽快完善产品技术要求,并依法依规完成变更。相关调查处理结果应当在提示函印发后30个工作日内录入国家医疗器械抽检信息系统。
(2)复检工作要求
2026年国家监督抽检的复检受理部门为医疗器械注册人、备案人或者进口产品代理人所在地省级药品监督管理部门。对同一检验报告的复检申请只办理一次。受理复检申请的省级药品监督管理部门确定复检机构进行复检,复检机构不得拒绝。
列入复检机构名单的检验机构,应当持续保持其相应品种及项目的检验能力、检验资质,有义务承接省级抽检和地方药品监督管理部门执法工作中的复检工作。当事人对检验结论有异议且无法通过复检验证的,可以向所在地省级药品监督管理部门提出异议申诉书面申请。
(3)检验结果处置要求
医疗器械注册人、备案人和被抽样单位收到产品不符合规定报告后,应当立即采取风险控制措施。药品监督管理部门应当及时组织调查处置,符合立案条件的,及时立案查处;涉嫌犯罪的,依法移交司法机关。
行业要闻
2.1 我国3月法定传染病情况(法定传染病.xlsx)
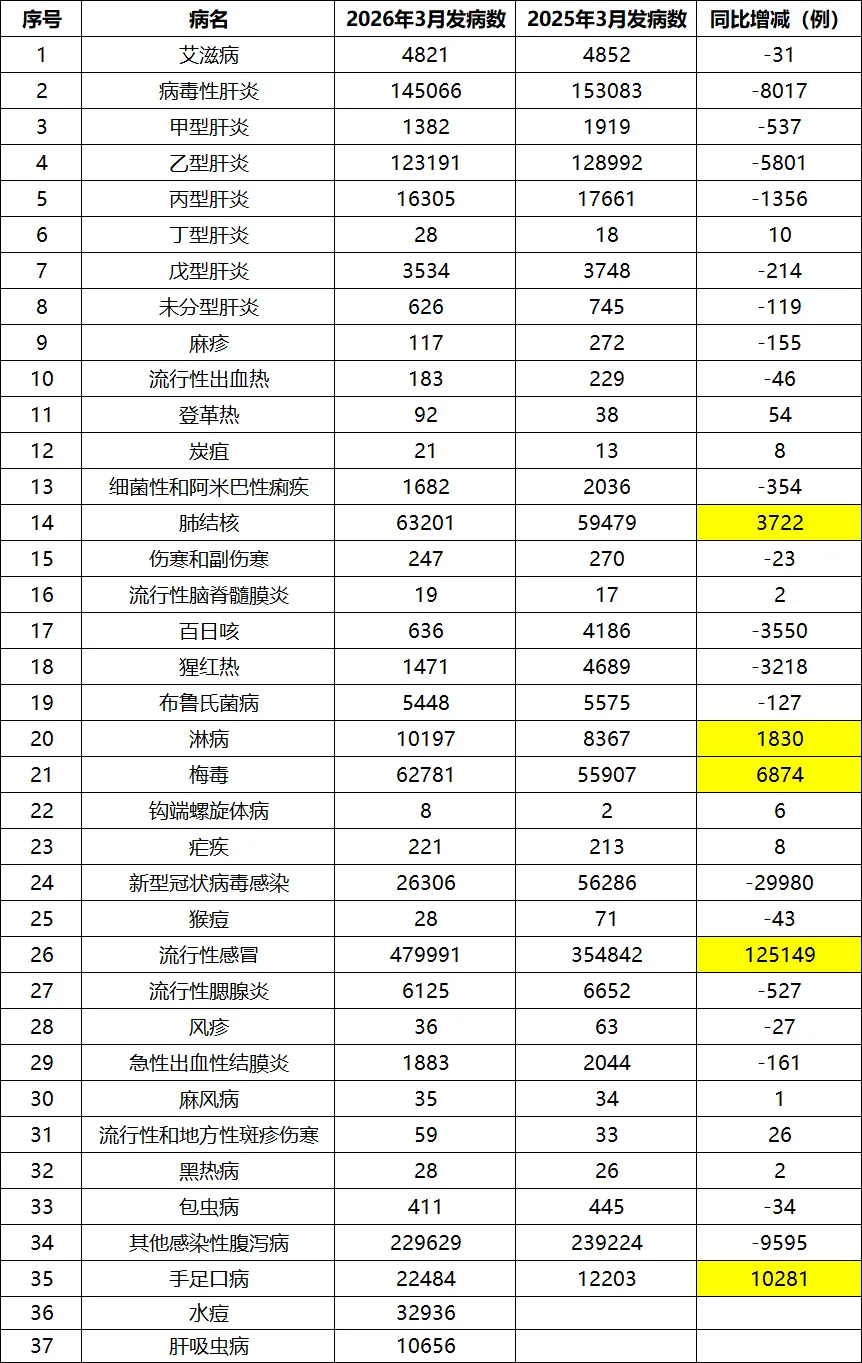
【提示】:肺结核、流感、手足口、淋病、性病同比有所增加。
2.2 近半月,我国三类试剂注册证获批情况(注册证号2026340XXXX,产品注册证信息.xls)
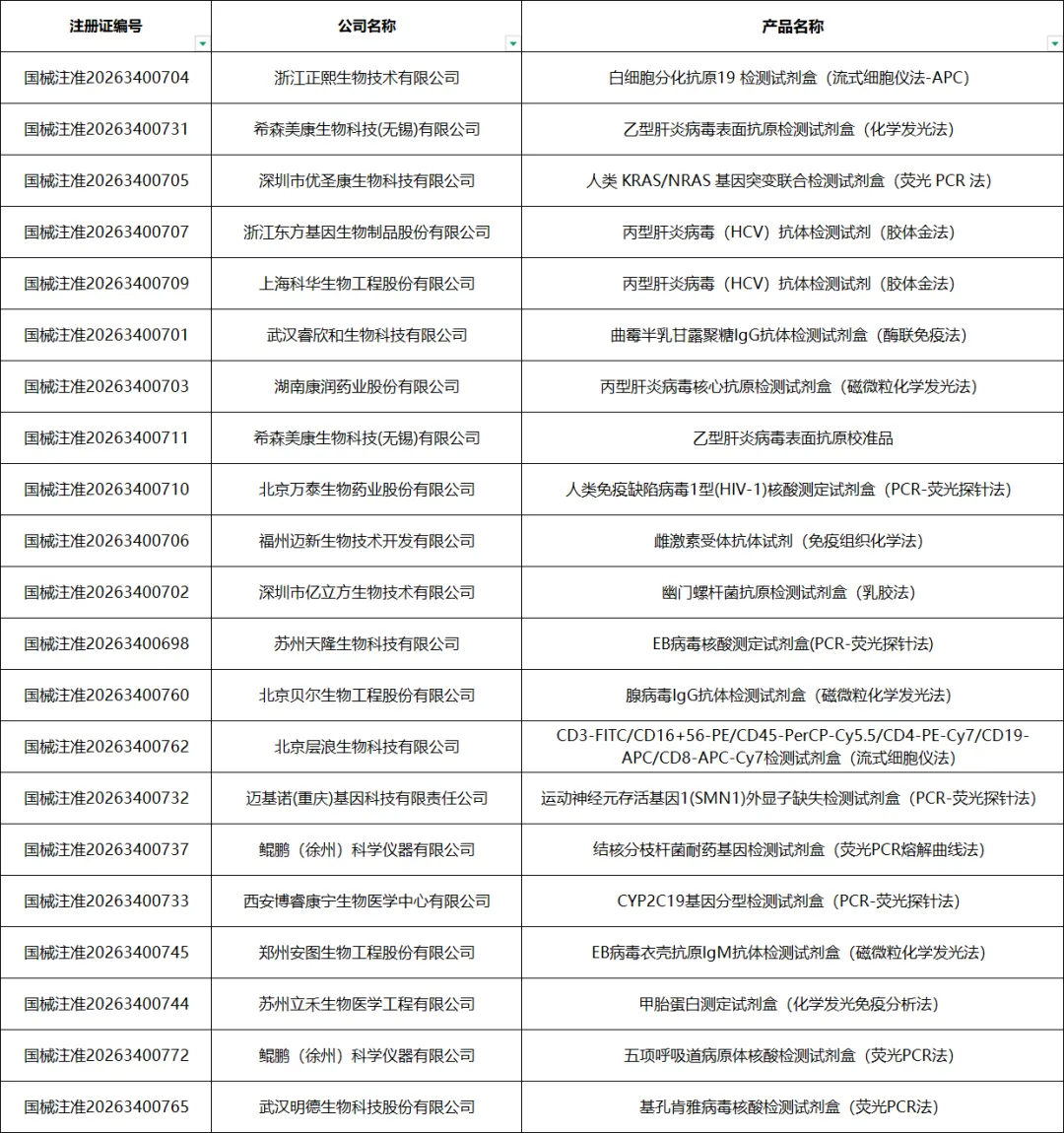
资本动态
3.1 IVD二级市场情况
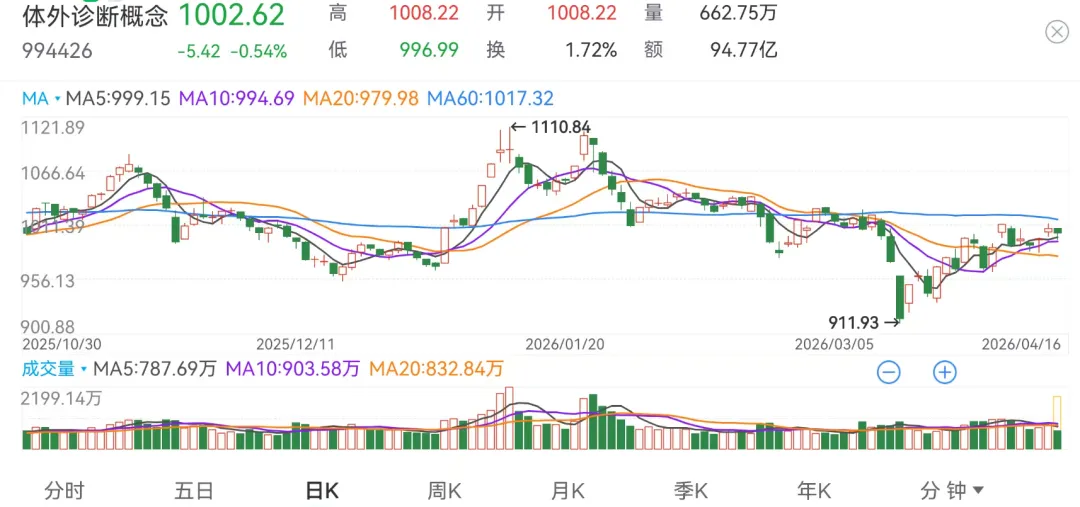
3.2 利德曼发布2025年报
2025年营业收入32,630.64万元,同比下降11.86%。分产品看,体外诊断试剂收入24,011.39万元,同比大降19.22%;诊断仪器业务收入3,228.24万元,逆势增长30.45%,成为增长的核心业务板块;生物化学原料收入1,324.36万元,同比下降7.46%;其他业务(主要为房屋租赁)收入4,066.66万元,同比增长19.94%。
2025年净利润为-2,298.31万元,较上年的-7,510.13万元,亏损幅度大幅收窄69.40%;扣非净利润为-3,146.54万元,上年为-9,747.21万元,亏损收窄67.72%。亏损收窄主要得益于费用管控效果显著,以及非经常性收益的支撑,但主业仍未实现盈利。
2025年公司期间费用合计17,157.18万元,同比上年的20,815.68万元下降17.58%,费用管控力度强劲。2025年末公司研发人员57人,较上年的71人减少14人,降幅19.72%;研发人员占总人数比例从15.17%降至13.57%。其中博士从6人降至3人,降幅50%,硕士从22人降至18人,降幅18.18%。
————END————


