线粒体重塑研究报告:冲刺间歇运动破坏线粒体超微结构,驱动人体产生独特的线粒体应激反应与重塑
Nature Communications :冲刺间歇运动破坏线粒体超微结构,驱动人体产生独特的线粒体应激反应与重塑出处:Botella J, Perri E, Caruana NJ, et al. Sprint interval exercise disrupts mitochondrial ultrastructure driving a unique mitochondrial stress response and remodelling in men. Nat Commun. 2025;17(1):71.
作者介绍:
运动是促进线粒体健康的关键生活方式干预措施,但不同运动处方调控线粒体重塑的分子机制仍不清楚。我们开展了一项随机对照试验,观察到与中等强度持续运动(MICE;n = 14)相比,冲刺间歇运动(SIE;n = 14)可诱导线粒体应激特征及线粒体未折叠蛋白反应(UPRmt)。SIE可触发线粒体形态与结构改变,同时激活整合应激反应(ISR)和线粒体质量控制(MQC)通路。经过8周训练后,中等强度持续训练(MICT)增加了线粒体含量和复合体I活性,并表现出三羧酸(TCA)循环及氧化磷酸化(OXPHOS)蛋白的富集;而冲刺间歇训练(SIT)则改善了呼吸功能,并上调了参与一碳代谢和蛋白质质量控制的通路。我们发现,仅在SIT后,COX7A2L在线粒体超复合体III2 +IV1中发生积累。这些发现阐明了运动强度如何塑造线粒体重塑,并为制定个体化运动处方提供了依据。
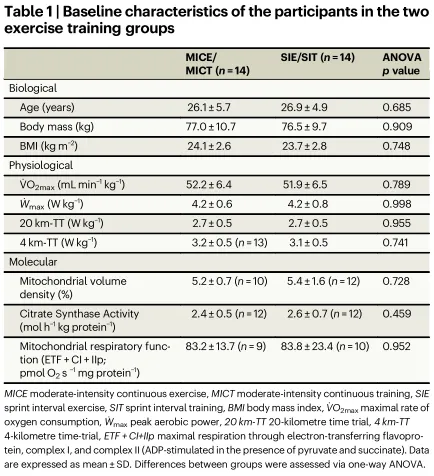
线粒体是参与多种生物学功能的关键细胞器,包括代谢、炎症和细胞死亡。¹因此,线粒体特征不佳(如呼吸功能下降)已被认为与多种疾病有关。²˒³而这些线粒体特征在运动员骨骼肌中往往会得到增强。⁴⁻⁷鉴于骨骼肌收缩具有巨大的能量需求,⁸运动能够提供强有力的刺激,从而引发线粒体含量、酶活性和呼吸链功能的持久变化,这并不令人意外。运动是一种公认可刺激新线粒体组分合成的干预方式,这一过程被称为线粒体生物发生。⁹˒¹⁰尽管其许多潜在机制仍知之甚少,¹¹˒¹²但运动仍然是预防非传染性疾病最有效的生活方式干预措施之一。¹³˒¹⁴运动的益处被认为源于肌肉收缩诱导的稳态扰动,这种扰动启动了分子图谱的协调性改变(即翻译后修饰和基因表达变化),旨在重新建立细胞稳态。¹⁵˒¹⁶这种反应在很大程度上依赖于运动的特征。¹⁷˒¹⁸阐明不同运动处方所影响的细胞程序,对于促进建立更具循证依据的运动指南以及制定更具针对性的运动干预措施以改善健康至关重要。¹⁹高强度间歇运动(HIIE)在过去几十年中因其在促进骨骼肌和心肺适应方面的有效性而日益受到关注,而这些适应传统上通常与中等强度持续运动(MICE)相关。²⁰⁻²²HIIE中时间效率最高的一种形式称为冲刺间歇运动(SIE),仅需进行4至6次30秒全力冲刺即可完成,²³因此在现代社会时间受限的背景下成为一种颇具吸引力的运动处方。²⁴˒²⁵尽管这一问题仍存在争议,但已有多种机制被提出用以解释SIE的高效性。一些研究表明,SIE与一种应激反应相关,可导致细胞钙泄漏,继而激活参与线粒体生物发生的相关通路。²⁶˒²⁷另有研究报道,SIE后而非MICE后,参与线粒体生物发生的核定位转录因子(如过氧化物酶体增殖物激活受体δ辅激活因子1α,PGC-1α)丰度增加。²⁸许多研究认为,这种更强的线粒体生物发生激活是促成SIE高效性的潜在机制之一。然而,一个相互矛盾的观察结果是,SIE在长期重复实施时(即运动训练中)并不总能转化为线粒体含量适应性更大的增加,²⁹⁻³¹这提示可能还有其他尚未被发现的机制参与了SIE效应的产生。已有假说认为,运动可促进线粒体兴奋性适应反应(即线粒体兴奋效应,mitohormesis),以重新建立线粒体稳态,从而提高机体对后续应激源的耐受性。³²多种通路已知可介导健康线粒体群的维持,例如调控线粒体动力学(融合、分裂)、线粒体质量控制(MQC;如线粒体自噬)以及线粒体未折叠蛋白反应(UPRmt)的通路。³³˒³⁴在小鼠中,已有研究表明运动会影响其中大多数通路,³⁵⁻³⁹但对于运动如何影响人类这些通路,⁴⁰˒⁴¹以及不同运动处方如何改变这些通路,目前认识仍然有限。鉴于高强度运动会引起更大的稳态扰动,一个合理的假设是,线粒体应激是促成SIE所致线粒体适应的重要机制。在本研究中,我们报道了SIE而非MICE会扰乱人骨骼肌线粒体超微结构,进而导致线粒体应激及UPRmt的转录激活。通过结合一系列互补技术(如RNA测序、电子显微镜、蛋白质组学),我们提供了有力证据表明,SIE可特异性诱导线粒体应激,并同时上调整合应激反应(ISR)和MQC通路,而这一过程在很大程度上独立于线粒体生物发生和动力学标志物。(也就是说,SIE并不是通过线粒体生物发生和动力学的变化导致的MQC的改变,这种变化应该是由SIE应激所独立介导的)经过长期重复干预(8周)后,仅中等强度持续训练(MICT)增加了线粒体含量标志物,而仅冲刺间歇训练(SIT)提高了线粒体呼吸链功能。在蛋白质组学分析的指导下,我们观察到SIT以不同方式重塑线粒体蛋白质组,并上调COX7A2L蛋白表达及其整合进入III2IV1呼吸超复合体,这为解释SIT高效性的潜在机制提供了依据。这些发现挑战了我们目前对运动特异性线粒体适应的认知,同时也支持采用个体化训练干预以实现特定线粒体重塑的重要性。多种线粒体特征的改善是运动训练的典型标志。⁴²˒⁴³尽管不同的线粒体适应已被认为与所规定运动的强度和容量有关,³⁰但这一问题仍存在争议。²⁹˒⁴⁴在本研究中,我们招募了28名健康男性,以揭示运动强度和运动容量的不同效应(表1和图1A)。我们选择SIE,是因为它是HIIE中强度最高的一种形式,并被广泛认为是一种高效且节省时间的运动方式。²³为研究运动容量的影响,我们设定了MICE,其通常被视为“传统”的耐力性或心肺运动形式。⁴⁵参与者依据其V̇O2max和Ẇmax,以随机平衡顺序被分配至两种运动组之一(表1)。后验分析显示,两组在年龄、人体测量学参数以及线粒体含量和呼吸功能标志物方面均相匹配(均p > 0.05;表1和源数据)。
在完成运动熟悉化、测试以及宏量营养素摄入标准化后,参与者完成了各自分配的实验试验,并采集了股外侧肌骨骼肌活检样本(图1A和图S1A)。尽管研究不同运动方式之间差异时常采用功量匹配的方法,但本研究无法采用该方法,因为更大的运动容量本身就意味着完成了更多的机械功。因此,为了突出每种运动的区别性特征,我们将两种运动设计为在组间强度和容量差异方面保持相近程度(图1B)。进行MICE的参与者完成了约5.2倍更高的运动容量,而进行SIE的参与者则以约4.7倍更高的强度运动。两种运动均引起血乳酸浓度升高(图1C),且SIE后的升高幅度大于MICE(约10倍对约2倍;p < 0.05)。SIE后乳酸更大幅度升高与既往证据一致,即运动强度是运动过程中糖酵解通量增加和乳酸生成增加的驱动因素。⁴⁶˒⁴⁷与此同时,仅SIE而非MICE导致血液H+浓度升高(p < 0.05;图1C),并引起更高的主观用力评分(p < 0.05;图S1B)。与MICE相比,SIE引发了更大的代谢扰动,这与既往研究结果一致。²⁸˒⁴⁸
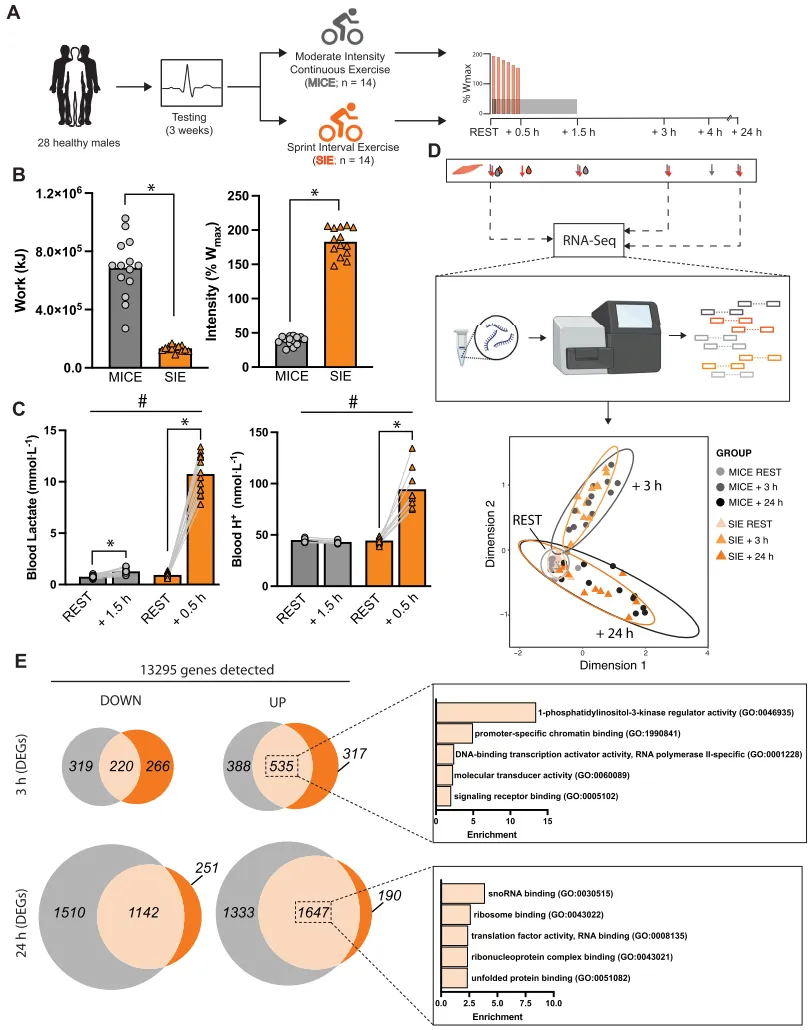
图1|实验性运动方案设计及运动特征示意图。
A 研究流程,包括受试者招募、测试以及分配至中等强度持续运动(MICE)或冲刺间歇运动(SIE)组。B MICE(n = 14)和SIE(n = 14)在实验性运动过程中达到的运动量和运动强度。
C MICE〔乳酸n = 14,H+ n = 7〕和SIE〔乳酸n = 14,H+ n = 9〕后血乳酸浓度和氢离子(H+)浓度的运动诱导性变化。D 所选肌肉活检时间点(灰色箭头表示MICE活检时间点;橙色箭头表示SIE活检时间点;每组n = 12)、采血时间点(灰色液滴表示MICE采血时间点;橙色液滴表示SIE采血时间点;每组n = 12),以及用于RNA测序的样本及其通过主成分分析(PCA)所示的分布,显示两组总体上呈共享聚类。E 维恩图显示各时间点共同和特异性差异表达基因(DEGs)的数量。过度代表分析(ORA)显示两种运动在3 h(恢复早期)和24 h(恢复晚期)共同调控的分子功能。
运动早期恢复阶段可观察到MICE与SIE之间的转录组分化
运动所致的生理适应被认为部分来源于针对运动刺激的协调性转录反应。¹⁵˒⁴⁹鉴于MICE与SIE之间存在截然不同的代谢和生理反应,我们假设这两种运动也会引发不同的转录反应。我们在静息状态(rest)以及从运动开始后早期恢复(+3 h)或晚期恢复(+24 h)时间点的肌肉样本中进行了RNA测序分析(图1D)。在全部样本中,我们共检测到13,295个基因转录本,其中有7,175个转录本在至少一种运动刺激和至少一个时间点下发生差异表达(约占检测到转录组的54%)。这一数量远超此前两项Meta分析中所鉴定的受运动影响的转录本数量,⁴⁹˒⁵⁰这可能归因于我们平行组研究设计所实现的更高标准化程度,以及纳入了24 h活检时间点。我们的数据提示,由于大多数研究仅在运动后最初数小时内采集活检样本,许多运动诱导的转录组变化一直处于“隐藏”状态。
在运动后的早期恢复阶段,MICE和SIE后分别有1,462个和1,338个转录本发生差异表达。在晚期恢复阶段,发生改变的转录本数量更多,MICE和SIE后分别有5,632个和3,230个差异表达转录本(图1E)。尽管此前一项Meta分析鉴定出159个遵循特定运动后变化轨迹的转录本(不考虑运动方式),⁵⁰但我们的结果揭示了更加广泛的时间效应。这些发现为表征运动转录反应随时间变化的复杂性提供了重要资源。⁵⁰˒⁵¹在不同运动组之间,早期和晚期恢复阶段分别存在755个和2,789个共有的差异表达转录本(图1E和源数据)。两组共同调控的转录本提示了耐力运动共有的转录反应,并显示在恢复早期(+3 h)和晚期(+24 h)存在一系列广泛细胞通路的过度代表(图1E和源数据)。尽管我们的实验设计使我们能够建立共同的早期和晚期转录组特征,未来研究仍需探索更为完整的运动诱导转录时间过程,以及不同细胞类型对这些转录变化的贡献。⁵²线粒体未折叠蛋白反应(UPRmt)是SIE后的特异性转录特征
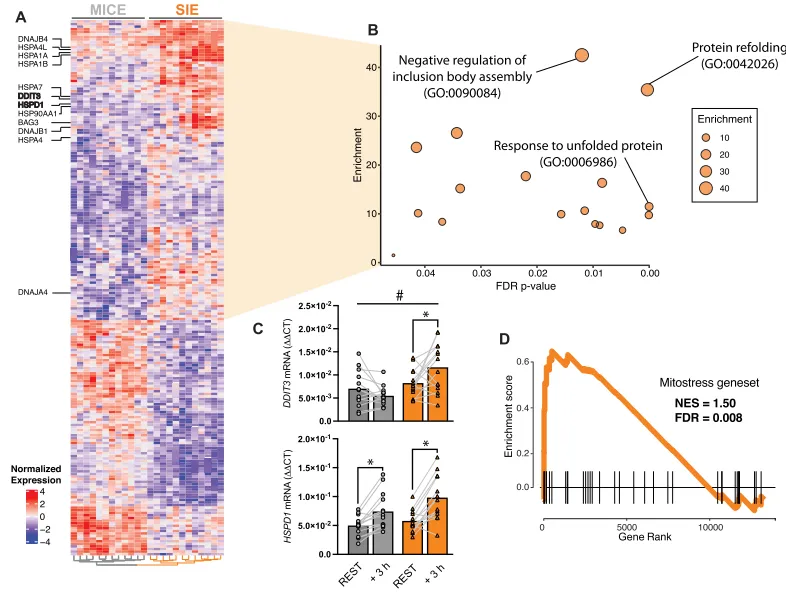
在确定不同类型耐力运动后存在共同的转录变化后,我们接下来旨在揭示MICE与SIE之间的转录差异。这些结果可能指向此前报道的SIE有益适应效应背后的分子信号通路。²³尽管在晚期恢复阶段(即24 h;图1E和源数据)观察到更多发生改变的转录本,但在该时间点MICE与SIE之间仅有16个转录本存在显著差异调控(校正后p < 0.05;源数据)。恢复早期组间差异更大,在运动后3 h时,MICE与SIE之间有207个转录本呈差异调控(源数据)。因此,我们将注意力集中于早期时间点(即3 h),并对这207个转录本进行了层次聚类分析,以进一步探究与这些转录本相关的潜在生物学过程(图2A)。在这些差异中,有116个转录本在SIE后上调幅度更大(另有91个在MICE后上调幅度更大)。通过过度代表分析(ORA),仅在SIE后上调幅度更大的基因列表中观察到显著富集。这些转录本包括大量胞质和线粒体热休克蛋白(HSP),并系统性富集于与蛋白折叠和未折叠蛋白反应(UPR)相关的术语(图2A、B)。
在SIE与MICE之间差异表达的基因中,有两个分别为DNA损伤诱导转录本3(DDIT3,也称CHOP)和热休克蛋白D家族成员1(HSPD1,也称HSP60),它们是最早被鉴定出的哺乳动物UPRmt组分。⁵³随后通过qPCR对这些发现进行了验证(图2C和图S2A),并进一步观察到,同样参与UPRmt的线粒体蛋白酶HSPE1在SIE后3 h升高幅度更大(图S2A)。这些结果提示,SIE后线粒体和胞质HSP发生协调性上调,这与UPRmt转录反应需要胞质和线粒体HSP协同激活的观点一致。⁵⁴˒⁵⁵为确认SIE后应激的线粒体来源,我们利用“mitostress”基因集对数据集进行了分析,该基因集由既往研究中在不同体外线粒体应激条件下共同上调的基因构成。⁵⁶与上述结果一致,“mitostress”基因集仅在SIE后显著富集〔标准化富集分数(NES)= 1.50;错误发现率(FDR)< 0.01;图2D〕。“mitostress”基因集的上调仅发生于SIE后的早期恢复阶段(图S2B),提示线粒体应激和UPRmt反应发生于SIE后的早期,并在恢复24 h时消退,这表明SIE是一种线粒体兴奋效应性应激源,即这种应激是可逆且具有适应性的。⁵⁷˒⁵⁸图2|MICE与SIE在恢复早期的转录组分化。
A 中等强度持续运动(MICE)和冲刺间歇运动(SIE)后3 h差异调控转录本的层次聚类。热图左侧列出了已知参与未折叠蛋白反应(UPR)的代表性转录本。B 采用过度代表分析(ORA)绘制的气泡图,显示仅在SIE后显著正向富集的通路。C DDIT3和HSPD1的mRNA水平——这两者是参与线粒体未折叠蛋白反应(UPRmt)的关键转录本,并经RNA测序鉴定为在SIE(n = 14)后较MICE(n = 13)上调幅度更大。D 先前鉴定的线粒体应激基因集(称为“mitostress”,引自Quiros等,2017)的基因集富集分析(GSEA),结果显示该基因集仅在SIE后富集。NES,标准化富集分数;FDR,错误发现率;GO,基因本体。
为进一步理解UPRmt转录上调之前发生的事件,我们随后采用透射电子显微镜(TEM)定量分析MICE和SIE前后线粒体的形态学及超微结构变化(图3A)。在所有形态学变量中,MICE后均未观察到显著变化(图3B;源数据),这与我们的RNA测序数据中该运动方式缺乏线粒体应激特征相一致(图S2B)。相反,SIE后线粒体圆形度显著增加,同时长宽比下降(提示线粒体复杂性下降;图3B)。我们还观察到SIE后线粒体大小增加(以面积衡量;图3B),这提示线粒体肿胀,⁵⁹并存在与RNA测序结果一致的线粒体应激。⁶⁰
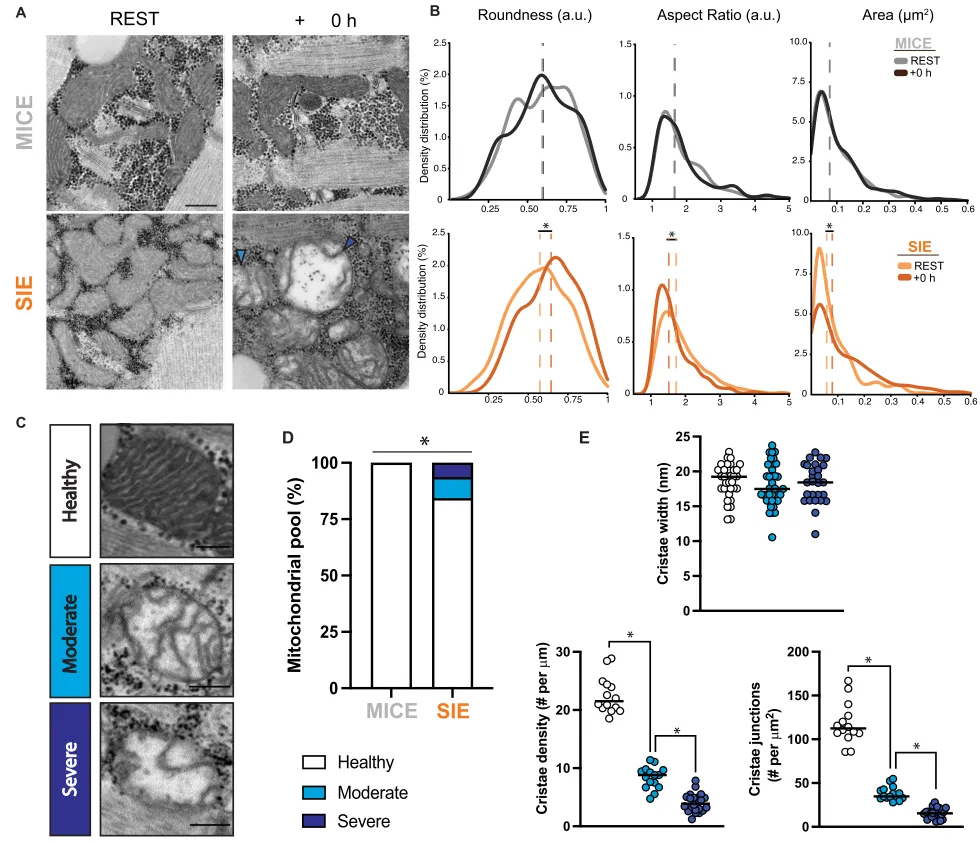
鉴于SIE后观察到明确的转录和形态学线粒体应激特征,我们进一步进行了定性分析,以检测是否存在线粒体超微结构紊乱。值得注意的是,在SIE后,平均有16%的分析线粒体群表现出超微结构紊乱的迹象(图3C、D);而这一现象在两组静息状态下以及MICE后均未观察到。这些线粒体紊乱进一步分为中度或重度,并与嵴密度下降及嵴连接数量减少相关,但与嵴宽度变化无关(图3E和源数据)。类似的线粒体超微结构紊乱此前已在非人类骨骼肌耐力运动后有所报道(如大鼠力竭跑步⁶¹以及马长时间跑步或冲刺后⁶²),但在人类中,中等强度耐力运动后此前并未观察到这种现象,⁶³这与我们在MICE后的结果一致。据我们所知,本研究结果首次报道了人类耐力运动后线粒体超微结构紊乱。线粒体超微结构受损可能会影响依赖膜电位的过程,如蛋白导入和ATP合成。⁶⁴˒⁶⁵综合来看,这些结果印证了我们的转录组学结果,并提示一种新的观点:SIE可急性诱发人类骨骼肌线粒体超微结构紊乱,并启动线粒体特异性应激反应。图3|SIE后线粒体形态学及超微结构紊乱。
A 中等强度持续运动(MICE;n = 4)和冲刺间歇运动(SIE;n = 5)前后骨骼肌的代表性透射电子显微镜(TEM)图像。浅蓝色箭头指示中度受损线粒体,深蓝色箭头指示重度受损线粒体。在MICE后+0 h获得的样本中未识别到受损线粒体。比例尺 = 0.5 µm。B MICE前后〔REST,n = 428;+0 h,n = 446〕和SIE前后〔REST,n = 603;+0 h,n = 551〕线粒体轮廓面积、圆形度和长宽比的密度分布。C 各类别健康、中度受损或重度受损线粒体的代表性图像。比例尺 = 0.2 µm。D MICE和SIE后被判定为健康、中度受损或重度受损的线粒体轮廓分布。E 各亚组代表性线粒体的线粒体嵴宽度(健康 = 22,中度 = 39,重度 = 27)、密度(健康 = 14,中度 = 15,重度 = 22)和连接数(健康 = 14,中度 = 15,重度 = 22)。*表示组间差异p < 0.05。数据以均值表示。B和D中的组间差异采用单因素方差分析评估。E采用单因素方差分析并结合Sidak多重比较检验。源数据见Source Data文件。
SIE后整合应激反应(ISR)和线粒体质量控制(MQC)通路上调
基于我们的转录组学(RNA-seq)和电子显微镜(TEM)结果,我们假设,与线粒体应激相关的通路会因所测试的两种运动方式不同而呈现差异性激活。在人类中,线粒体应激可通过整合应激反应(ISR)信号通路恢复细胞稳态。⁵⁶˒⁶⁶⁻⁶⁸因此,我们检测了ISR因子真核翻译起始因子2α(eIF2α)的磷酸化水平,以及蛋白磷酸酶1调节亚基15A(PPP1R15A,也称GADD34)mRNA的表达,这两者均会在ISR激活后升高。⁶⁸与我们的假设一致,我们观察到,SIE后eIF2α磷酸化和PPP1R15A mRNA表达的升高幅度均大于MICE后(图4A)。同样,我们还观察到,SIE后激活转录因子3(ATF3)mRNA和成纤维细胞生长因子21(FGF21)mRNA的升高幅度更大(图S3A),而这两者均已知会在骨骼肌慢性线粒体应激后上调。⁶⁹˒⁷⁰然而,我们并未观察到其他经典ISR和线粒体应激相关基因的变化,这些基因此前曾被报道可由非运动性应激源诱导,⁶⁹˒⁷⁰如TRIB3、ATF4和ATF5 mRNA(图S3B)。我们也未观察到OMA1蛋白含量的变化(图S3D),而此前有研究报道其会在体外线粒体应激后发生降解。⁶⁶这种差异可能与应激源的类型(即运动)、幅度(即受损线粒体数量中等)和持续时间有关——SIE仅需3 min运动,而既往研究中的应激持续时间为6–24 h(即体外实验⁵⁶˒⁷¹)或数年(即线粒体肌病⁶⁹˒⁷⁰)。尽管仍需进一步研究,我们的结果提示,超高强度运动可诱导一种特异性的ISR和线粒体应激反应。
SIE后观察到的线粒体超微结构破坏(图3C)提示,这种运动方式后可能需要通过线粒体自噬增强线粒体质量控制(MQC)。为评估线粒体自噬,我们检测了Unc-51样自噬激活激酶1(ULK1)丝氨酸556位点的磷酸化水平(因其在运动诱导的线粒体自噬中具有机制性作用)。³⁶仅在SIE后+1.5 h观察到ULK1在S566位点的磷酸化上调,并且在整个恢复期内表现出组别效应(图4B、C)。然而,在LC3B-II或p62蛋白丰度方面,我们未观察到组间差异(图4B、C),提示这一效应独立于一般性自噬。⁷²随后,我们筛查了一项近期关于MICE和SIE的人体磷酸化蛋白质组学数据集,以识别运动后参与MQC的磷酸化位点。¹⁶该数据集揭示了多个仅受SIE调控的磷酸化位点,包括eIF2α、线粒体自噬受体Optineurin(OPTN)丝氨酸177位点(此前已与线粒体自噬相关⁷³⁻⁷⁷)、自噬受体p62酪氨酸269位点(与自噬调控相关⁷⁸),以及多个HSP(图S3C);这些发现进一步支持SIE后MQC上调幅度更大。通过TEM,我们仅在SIE后观察到多种与MQC相关的事件,如线粒体自噬小体、线粒体降解(图4D)以及自噬小体膜与线粒体外膜的对接(图S3E)。综合来看,这些发现支持我们的假设,即SIE是线粒体应激的强效诱导因素,可导致UPRmt上调,并伴随ISR和MQC通路的激活(图4E)。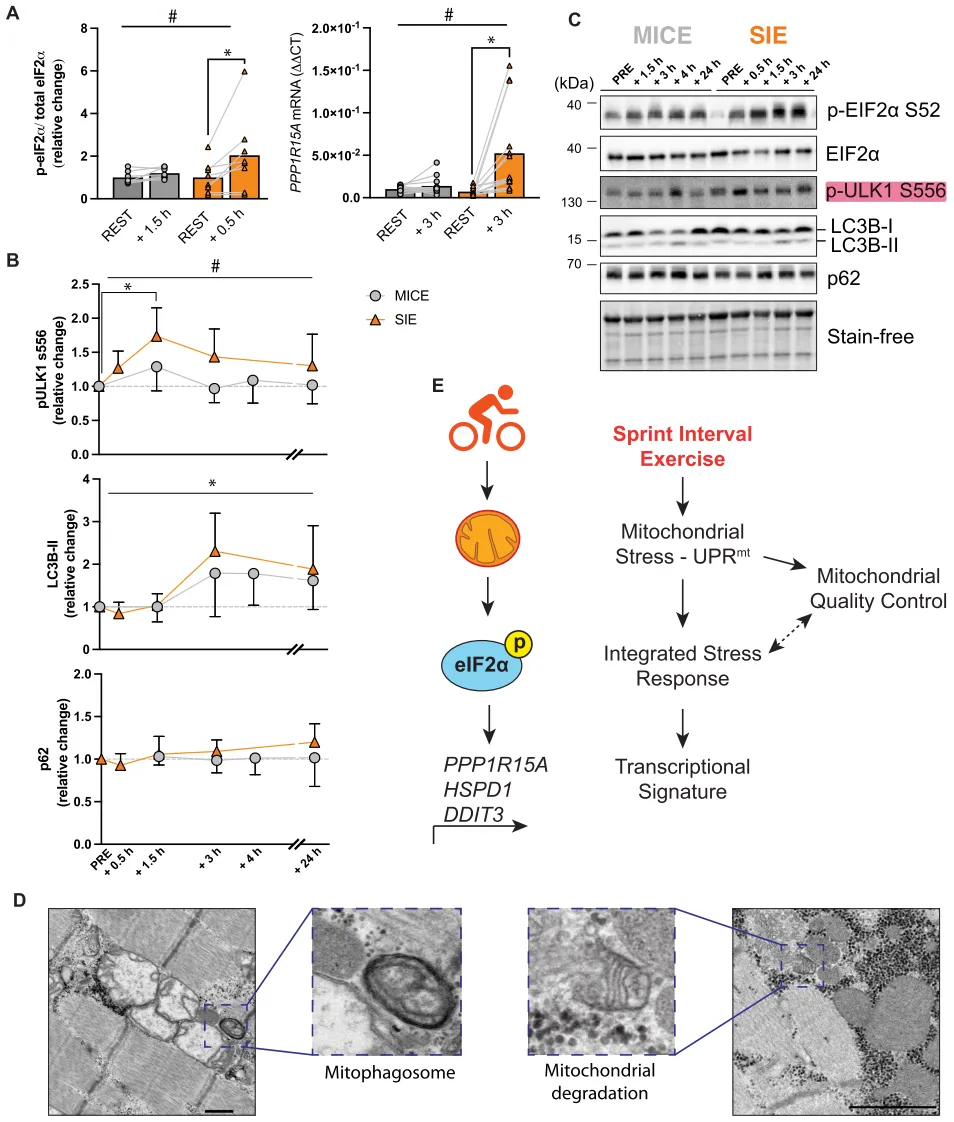 A 运动诱导的整合应激反应(ISR)标志物升高〔eIF2α丝氨酸52位点磷酸化:MICE n = 7,SIE n = 8;PPP1R15A mRNA:MICE n = 13,SIE n = 14〕。⁶⁸B 中等强度持续运动(MICE;pULK1 S556和LC3B均n = 13,p62为n = 9)和冲刺间歇运动(SIE;pULK1 S556和LC3B均n = 14,p62为n = 11)后关键自噬和线粒体自噬蛋白变化的时间过程。C 所分析蛋白的代表性Western blot图像。无染色图像显示各样本间蛋白上样量一致。D SIE后显微图像,显示肿胀的线粒体聚集在一起,邻近有一个线粒体自噬小体,以及一个线粒体降解事件。比例尺 = 0.5 µm。E SIE如何通过ISR感知线粒体应激而启动独特转录特征的模型。*表示组间差异或主效应p < 0.05;#表示时间×组别交互作用p < 0.05。A中数据以均值表示,B中数据以均值 ± 95%置信区间表示。A和B中的组间差异采用双因素方差分析并结合Sidak多重比较检验评估。源数据见Source Data文件。
A 运动诱导的整合应激反应(ISR)标志物升高〔eIF2α丝氨酸52位点磷酸化:MICE n = 7,SIE n = 8;PPP1R15A mRNA:MICE n = 13,SIE n = 14〕。⁶⁸B 中等强度持续运动(MICE;pULK1 S556和LC3B均n = 13,p62为n = 9)和冲刺间歇运动(SIE;pULK1 S556和LC3B均n = 14,p62为n = 11)后关键自噬和线粒体自噬蛋白变化的时间过程。C 所分析蛋白的代表性Western blot图像。无染色图像显示各样本间蛋白上样量一致。D SIE后显微图像,显示肿胀的线粒体聚集在一起,邻近有一个线粒体自噬小体,以及一个线粒体降解事件。比例尺 = 0.5 µm。E SIE如何通过ISR感知线粒体应激而启动独特转录特征的模型。*表示组间差异或主效应p < 0.05;#表示时间×组别交互作用p < 0.05。A中数据以均值表示,B中数据以均值 ± 95%置信区间表示。A和B中的组间差异采用双因素方差分析并结合Sidak多重比较检验评估。源数据见Source Data文件。MICE与SIE后线粒体生物发生和动力学受到相似调控
由于运动已知可增加与线粒体生物发生相关基因的表达,¹⁷˒⁴²且运动诱导这些基因更大程度上调仍被认为是SIE高效性的潜在机制之一,²⁶˒²⁸因此我们进一步探讨了线粒体生物发生标志物的基因表达水平。我们观察到,所谓线粒体生物发生的“主调控因子”PGC1α(由PPARGC1A基因编码)在两种运动后转录水平均有类似升高,仅在不同时间点存在轻微组间差异,且有时偏向任一组(图S4A)。在过氧化物酶体增殖物激活受体α(PPARα)或β(PPARβ)的转录反应方面,组间也无差异(图S4A)。这些结果总体提示,MICE和SIE后常见线粒体生物发生标志物的转录激活在很大程度上是共享的。
鉴于此前研究提出线粒体动力学成分会受到运动调控,³⁵˒⁴⁰我们还进一步探讨了其参与情况(主要终点)。参照既往研究的方法,³⁷我们从TEM图像中定量分析了线粒体接触位点(作为线粒体预融合事件的替代指标)和线粒体缢缩事件(作为预分裂事件的替代指标)。我们观察到,线粒体接触位点和缢缩事件均存在运动诱导效应,但组间无差异(图S4B)。然而,在SIE后,我们观察到缢缩事件特异性发生在线粒体超微结构受损区域附近的线粒体末端(图S4C)——这是一种可预测线粒体降解的线粒体分裂特征。⁷⁹在mRNA水平上,除线粒体延长因子2(MIEF2,也称MiD49)外,我们未观察到大多数线粒体动力学因子的组间表达差异。MIEF2编码动力蛋白相关蛋白1(DRP1,驱动线粒体分裂的GTP酶)的线粒体分裂受体,在SIE恢复过程中相较于MICE呈现不同调控模式,这可能提示分裂需求增加(图S4A)。然而,在蛋白水平上,我们未观察到线粒体融合蛋白2(MFN2)或分裂因子1(FIS1)的差异(图S4D)。这些结果提示,MICE与SIE后线粒体生物发生和动力学标志物受到相似调控。
鉴于单次SIE或MICE后观察到不同反应,我们进一步探讨这些差异是否会导致训练后线粒体重塑的分化,即数周内重复运动后所形成的差异。为研究训练诱导的线粒体重塑,在28名受试者中有24人完成了为期8周、每周3–4次的训练(共29次运动),并在最后一次运动后72 h获取了最终肌肉样本(图5A)。在心肺适能和耐力表现指标方面,如最大有氧功率、4 km计时赛(TT)成绩和20 km计时赛成绩,训练均表现出显著主效应(均p < 0.05)(图S5A)。
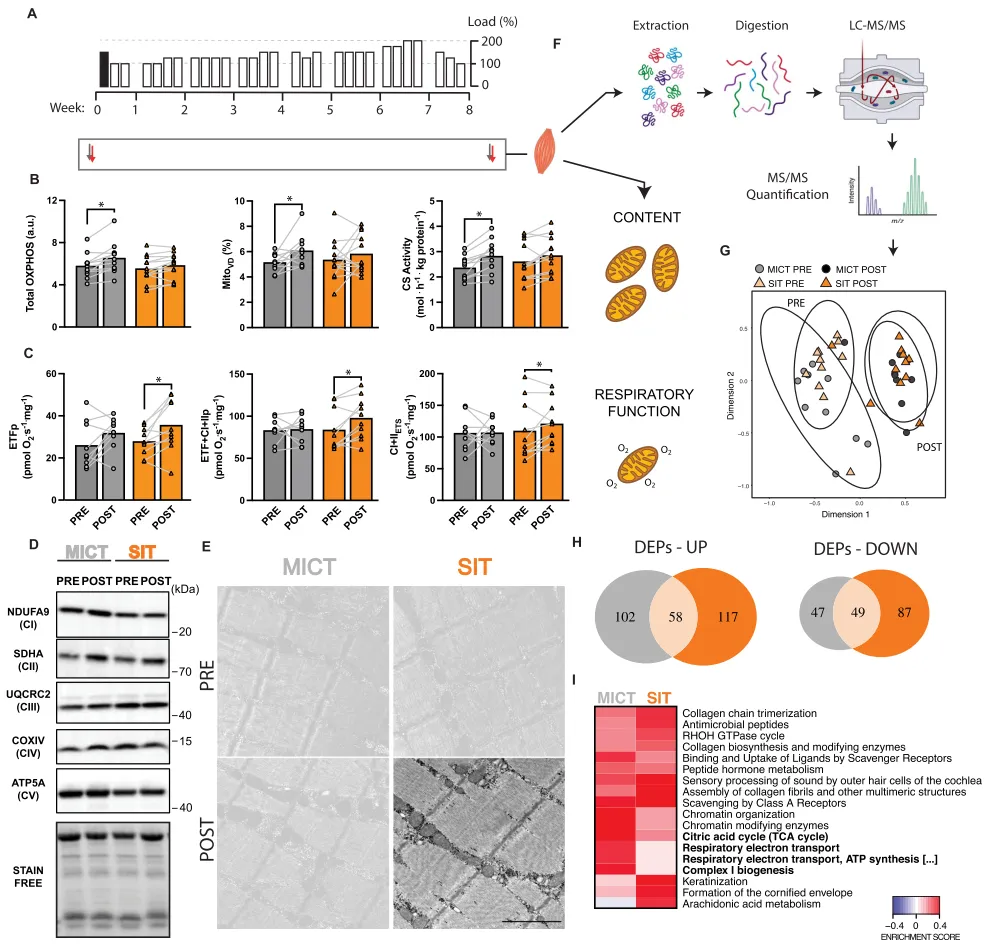
与我们此前关于运动容量或强度驱动线粒体重塑分化的研究结果一致,²⁹⁻³¹˒⁸⁰我们观察到,MICT可显著增加五种氧化磷酸化复合体(OXPHOS)代表性亚基的总蛋白含量(图5B、D)、线粒体体积分数(MitoVD;图5B、E;主要终点)以及柠檬酸合酶活性(CS;图5B;主要终点)。然而,在SIT后,这些线粒体含量标志物均未发生显著变化(均p > 0.05)。值得注意的是,MICT完成了5倍更高的训练容量,但这并未转化为任何线粒体含量标志物约5倍更大的升高,提示训练容量与其他因素(如强度)的相互作用可能对于最大化训练诱导的线粒体含量变化至关重要。这一假设也得到既往研究支持:在持续32天、训练容量极高(342 ± 42 min/天)但强度较低的越野滑雪训练后,MitoVD并未发生变化。⁸¹随后,我们在全肌通透化肌纤维中评估了不同呼吸底物刺激下的线粒体功能(主要终点)。在SIT后而非MICT后,我们观察到脂肪酸氧化在线粒体磷酸化状态下的呼吸链功能显著增加[电子转移黄素蛋白(ETFp)]。同样,仅在SIT后加入复合体I和复合体II相关底物后[ETF + CIp和ETF + CI + CIIP,见“方法”]观察到呼吸功能升高(p < 0.05;图5C和图S5B)。这与既往研究一致,即运动强度是线粒体呼吸链功能变化的关键驱动因素。²⁸相反,对呼吸链各单个酶活性的分光光度法测定显示,仅在MICT后而非SIT后,复合体I(CI)活性显著增加(图S6B)。因此,尽管仅MICT增加了线粒体含量和CI活性,但仅SIT——其与线粒体应激及质量控制通路上调相关(见图4E)——提高了线粒体呼吸速率。有趣的是,SIT后呼吸速率升高并未伴随线粒体含量或CI活性的显著变化。这些发现进一步证明,如既往研究所提示,离体线粒体呼吸功能的变化可以与线粒体含量和复合体活性的变化相分离。³¹˒⁸²图5|MICT和SIT后骨骼肌蛋白质组重塑存在差异。
A 8周内完成的运动训练课程示意图。黑色部分表示采集肌肉活检的实验性运动课程。B 来自整体肌肉的线粒体含量标志物,包括总氧化磷酸化(OXPHOS)蛋白含量(左图;MICT,n = 11;SIT,n = 12;a.u.,任意单位)、线粒体体积分数(MitoVD;中图;MICT,n = 10;SIT,n = 12)和柠檬酸合酶活性(CS;右图;MICT,n = 11;SIT,n = 12)。C 在线粒体通透化肌纤维中测定线粒体呼吸功能。左图:电子转移黄素蛋白(ETFp)介导的呼吸〔反应体系含0.2 mM辛酰肉碱、2 mM苹果酸、3 mM MgCl2和5 mM ADP〕;中图:加入复合体I和复合体II相关底物后的呼吸(ETF + CI + CIIP;反应体系含5 mM丙酮酸、10 mM琥珀酸、3 mM MgCl2和5 mM ADP);右图:经解偶联剂FCCP滴定〔0.7–1.5 mM〕后获得的电子传递系统(ETS)最大容量;分别为MICT(n = 8)和SIT(n = 10)。详见“材料与方法”。D 用于计算总OXPHOS丰度的代表性蛋白条带图。E 各组运动训练前(PRE)和训练后(POST)的代表性显微图像。比例尺 = 1 µm。F 蛋白质组学分析流程。G 两组蛋白质组分析的主成分分析(PCA)(MICT,n = 11;SIT,n = 12)。H 维恩图显示,尽管PCA图总体相似,但差异表达蛋白仅有一部分为两组共有。I 基于Reactome通路的组间蛋白富集分析。*表示主效应p < 0.05。数据以均值表示。B和C中的数据采用预先设定的单因素方差分析。源数据见Source Data文件。使用BioRender制作。Bishop, D.
MICT/SIT之间全蛋白质组水平的差异性重塑提示线粒体特异性重塑
在确定MICT和SIT会导致不同的线粒体重塑后,我们进一步采用蛋白质组学分析,以鉴定在整体肌肉水平上是否也存在线粒体之外的蛋白通路发生差异性重塑。我们对全肌裂解液进行了无标记蛋白质组学分析(图5F),并在所有样本中定量到2478种蛋白,这与近期研究结果一致。⁸³˒⁸⁴差异表达分析显示,在检测到的蛋白中,约10%的蛋白丰度在SIT(250种蛋白)和MICT(230种蛋白)后发生了显著改变(源数据)。主成分分析(PCA)显示,在蛋白质组水平上,两组均表现出明确的运动训练效应(图5G),这进一步证实了运动训练对骨骼肌可塑性的公认影响。⁸⁵鉴于每种运动方式均调控了大量差异蛋白(373种为特有,107种为共有;图5H),我们随后采用多维基因集富集分析(GSEA)方法,以展示MICT和SIT训练效应的协调性或差异性。⁸⁶采用Reactome数据库分析显示,MICT后富集程度最高且与SIT显著不同的通路包括电子传递链(ETC)、三羧酸循环(TCA)以及复合体I生物发生(图5I)。
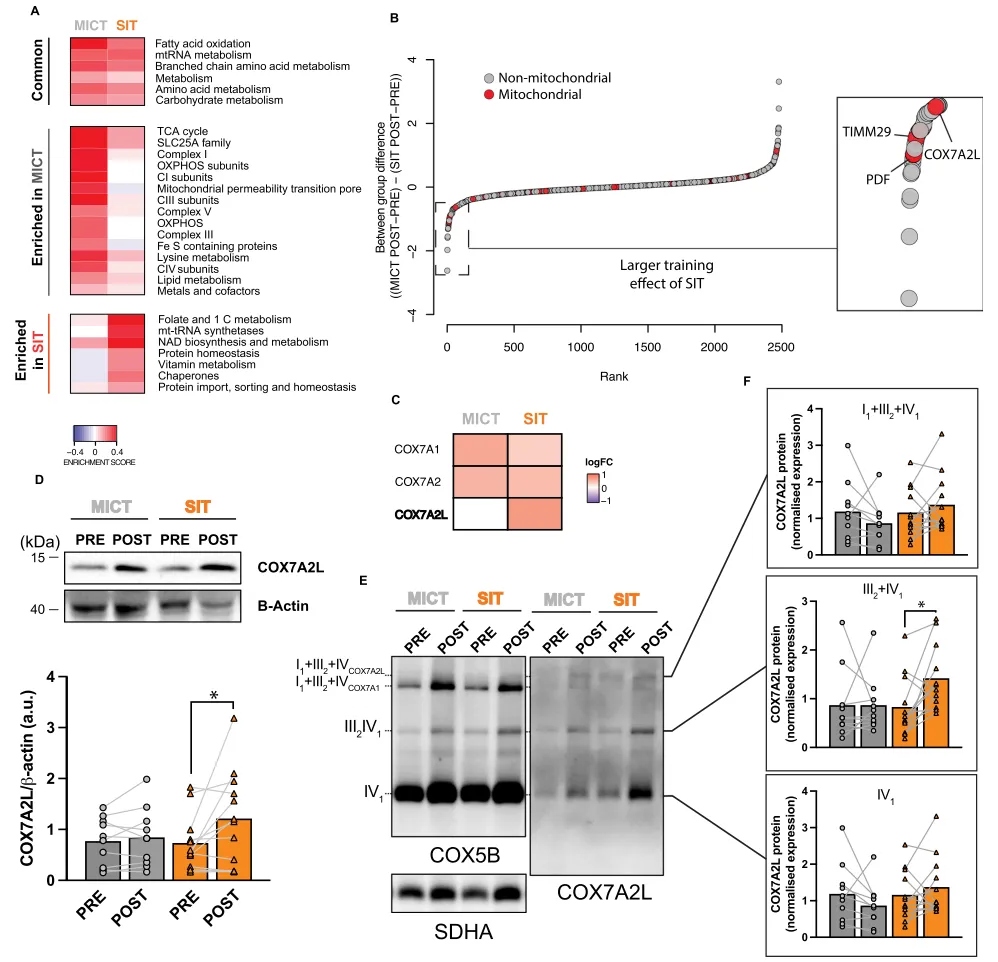
上述结果提示,训练诱导的线粒体蛋白质组变化存在差异,并与我们的生化和显微分析结果一致。随后,我们再次回到蛋白质组富集分析,但这次采用MitoCarta 3.0通路数据库。⁸⁷该数据库是针对线粒体蛋白高度整理的注释体系。在MICT和SIT后均显著富集的通路中,包括脂肪酸氧化、氨基酸代谢、线粒体RNA代谢以及碳水化合物代谢,这提示MICT和SIT均可引发广泛的代谢适应(图6A)。MICT后富集的通路不仅包括预期的TCA循环和ETC通路,还包括溶质载体家族SLC25A、线粒体通透性转换孔、脂质代谢、铁硫蛋白以及赖氨酸代谢(图6A)。仅有少数通路在SIT后呈特异性富集,其中包括叶酸和一碳(1C)代谢、线粒体tRNA合成酶、烟酰胺腺嘌呤二核苷酸(NAD+)生物合成与代谢,以及蛋白导入、分选和稳态维持。SIT后上调的部分通路,包括1C代谢、NAD+代谢和蛋白稳态,已在体外和体内线粒体应激模型中被广泛证实发生失调。⁶⁹⁻⁷¹因此,我们的蛋白质组学结果提示,SIE后观察到的线粒体应激和UPRmt可能会影响运动训练所致的线粒体蛋白质组重塑。此外,MICT和SIT后这种差异性的线粒体特异性蛋白质组重塑,也与这样一种观点一致,即通过给予不同运动方案,可以实现特定类型的线粒体重塑。⁸³最后,我们进一步思考,SIT为何能够在线粒体含量标志物或OXPHOS蛋白丰度并未同步增加的情况下,提高线粒体呼吸链功能。为此,我们利用全面的全蛋白质组分析结果,根据训练诱导的组间差异幅度对蛋白进行了排序(图6B和源数据)。我们将注意力集中于那些在SIT后变化幅度大于MICT的线粒体蛋白。在发现的前三位线粒体蛋白中,分别为肽去甲酰酶(PDF)、线粒体内膜转位酶29(TIMM29)和细胞色素c氧化酶亚基7A2样蛋白(COX7A2L,也称超复合体组装因子1,SCAF1)。这些蛋白分别参与线粒体蛋白合成、⁸⁸内膜蛋白导入⁸⁹以及呼吸链超复合体(SCs)的组装。⁹⁰我们重点关注了COX7A2L(图6C),因为既往研究表明其与肌肉功能标志物相关。⁹¹COX7A2L还是一个具有吸引力的候选分子,因为其表达可在ISR激活后被诱导,⁹²而ISR在SIE后上调幅度更大(见图4)。此外,在糖酵解代谢更活跃的条件下,COX7A2L被认为可促进SC III2 +IV1以及S-respirasome〔含COX7A2L的SC I1 +III2 +IV1-2〕的形成,⁹³而我们的数据也显示,与MICE相比,SIE引起更强的糖酵解激活(图1C)。最后,我们并未观察到其他任何OXPHOS组分仅在SIT后发生蛋白富集。免疫印迹分析证实,仅在SIT后,COX7A2L蛋白丰度显著升高(图6D),而MICT后并无此变化,且这一变化独立于线粒体含量标志物的改变(图5B)。相反,经典COX7A1蛋白水平仅在MICT后显著升高(图6C和源数据)。这一观察结果提示,可能存在一种由COX7A介导的呼吸链复合体及超复合体重组,以使线粒体呼吸功能适应MICT(更偏氧化代谢)和SIT(更偏糖酵解代谢)所诱导的不同代谢条件。据我们所知,此前尚无研究探讨COX7A2L在人类训练诱导线粒体适应中的潜在作用。既往研究表明,COX7A2L对于驱动不同超复合体结构的形成至关重要。⁹³⁻⁹⁵既往证据显示,经典COX7A1/2蛋白是可互换的。在促进氧化代谢的条件下,更高效的C-MRC组织形式更易形成〔I1 + III2 +IV1-2,含COX7A1/2,以及游离的CIII2和CIV〕。相反,在促进糖酵解代谢的条件下,COX7A2L在促进较低效率的S-MRC形成中发挥关键作用〔含COX7A2L的I1 + III2 +IV1-2以及SC III2 +IV1〕。⁹³通过蓝色天然聚丙烯酰胺凝胶电泳(blue-native PAGE)(图6E和图S6A),我们探讨了MICT或SIT诱导的特定COX7A亚型变化是否与超复合体和respirasome的不同变化相关。值得注意的是,我们观察到,SIT诱导的COX7A2L水平升高与SC III2 +IV1显著积累相关,但与含COX7A2L的respirasome(I1 +III2 +IV1-2)积累无关(图6F)。结合既往结构研究结果,即当CIII2和CIV组装成该超复合体时可获得催化优势,⁹⁵因此,仅在SIT后SC III2 +IV1更多积累,可能有助于解释SIT而非MICT后线粒体呼吸功能的显著增强(图5C)。然而,SIT后COX7A2L蛋白水平相对变化(无论是在整体肌肉水平还是在各超复合体内)与线粒体呼吸功能变化之间均无显著相关性(图S6C),这提示可能还有其他因素参与了SIT后呼吸功能增强。值得注意的是,我们观察到,急性SIE诱导的ISR激活〔以eIF2α磷酸化衡量〕与训练诱导的COX7A2L整合进入SC III2 +IV1和respirasome(I1 +III2 +IV1-2)之间存在显著关联。图6|线粒体特异性蛋白质组重塑揭示由COX7A2L蛋白驱动的差异性超复合体重塑。A 采用mitch软件包并结合MitoCarta 3.0基因集进行的二维差异蛋白富集分析。B MICT和SIT后训练诱导的各个蛋白相对丰度变化比较分析;依据MitoCarta 3.0定义为线粒体蛋白的蛋白以红色标示。C COX7A2L被鉴定为MICT(n = 10)与SIT(n = 12)之间差异调控的蛋白,同时还与其他COX7A家族成员进行了比较。D 全肌分析中COX7A2L和看家蛋白β-actin的代表性SDS-PAGE条带图(a.u.,任意单位)。下图表示全肌裂解液中COX7A2L蛋白水平在MICT前后(PRE和POST;n = 10)及SIT前后(PRE和POST;n = 12)的变化,显示仅在SIT后显著增加。E MICT(n = 10)和SIT(n = 12)后呼吸链复合体及超复合体中COX7A2L相对丰度及分布的代表性BN-PAGE条带图。F MICT(n = 10)和SIT(n = 12)后各超复合体组分中COX7A2L蛋白丰度的标准化变化(以柠檬酸合酶活性进行标准化)定量结果。*表示主效应p < 0.05。数据以均值表示。D和F中的组间差异采用预先设定的单因素方差分析评估。源数据见Source Data文件。在本研究中,我们表明,冲刺间歇运动(SIE)可特异性诱导线粒体超微结构紊乱,且这一变化先于线粒体应激的转录特征以及线粒体未折叠蛋白反应(UPRmt)的激活而出现。这些变化仅见于SIE后,而非MICE后,并且还伴随着整合应激反应(ISR)和线粒体质量控制(MQC)通路更大程度的激活。这些独特的急性反应进一步对应于不同的线粒体重塑——中等强度持续训练(MICT)的特征是线粒体含量标志物增加,而冲刺间歇训练(SIT)则导致线粒体呼吸链功能增强。后续蛋白质组学分析显示,SIT后涉及一碳(1C)代谢、NAD+代谢以及线粒体蛋白质量控制通路的特异性富集。我们还鉴定到仅在SIT后出现的、由COX7A2L介导的III2 +IV1呼吸链超复合体积累。我们的结果为阐明不同运动处方如何实现不同类型的线粒体重塑提供了有价值的分子机制见解。我们的研究发现表明,超高强度冲刺运动可在人类骨骼肌中诱发线粒体结构紊乱,并激活线粒体特异性应激反应。
尽管运动的健康获益已广为人知,但其潜在分子机制仍仅部分得到阐明。¹¹运动处方(如运动强度的选择)被普遍认为是优化运动获益的关键变量。⁹⁶˒⁹⁷在本研究中,我们表明,SIE和MICE均可诱导在很大程度上共享的运动转录反应(图1)。然而,SIE在恢复早期产生了独特的分子特征,其特征为UPRmt及相关线粒体应激通路上调(图2)。这与小鼠研究中关于运动可激活内质网未折叠蛋白反应(UPRER)的报道一致,⁹⁸但UPRmt在大多数运动研究中,尤其是涉及人类的研究中,仍未得到充分探索。我们的结果提示,SIE后而非MICE后出现的线粒体紊乱,其特征为线粒体超微结构和形态学紊乱,而这很可能促成了UPRmt以及ISR和MQC通路的激活。UPRmt的适应性在很大程度上似乎取决于应激发生的组织、持续性及其可逆性。⁵⁸事实上,伴有线粒体遗传缺陷的骨骼肌肌病表现为一种看似适应不良的慢性线粒体应激。⁶⁹˒⁷⁰相比之下,我们推测,冲刺间歇运动所引发的这种短暂且瞬时的应激,使其成为一种强有力的线粒体兴奋效应事件,从而导致骨骼肌发生适应性重塑。线粒体应激的瞬时性也得到了我们观察结果的支持,即SIE诱导的线粒体应激特征在运动后24 h已不再存在(图S2)。我们的结果还有助于解释此前的报道,即在过量高强度训练后不久采集活检时,骨骼肌中可观察到线粒体功能受损,⁹⁹˒¹⁰⁰而在肌肉取样前给予充分恢复时则不会观察到此现象。⁸³˒¹⁰¹值得进一步探讨的是,如果运动间歇之间恢复不足,反复的线粒体应激是否可能构成某些运动训练方案产生适应不良效应的基础。鉴于大量证据表明,高强度间歇训练在改善多种代谢性疾病和年龄相关疾病指标方面更为有效,目前仍需进一步阐明,在本研究中看起来主要特异于冲刺间歇运动的UPRmt激活,是否也构成这些获益的部分基础。长期以来,人们已知耐力训练可提高线粒体含量和呼吸链功能,并常将其描述为按比例同步发生的适应。¹⁰然而,与这一长期持有的观点相反,我们的结果表明,不同运动处方会在线粒体含量、呼吸链功能和线粒体蛋白质组方面产生特异且分化的改变(图5)。MICT增加了多个线粒体含量标志物和CI酶活性,而这些变化在SIT后均未达到显著水平,这与既往文献一致。²⁸˒¹⁰²相比之下,SIT的特征是线粒体呼吸链功能的功能性增强,以及与NAD+代谢、蛋白导入、蛋白折叠和1C代谢相关的线粒体蛋白质组特异性重塑(图5);这些通路均是UPRmt激活及其反应中的关键通路,⁵⁴˒⁷¹而UPRmt在本研究中同样主要特异于冲刺间歇运动。线粒体结构紊乱以及线粒体应激和MQC通路激活增强,是否可能通过增强线粒体自噬(如选择性去除“适应性较差”的线粒体)而促进线粒体呼吸功能改善,仍有待进一步研究。SIT另一项独特的适应表现为COX7A2L蛋白丰度显著增加,且主要积累于III2 +IV1超复合体中(图6)。这与既往研究结果一致,即在主要依赖糖酵解代谢的细胞中,COX7A2L介导的III2 +IV1超复合体积累是一种优先的结构组织形式,⁹³而这种代谢状态正如SIE后所发生的那样(见图1C)。此外,既往研究还将哺乳动物细胞中由COX7A2L介导的超复合体组装与ISR激活联系起来,⁹²而本研究中SIE后ISR上调幅度更大(图4),并且与训练诱导的COX7A2L整合进入超复合体呈正相关。有趣的是,已有研究表明,ISR激活会降低TCA循环中间代谢物水平,同时导致糖酵解中间产物积累。¹⁰³因此,我们推测,SIT后观察到的COX7A2L介导重塑,可能有助于在应激条件下通过促进糖酵解通量来维持线粒体生物能量学。最后一个观察结果是,SIT后SC III2 +IV1积累更多,但这并未与SIT后呼吸链功能更大幅度增强相关(图S6C)。尽管超复合体的功能意义仍存在争议,但我们的研究结果与这样一种观点一致:超复合体形成的主要作用是提供结构稳定性,而非在呼吸过程中增强复合体间的电子传递。⁹³˒¹⁰⁴˒¹⁰⁵因此,尽管COX7A2L及含COX7A2L的SC III2 +IV1丰度增加仅见于SIT后,但其功能学意义仍需进一步研究。仍需更多研究以明确线粒体复合体的超分子调控是否会影响人类运动训练后的线粒体生物能量学。⁸³˒¹⁰⁶总之,我们的研究结果支持这样一种观点,即冲刺间歇运动是人类中的一种天然线粒体兴奋效应性应激源。我们进一步强调了采用个体化训练干预以实现特定线粒体重塑的重要性,并为不同运动方式的分子反应提供了见解。由于人们普遍认为,运动的许多健康获益源于线粒体的改变,因此这些结果可用于优化运动处方,从而实现对人类健康具有重要意义的靶向线粒体适应。