Keytruda:帕博利珠单抗
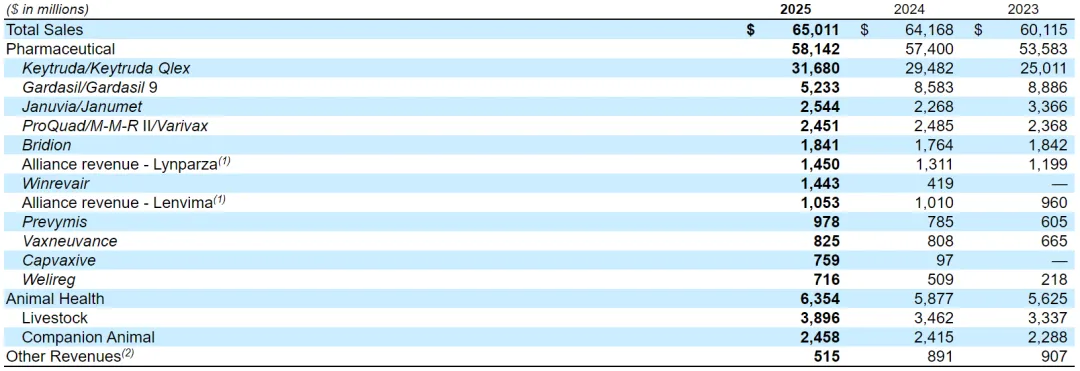
Keytruda是一种抗PD-1疗法,已在美国获得超40个适应症的批准,包括19个肿瘤类型和2个与肿瘤无关的适应症,其中许多适应症也已在全球市场获得类似批准,Keytruda临床开发计划包括广泛的癌症类型的研究。
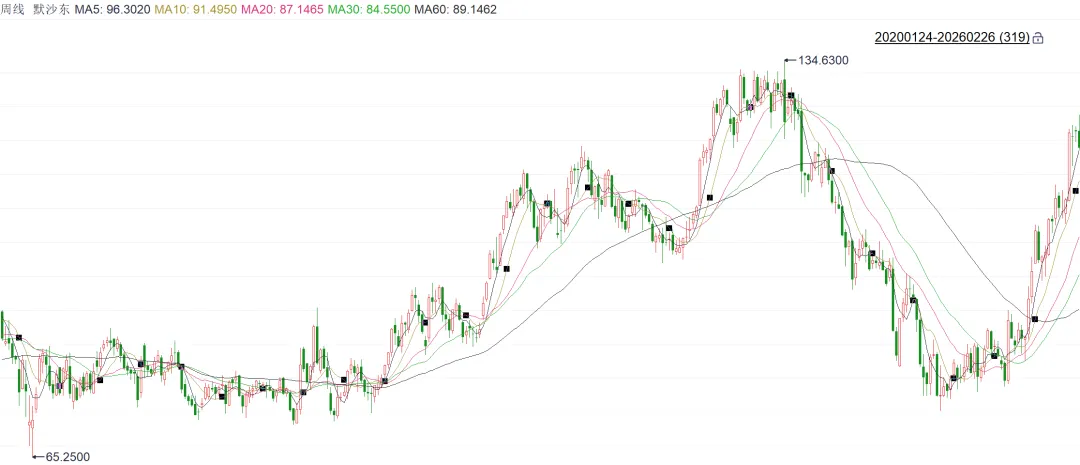
Keytruda是2023–2024 年全球药王,它是首个以肿瘤免疫治疗登顶全球销冠的药物,也是肿瘤领域商业化标杆,公司股价在2022-2023年期间翻了一倍。
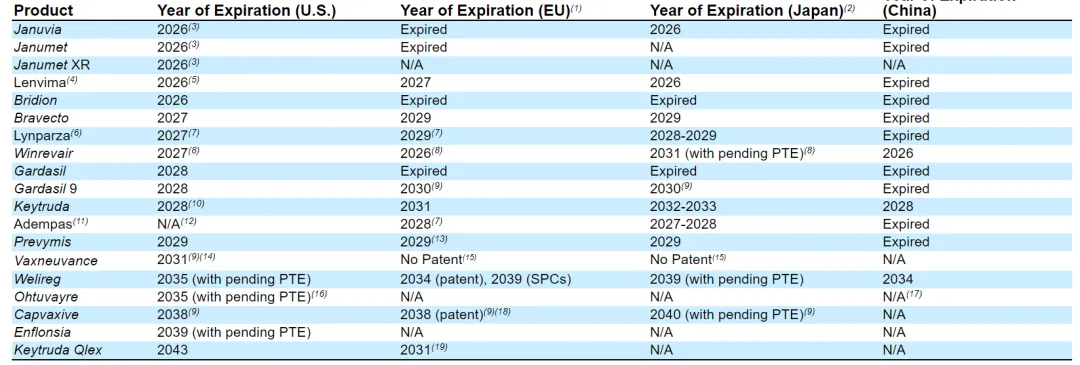
Keytruda的美国、中国专利将于2028年到期,欧盟专利2031年到期,日本专利2032-2033年之间陆续到期,预计未来两三年将继续贡献现金流。
2025年1月,中国国家药品监督管理局(NMPA)批准与抗体-药物偶联物(ADC)enfortumab vedotin联合用于治疗成人局部晚期或转移性尿路上皮癌。
2025年4月,欧盟委员会(EC)批准联合培美曲塞和化疗用于不可切除的非上皮样恶性胸膜间皮瘤成人患者的一线治疗。
2025年5月,日本厚生劳动省(MHLW)批准联合曲妥珠单抗和化疗用于不可切除、晚期或复发性HER2阳性胃癌或GEJ腺癌患者的一线治疗。
2025年5月,日本MHLW批准联合培美曲塞和化疗治疗不可切除、晚期或复发的转移性恶性胸膜间皮瘤。
2025年6月,美国食品药品监督管理局(FDA)批准用于治疗PD-L(CPS)≥ 1的可切除局部晚期HNSCC成人患者。
2025年6月,中国NMPA批准联合仑维玛治疗不可切除、非转移性HCC患者。
2025年10月,EC批准作为单一疗法治疗可切除的局部晚期HNSCC。
2025年11月,FDA批准与Padcev(enfortumab vedotin-ejfv)联合治疗MIBC成人患者。
2026年2月,中国NMPA批准用于某些原发性晚期或复发性子宫内膜癌患者的一线治疗。
2026年2月,FDA批准联合紫杉醇,联合或不联合贝伐珠单抗,用于治疗PD-L1(CPS ≥ 1)的上皮性卵巢、输卵管或原发性腹膜癌成人患者。
2026年2月,日本MHLW批准用于局部晚期HNSCC的辅助治疗。
Keytruda Qlex(皮下注射型)
2025年以来获批的重要适应症
2025年9月,FDA批准大多数成人实体瘤适应症。
2025年10月,FDA批准用于治疗PD-L1(CPS)≥ 1的可切除局部晚期HNSCC成人患者。
2025年11月,EC批准新的皮下给药途径适用于欧盟批准的所有成人适应症。
2026年2月,FDA批准联合紫杉醇,联合或不联合贝伐珠单抗,用于治疗PD-L1(CPS ≥ 1)的上皮性卵巢、输卵管或原发性腹膜癌成人患者。


