导读
不可手术局部晚期或转移性尿路上皮癌的一线治疗长期依赖含铂化疗,或含铂化疗联合免疫检查点抑制剂治疗;但人群异质性大,且临床上相当一部分患者因肾功能或体能状态等原因不耐受含铂方案,治疗起手方案始终存在“疗效—耐受”的难以平衡。HER-2 过表达在尿路上皮癌中并非罕见分子特征,既往 HER-2 靶向的 ADC 单药(RC-48)已显示出初步临床活性,并获得国内适应症;而与 PD-1 免疫治疗联用也出现了令人期待的抗肿瘤信号,使得“HER-2-ADC + PD-1抗体 能否在一线建立新标准、以及 HER-2 低表达(IHC 1+)能否进入获益范围”成为一个直接而关键的问题。
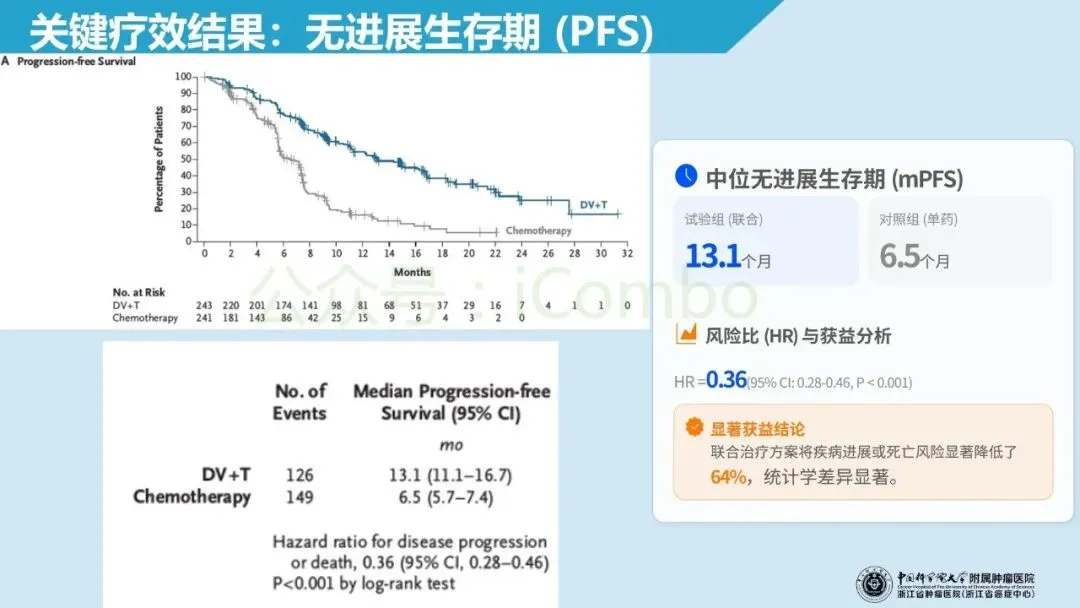
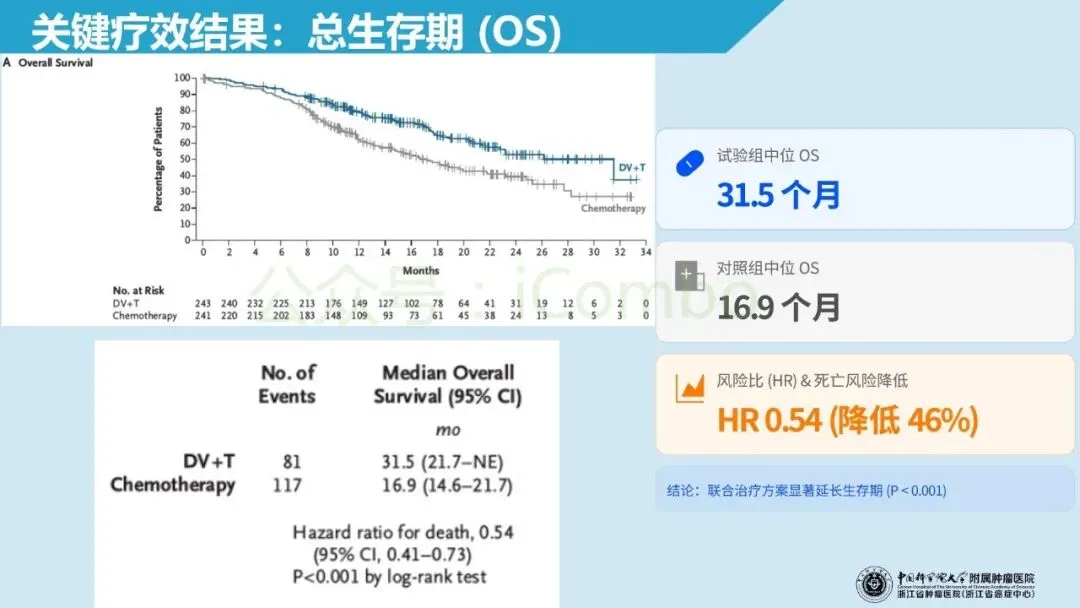
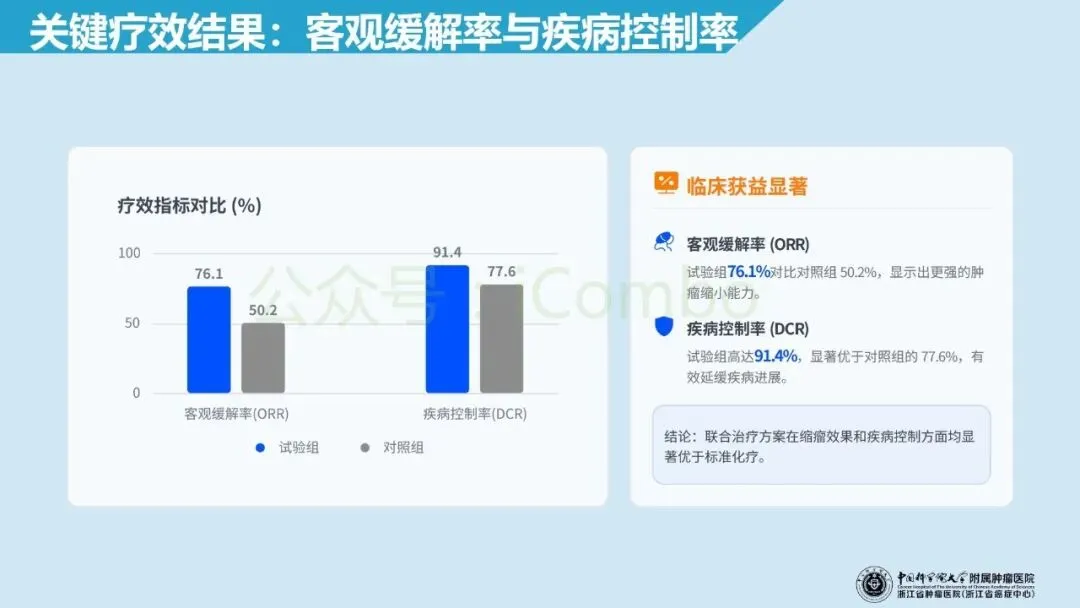
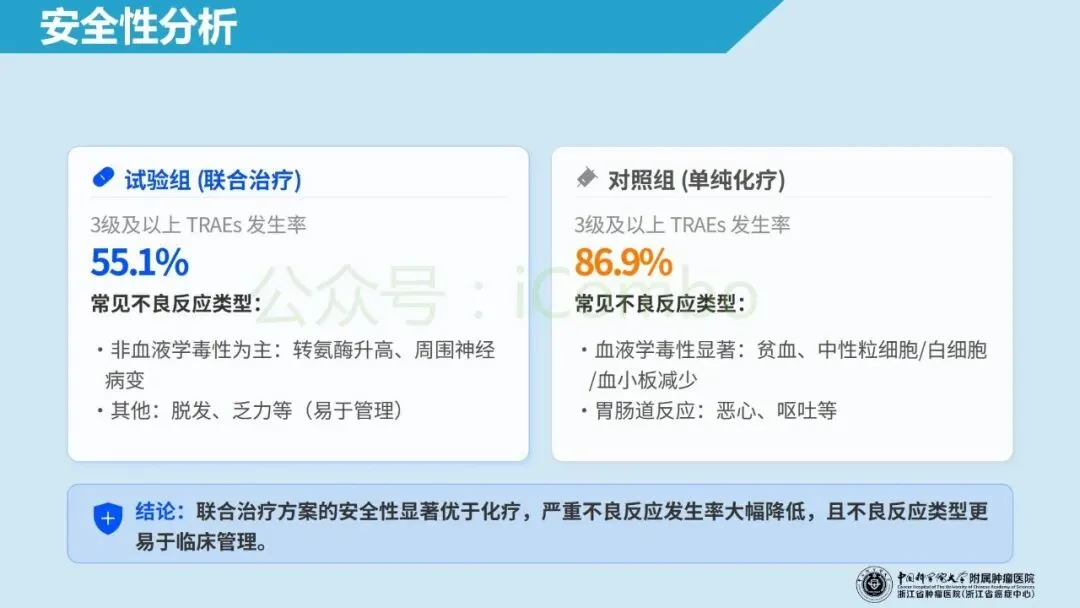
北京大学肿瘤医院郭军教授领导的RC48-C016 Ⅲ期多中心开放标签随机对照试验纳入 HER-2 表达(IHC 1+/2+/3+)的不可手术的局部晚期或转移性尿路上皮癌初治人群,1:1 分配至 维迪西妥单抗(disitamab vedotin 2.0 mg/kg)联合特瑞普利(toripalimab 3 mg/kg/2周)或吉西他滨联合顺铂/卡铂(每3周),双主要终点为盲态独立评审的无进展生存期(PFS)与总生存期(OS)。在中位随访 18.2 个月、共 484 例随机入组的预设分析中,联合组中位PFS为 13.1 个月(化疗组 6.5 个月;HR 0.36),中位OS为 31.5 个月(化疗组 16.9 个月;HR 0.54),均显著优于化疗;同时客观缓解率更高(76.1% vs 50.2%),且≥3级治疗相关不良事件比例更低(55.1% vs 86.9%)。这些结果支持将 HER-2 IHC 作为可落地的一线分层入口,并为“HER2-ADC + 免疫”在尿路上皮癌中的前移应用提供了强有力的循证依据。
至此,在国内尿路上皮癌一线的方案进入ADC联合免疫的年代,对于HER2表达阳性的患者可选用上述HER-2ADC联合免疫方案;Nectin-4 ADC联合免疫治疗是另外一个可选择方案;两种方案谁更优,尚不可得知,需要根据头对头研究结果来判断。可以猜想的是两种ADC的PAYLOAD类似,估计会存在交叉耐药现象;总之含铂化疗不再作为尿路上皮癌一线唯一的选择(N Engl J Med. 2025 Dec 11;393(23):2324-2337.doi: 10.1056/NEJMoa2511648)。









读书报告人:侯皓天
浙江省肿瘤医院 内科

编审:李婧婧、张晓实
版权声明:本平台旨在帮助医疗卫生专业人士更好地了解相关疾病领域最新进展。本平台对发布的资讯内容,并不代表同意其描述和观点,仅为提供更多信息。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。仅供医疗卫生专业人士为了解资讯使用,该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解资讯以外的目的,本平台及作者不承担相关责任。



