

扫描二维码
进入投稿专区
 刘凤林教授
刘凤林教授 陶凯教授
陶凯教授 李伟教授
李伟教授
余江教授
 徐皓教授
徐皓教授 陈杰教授
陈杰教授李双喜6 张健7 马志明8 王桂华9 高志冬10
李伟11 陶凯12 刘凤林1
通信作者:刘凤林 陶凯 李伟
陈杰、余江、徐皓对本文有同等贡献
1复旦大学附属肿瘤医院胃外二科,上海
2南方医科大学南方医院胃肠外科,广州
3南京医科大学第一附属医院胃外科,南京
4浙江省肿瘤医院胃外科,杭州
5西安交通大学第一附属医院普通外科,西安
6北京大学肿瘤医院胃肠肿瘤中心,北京
7浙江大学医学院附属第一医院胃肠外科,杭州
8吉林大学第二医院胃肠外科,长春
9华中科技大学同济医学院附属同济医院胃肠外科,武汉
10北京大学人民医院胃肠外科,北京
11吉林大学第一医院普通外科中心胃结直肠外科,长春
12山西省肿瘤医院胃肠外科,太原
摘 要
目的 探讨影响Ⅰ期胃癌患者根治术后预后因素及辅助化疗的应用价值。方法 采用多中心真实世界研究方法。收集2000年1月至2024年12月复旦大学附属肿瘤医院等全国12家医学中心收治的6366例Ⅰ期胃癌患者的临床病理资料;男4 612例,女1754例;年龄为60(21~91)岁;ⅠA期3936例,ⅠB期2 430例。患者均行根治性R0切除术。观察指标:(1)临床病理特征。(2)术后预后影响因素分析。(3)术后辅助化疗与预后的关系。计数资料组间比较采用χ²检验。结合临床公认影响预后的因素,将单因素分析中P<0.05的指标纳入多因素分析。单因素和多因素分析采用Cox风险回归模型。采用Kaplan‑Meier法计算生存率并绘制生存曲线,Log‑rank检验进行生存分析。结果 (1)临床病理特征:6366例患者中,<60岁、≥60岁分别为3139、3227例;T分期T1期、T2期分别为5491、875例,其中T1a期、T1b期分别为2735、2756例;肿瘤位于贲门胃底、胃体和(或)胃角、胃窦分别为1381、1318、3667例;肿瘤分化程度高分化、中分化、低分化分别为405、2859、3102例;淋巴结清扫范围D0、D1、D1+、D2分别为9、1476、2795、2086例;淋巴结清扫数目<16枚、≥16枚分别为528、5 838例;手术方式为近端胃大部切除术、远端胃大部切除术、全胃切除术、中段胃切除术分别为468、4778、1102、18例;脉管侵犯阴性、阳性分别为5355、1011例;神经侵犯阴性、阳性分别为5376、990例;癌胚抗原<5μg/L、≥5μg/L分别为5833、533例;CA19-9<37U/mL、≥37U/mL分别为6149、217例;未行术后辅助化疗、行术后辅助化疗分别为5888、478例,其中行术后辅助化疗患者T1N0M0期、T1N1M0期、T2N0M0期分别为181、153、144例。(2)术后预后影响因素分析:多因素分析结果示男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、手术方式为近端胃大部切除术、手术方式为远端胃大部切除术、脉管侵犯阳性、神经侵犯阳性、癌胚抗原≥5μg/L、CA19‑9≥37U/mL是影响Ⅰ期胃癌患者根治术后10年无病生存期的独立危险因素(风险比=1.599、2.507、1.713、0.576、1.585、0.724、1.653、0.657、1.504、1.628,95%可信区间为1.194~2.142、1.973~3.186、1.268~2.313、0.438~0.757、1.107~2.271、0.545~0.963、1.232~2.217、0.470~0.919、1.094~2.068、1.040~2.549,P<0.05)。男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、手术方式为近端胃大部切除术、手术方式为远端胃大部切除术、脉管侵犯阳性、CA19‑9≥37U/mL是Ⅰ期胃癌患者根治术后10年总生存期的独立危险因素(风险比=1.483、4.010、1.366、0.761、1.630、1.316、1.376、1.560,95%可信区间为1.186~1.853、3.255~4.940、1.051~1.776、0.597~0.970、1.154~2.302、1.018~1.702、1.086~1.744、1.069~2.278,P<0.05);术后辅助化疗是Ⅰ期胃癌患者根治术后10年总生存期的独立保护因素(风险比=0.559,95%可信区间为0.358~0.874,P<0.05)。(3)术后辅助化疗与预后的关系:术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为91.0%、90.9%,10年总生存率分别为90.2%、86.3%,两者10年无病生存率比较,差异无统计学意义(χ²=0.015,P>0.05);两者10年总生存率比较,差异有统计学意义(χ²=6.691,P<0.05)。T1N0M0期、T1N1M0期、T2N0M0期术后行辅助化疗患者10年无病生存率分别为87.3%、92.8%、95.6%,10年总生存率分别为88.8%、88.7%、95.0%,3者上述指标比较,差异均无统计学意义(P>0.05)。T1N0M0期、T1N1M0期、T2N0M0期术后未行辅助化疗患者10年无病生存率分别为92.4%、91.1%、82.3%,10年总生存率分别为87.2%、89.0%、78.5%,3者上述指标比较,差异均有统计学意义(P<0.05)。结论 男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、脉管侵犯阳性、CA19‑9≥37U/mL是影响Ⅰ期胃癌根治术后预后的独立危险因素,术后辅助化疗是术后10年总生存期的独立保护因素。与T1N1M0比较,T2N0M0期患者复发及生存风险较高,术后辅助化疗更能使其生存获益。
关 键 词
胃癌是全世界常见恶性肿瘤。早诊策略让Ⅰ期胃癌患者比例逐年增加,根治性手术是其首选治疗方案[1]。Ⅰ期胃癌约有10%的肿瘤复发率,这在大规模人群中构成显著的健康负担[2‑3]。已有研究结果显示:年龄、性别、肿瘤分化程度、脉管和神经侵犯等因素的风险权重结论不一,辅助化疗在Ⅰ期胃癌中的应用价值也未达成共识[4‑8]。精准锁定高危因素并行个体化干预,是其疗效突破的关键。本研究回顾性分析2000年1月至2024年12月全国12家医学中心收治的6366例(复旦大学附属肿瘤医院2548例、山西省肿瘤医院1044例、吉林大学第一医院851例、南方医科大学南方医院475例、南京医科大学第一附属医院428例、浙江省肿瘤医院332例、西安交通大学第一附属医院238例、北京大学肿瘤医院174例、浙江大学医学院附属第一医院118例、吉林大学第二医院90例、华中科技大学同济医学院附属同济医院52例、北京大学人民医院16例)Ⅰ期胃癌患者的临床病理资料,探讨影响患者根治术后预后因素及辅助化疗的应用价值。
资料与方法
一、一般资料
采用多中心真实世界研究方法。收集6 366例Ⅰ期胃癌患者的临床病理资料;男4612例,女1754例;年龄为60(21~91)岁;ⅠA期3936例,ⅠB期2430例。患者均行根治性R0切除术。本研究通过复旦大学附属肿瘤医院医学伦理委员会审批,批号为050432-4-1911D。免除患者知情同意。
二、纳入标准和排除标准
纳入标准:(1)病理学检查证实为Ⅰ期胃癌(T1N0M0期、T1N1M0期和T2N0M0期)。(2)行根治性切除术。(3)病理学检查证实为R0切除。
排除标准:(1)临床或病理资料不完整。(2)接受新辅助治疗。(3)有其他恶性肿瘤病史或合并其他恶性肿瘤。(4)随访或生存时间<3个月。
三、治疗方法
根据各医学中心及患者情况(尤其是脉管侵犯阳性、神经侵犯阳性、低组织学分级、区域淋巴结转移或微小残留病灶阳性患者)给予术后辅助化疗,治疗方案主要为替吉奥单药治疗,少数患者使用SOX方案(替吉奥+奥沙利铂)或FOLFOX方案(奥沙利铂+氟尿嘧啶+亚叶酸钙)。
四、观察指标和评价标准
观察指标:(1)临床病理特征。(2)术后预后影响因素分析。(3)术后辅助化疗与预后的关系。
评价标准:N1分期根据转移淋巴结的数目分为Ln1(1枚)和Ln2(2枚)。无病生存期定义为从手术日期到局部复发或出现任何远处转移日期的时间。总生存期定义为从手术日期至因任何原因死亡的日期或末次随访日期的时间。
五、统计学分析
应用R(版本4.4.1)统计软件进行分析。偏态分布的计量资料以M(范围)表示。计数资料以绝对数表示,组间比较采用χ2检验。结合临床公认影响预后的因素,将单因素分析中P<0.05的指标纳入多因素分析。单因素和多因素分析采用Cox风险回归模型。采用Kaplan‑Meier法计算生存率并绘制生存曲线,Log-rank检验进行生存分析。P<0.05为差异有统计学意义。
结 果
一、临床病理特征
6366例患者中,<60岁、≥60岁分别为3139、3227例;T分期T1期、T2期分别为5491、875例,其中T1a期、T1b期分别为2735、2 756例;肿瘤位于贲门胃底、胃体和(或)胃角、胃窦分别为1381、1318、3667例;肿瘤分化程度高分化、中分化、低分化分别为405、2859、3102例;淋巴结清扫范围D0、D1、D1+、D2分别为9、1476、2795、2086例;淋巴结清扫数目<16枚、≥16枚分别为528、5838例;手术方式为近端胃大部切除术、远端胃大部切除术、全胃切除术、中段胃切除术分别为468、4778、1102、18例;脉管侵犯阴性、阳性分别为5355、1011例;神经侵犯阴性、阳性分别为5376、990例;CEA<5μg/L、≥5μg/L分别为5833、533例;CA19-9<37U/mL、≥37U/mL分别为6149、217例;未行术后辅助化疗、行术后辅助化疗分别为5888、478例,其中行术后辅助化疗患者T1N0M0期、T1N1M0期、T2N0M0期分别为181、153、144例。
二、术后预后影响因素分析
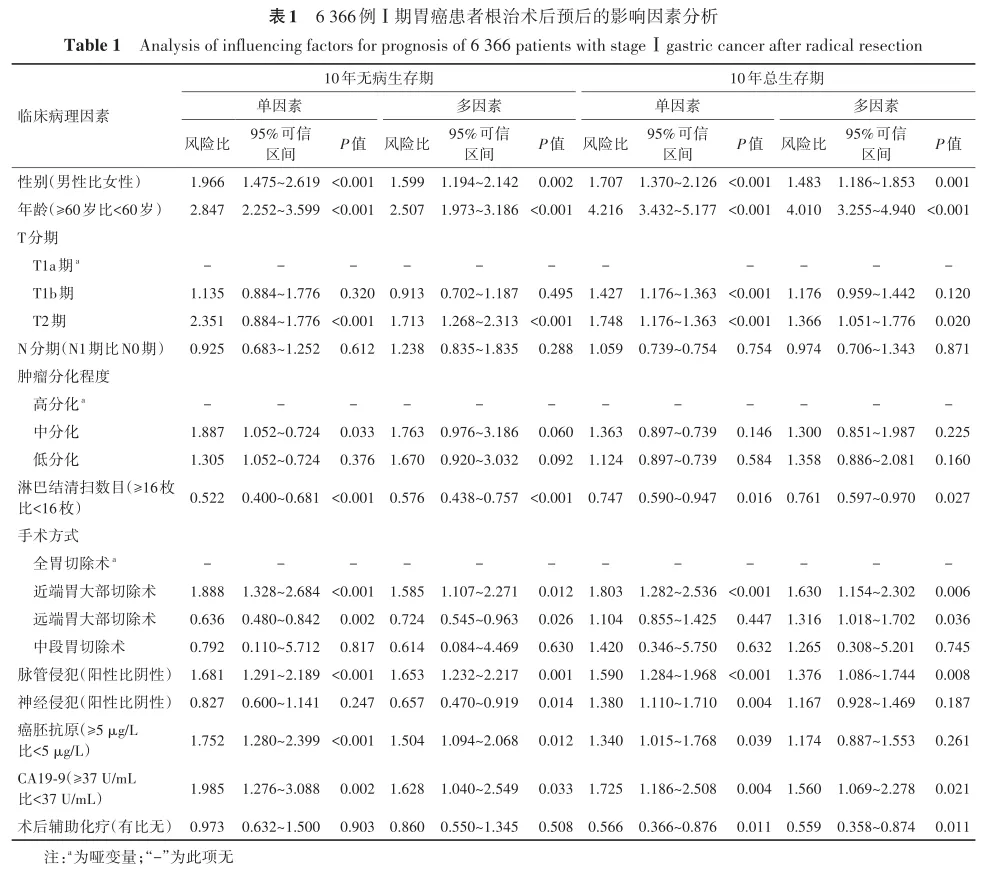
单因素分析结果显示:性别、年龄、T分期、淋巴结清扫数目、手术方式、脉管侵犯、CEA、CA19‑9是影响Ⅰ期胃癌患者根治术后10年无病生存期和总生存期的相关因素(P<0.05);肿瘤分化程度是影响Ⅰ期胃癌患者根治术后10年无病生存期的相关因素(P<0.05),但不是影响术后10年总生存期的相关因素(P>0.05);神经侵犯、术后辅助化疗不是影响Ⅰ期胃癌患者根治术后10年无病生存期的相关因素(P>0.05),是影响术后10年总生存期的相关因素(P<0.05)。N分期均不是影响Ⅰ期胃癌患者根治术后10年无病生存期和总生存期的相关因素(P>0.05)。见表1。
多因素分析结果显示:男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、手术方式为近端胃大部切除术、手术方式为远端胃大部切除术、脉管侵犯阳性、神经侵犯阳性、CEA≥5μg/L、CA19-9≥37U/mL是影响Ⅰ期胃癌患者根治术后10年无病生存期的独立危险因素(P<0.05);男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、手术方式为近端胃大部切除术、手术方式为远端胃大部切除术、脉管侵犯阳性、CA19‑9≥37U/mL是Ⅰ期胃癌患者根治术后10年总生存期的独立危险因素(P<0.05);术后辅助化疗是Ⅰ期胃癌患者术后10年总生存期的独立保护因素(P<0.05)。见表1。
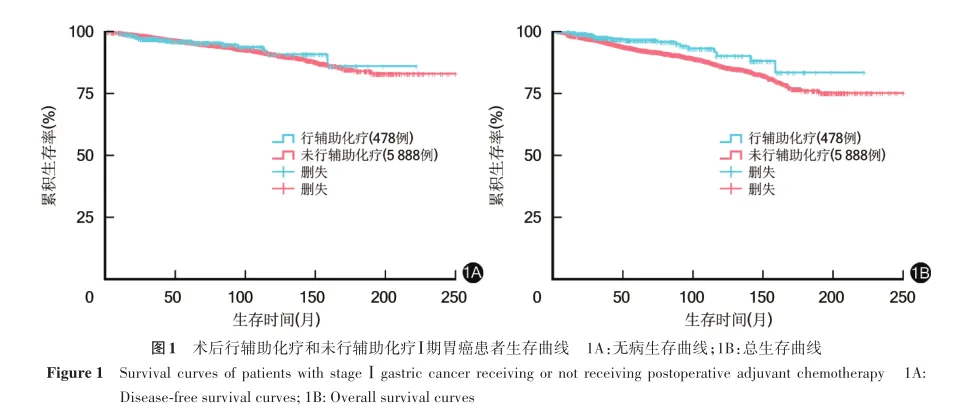
三、术后辅助化疗与预后的关系
术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为91.0%、90.9%,10年总生存率分别为90.2%、86.3%,两者10年无病生存率比较,差异无统计学意义(χ2=0.015,P=0.903);两者10年总生存率比较,差异有统计学意义(χ2=6.691,P=0.009)。见图1。
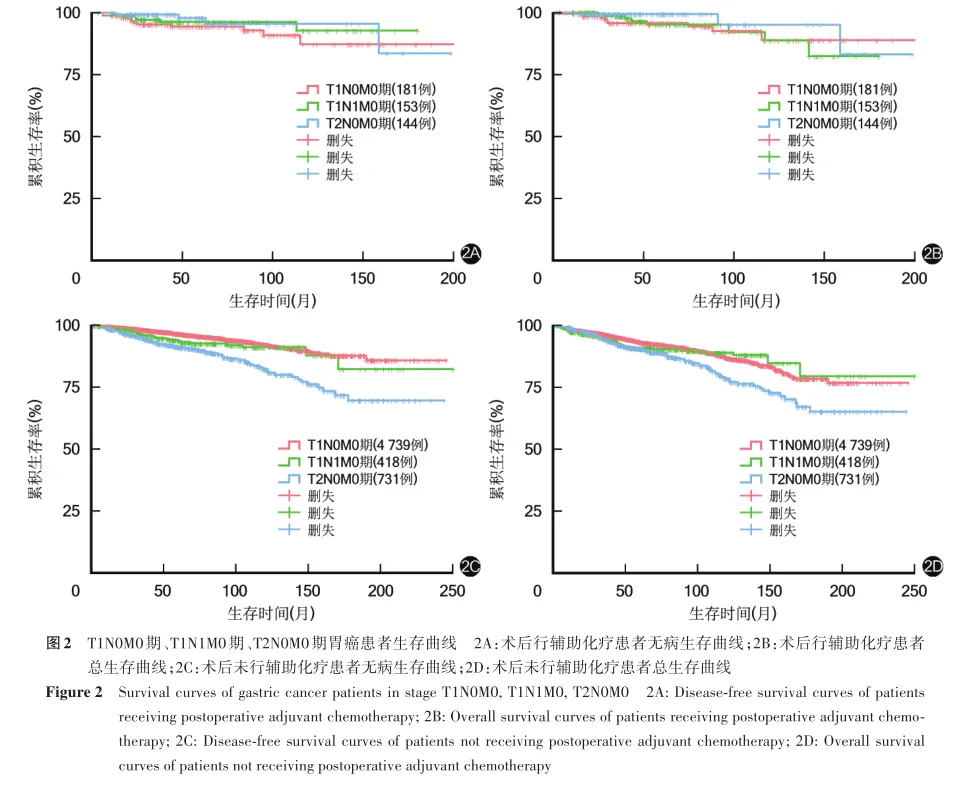
T1N0M0期、T1N1M0期、T2N0M0期术后行辅助化疗患者10年无病生存率分别为87.3%、92.8%、95.6%,10年总生存率分别为88.8%、88.7%、95.0%,3者上述指标比较,差异均无统计学意义(χ2=2.110,1.684,P=0.348,0.431)。T1N0M0期、T1N1M0期、T2N0M0期术后未行辅助化疗患者10年无病生存率分别为92.4%、91.1%、82.3%,10年总生存率分别为87.2%、89.0%、78.5%,3者上述指标比较,差异均有统计学意义(χ2=53.858,16.463,P<0.001,<0.001)。见图2。
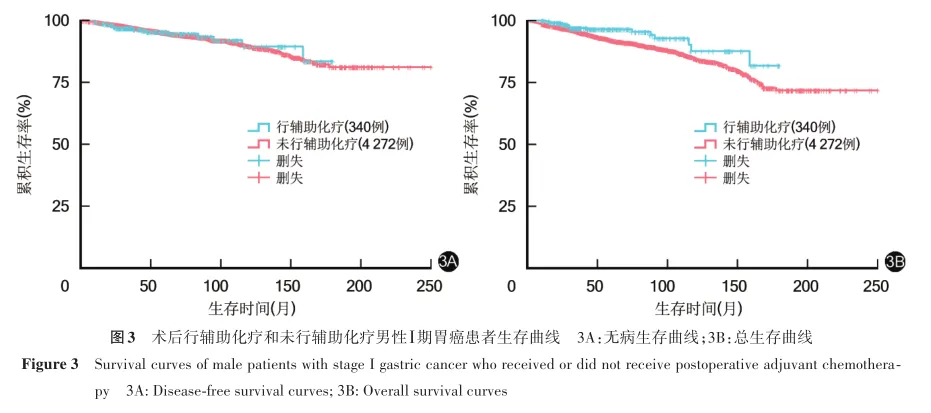
进一步分析,男性患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为89.5%、89.9%,10年总生存率分别为87.7%、84.8%,两者10年无病生存率比较,差异无统计学意义(χ2=0.001,P=0.977),10年总生存率比较,差异有统计学意义(χ2=5.619,P=0.018)。见图3。
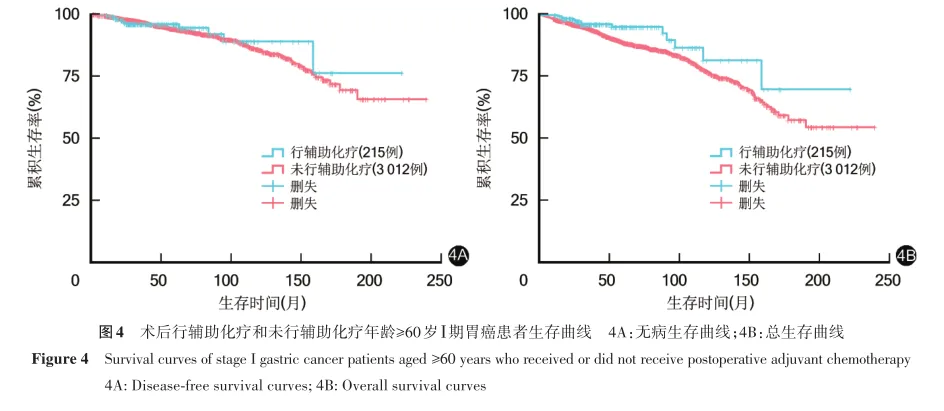
年龄≥60岁患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为89.0%、85.9%,10年总生存率分别为81.3%、77.0%,两者10年无病生存率比较,差异无统计学意义(χ2=0.164,P=0.686);两者10年总生存率比较,差异有统计学意义(χ2=4.393,P=0.036)。见图4。
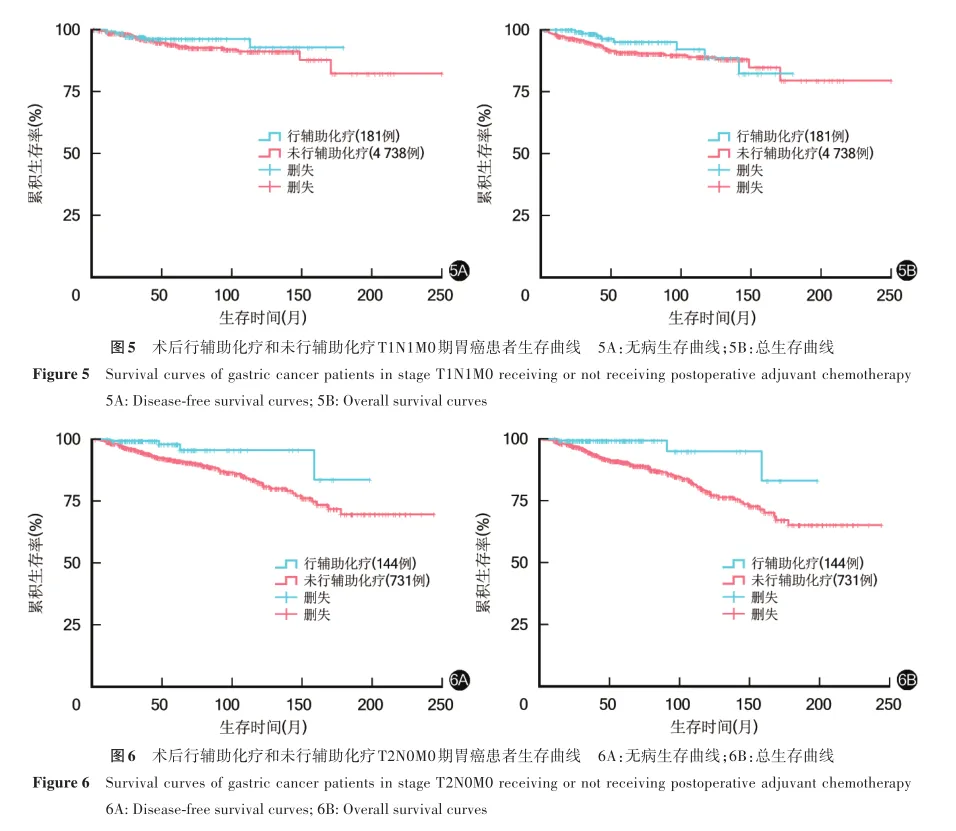
T1N1M0期患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为92.8%、91.2%,10年总生存率分别为88.7%、89.0%,两者上述指标比较,差异均无统计学意义(χ2=0.741,1.260,P=0.389,0.264)。见图5。T2N0M0期患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为95.6%、82.3%,10年总生存率分别为95.0%、78.5%,两者上述指标比较,差异均有统计学意义(χ2=5.608,8.469,P=0.018,0.004)。见图6。
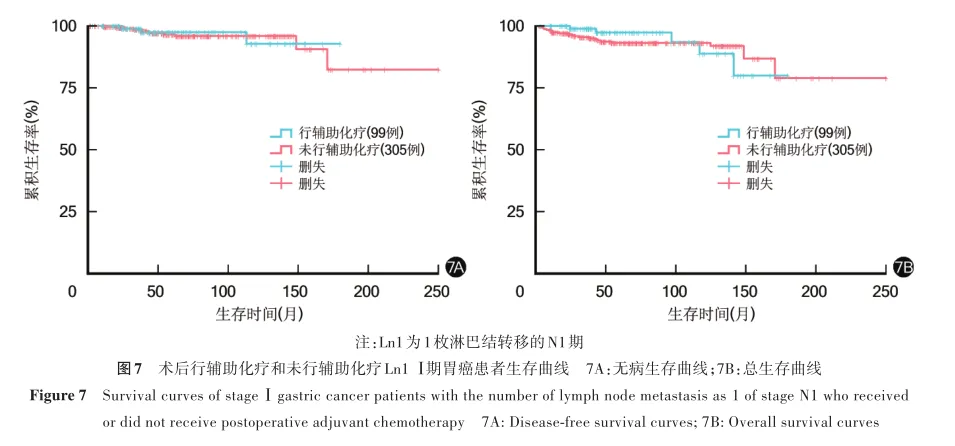
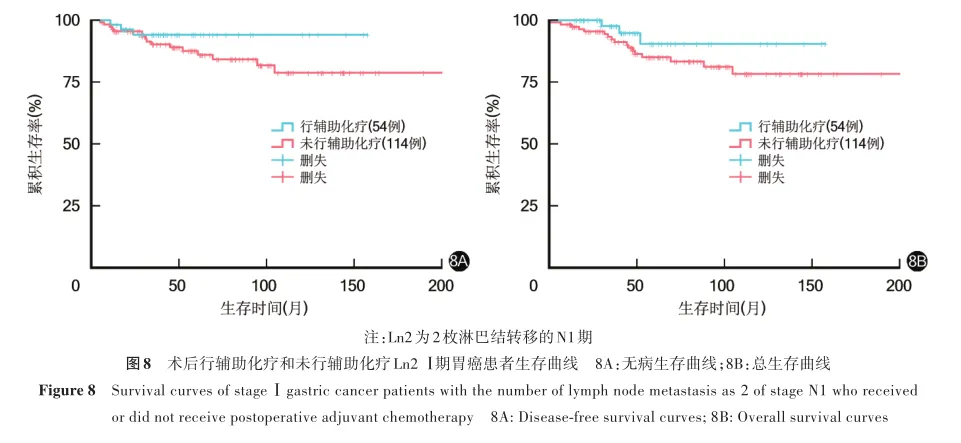
Ln1、Ln2患者10年无病生存率分别为91.3%、92.0%,10年总生存率分别为94.4%、80.0%;两者上述指标比较,差异均无统计学意义(χ2=3.337,2.784,P=0.068,0.095)。其中Ln1患者术后行辅助化疗、未行辅助化疗10年无病生存率分别为92.8%、95.9%,10年总生存率分别为88.8%、93.1%,两者上述指标比较,差异均无统计学意义(χ2=0.006,0.187,P=0.665,0.926)。见图7。Ln2患者术后行辅助化疗、未行辅助化疗10年无病生存率分别为94.1%、78.8%,10年总生存率分别为90.4%、78.3%;两者上述指标比较,差异均无统计学意义(χ2=1.650,1.709,P=0.199,0.191)。见图8。
淋巴结清扫数目<16枚的患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为100.0%、85.8%,10年总生存率分别为100.0%、83.2%,两者上述指标比较,差异均无统计学意义(χ2=1.219,1.649,P=0.270,0.199)。见图9。
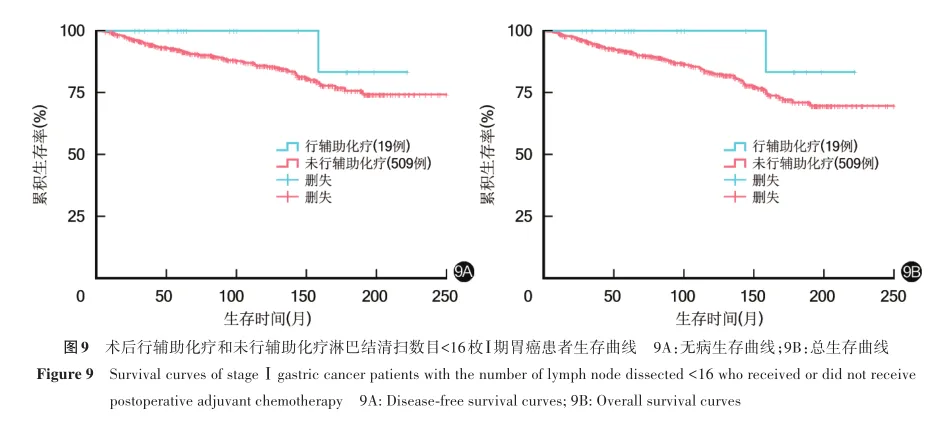
脉管侵犯阳性患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为86.8%、86.3%,10年总生存率分别为91.6%、80.4%,两者10年无病生存率比较,差异无统计学意义(χ2=2.119,P=0.145),两者10年总生存率比较,差异有统计学意义(χ2=18.465,P=0.007)。见图10。
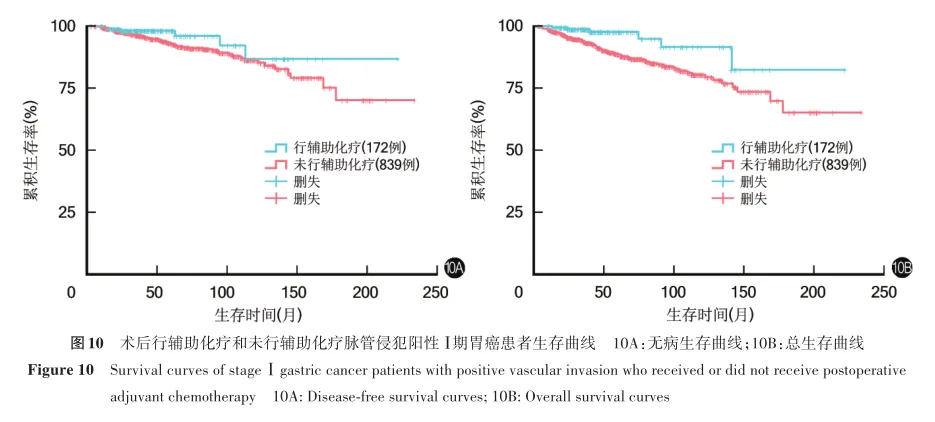
神经侵犯阳性患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为95.8%、91.0%,10年总生存率分别为100.0%、84.5%,两者10年无病生存率比较,差异无统计学意义(χ2=3.250,P=0.071),两者10年总生存率比较,差异有统计学意义(χ2=13.473,P<0.001)。见图11。
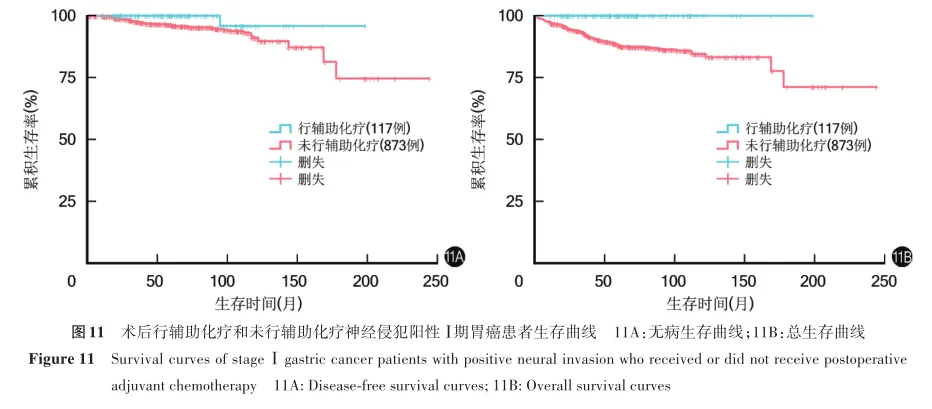
CEA≥5μg/L患者中,术后行辅助化疗与未行辅助化疗患者10年无病生存率分别为83.2%、85.6%,10年总生存率分别为82.2%、82.3%;两者上述指标比较,差异均无统计学意义(χ2=2.574,0.644,P=0.109,0.422)。见图12。
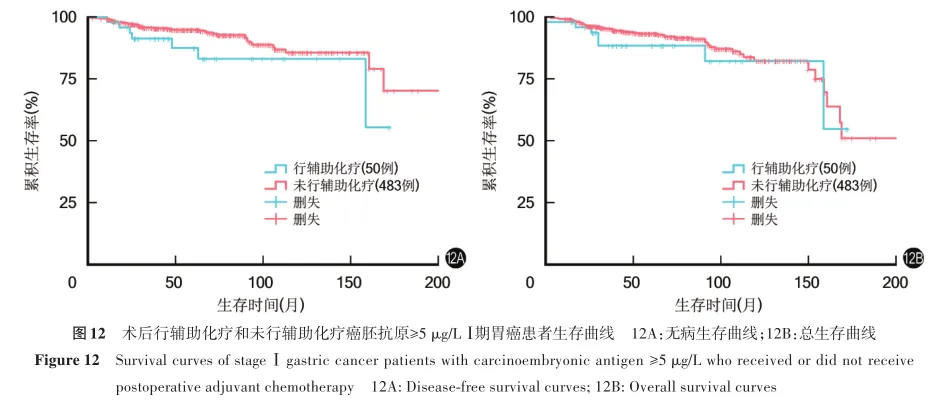
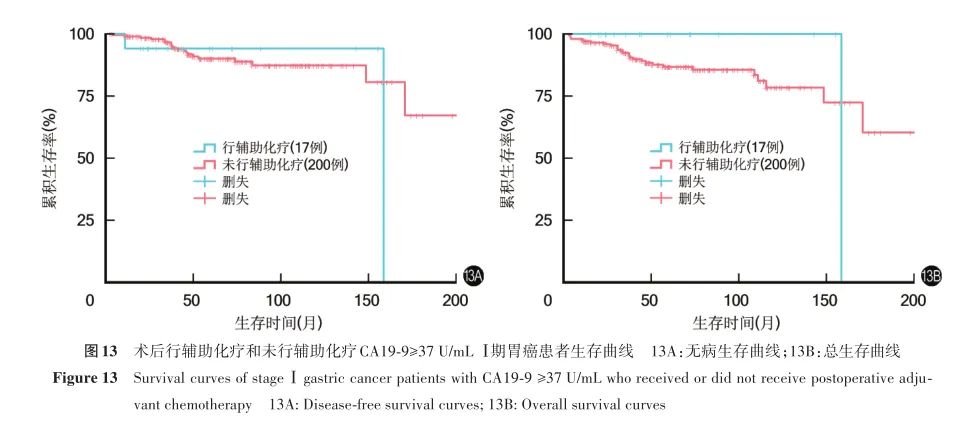
CA19-9≥37U/mL患者中,术后行辅助化疗、未行辅助化疗患者10年无病生存率分别为94.1%、87.3%,10年总生存率分别为100.0%、78.4%,两者上述指标比较,差异均无统计学意义(χ2=0.236,0.602,P=0.627,0.438)。见图13。
讨 论
本研究结果显示:Ⅰ期胃癌患者术后预后存在显著异质性,精准识别高危人群并给予个体化精准治疗十分重要。
多因素分析结果显示:男性、年龄≥60岁、淋巴结清扫数目<16枚、手术方式为近端和远端胃大部切除术、T分期为T2期、脉管侵犯阳性及CA19‑9≥37U/mL是影响Ⅰ期胃癌患者根治术后长期生存的独立危险因素。其中,男性患者预后较差,可能与男性有吸烟、饮酒等不良生活习惯,以及缺失雌激素有关,这与Sasazuki等[9]的研究结论一致。胃癌发病年龄也是有争议的预后因素[10-11]。有研究结果显示:发病年龄较年轻(<50岁)的胃癌患者通常预后较差[12]。这可能与病因学基础上较早发病的肿瘤更多由胚系或体系基因变异驱动,而非累积的环境风险所导致[13],使肿瘤倾向更强的恶性特征有关[14]。然而,有研究结果显示:高龄(≥60岁)是影响胃癌患者生存期的独立危险因素,主要机制可能与老年患者机体功能衰退、合并症较多,以及对治疗耐受性较差有关[15-16]。此外,年轻患者对于疾病的认知以及治疗积极性通常强于老年患者,有利于开展更合理、完善的术后管理。本研究作为大样本真实世界研究,其结果与韩国一项基于国家登记数据库的大规模研究相似[17]。该研究发现高龄是影响Ⅰ期胃癌患者预后的独立因素。因此,笔者认为:尽管年轻患者的肿瘤更具侵袭性,但其充沛的体能、更好的恢复与免疫潜能,以及对治疗更高的耐受阈值,共同奠定了接受标准胃癌根治术后仍获良好预后的内在基础。
未行辅助化疗Ⅰ期胃癌患者中,T2N0M0期患者表现出比T1N1M0期更差的预后,这与笔者前期研究结果一致[18]。其可能原因包括:(1)分期迁移。T2N0期患者若淋巴结清扫不充分,可能会遗漏淋巴结微转移,造成分期不准或被低估。Zhao等[19]的研究结果显示:淋巴结检出数目不足是Ⅰ期胃癌预后不良的重要预测因素,与本研究结果一致。(2)肿瘤生物学行为。T2期肿瘤穿透黏膜下层侵入固有肌层,其发生脉管侵犯和微转移的可能性更高。已有研究结果显示:肿瘤浸润深度是影响胃癌预后的独立指标,在特定情况下,T分期(T2期)比单纯的少数淋巴结转移(N1期)预测预后效能更佳[20‑22]。(3)治疗策略差异。淋巴结转移是早期胃癌复发转移的高危因素[23]。临床实践中,对于T1N1期患者,医师更倾向于推荐术后辅助化疗;而对于T2N0期患者,常被视为中低危患者而倾向于选择随访观察。
与全胃切除术比较,远端或近端胃大部切除术是影响患者10年无病生存期和总生存期的危险因素。这可能与选择偏倚相关,而非手术本身的优势。Jiang等[24]也报道了类似结果,并认为肿瘤部位是影响患者预后的独立因素,但需要在解读手术方式对预后的影响时审慎看待。当然,由于早期胃癌患者的异质性,全胃切除术的手术范围可能更好地覆盖了早期胃癌的微小浸润或转移病灶,从而降低了患者术后复发转移的风险。
对于辅助化疗价值,本研究结果显示:术后辅助化疗是10年总生存期的独立保护因素。进一步分层分析揭示了辅助化疗的获益人群存在明显差异。辅助化疗能显著提高T2N0M0期患者生存率;然而,在T1N1M0期患者中,术后辅助化疗并未带来生存获益。该反差提示:以淋巴结转移状态作为辅助化疗主要指征的策略在Ⅰ期胃癌中可能需要优化或调整。该发现与日本一项回顾性研究结果部分吻合,该研究提示T2N0期患者可能从辅助治疗中获益[25]。
基于以上发现,对于ⅠB期(T1N1M0期、T2N0M0期)胃癌患者术后是否需行辅助化疗的问题,笔者建议采取精细化分层决策。对于T2N0期患者,应积极推荐术后辅助化疗。对于T1N1期患者,则应综合评估其是否合并其他高危因素,对于无高危因素患者,或许可以选择更为谨慎的观察随访策略。
本研究的局限性:回顾性研究的选择偏倚和混杂因素影响,导致T分期、N分期单因素分析与多因素分析HR值不一致,无法判断上述指标是保护因素还是危险因素,不具备科学解释价值。辅助化疗的方案和周期未统一,可能对结果产生影响。未来需要开展前瞻性RCT,特别是针对T2N0期与T1N1期患者的辅助化疗价值进行深入探讨,从而进一步明确最佳治疗策略。
综上,Ⅰ期胃癌患者根治术后预后存在显著异质性。男性、年龄≥60岁、T分期为T2期、淋巴结清扫数目<16枚、脉管侵犯阳性及CA19‑9≥37U/mL是影响Ⅰ期胃癌根治术后预后的独立危险因素。术后辅助化疗能改善高危患者预后;与T1N1M0期比较,T2N0M0期患者复发及生存风险较高,术后辅助化疗更能使其生存获益。
利益冲突 作者声明不存在利益冲突
作者贡献声明陈杰:数据统计分析,论文撰写;徐志远、樊林、李双喜、张健、马志明、王桂华、高志冬、徐皓、余江、李伟、陶凯、刘凤林:研究方案制订,数据收集与整理;刘凤林:课题设计,论文审阅
志谢 中华消化外科菁英荟胃肠外科学组
撰文:刘凤林
供图:刘凤林
编辑:睢晓彤
审核:陈 敏




