
首先项目从小试过程到商业量产是需要经过多角度,多专业去团队协作,而且从战略层面确保产品能够稳定的实现量产。
今天的主题,就是让大家深度思考下,我们为什么要逐级放大,为什么不从小试完成后,直接进入商业批的批量(这里强调下,不是商业批,而是商业批的批量)。
本文总结内容比较长,建议收藏后反复阅读
写的不易,帮忙点赞关注我
1, 逐级放大一般的放大逻辑为:
1、根据团队经验放大:主要是凭借经验,已经不同的项目工艺本身来逐级放大。
2、项目相似放大:一般为应用相似性原理来进行逐级放大。但是,相似性放大适用于物理过程放大,而不适用化学过程放大,因为化学过程放大涉及放大效应。
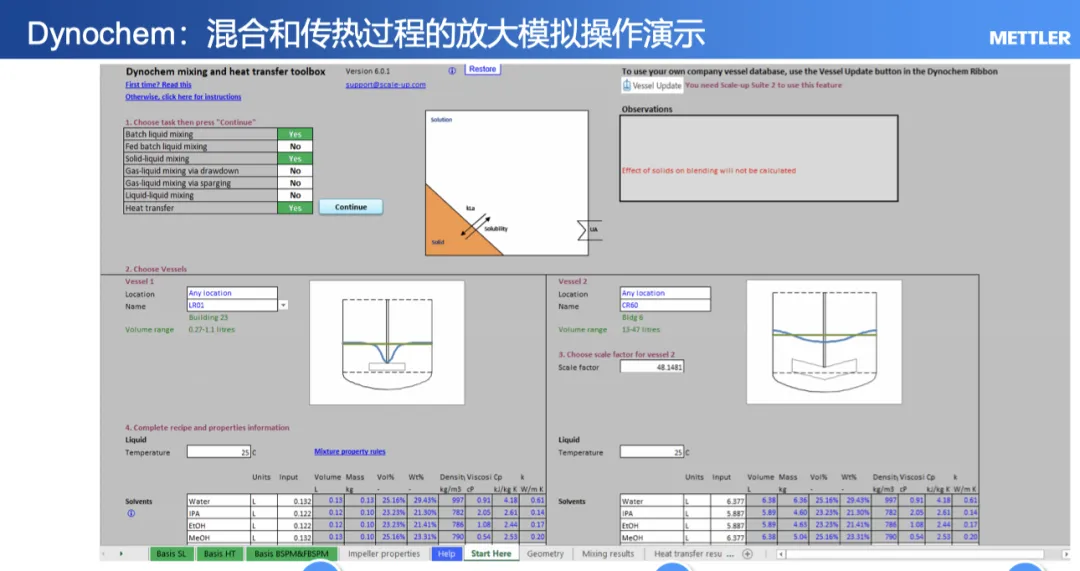
3、依托数学模拟放大:是应用电脑计算放大,通过专业的计算软件,进行模拟放大,例如Dynochem软件。此外,利用安全实验室的Optimax 设备来替代大型中间装置,为工业化装置提供精确的设计数据。其优点是费用低廉,工艺优化速度快。
2, 逐级放大常常需考虑的几个因素:
1、工艺路线和单元反应操作方法的最终确定。
2、设备材质和型号的选择。
3、搅拌器型式和搅拌速度的考察。
4、反应条件的进一步研究。
5、工艺流程和操作方法的确定。
6、进行物料衡算。
7、原材料,中间体的物理性质和化工常数的测定。8、原材料中间体质量标准的制订。
9、消耗定额,原材料成本,操作工时与生产周期等的确定。
10、从实验室研究至中试生产。
下面我从几个维度去考虑逐级放大的重要性
01
从质量角度来分析
不同法规体系(如中国NMPA、美国FDA、欧盟EMA等)对于药品生产从小试到中试,再到商业批的放大过程,都没有明确、统一地规定一个具体的数字倍数限制(例如“不得超过10倍”)。
法规的核心原则是 “质量源于设计” 和 “工艺一致性” ,而不是简单粗暴地限制放大倍数。规定的核心在于 “变更管理” 和 “工艺验证”,要求企业通过系统的研究和数据来证明放大后的工艺是稳定、可靠、并能持续生产出符合质量标准的药品。
虽然法规没有硬性数字规定,但行业内基于科学和风险控制,形成了一些普遍接受的实践共识:
1. 小试 → 中试 (工艺开发/转移阶段)
目的: 确定关键工艺参数,建立设计空间,生产用于毒理研究、临床试验的样品。
常见倍数: 放大倍数相对灵活,可能是10倍、50倍甚至更高。但关键在于,中试规模必须能够充分模拟商业生产的工艺条件。例如,如果商业生产使用干燥设备(例如双锥真空烘箱),中试阶段应使用原理相同的缩小型号,而不仅仅是平板真空烘箱。
核心要求: 设备相似性。关注混合效率、传热传质、干燥动力学等关键单元操作在规模变化时的表现。
2. 中试 → 商业批 (工艺验证/上市申报阶段)
目的: 证明工艺在商业化规模下的稳健性,完成工艺验证,生产稳定性考察批次和上市产品。
常见倍数: 通常不超过10倍。这是一个广泛遵循的行业惯例。更大的倍数会带来更高的不可预测性和风险。
核心要求:
工艺一致性: 商业批的工艺参数必须在中试确定的范围内。
设备原理相同: 商业生产设备应与中试设备在原理上一致(如都是双锥真空烘箱干燥,而非平板真空烘箱或鼓风烘箱)。
批量代表性: 用于稳定性研究的批次(通常为中试或小商业批)的批量,应能代表最终商业化批量的质量属性。中国NMPA通常要求申报批量(中试批)至少达到商业化批量的1/10。
02
从安全角度分析
与GMP法规类似,EHS(环境、健康与安全)法规体系通常也没有直接规定“从小试到中试/商业批的具体放大倍数”。
但是,EHS法规对生产规模变化有极其严格且明确的管控逻辑,其核心是 “基于风险的许可与监管” 。规模的放大,直接触发了不同级别、更严格的EHS合规要求。
以下是EHS法规在不同阶段的管控要点,其严格程度与生产规模/数量呈指数级增长关系:
一、 EHS法规的管控逻辑:基于规模的“阈值管理”
EHS法规通过设定一系列物理量阈值来触发不同的法律义务。放大过程最可能跨越这些阈值,从而引发合规体系的根本性改变。
环境法规:
核心法规: 《环境保护法》、《环境影响评价法》、《水污染防治法》、《大气污染防治法》、《固体废物污染环境防治法》等。
关键要求:
环评等级: 根据《建设项目环境影响评价分类管理名录》,项目的性质、规模和工艺决定是需要编制 “环境影响报告书” (最严)、“环境影响报告表”,还是只需“登记表”。小试在实验室层面可能豁免,但中试或商业化项目几乎必然需要完成正式环评审批。
污染物排放总量: 规模放大后,废水、废气、危废的预计排放量会增加。一旦超过地方环保部门核定的排放总量指标,项目将无法获批。
危险化学品临界量: 根据《危险化学品重大危险源辨识》标准,厂区内危险化学品的储存和使用量超过规定的临界量,即构成重大危险源,将面临最严格的安全监管(如定期安全评价、实时监控、应急准备等)。
职业健康与安全法规:
核心法规: 《安全生产法》、《职业病防治法》、《危险化学品安全管理条例》等。
关键要求:
安全设施“三同时”: 新建、改建、扩建项目(规模放大即属于此类)的安全设施必须与主体工程同时设计、同时施工、同时投入生产和使用,并需要通过安全审查。
职业病危害评价: 同样需要履行 “三同时” 手续。项目规模扩大,接触职业病危害因素(如粉尘、有机溶剂、活性药物成分)的员工数量和暴露水平可能变化,必须重新进行职业病危害预评价和控制效果评价。
03
从项目管理角度来分析
项目管理角度来看,中试放大不是一个单纯的“技术步骤”,而是一个高风险、高投入、多目标并行的关键决策关口。其重要性是逐级递增的,可以形象地比喻为项目从“纸上谈兵”到“真枪实弹”作战的 “战略枢纽” 和 “风险控制阀门”。
以下是基于项目管理经典维度(范围、进度、成本、风险、资源)分析的逐级重要性:
一、 各级重要性的具体内涵与管理要点
?技术可行性
这是放大最基本、最首要的重要性层级。项目在此阶段面临“猝死”风险。
工艺路线固化: 确认实验室路线在大规模设备上是否可行,发现并解决“实验室发现不了的问题”(如传热、传质效率差异等)。
关键工艺参数范围确认: 为商业化生产提供精确的操作窗口,这是后续工艺验证和质量控制的基础。
设备选型与适配性测试: 初步确认生产设备的型号、材质对工艺的适应性。
重要性体现:
决定项目是否继续: 如果中试放大失败,证明工艺不具备工业化条件,项目可能直接终止,避免后续更大损失。
产生核心数据资产: 生成用于IND或上市申请的关键批次的CMC数据资产。
?风险与管理
技术风险:
工艺放大风险: 通过质量风险管理工具系统评估。
质量风险: 确保中试产品与临床样品质量一致。
合规与EHS风险:
如前所述,规模放大触发新的环评、安评、职评要求。项目必须规划出足够的时间和预算来完成这些行政审批。
工艺安全数据在此阶段必须完善,以设计商业化的安全防护系统。
供应链与成本风险:
测试关键起始物料、中间体的大规模采购可行性、质量稳定性和成本。
初步核算“项目成本”,对项目的商业价值进行早期财务验证。
资源与进度风险:
中试需要跨部门协作,资源争夺激烈。项目经理需强力协调研发、生产、EHS、质量、工程等多部门。
中试延期将直接导致后续临床研究或上市申请的整体延期,时间成本极高。
?商业决策
这是放大过程的终极价值体现,直接决定产品的商业竞争力。
关键决策:
准确的商业生产成本模型: 基于中试的物料消耗、设备工时、能耗等数据,可以相对精确地预测商业化成本。这是决定产品定价、利润率和项目投资回报率的核心。
供应链可行性报告: 确认关键原料的供应商能否稳定供应商业批所需量,并符合质量与法规要求。
固定资产投资决策支持: 为商业生产车间的设计、设备采购和产能规划提供直接依据。错误的产能规划将导致巨大的资本浪费或产能瓶颈。
重要性体现:
决定“要不要建厂”或“建多大”: 是公司进行数百万乃至数亿元固定资产投资前的最后一道、也是最关键的实际验证。
决定项目的商业生命力: 即使技术成功,如果中试暴露出的成本过高或供应链不可靠,项目也可能在上市前被终止。
二、 项目管理视角下的核心策略
将中试放大设置为一个明确的点位 。只有当中试结果通过跨部门项目会,证明达到了预定的技术、EHS、成本目标后,项目才能获得批准和资源,进入下一阶段。
实施“集成项目团队”: 成立由研发、生产、工程、EHS、质量、供应链、BD共同组成的团队,确保所有维度的考量都被纳入放大计划。
强化风险管理: 从项目启动就建立中试放大的项目总计划跟踪表,并持续更新和应对。特别是对“进度杀手”(如因设备原因导致的延迟)和“成本杀手”(如关键参数影响了收率)进行重点监控。
数据驱动的决策: 一切决策(是否放大、放大到多少、下一步怎么走)都必须基于从中试中获得的数据,而非经验或猜测。
总结
GMP关注的是“产品品质的一致性”,而EHS关注的是“过程风险的可控性”。
GMP: 通过工艺验证和变更控制来保证质量,强调“可比性”。
EHS: 通过行政许可和工程控制来管理风险,强调“合规性”。
项目从小试到商业化量产,经过多角度去分析风险可控,从大到公司战略及小到部门实施都是要求我们必须逐级放大,这就是我们为什么要按以上这些控制来做项目的原因。
下期预告:
我们将深入探讨《中试完成后,怎么“流畅”过渡到商业化生产》,欢迎持续关注。
欢迎在评论区留言分享,你的真实案例可能就是下一篇专题的灵感来源。
关注我,每天好文章推送给您
未来计划:
关于中试的知识分享会按一整个系列写完。
下一个主题以《工厂管理》为核心,系统地分享工厂管理知识。
原料药放大与生产笔记 专注于原料药及中间体中试,生产,工厂管理,只谈干货,知识分享 贝克的猫



