一:微创外科的哲学演进与LECS的诞生逻辑
1.1从“切除中心论”到“功能保留论”的范式转移
在20世纪末,微创外科的核心逻辑是“小切口完成大手术”。然而,随着早期胃癌(EGC)和胃肠间质瘤(GIST)检出率的提高,外科医生面临一个新的悖论:为了切除一个几厘米的肿瘤,往往需要切除半个甚至整个胃。这种“过度治疗”严重影响了患者的术后生活质量
双镜联合手术(Laparoscopic and Endoscopic Cooperative Surgery, LECS)的诞生,本质上是外科微创化与内镜外科化在技术临界点的必然相遇。它标志着手术哲学从“解剖学切除”向“功能学重建”的深刻转变
1.2全球历史考证:Hiki教授的奠基与流派争鸣
世界首例(2006年):日本比木直树(Naoki Hiki)教授在2006年首次报道了利用腹腔镜与胃镜联合切除胃间质瘤。这一术式被称为“经典LECS”,其核心在于利用胃镜进行精确的黏膜下切开,再由腹腔镜完成浆肌层的切除
世界第一台双镜联合手术:
时间:2006年
术者:日本庆应义塾大学的HikiN教授团队
病例:一名胃粘膜下肿瘤(SMT)患者
效果:通过内镜确定切缘,腹腔镜完成切除与缝合,成功实现了胃壁的最小化切除,保留了胃的功能,患者术后恢复极快,无并发症
流派演进:
NEWS(Non-exposedEndoscopicWall-inversionSurgery):为了解决恶性肿瘤细胞腹腔种植风险,NEWS术式实现了“非暴露”切除
CLEAN-NET:进一步优化了切缘的精准度
EFTR(EndoscopicFull-thicknessResection):内镜全层切除术的出现,使得双镜联合的边界更加模糊,协作更加紧密
1.3中国历史考证:从追随到并跑
中国微创元年(1991年):云南曲靖医院完成了中国首例腹腔镜胆囊切除术。同年,郑民华教授将腹腔镜技术带回上海瑞金医院
中国第一台双镜联合手术:
时间:2000年代初期(约2004-2005年间)
代表人物:上海交通大学医学院附属瑞金医院郑民华教授团队
病例:胃间质瘤
效果:利用腹腔镜的视野优势与内镜的腔内定位优势,解决了早期胃间质瘤定位难、切除范围过大的痛点
LECS的引入(2005-2012年):中国首例针对胃肿瘤的LECS手术大约在2005年前后由上海、北京等地的顶级中心率先开展。这一时期,中国医生开始意识到,单纯的腹腔镜切除在处理贲门、幽门等“不利部位”肿瘤时存在巨大局限,内镜的介入提供了“上帝视角”
二:全球与中国LECS专家共识文献全景总结
通过对过去20年文献的系统梳理,LECS的标准化进程可分为三个阶段:
2.1奠基期(2006-2015):术式探索与安全性验证
核心文献:Laparoscopicandendoscopiccooperativesurgeryforgastrointestinalstromaltumorofthestomach. (2008),JapaneseGastricCancerTreatmentGuidelines(2014)
关键结论:验证了LECS在保留胃功能、缩短手术时间及减少并发症方面的显著优势,首次将LECS纳入胃肿瘤微创治疗规范
2.2规范期(2016-2023):适应症拓展与多学科协作
核心文献:日本《胃间质瘤诊疗指南》、中国《胃肠间质瘤规范化外科治疗专家共识》(2015),《腹腔镜联合内镜手术治疗胃肠道肿瘤中国专家共识》(2017),《早期胃癌双镜联合手术临床实践指南》(2021)
关键结论:中国首个针对LECS的系统性指导文件,细化了LECS在早期胃癌中的应用指征,明确了直径≤2cm及2-5cm胃GIST的微创治疗路径,LECS被正式列为推荐术式
2.3引领期(2024-2026):中国方案的崛起
2024年《中国胃肿瘤LECS临床应用专家共识》:由中华医学会外科学分会牵头,系统规范了经典LECS、NEWS、CLEAN-NET的操作流程,引入了机器人辅助与人工智能导航的最新进展
2025年《中国胃肠道肿瘤双镜联合手术临床实践指南(深圳)》:首次将区域性医疗协作经验上升为国家级指南
2026年《早期胃癌LECS-SNNS多学科实践共识》:探讨了前哨淋巴结导航(SNNS)与LECS的深度融合,标志着中国在精准微创领域开始引领全球,LECS进入“功能保全+精准分期”的新阶段
三:组织社会学复旦前50医院的领导架构与博弈
3.1“外科院⻓”与“内镜院⻓”的权⼒博弈
在三甲医院的行政架构中,双镜联合手术的推进往往面临“谁主导”的问题
外科主导型(如瑞⾦医院):在 院长宁光院士的指导下,普外科主任郑民华教授的领导下,瑞金医院在腹腔镜技术上具有天然的统治力。在这种模式下,内镜往往作为外科手术的“辅助工具”,外科内镜医生在术中提供定位支持
内镜主导型(如中⼭医院):院长周俭院士(肝外科专家)对内镜中心主任周平红教授的全力支持,创造了全球独一无二的“中山模式”。在这里,内镜中心拥有独立的手术室、⿇醉团队和病房,内镜医生不仅做诊断,更主导了大量的LECS手术
外科/内镜深度协作型(如仁济医院):在 院长夏强院士(肝移植专家)的指导下,胃肠外科张子臻主任、内镜中心李晓波主任的深度协作,实现了真正的MDT(多学科协作)
3.2上海地区标杆医院深度解剖
医院名称 | 整合模式 | 核⼼主任(外科/内镜) | 分⼯细节 | 年⼿术量 (LECS相关) |
复旦中⼭ | 内镜中心主导 | 周平红 | 内镜医生主导全层切除,外科医生辅助浆膜缝合,内镜外科化,技术难度极高 | 约800-1200例 |
上海瑞⾦ | 外科内镜一体化 | 郑⺠华 | 外科医生同时掌握两镜,实现“单人双镜”操作,微创外科引领,流程标准化 | 约600-900例 |
上海仁济 | 胃肠外科主导协作 | 张⼦臻 | 外科医生主导腹腔镜、机器人,外科内镜医生负责术中定位与黏膜切开,胃肠外科与消化内镜深度协同 | 约 600-1000例 |
核⼼主任画像:
周平红(中⼭):被誉为“大国工匠”,其内镜手术风格极其大胆且精准,打破了内外科的界限
郑⺠华(瑞⾦):中国腹腔镜的开拓者,强调手术的规范化与微创理念的普及
张⼦臻(仁济):中生代领军人物,擅长复杂胃肠肿瘤的微创处理,强调外科技术的精细化
四:技术融合前沿机器⼈与⼀次性内镜的“握⼿”
4.1⼿术机器⼈与内镜的底层协议集成
目前的LECS正在从“物理联合”向“数字融合”演进
机器⼈辅助LECS:达芬奇机器人的机械臂提供了超越人手的灵活性,特别是在处理胃后壁、贲门等死角时
画中画(PiP)技术:未来的趋势是内镜图像直接集成在机器人的主控台上,外科医生无需抬头看显⽰器,即可实现“虚实结合”的操作
4.2⼀次性胃肠镜在LECS中的战略价值
一次性内镜不仅是感控的产物,更是数字化⼿术室的⼊⼝
零周转时间:在复合手术室中,一次性内镜无需洗消,极大提升了手术室的周转效率
数据⼀致性:每一根一次性内镜的图像传感器都是全新的,保证了手术视频的高质量记录,为AI辅助诊断提供了标准化的数据源
五:院⻓级经济学精算⼀次性内镜的性价⽐临界点
5.1成本结构的深度拆解
作为医院管理者,必须从全⽣命周期成本(LCC)的角度评估设备投入
复⽤内镜系统(Olympus/Fujifilm):
CAPEX(初始投⼊):一套主机(350万)+2根镜子(80万)=430万
OPEX(运营成本):洗消液、人工、水电、维修保养(年均25万)
折旧与损耗:按5年折旧,单次手术分摊约1200元
感控⻛险成本:潜在的交叉感染赔偿风险(隐性成本)
⼀次性内镜系统:
CAPEX:移动便携式主机(50万)
OPEX:单次耗材单价(8000-10000元)
隐性收益:提升手术室周转率(单台手术节省洗消时间30-45分钟)
5.2经济学模型:年手术量与性价比的平衡点
基于上述数据,我们构建了以下模型:
总成本(TC)=CAPEX/5+(OPEX_per_case*N)+Maintenance
通过计算得出:
当N<1150例/年时,一次性内镜的总成本低于复用内镜
院长视角下的决策逻辑:对于绝大多数三甲医院的单一科室(如胃肠外科或内镜中心),年LECS手术量很难突破1000例。因此,采用一次性内镜是目前最具性价比的战略选择
5.3DRG/DIP支付政策下的边际贡献分析
在DRG支付体系下,手术耗材被视为成本而非利润
一次性内镜虽然增加了单次耗材费,但通过缩短住院天数和降低并发症率,可以显著提升医院在DRG分组下的结余。
六:未来专家共识构建与“上海方案”引领全球
6.1《一次性内镜在双镜联合手术中的应用专家共识》书写建议
未来共识应重点解决以下四个核心问题 :
1.技术准入标准:明确一次性内镜在LECS中的图像分辨率、操控性及耐用性要求
2.感控流程再造:制定一次性内镜在复合手术室中的“即插即用”标准操作流程
3.经济学评价体系:建立基于“卫生技术评估(HTA)”的成本效益评价模型
4.多学科协作机制:明确外科与内镜医生在一次性内镜操作中的职责边界
6.2“上海方案”:引领全球微创外科的战略路径
上海应利用其在高端医疗器械研发(如微创机器人、联影医疗)与顶级临床中心的双重优势,输出“机器人+一次性内镜+AI辅助”的整体解决方案
引领逻辑:从“术式创新”转向“标准输出”。通过制定国际指南,让全球医生学习“上海标准”,从而带动国产高端医疗器械的全球化
七:院长级整体解决方案建议
1.空间整合:建设“一站式微创介入中心”,打破物理隔阂
2.设备整合:配置“机器人+一次性内镜”的黄金组合,降低初始CAPEX压力
3.人才整合:建立“双栖医生”培养计划,打破学科壁垒
4.管理整合:建立跨学科的绩效分成机制,实现利益共享
双镜联合手术
腹腔镜与内镜联合技术(双镜联合技术)(laparoscopic and endoscopic cooperative surgery,LECS)是近年来新兴的微创外科技术。既往在单独应用腹腔镜进行手术时,由于缺乏精细的触觉,故而探查不易发现较小的病灶(瘤体直径小于2cm或2cm左右)。此外,由于腹腔镜器械的限制,探寻时更不易发现胃十二指肠后壁及腔内生长的肿瘤,从而易造成病灶切除的遗漏,并导致中转开腹手术。在这种情况下,术中胃镜对病灶进行定位,对于保障腹腔镜手术的顺利进行显得尤为必要
另外,对于胃镜检查下发现的GIST病灶,由于其多起源于固有肌层,单纯在胃镜下处理风险较大,手术时间又较长。腹腔镜的存在可以协助内镜操作,及时发现并处理内镜下切除的并发症,增加手术安全性和效率。可以说,双镜联合技术充分发挥了腹腔镜和内镜各自的优势,取长补短,弥补了单独应用腹腔镜或内镜的不足,进一步拓展了微创外科技术的应用范围
【病例摘要】
患者,女性,41岁,2018年7月进食油腻食物后出现腹胀,伴恶心,无呕吐、头晕、头痛、乏力、黑矇。咳少量白色痰,无咯血、胸痛、胸闷等症状。患者平素高盐饮食。遂于当地医院就诊,2018年8月10日胃镜示萎缩性胃炎,胃体局部隆起(黏膜下病变,建议超声内镜检查),胃窦息肉样变。胃黏膜活检病理示胃窦慢性非萎缩性胃炎(急性活动期),HP(+)
外院予抗HP治疗,2周后患者自觉症状缓解。为求进一步治疗,患者前往上海交通大学医学院附属仁济医院就诊。2018年8月20日超声胃镜示胃GIST可能。2018年8月25日胃增强CT示胃体小弯侧占位,倾向于黏膜下来源,考虑GIST可能大;肝脏多发微小囊肿,胆囊腺肌症。扫及两侧胸腔少量积液。患者自起病以来,大便正常,睡眠饮食可,体重1个月内下降2.5kg
既往史及家族史
既往体健,否认药物过敏史;父母健在,家族中无类似病史
体格检查
生命体征平稳,皮肤黏膜无黄染、无苍白。腹部平坦,未见胃肠型及蠕动波。腹软,无压痛、反跳痛,无腹部包块,无肌紧张;肠鸣音正常
辅助检查
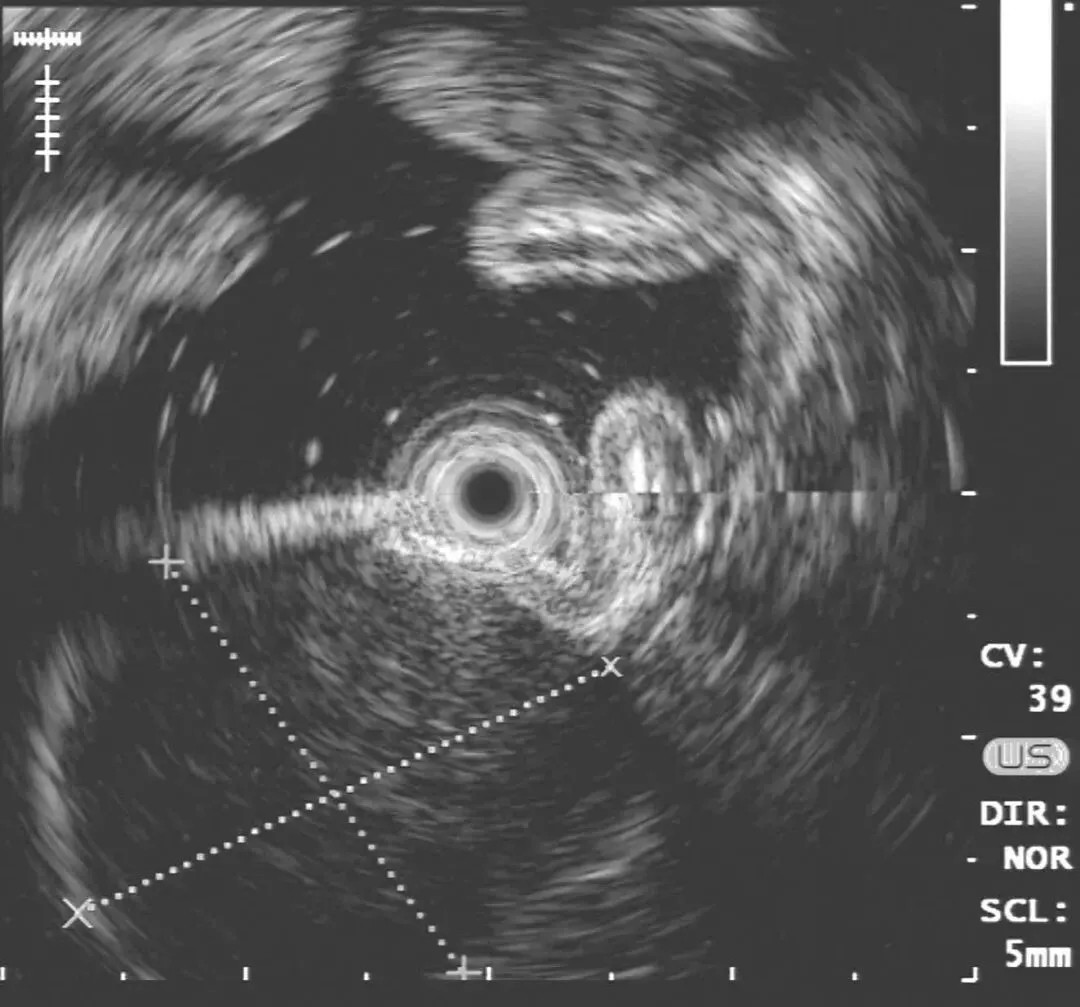
超声胃镜:胃体上段后壁可见一隆起病灶,隆起处为一低回声团块,内回声尚均匀,起源于第四层,向腔内外突出(图2-1)
胃增强CT:胃体小弯侧占位,CT表现倾向于黏膜下来源,考虑GIST可能大,建议结合内镜及病理结果。肝脏多发微小囊肿。胆囊腺肌症。扫及两侧胸腔少量积液(图2-2)
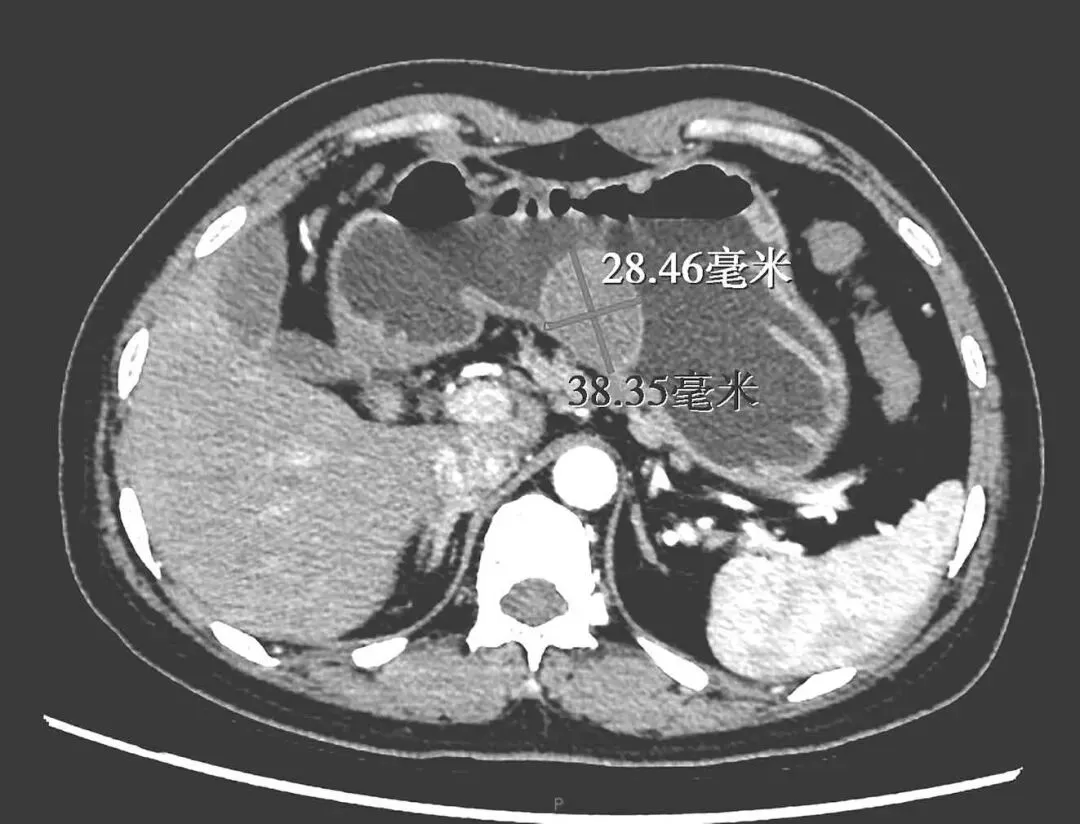
2-2 CT提示胃体小弯侧占位
初步诊断
【治疗过程】
(一)病例分析
(二)治疗方案
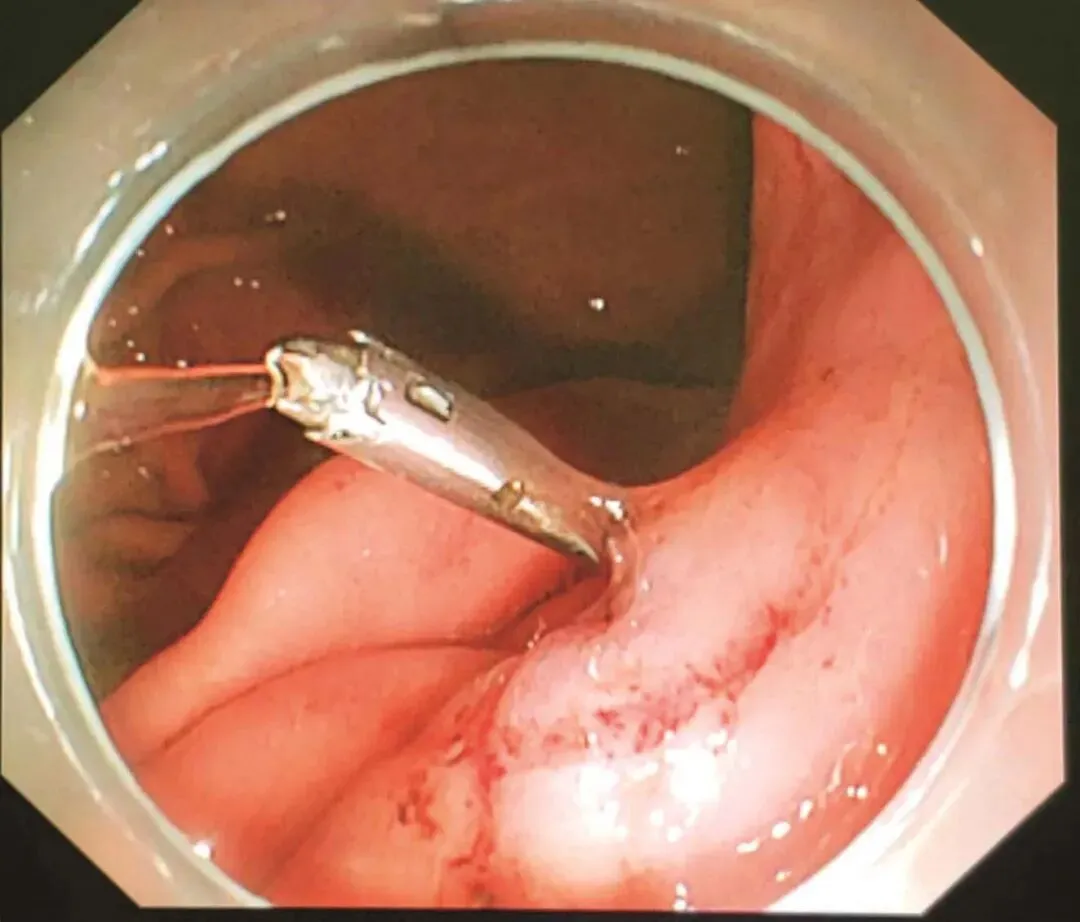
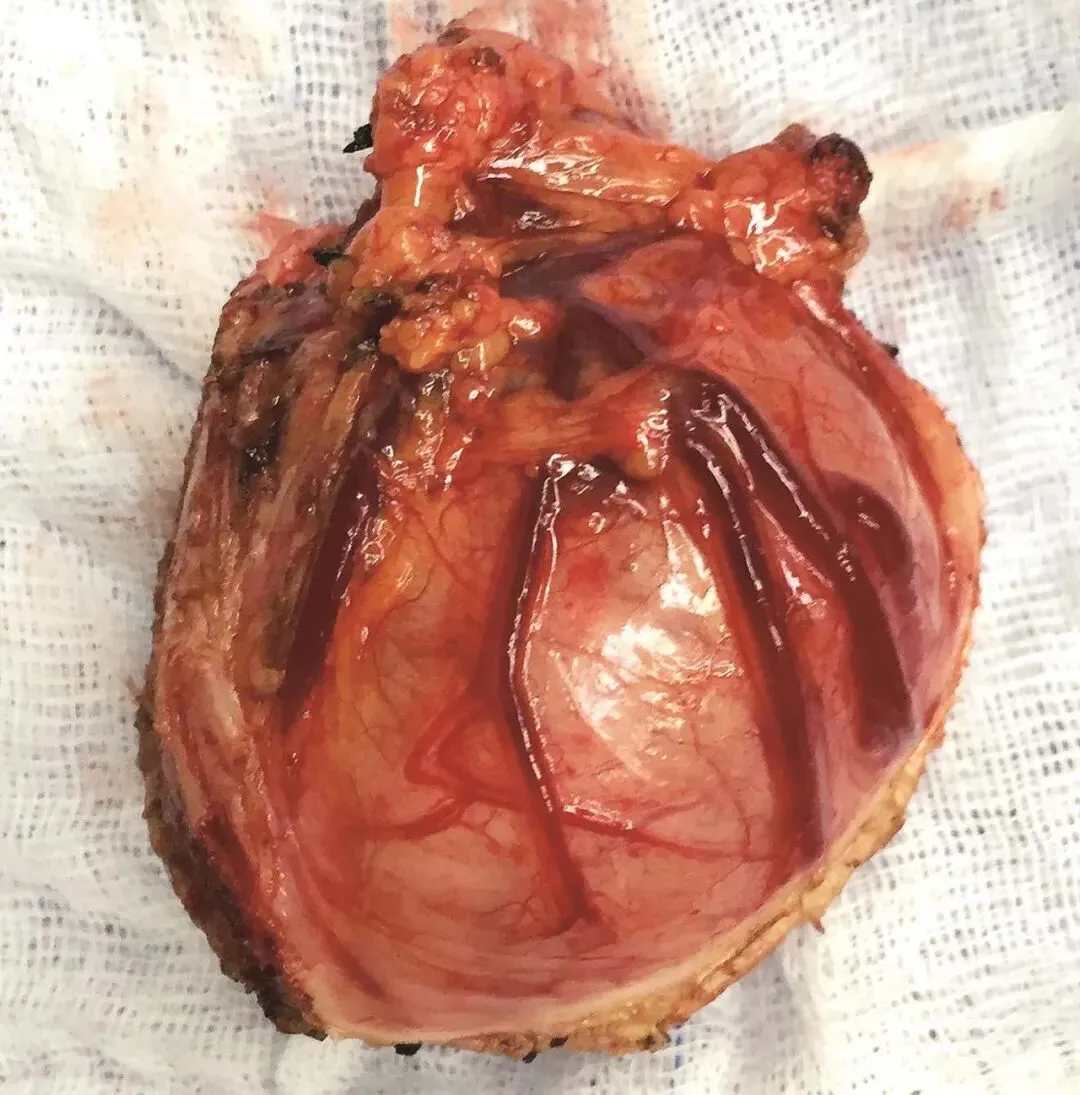
患者于2018年08月30日在笔者单位接受“腹腔镜+胃镜双镜联合胃肿瘤切除术”,胃肠外科与消化科医师共同上台。术中内镜见胃体小弯侧后壁直径4cm黏膜下肿瘤,腔内生长,未侵犯胃黏膜及浆膜(图2-3),胃周淋巴结无肿大,小网膜囊内可及直径1cm钙化脂肪结节一枚,肝脏、盆腔、腹膜未及转移灶。经口置入内镜,探查肿瘤,于肿瘤边缘黏膜下注水(图2-4);内镜指引下,腹腔镜下以超声刀距肿瘤边缘1cm切开胃壁浆膜,沿肿瘤包膜外,全层切开胃壁,完整切除肿瘤(图2-5);以3-0可吸收线间断全层缝合胃壁缺损;术中胃镜检查胃创面;创面部分黏膜缺损处内镜下以钛夹封闭(图2-6);肿瘤标本置于标本袋内,经脐部戳孔处取出(图2-7)
(三)术后病理及基因检测
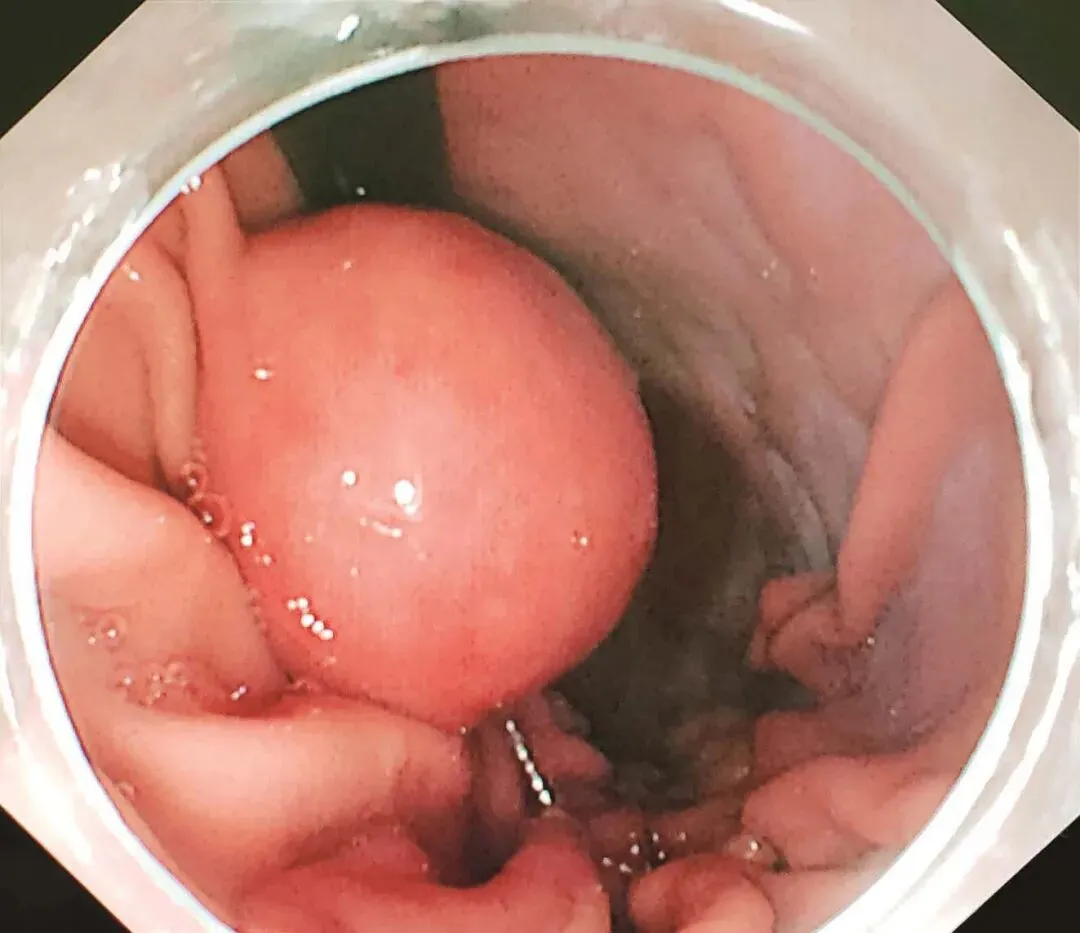
图2-3 术中内镜探查肿瘤
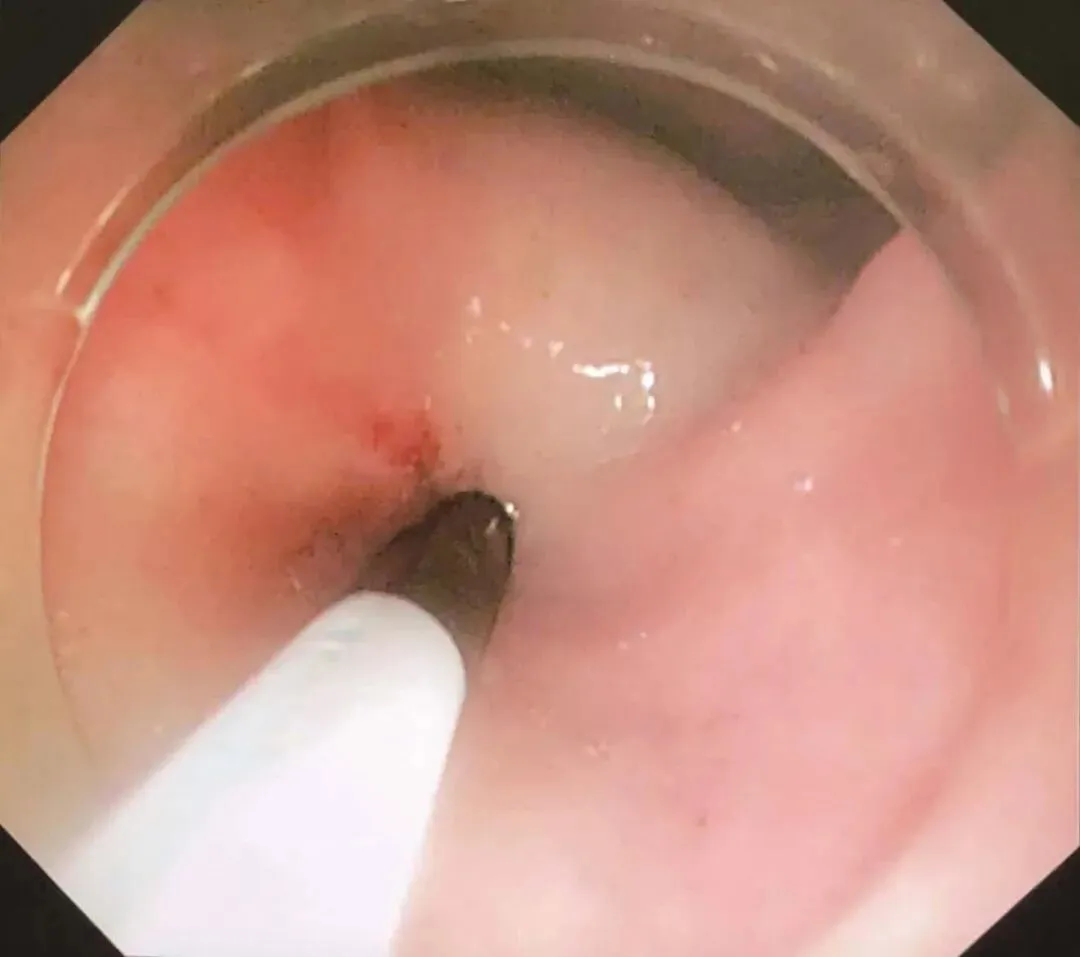
图2-4 术中内镜下于肿瘤边缘黏膜下注水
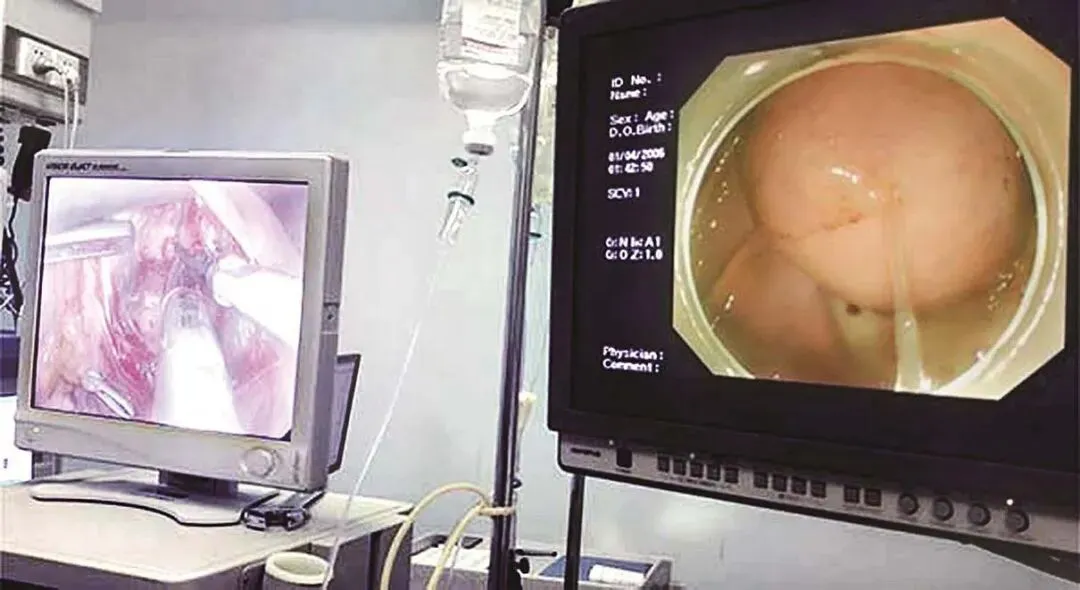
图2-5 术中内镜监视下由外科医师完成腹腔镜下肿瘤切除