XENE系列2:K通道药物与癫痫治疗
K离子通道激动剂——打开新大门的"钥匙"
2026年3月|非投资建议,仅供参考
?一句话看懂癫痫
癫痫(俗称"羊癫疯")的本质,是大脑神经元突然"短路放电"——兴奋性神经递质(谷氨酸)踩死油门,抑制性神经递质(GABA)刹车失灵,神经元群体性失控放电,引发反复发作。
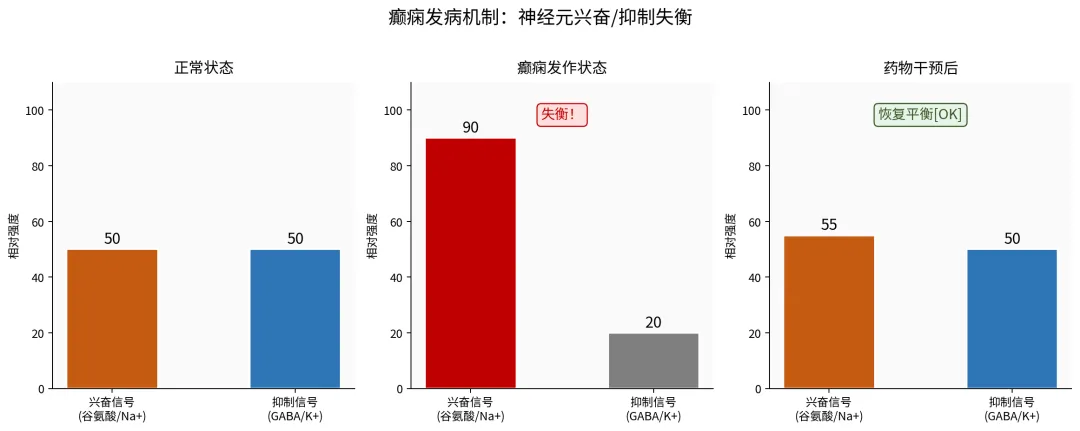
图1:癫痫发病机制——兴奋/抑制失衡与各类药物作用靶点
?患者规模:全球超7,000万癫痫患者,中国约900万(患病率约7‰),美国约340万。约1/3为"难治性癫痫",即两种或以上药物联合也无法控制发作,这部分患者是新药最迫切的目标群体。 |
?现有癫痫药物:三十年江山,一个痛点
过去30年,全球上市的抗发作药物(ASM)已超30种,但疗效与安全性的天花板清晰可见——大多数机制(Na⁺通道阻断、GABA增强、SV2A调节)只是从不同角度"踩刹车",约36%的患者无论叠加多少药物,仍无法控制发作。
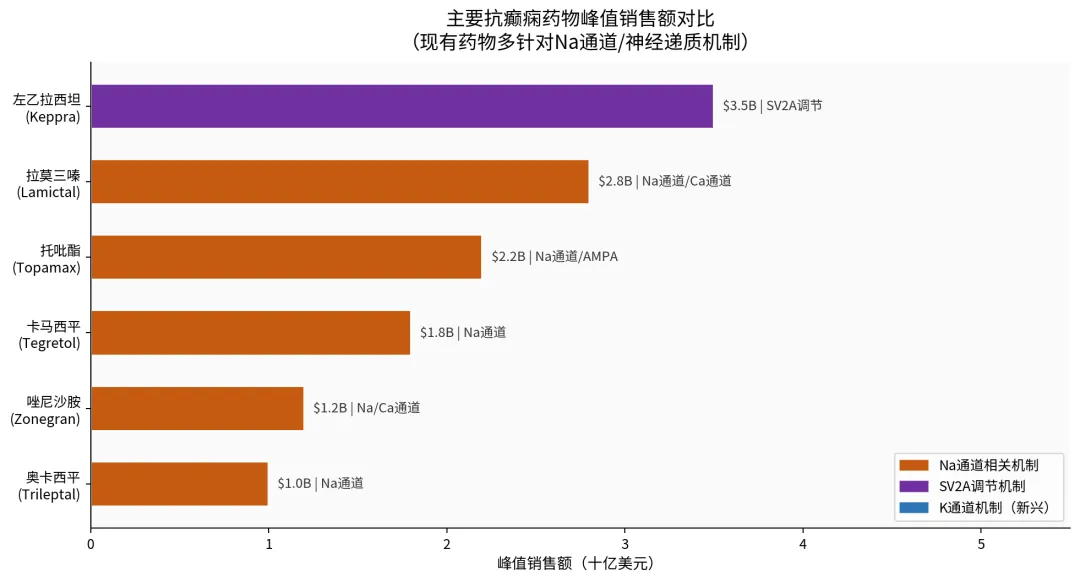
图2:主要商业化癫痫药物销售峰值对比(百万美元)
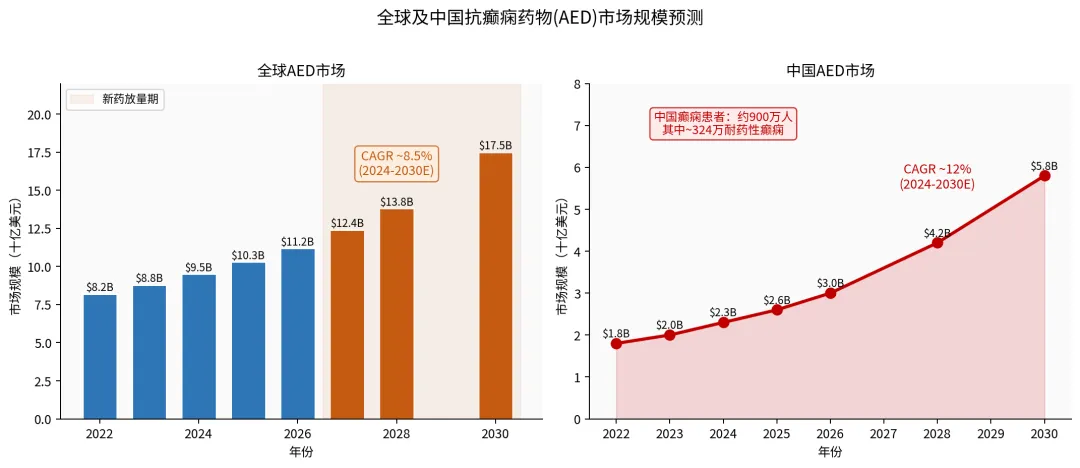
图3:全球与中国AED市场规模预测(2020-2034E)
⚡离子通道:神经元的"开关"
神经元每次"放电"(动作电位),都经历一个有序过程:Na⁺通道开放→去极化→K⁺通道(Kv7)开放→复极化回到静息。这个K⁺通道产生的"M电流",是神经元天然的"刹车系统"——它在阈值附近就能激活,有效防止神经元反复放电。
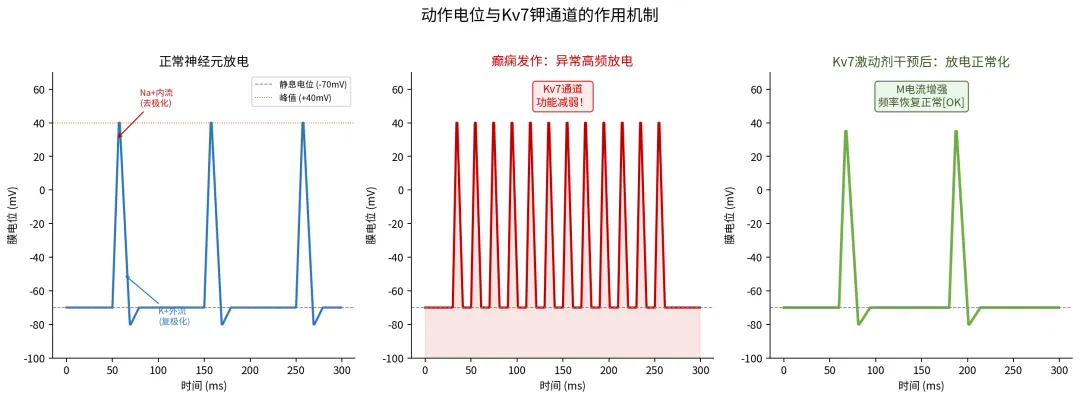
图4:动作电位示意图(左)与正常/癫痫/Kv7激动剂治疗放电模式对比(右)
现有大多数药物走的是"阻断Na⁺通道"路线——在触发环节踩刹车。这固然有效,但对已经耐药的患者,换汤不换药的作用越来越小。
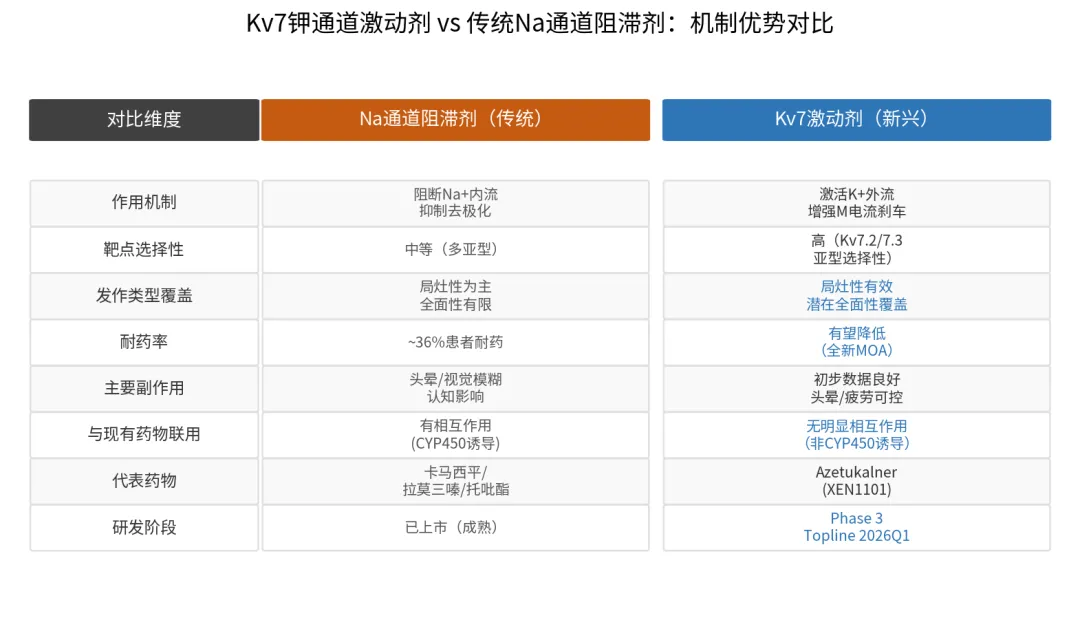
图5:Kv7 K⁺通道激动剂 vs Na⁺通道阻断剂——机制与优劣全面对比
?K离子通道激动剂的差异化逻辑:它不是"阻断",而是"增强"——激活Kv7.2/7.3通道,放大神经元自带的刹车系统(M电流),让大脑在过度兴奋之前就自动降速。对Na⁺通道药物已耐药的患者,这是真正的"换道超车",而非同一条路上的又一辆车。 |
?在研K通道药物:谁跑在前面?
目前进入临床阶段的Kv7激动剂主要有两个选手:
•Xenon Pharmaceuticals(XENE)的Azetukalner(AZK):Kv7.2/7.3高选择性,目前进度最快,处于Phase 3,最关键的FOS(局灶性发作)3期TLD将在2026年3月读出 ★
•Biohaven(BHVN)的Opakalim:Kv7泛亚型激动剂,Phase 2/3,落后约1-2年,TLD预计2026年下半年
历史上,GSK的Ezogabine(2011年上市/2017年退市)是Kv7靶点已经获得MOA验证的前辈,只因靶点选择性不足导致视网膜色素沉着和尿潴留副作用而退市。新一代药物(AZK)通过聚焦Kv7.2/3神经元亚型,规避了这些问题。
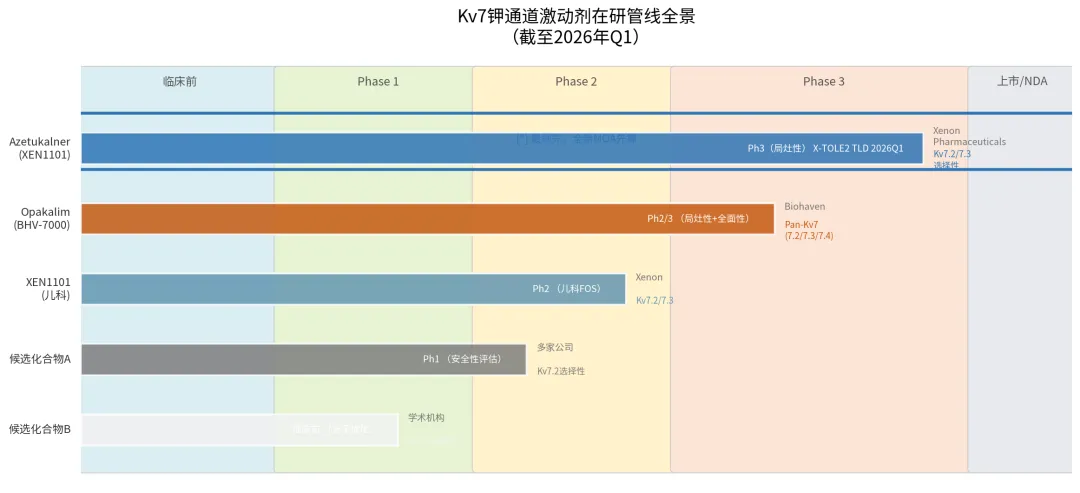
图6:在研K离子通道(Kv7)药物竞争格局一览(截至2026年3月)
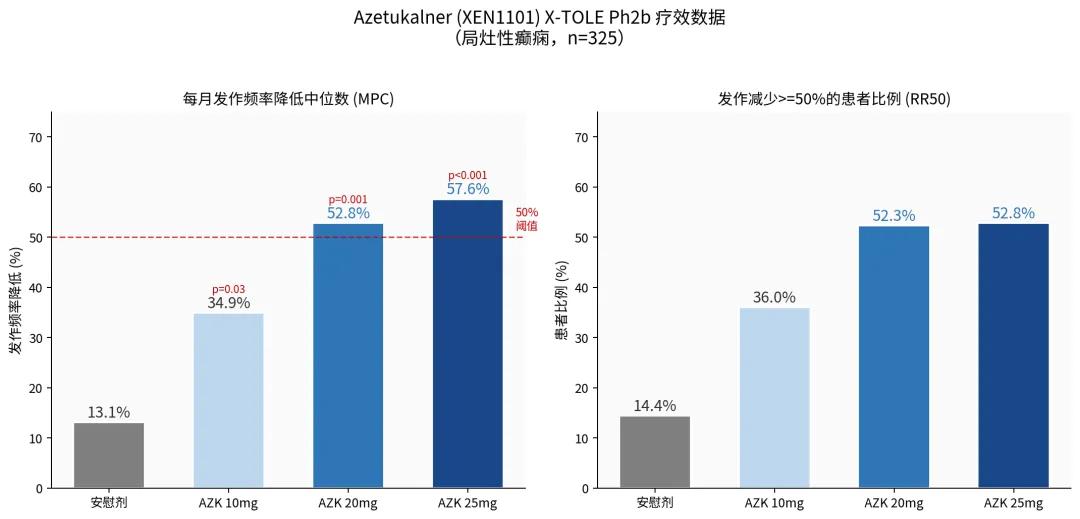
图7:Azetukalner Ph2 X-TOLE关键疗效数据——发作频率降低(左)与应答率(右)
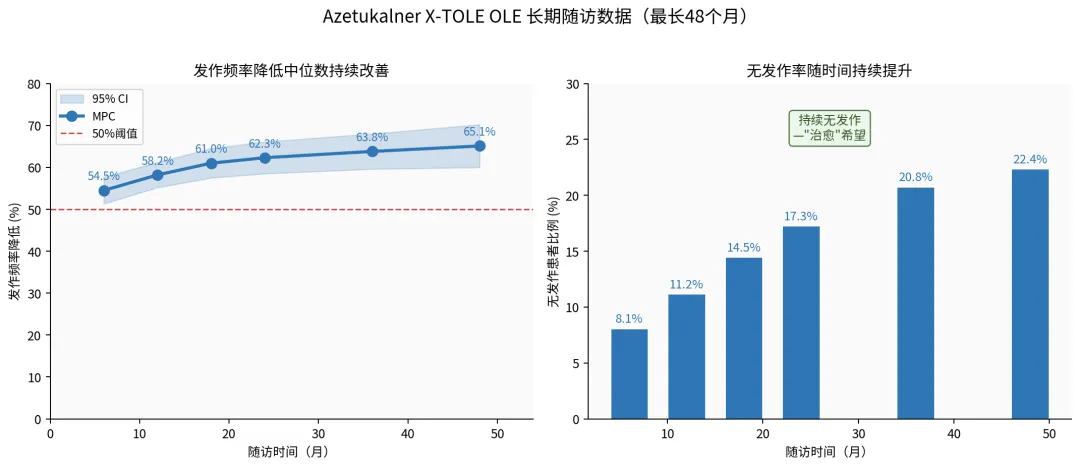
图8:Azetukalner X-TOLE OLE 长期数据(48个月持续深化)
?关于XENE的Azetukalner
XENE(Xenon Pharmaceuticals,纳斯达克上市)的Azetukalner是目前进度最领先的Kv7.2/3选择性激动剂。Ph2数据显示,每日一次口服(无需titration)可将FOS发作频率降低约53%(最高剂量组),应答率达54.5%;7年开放标签数据持续深化且无耐受迹象。它同时在MDD(重度抑郁)等神经精神适应症推进3期——K通道在情绪调节中的潜在作用,让它的想象空间远超单纯的癫痫药。更多细节分析我们将在下一篇文章中展开。
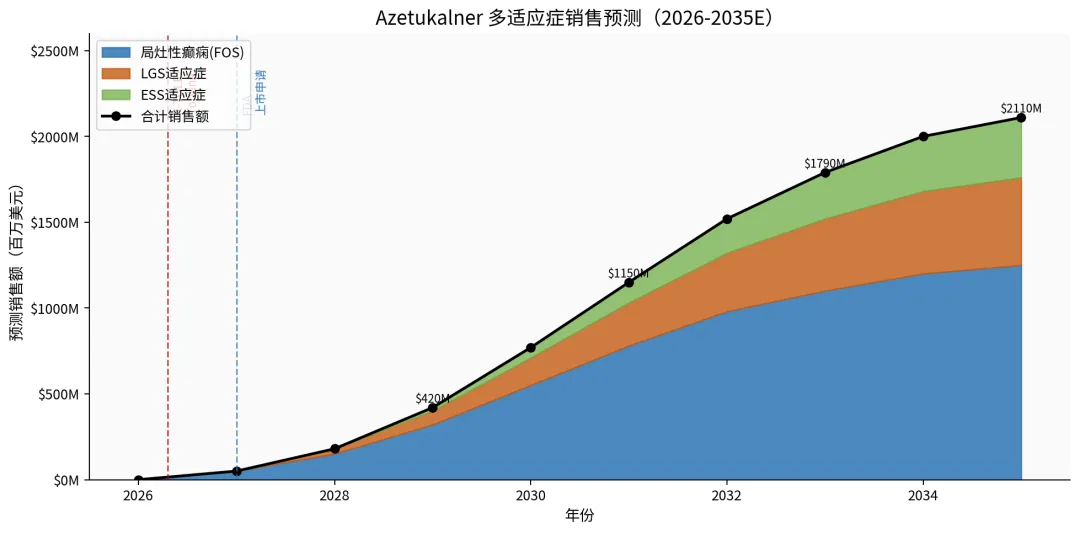
图9:Azetukalner各适应症销售预测(风险调整,基础情景)
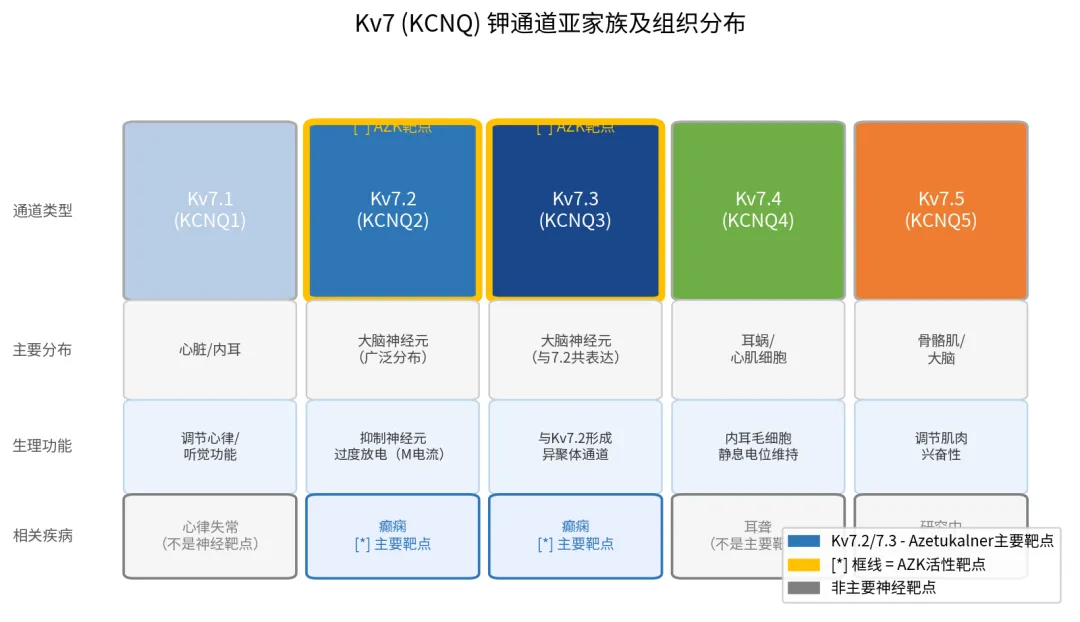
图10:Kv7通道亚型图谱——为什么选择性很重要?
?一句话总结
癫痫治疗经历了30年的Nav/GABA/SV2A式"老路",约36%难治性患者始终等不到突破。Kv7 K⁺通道激动剂代表真正意义上的新机制——增强神经元自带刹车(M电流),与现有所有药物无交叉耐药。XENE的Azetukalner是目前最领先的选手,2026年3月3期数据是近期最大催化剂。如果成功,它将成为耐药性FOS患者十余年来等来的第一把新钥匙。 |
参考资料
·XENE公司公告;
·专家访谈(2025年6-10月);
·Fortune Business Insights全球AED市场报告2024;
·中国抗癫痫协会诊疗指南2023版;


