|中肽生化内容团队编辑

1.FDA释放多肽松绑政策信号
2026年2月27日,美国卫生与公众服务部部长 Robert F. Kennedy Jr. 在播客节目 Joe Rogan Experience 第2461期中提到,FDA正在讨论将此前被列入 Category 2 的一批多肽重新纳入 Category 1 的可能性。该表态对于多肽药物的合法使用将是一件极其重要的事件,涉及到非常广泛的患者群体和适应症类别。
根据节目中的表述,大约14种多肽可能重新获得配制(Compounding)资格。消息发布后,美国再生医学诊所、抗衰老医疗机构、功能医学医生以及配制药房行业迅速开始关注这一变化,因为这些多肽在2023年至2024年间被FDA禁止用于药房配制,这一政策在实施后对整个市场结构产生了明显影响。
需要说明的是,目前这一政策仍停留在公开表态阶段,FDA尚未发布正式监管文件,因此相关多肽的法律地位尚未发生变化。只有在FDA更新503A bulk drug substances名单并完成必要程序后,这些多肽的配制资格才会真正改变。然而在监管体系内部,重新评估已经开始出现迹象。
2024年9月,FDA曾将CJC-1295、Ipamorelin、Thymosin Alpha-1、AOD-9604以及Selank五种多肽从Category 2名单中移出,并提交药房配制咨询委员会(PCAC)进行评估。这一程序通常被视为重新评估配制资格的重要步骤,因此2026年初的政策讨论并非突然出现,而是过去两年监管争议逐渐累积后的结果。
这一政策讨论的意义在于,美国监管体系正在重新审视多肽配制的整体框架。过去两年中,一批多肽被完全排除在合法配制渠道之外,而市场需求并未随之消失。监管层需要面对的问题是,在完全禁止的情况下,需求转移到了哪些渠道,以及这一结果是否符合公共卫生目标。
2.制度背景:503A与503B体系
美国配制药房体系主要建立在《联邦食品、药品和化妆品法案》下的两个监管框架之上,即503A配制药房和503B外包制剂生产设施。此次讨论的多肽重新分类,直接对应的是503A框架下的配制原料管理政策。
503A配制药房本质上属于传统意义上的处方配制药房,其法律定位是为个体患者提供工业化成药无法满足的个性化制剂服务。它的前提是先有明确患者,再有明确处方,最后才发生配制行为。也就是说,503A药房不能把某种药物当作标准商品提前大批量做出来放在货架上等待销售,也不能面向市场持续生产某一种固定配方的药物。它所配制的产品必须与具体患者的治疗需要直接对应,例如剂量规格不适合、辅料不耐受、需要特殊剂型,或者临床上确实存在个体化调整的必要。正因为其法律基础建立在个体化医疗之上,503A体系一直被视为对上市药品体系的补充,而不是一个可以与工业化制药平行竞争的大规模供给体系。
从监管分工来看,503A药房的主要执法主体通常是各州药房委员会。州一级监管更关注药房执照、药师执业、处方合规、配制环境、无菌操作、记录留存以及州法下的药房经营规范。FDA并不是完全不管503A,而是通常不承担这类药房的日常一线监管职责。FDA介入的情形往往出现在联邦法问题已经被触发的时候,例如药房使用了不符合要求的原料、配制的产品实质上成为对上市药的商业化复制、存在跨州大范围分销、产品造成严重安全事件,或者所涉及的原料本身就被FDA认定存在潜在显著安全风险。在这些情况下,问题就不再只是一个州内药房执业管理问题,而会上升到《联邦食品、药品和化妆品法》层面的未批准新药、掺假、标签不当或非法配制问题。
还要再强调一点,503A药房虽然不能进行“规模化生产”,但现实中并不等于它完全不能预先准备任何东西。美国法规允许在一定条件下基于历史处方记录进行有限度的提前配制,但这种提前量必须建立在真实处方需求的可预见性上,不能演变成持续性的标准化批量制造。监管真正要防止的是,一家本应服务个体处方需求的药房,实际上却以配制名义做成了小型药厂。这也是503A与503B之间最核心的边界之一。503B可以面向医疗机构批量供货,但要接受更高等级的FDA监管和cGMP要求;503A则保留更大的灵活性,但其前提是始终围绕具体患者处方展开。
503B外包设施属于美国在配制药监管上的一套强化监管安排,其制度起点是2012年由新英格兰复方中心引发的真菌性脑膜炎事件。那次事件暴露出传统配制体系在无菌制剂大规模生产、跨州分销和质量体系控制方面存在明显漏洞。随后,美国国会于2013年通过《药品质量与安全法案》(Drug Quality and Security Act, DQSA),在《联邦食品、药品和化妆品法》中新增了 Section 503B,专门设立外包制剂生产设施(outsourcing facility )这一类别。FDA明确说明,503B是DQSA于2013年11月27日签署后加入联邦法规的新制度安排,其目的就是为那些已经不再局限于传统个体化配制、而是面向医疗机构稳定供货的配制主体建立一套更高等级的联邦监管框架。
503B设施与503A药房最核心的差别,在于它不再严格依赖每一笔业务都先有具体患者处方。按照FDA对503B的解释,outsourcing facility 可以在没有“明确的个体患者”处方的情况下进行配制,并可直接向医院、门诊、诊所等医疗机构供货,因此它承担的角色更接近医疗体系中的标准化制剂供应方,而不再只是传统意义上围绕单个患者需求运转的药房。也正因为如此,503B设施可以进行更大规模、更连续的生产和跨州分销,但前提是必须自愿向FDA注册、按要求报告其配制产品,并满足Section 503B规定的全部条件。FDA同时强调,所谓注册为outsourcing facility,并不等于其产品获得FDA批准;它只意味着该设施进入了503B监管框架,必须接受更直接、更频繁的联邦监管。
503B设施生产的药品虽然可以豁免新药审批等部分要求,但它们并不豁免现行药品生产质量管理规范,也就是cGMP要求。FDA的公开说明反复强调,outsourcing facilities 必须遵守cGMP,并接受FDA检查;同时还要向FDA定期提交所配制药品的清单、活性成分来源、剂型、规格、包装和产量等信息。503B并不是让配制主体获得更大自由度而少受监管,恰恰相反,它是以更严格的质量体系、更高的合规成本和更直接的FDA监督,换取更强的供货能力和更大的市场覆盖范围。也正因为这一体系的建设和维持成本显著高于503A,美国真正登记在册的503B设施数量一直远少于传统配制药房。
在这次多肽政策讨论中,直接涉及的制度对象仍然是503A体系下的配制原料分类,因为Category 2名单本身就属于503A配制框架的一部分。503B的意义主要体现在后续产业层面。一旦部分多肽重新回到合法配制渠道,具备更强质量体系和批量供货能力的503B外包生产设施,可能在医院、诊所和连锁医疗机构采购中发挥更大作用。对于注射类多肽这类对无菌控制、批次一致性和原料质量要求更高的产品,503B体系的承接能力会比传统503A药房更强。
多肽能否进入合法配制渠道,与 FDA 制定的 503A 大批量原料药管理框架直接相关。这套框架讨论的并不是药物能否作为正式处方药上市,而是某种活性物质能否被 503A 配制药房用作个体化制剂原料。
Category 1 表示 FDA 在继续评估期间通常不会就该原料的配制行为主动采取执法行动,因此在实践中往往被视为仍保留配制空间。这里需要特别说明,进入 Category 1 也不等于获得 FDA 批准上市;一些并没有 FDA 批准药品版本的活性物质,只要没有被列入限制名单、原料来源符合要求,并且配制行为建立在具体患者处方基础上,仍然可能通过 503A 体系进入临床使用。Semax 这类多肽过去之所以能够在部分医疗机构和配制药房体系中出现,依靠的就是这一逻辑。
Category 2 则意味着 FDA 已经识别出潜在显著安全风险,因此通常会对相关原料的配制行为采取执法行动。一旦某种物质被列入 Category 2,503A 配制药房实际上就失去了继续使用该原料的空间,即使存在医生处方或患者需求,也不能作为合法配制原料使用。
Category 3 的含义则不同,它并不代表 FDA 已经认定存在明确安全风险,而是因为提交的安全性或质量资料不足,无法支持其进入Category 1 名单。但在实践中,这类物质同样缺乏稳定的合法配制基础,因为 FDA 并未给予执法宽容空间,药房如果使用这类原料配制药物,仍然面临监管风险。
对多肽市场而言,某种多肽一旦进入 Category 2,503A 配制药房、临床医生和患者之间的合法路径就会明显收缩,需求随后往往会转向研究级产品和灰色市场。
3.2023年的监管收紧
2023年10月,FDA将一批常见多肽列入Category 2,这一决定迅速改变了美国多肽治疗市场的供应格局。
这19种多肽大致可分为四类。第一类是组织修复与愈合类,包括 BPC-157、TB-500 和 GHK-Cu。BPC-157 主要与肠道修复、组织修复和抗炎作用联系在一起;TB-500 主要与细胞迁移和创伤愈合相关;GHK-Cu 则更多与胶原合成、组织重塑和抗衰老方向相关。这几种多肽常被联合使用,以覆盖不同修复机制。
第二类是生长激素轴与代谢类,包括 CJC-1295、Ipamorelin、AOD-9604、GHRP-2、GHRP-6 和 PEG-MGF。CJC-1295 属于 GHRH (生长激素释放激素)类似物,刺激内源性生长激素分泌;Ipamorelin 是选择性生长激素促分泌剂;AOD-9604 主要针对脂解和脂肪代谢;GHRP-2 和 GHRP-6 通过 ghrelin (饥饿素)受体通路刺激 GH 分泌;PEG-MGF 则主要与肌肉恢复和生长联系在一起。这一组多肽基本围绕代谢优化、GH(生长激素)轴调节和运动恢复展开。
第三类是认知与神经系统类,包括 Semax、Selank 和 Emideltide(DSIP)。Semax 被描述为合成促智多肽,重点在 BDNF 增强、神经保护和认知功能支持;Selank 与 GABA、5-HT 系统调节相关,主要指向抗焦虑和抗应激;DSIP 则主要与深度睡眠、恢复性睡眠和昼夜节律调节有关。
第四类是免疫、抗炎与抗衰老类,包括 Thymosin Alpha-1、KPV、MOTS-C、Epitalon、Kisspeptin-10、Melanotan II 和 Cathelicidin LL-37。Thymosin Alpha-1 是这组里争议最大的一个,它在30多个国家获批用于乙肝、丙肝和癌症相关管理;KPV 主要与抗炎、肠道炎症和免疫调节相关;MOTS-C 与线粒体代谢、胰岛素敏感性和AMPK激活相关;Epitalon 主要与端粒酶和抗衰老研究相关;Kisspeptin-10 涉及生殖激素信号;Melanotan II 与晒黑和性功能用途相关,但安全性争议更大;LL-37 属于抗菌肽,和先天免疫防御有关。
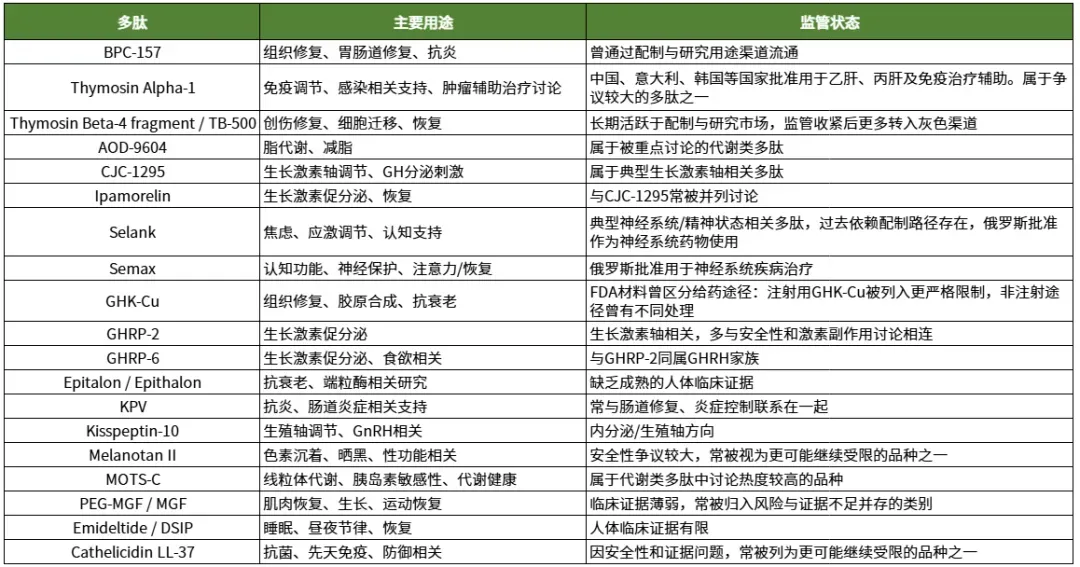
从监管批准状态看,这一类多肽的共同特征,是没有美国FDA批准的上市药品身份。它们过去能够在部分医疗机构和配制药房体系中出现,依靠的是503A配制路径,而不是正式新药批准路径。Semax就是一个典型例子:它在美国并不是FDA批准药物,但在配制监管相对宽松、且未被列入更严格限制名单的阶段,仍可能通过个体化配制路径进入部分临床使用场景。Thymosin Alpha-1的情况稍有不同。FDA在2024年PCAC背景文件中提到,thymosin alpha-1并未获美国批准,但曾被报告在亚太、拉美、东欧和中东部分国家用于乙肝、丙肝、疫苗佐剂或肿瘤辅助治疗,FDA同时也明确表示其无法独立核实所有国家的批准信息,并指出该物质在美国、日本和欧洲大部分地区并未获批。也就是说,这批被列入Category 2的多肽中,个别品种在海外存在一定医疗使用历史,但在美国整体上仍属于未正式批准上市、主要依赖配制或研究用途流通的活性物质。
FDA给出的监管理由主要包括三方面。第一是缺乏充分的人体安全数据,第二是潜在免疫原性风险,第三是多肽合成过程中可能产生杂质。从监管逻辑来看,这属于预防性管理方式,即在缺乏明确安全证据时先采取限制措施,以避免潜在风险。
在Category 2政策实施之前,这些多肽在美国再生医学诊所、抗衰老医疗机构以及功能医学诊所中被广泛使用。大量诊所依赖配制药房提供这些制剂,因此Category 2政策出台后,相关治疗方案迅速中断。
4.监管后果:研究级多肽灰色市场迅速扩大
Category 2政策实施后,多肽需求并没有随着合法配制渠道的收缩而同步消失。对不少使用者而言,被切断的只是原先通过503A配制药房获取产品的路径,组织修复、减脂、认知提升、抗衰老和健身恢复相关需求依旧存在,市场因此迅速转向research-use-only(仅限研究)多肽供应商。这类产品通常以科研试剂名义销售,包装上标注仅限研究用途或不得用于人体,同时在法律表述上尽量避免直接触碰药品宣传和临床治疗边界。BPC-157、TB-500等未经批准的多肽通过社交媒体、健康博主及线上商家持续扩散,而且这类未获批准的肽类产品在大型电商和跨境渠道上仍可见到大量销售信息,说明合法医疗路径收缩之后,线上灰色供应链并未同步收缩。
这种灰色链条之所以能够扩大,一个重要原因在于它利用了研究用途与人体使用之间的监管缝隙。卖家表面上出售的是科研材料,网页上往往附带免责声明,但实际运营方式又会通过溶解说明、剂量计算器、用户讨论区和隐性场景暗示,把产品导向真实消费人群。FDA近年的执法重点也恰恰集中在这里。2024年,FDA针对多家research peptides网站发出警告信,认为其销售的semaglutide、tirzepatide等产品属于未经批准的新药和标签不当药品,说明监管机构已经不再满足于只看网站上是否写了“research use only”,而是会结合营销内容和实际用途判断其是否在规避药品监管。法律界对近年执法趋势的总结也指出,FDA正在加强对在线多肽销售的关注,尤其针对那些表面标注科研用途、实际却在暗示或推动人体使用的平台。
更深一层的问题在于,灰色市场扩张并不只是合规风险,它还会迅速转化为质量风险。研究级多肽通常不进入药品质量体系,不受503A、503B或cGMP同等级别控制,批次一致性、身份确认、纯度控制、内毒素和无菌保障都可能明显弱于正规医药供应链。FDA、USP以及多篇技术文献都强调,肽类药物中的相关杂质、插入缺失序列、消旋、脱氨及其他工艺副产物需要被严格控制,某些新杂质即使比例不高,也可能带来免疫原性和安全性问题。FDA针对合成肽仿制药的指导原则要求对0.10%以上的新的肽类杂质进行识别和说明,部分技术资料还强调,新出现的肽类杂质一旦高于0.5%,就需要进一步评估其免疫原性风险。这意味着,对本就结构敏感、工艺复杂的多肽而言,质量风险往往并不表现为简单的真假问题,而是表现为序列相关杂质、纯度不足、批次差异以及工艺副产物带来的不确定性。
因此,Category 2政策带来的一个现实后果,并不是需求被消灭,而是需求从受监管的配制体系转移到了更难追踪、质量更不透明的灰色市场。对监管者而言,这构成了一个越来越难回避的政策悖论:限制合法配制的初衷原本是降低潜在风险,但在需求持续存在的情况下,结果可能是把一部分消费者推向质量控制更弱、信息更不透明、售后责任更模糊的供应链。也正是在这个意义上,2026年初围绕约14种多肽可能重新回到Category 1的讨论,不只是一次配制名单调整,而是对过去两年监管效果的一次现实检验。
多肽监管变化的另一背景是GLP-1药物短缺的结束。2022年至2024年期间,semaglutide和tirzepatide因需求快速增长出现供应短缺。根据美国法律,在药物短缺期间,配制药房可以生产与品牌药物相同成分的制剂。大量503A和503B设施因此进入GLP-1配制市场。配制制剂价格通常为每月200至500美元,而品牌药物价格约为900至1300美元,这一差距使许多患者能够负担治疗费用。
随着生产能力恢复,FDA宣布tirzepatide短缺在2024年10月结束,semaglutide短缺在2025年2月结束。短缺结束后,503A药房需在60天内停止配制,503B设施需在90天内停止配制。这一变化使配制GLP-1市场迅速消失,也对许多配制药房的经营造成冲击。
5.政策重新评估:监管层开始面对新的现实
在Category 2限制和GLP-1配制结束的双重背景下,多肽监管问题逐渐进入政策讨论。一些配制药房和医疗机构认为,FDA在将多肽列入Category 2时缺乏明确安全信号,并未充分遵循必要评估程序。同时,监管机构也开始关注灰色市场扩张问题。部分政策讨论认为,在严格监管框架下恢复部分多肽配制渠道,有助于将需求重新引导至受监管体系。
2026年初的政策表态正是在这一背景下出现。最终名单仍需等待FDA正式公告。需要强调的是,即使多肽重新进入Category 1,这些多肽也不等同于FDA批准药物。Category 1仅表示原料可以用于配制药房制剂,药物批准仍需要完整的临床试验数据。
同时需要强调的是,并非19种多肽都会被重新放开。大约仍有5种更可能继续留在 Category 2 名单中,原因主要是人体安全数据较弱,或存在更明显的安全顾虑。被点名最可能继续受限的包括 Melanotan II、Cathelicidin LL-37、GHRP-2、Ipamorelin 和 PEG-MGF。对应原因分别是:Melanotan II 涉及恶心、心血管效应及潜在黑色素瘤风险;LL-37 缺乏足够人体安全数据;GHRP-2 可能引起皮质醇和催乳素升高;Ipamorelin 可能还需要进一步 PCAC 审查;PEG-MGF 的临床证据相对薄弱。
6.产业影响:多肽供应链可能出现新的变化
如果部分多肽最终恢复Category 1资格,美国多肽产业链很可能出现一轮结构性重组。最直接的变化会先发生在配制端。过去两年中,一批原本依赖503A配制药房流通的多肽被移出合法渠道,配制药房失去的并不只是几个具体品种,而是一整类围绕组织修复、免疫调节、代谢优化、神经调节和抗衰老需求形成的业务来源。一旦这些多肽重新回到Category 1,意味着在符合处方、原料和质量要求的前提下,503A体系重新获得操作空间,诊所、医生与药房之间原本被切断的路径会恢复运转。对配制药房而言,这不只是业务回补,更意味着它们重新获得了对一部分高毛利、高黏性患者群体的服务能力。对于长期依赖再生医学、功能医学和抗衰老诊所订单的药房来说,这类多肽的回归很可能比单纯新增几个SKU更重要,因为它关系到整套个体化治疗方案能否重建。
需求端的回流也会随之发生。过去Category 2实施后,多肽需求并没有消失,而是外溢到了research-use-only市场、跨境采购渠道和各种灰色平台。这些需求原本就具有较强的支付意愿,只是因为合法医疗路径被压缩,才被迫转向监管更弱的渠道。一旦部分多肽重新进入Category 1,这部分需求中相当一部分有可能回流至医生处方和配制药房体系。对于真正长期使用多肽的人群来说,医疗监督、配方稳定性、剂量准确性和质量可追溯性本来就具有价值,只是在合法渠道关闭时没有替代选项。只要处方路径重新打开,部分消费者会更愿意为合规性和质量保障支付溢价。这会对研究级多肽市场形成挤压,尤其是那些依赖“research only”标签但实际上服务人体使用需求的平台,其商业空间可能受到明显冲击。不过这种冲击不会是完全替代关系。价格敏感型用户、追求匿名购买的人群,以及某些仍然未被放开的多肽需求,仍会留在灰色市场,因此更可能出现的结果是市场重新分层,而不是灰色市场彻底消失。
配制端之外,更值得重视的是上游原料供应链的变化。多肽合成并不是一个低门槛的化学原料生意,它涉及固相多肽合成工艺、氨基酸保护策略、缩合效率控制、缺失肽和错配肽杂质控制、纯化工艺放大以及批次一致性管理。对于注射类多肽而言,还要进一步考虑残留溶剂、内毒素、无菌保障以及更严格的质量放行标准。换句话说,合法配制渠道恢复之后,真正受益是那些能够提供医药级原料、建立稳定质量体系并满足可追溯要求的供应商。过去灰色市场大量使用的研究级原料,将逐渐被排除在市场供求链之外。一旦需求重新回流到503A甚至未来可能外溢到503B体系,市场对原料的要求会从“有没有货”快速转向“纯度、杂质谱、批间一致性和文件体系是否过关”。这意味着上游原料端会出现一次明显的质量分层,真正具备GMP能力、分析方法开发能力和稳定放大能力的多肽API企业,可能获得新的订单机会,而那些只适合供应研究市场的小型厂家则很难直接承接这波需求。
这一变化对中游也会带来新的筛选机制。合法配制渠道恢复后,诊所和药房不会只比较价格,还会重新关注谁能稳定供货、谁的原料文件完整、谁的质量投诉风险更低。过去在研究级市场里,供应商往往依靠营销、社群传播和价格优势吸引用户,但在配制体系中,决定竞争力的因素会转向更传统的医药工业能力,包括原料合规性、分析报告的完整性、供应连续性,以及是否能在监管询问时拿出足够扎实的技术文件。对药房来说,多肽原料不是普通消费品,而是可能直接触发联邦和州监管责任的关键输入。如果一类多肽重新合法化,药房首先要解决的不是如何扩大销量,而是如何找到能够长期稳定配合审计和质量要求的供应商。这会推动原料市场向头部集中,也会让具备审计能力和客户支持能力的企业更有优势。
恢复Category 1资格还可能对美国多肽市场的商业模式产生更深层的影响。过去两年里,很多诊所和医生在合法路径收缩后,实际上处于一种尴尬状态:患者有需求,研究级市场有供给,但医生无法在标准医疗体系中稳定管理这些用药行为。部分多肽一旦回到Category 1,诊所端就有机会重新把这类需求纳入处方、随访和联合治疗方案之中。这样带来的不只是单个产品销量恢复,而是整套服务模式的重建。再生医学诊所、功能医学机构、激素管理诊所和部分抗衰老中心,可能会重新把多肽纳入组合治疗方案,例如将组织修复类多肽与康复治疗、将代谢类多肽与体重管理、将神经调节类多肽与睡眠或认知干预一起设计。对这些机构来说,多肽的价值从来不只是产品本身,而是它能否成为高客单价、长期管理型服务的一部分。监管放松如果落地,真正恢复的将不仅是原料流通,而是一套围绕多肽形成的医疗服务收入模型。
如果把视角放到中国企业身上,这一点尤其重要。中国本来就在全球多肽原料供应中占据优势,具备较强的固相合成能力、规模化生产能力和成本控制能力。过去在大量多肽需求停留在研究级市场时,这种优势并不总能转化为稳定的高质量利润,因为研究级市场价格透明度低、客户黏性弱、质量要求分化明显,竞争往往停留在低门槛层面。一旦美国合法配制渠道恢复,对中国企业的机会是进入一个要求更高、但也更容易形成长期合作关系的供应链层级。谁能证明自己的产品质量稳定,谁能把分析方法、杂质控制、批次一致性和注册支持做扎实,谁就更有机会进入受监管的配制原料链条。对中国多肽企业而言,这可能意味着从研究级市场供货商向医药级原料供应商进一步升级;对中小企业而言,则意味着市场门槛提高,单纯依赖低价竞争会越来越难。
因此,Category 1资格恢复的产业意义,远不止几个多肽重新可以配制这么简单。它会重新连接诊所、医生、药房和原料供应商之间被打断的链条,也会推动市场从灰色流通重新向质量驱动和合规驱动的方向移动。对美国本土配制体系来说,这是业务回流;对上游原料端来说,这是一次从量的竞争走向质量竞争的机会窗口。对中国企业而言,这件事真正值得关注的地方,是美国多肽市场如果重新建立起一条更稳定、更合规的配制供应链,谁有能力进入这条链,谁就有机会在未来几年获得比灰色市场更稳固、更高质量的增长空间。
Ref.
Potential FDA Peptide Reclassification 2026 – What It Means for Patients. Beverly Hills Rejuvenation Centers. 27. 02. 2026.
The FDA Peptide Regulations Explained: What’s Legal, What’s Not, and What’s Coming. Medium. 06. 02. 2026.
Mitchell, S. FDA Peptide Regulations 2026: What You Need to Know. Peptide Laws. 11. 02. 2026.


