
牙周病的典型特征是牙周复合体软硬组织的进行性破坏,这一过程由菌群失调的微生物群落与牙龈及牙周组织内异常的免疫反应之间的相互作用所介导。随着常驻口腔微生物群变得失调,假定的牙周病原体得以富集,而炎症反应则引发组织破坏,从而形成一个由蛋白水解、炎症和牙周病原体富集组成的、持续不断的正反馈循环。关键微生物病原体和持续的牙龈炎症对牙周病的进展至关重要。然而,近期研究揭示了先前未识别的微生物在疾病进展中的重要性,包括多种病毒、噬菌体和细菌种类。此外,近年来,新发现的免疫学和遗传学机制,以及环境宿主因素(包括饮食和生活方式),已被确认为牙周炎的进一步促成因素。这些因素共同扩展了既定的牙周病进展理论。与此相一致,维持牙周健康和治疗现有疾病的新理念也已被探索,例如应用口服益生菌来限制和减缓疾病进展。全身性宿主病理状态(如自身免疫性疾病和糖尿病)在牙周病发病机制中的作用已得到充分关注。近期研究还发现了牙周病在加剧远端部位全身性疾病状态中的相互影响的重要性,例如在阿尔茨海默病、炎症性肠病和口腔癌中,这进一步强调了口腔在全身健康中的重要性。在此,我们回顾了关于牙周病进展的长期知识,同时整合了拓宽我们对牙周健康和疾病理解的新的研究概念。此外,我们深入探讨了可能用于解决牙周病基础知识中重大空白的创新性假设。
【4月27-28日·深圳站/5月16-17日·昆明站】牙周手术基础实战班-佟旭

口腔微生物组:口腔是大约700种细菌的家园,它们共同构成了口腔微生物组(Deo and Deshmukh, 2019)。口腔微生物组由独特且多样化的微生物生态系统组成,这些微生物之间进行着代谢和物理上的相互作用。这些相互作用导致复杂生物膜群落的形成,其中物理化学梯度为具有不同代谢需求的微生物创造了独特的生态位(Rosan and Lamont, 2000; Kim et al., 2020)。Mark Welch等人的研究展示了健康龈上菌斑的空间化学结构,其被描述为一种呈放射状排列的"刺猬状"结构(Mark Welch et al., 2016)。在此模型中,棒状杆菌属(Corynebacterium spp.)锚定于早期定植菌(如放线菌属(Actinomyces spp.)和链球菌属(Streptococcus spp.)),并径向向外延伸,形成一个长的环状结构。嗜血杆菌属(Haemophilus)、聚集杆菌属(Aggregatibacter)和奈瑟菌科(Neisseriaceae)附着在环状结构的尖端,占据富含氧气和营养的周边区域。周边氧化性物种的代谢产物在生物膜中心创造了一个缺氧环境,嗜二氧化碳的厌氧菌(如二氧化碳嗜纤维菌属(Capnocytophaga)、纤毛菌属(Leptotrichia)和梭杆菌属(Fusobacterium))则在环状结构的中部繁盛。该研究还发现,健康受试者的龈上菌斑和龈下菌斑在组成上具有惊人的相似性,鉴定出13个丰度至少为3%的属,它们构成了龈上菌斑所有测序序列的85%和龈下菌斑的80%以上(Mark Welch et al., 2016)。当口腔生物膜的复杂生态系统受到干扰时,微生物失调随之发生(Hajishengallis and Lamont, 2012)。这种微生物群落动态的破坏在牙龈炎的病因学和牙周病的发展中起着重要作用。牙周炎的特征还在于免疫失调、炎症以及牙周病原体代表性增加,这些因素双向促进,共同驱动牙周支持组织(包括牙周膜和牙槽骨)的破坏(Ebersole et al., 2013)。慢性炎症性疾病(远离口腔的部位)对牙周炎的影响,以及牙周炎在全身性炎症中新出现的角色,在牙周病的发病机制中也逐渐得到认识(Qasim et al., 2020)。
走向"坏"的一面由Lamont和Hajishengallis(2013)提出的多微生物协同模型,整合了牙周病病因学各种观点中的多个方面(Hajishengallis and Lamont, 2013)。例如,Marsh(1994)提出的生态菌斑假说、Socransky等人(1998)发现的红色复合体、Hajishengallis等人(2011)提出的关键病原体与共生菌之间协同相互作用的模型,以及关于描绘健康和疾病状态下免疫网络的研究(Dutzan et al., 2016),都被综合起来以把握疾病进展的复杂性,包括协同微生物群落以及关键病原体的作用,以及口腔免疫网络失调的作用。人们普遍认为,牙周炎是由多种因素驱动的,包括宿主免疫、宿主环境因素以及对疾病病因学至关重要的关键牙周病原体。Socransky等人(1998)定义了一个牙周炎中多物种相互作用的综合模型,他们使用基因组DNA探针和棋盘DNA-DNA杂交技术,鉴定出牙龈卟啉单胞菌(Porphyromonas gingivalis)、福赛斯坦纳菌(Tannerella forsythia)和齿垢密螺旋体(Treponema denticola)是随着牙周病严重程度增加而更频繁地一起出现的物种,由此创造了"红色复合体"这一聚类名称(Socransky et al., 1998; Holt and Ebersole, 2005)。然而,多年来,与牙周炎相关的菌属已扩展到红色复合体之外,包括啮蚀艾肯菌(Filifactor alocis)、卟啉单胞菌属(Porphyromonas)、互养菌门(Synergistetes)和消化链球菌科(Peptostreptococcaceae)(Griffen et al., 2012; Abusleme et al., 2013),以及与侵袭性牙周炎相关的伴放线聚集杆菌(Actinomyces actinomycetemcomitans)(Slots et al., 1980; Haubek et al., 2008)。
许多研究调查了特定门和属的丰度如何区分牙周健康与疾病。尽管研究之间存在许多差异,但不同研究者均发现,在牙周炎中,最丰富的四个门(拟杆菌门(Bacteroidetes)、放线菌门(Actinobacteria)、变形菌门(Proteobacteria)和厚壁菌门(Firmicutes))的相对比例发生变化,更具体地说,是变形菌门和放线菌门丰度减少,而拟杆菌门和厚壁菌门丰度增加,这一现象在不同研究者中是一致的(Griffen et al., 2012; Wang et al., 2013; Cai et al., 2021)。在属水平上,密螺旋体属(Treponema)在牙周病中代表性过高(Abusleme et al., 2013; Cai et al., 2021),而相反,罗氏菌属(Rothia)、放线菌属(Actinomyces)和奈瑟菌属(Neisseria)在健康状态下的群落中占主导地位(Abusleme et al., 2013; Rosier et al., 2020; Cai et al., 2021)。随着对牙周炎病因学相关物种理解的加深,这些病原体、病原共生菌和口腔共生菌之间及相互间的关系揭示了一个复杂的网络,该网络由口腔微生物组成员之间的拮抗和协同相互作用组成。例如,已证明病原共生菌具核梭杆菌(Fusobacterium nucleatum)能提高假定的牙周病原体牙龈卟啉单胞菌在有氧条件下的生存能力(Bradshaw et al., 1998)。病原体-病原体之间的增强作用已通过齿垢密螺旋体和牙龈卟啉单胞菌之间的互惠相互作用得到证明,其中齿垢密螺旋体从牙龈卟啉单胞菌代谢产生的琥珀酸中获益(Grenier, 1992)。此外,Tan等人(2014)发现,与单一培养相比,共培养时齿垢密螺旋体和牙龈卟啉单胞菌的密度显著增加(Yamada et al., 2005; Ng et al., 2019)。研究还发现,这两个物种在共培养中通过改变许多基因的表达来相互应答,包括齿垢密螺旋体中谷氨酸和甘氨酸的分解代谢改变,以及牙龈卟啉单胞体中脂肪酸和焦磷酸硫胺素合成的改变(Tan et al., 2014)。此外,均与局限性侵袭性牙周炎相关的伴放线聚集杆菌和啮蚀艾肯菌表现出互惠的群落生长(Wang et al., 2013)。牙周病原体的双物种相互作用与疾病严重程度的关系也在小鼠模型中得到了证实,其中福赛斯坦纳菌和具核梭杆菌的共感染与单一物种感染组相比,诱导了显著更严重的牙槽骨丧失(Settem et al., 2012)。此外,共生菌-病原体相互作用在疾病加剧中的作用已通过戈登链球菌(Streptococcus gordonii)与牙龈卟啉单胞菌的双物种感染得到证实,与单一物种感染相比,这种感染促进了显著更严重的骨丧失(Daep et al., 2011)。与病原体-共生菌相互作用相一致,发现牙龈卟啉单胞菌与口腔链球菌(Streptococcus oralis)有很强的关联性(Maeda et al., 2004)。
Peterson等人(2014)的一项研究分析了口腔微生物组的合作与拮抗关系,揭示了大多数物种间相互作用是正相关的。这个正相关的网络包括拟杆菌属(Bacteroides)、真杆菌属(Eubacterium)、啮蚀艾肯菌属(Filifactor)、梭杆菌属(Fusobacterium)、消化链球菌属(Peptostreptococcus)、弯曲杆菌属(Campylobacter)、约翰逊菌属(Johnsonella)和细小单胞菌属(Parvimonas)(Peterson et al., 2014)。该研究支持了其他研究结果,这些结果已确定,由于种间协同和拮抗作用,单一物种丰度的变化通常伴随着其他物种的同时变化(Henne et al., 2014; Zhou et al., 2016; Abusleme et al., 2021)。为了揭示与特定转录本相关的功能,该研究还分析了微生物样本的转录组,发现编码核糖体亚基生物发生和碳水化合物利用的转录本在总样本中最丰富(分别为8.9%和10%)。他们还发现大多数应激反应转录本(50-75%)与氧化应激有关(Peterson et al., 2014)。尽管该研究未专门关注与牙周病相关的功能网络,但它仍然强调了不仅了解口腔微生物组的组成,而且了解健康状态下存在的、在疾病状态下可能被扰动的功能网络的重要性。必须对健康和疾病中的协同关系,以及这些相互作用如何共同转化为群落结构变化和疾病出现、进展、严重程度及治疗反应进行更多研究(Takahashi, 2015)。
结构决定功能利用多组学方法来解决微生物群落功能和潜在机制的问题,进一步促进了我们对健康与牙周炎中微生物组成的理解,并且还鉴定了在牙周病中代表性过高的功能基因和微生物代谢途径。Wang等人(2013)发现,在牙周炎中,四个最丰富的门(拟杆菌门、放线菌门、变形菌门和厚壁菌门)之间存在显著差异,在患病队列中,聚糖生物合成和代谢代表性过高,而碳水化合物代谢、氨基酸代谢、能量代谢、脂质代谢、膜转运和信号转导则代表性不足(Wang et al., 2013)。对来自九篇同行评审出版物的汇总数据(共包含来自牙周炎患者和健康受试者的943个龈下样本)进行的宏基因组分析,鉴定出每个队列特有的富集途径:细胞运动性、细胞加工和信号传导、核苷酸代谢、辅因子和维生素的代谢以及神经系统功能存在显著差异(p<0.05),牙周炎患者的细菌运动蛋白及其组装增加。此外,酮体的合成与降解、氮代谢和硫代谢也存在显著差异(p<0.05)(Cai et al., 2021)。
在一项实验性牙龈炎模型的多组学分析中,发现停止口腔卫生措施后24至72小时内,微生物组成、代谢产物产生和唾液细胞因子均发生改变,从而提示了疾病发生和进展的关键窗口期。随后将实验性牙龈炎模型的结果与先前发表的微生物组数据集的原始数据进行比较。研究发现,不同研究之间的微生物群落变化存在深刻的相似性,这些研究的队列涵盖英国、美国和中国(Huang et al., 2021)。Yost等人(2015)的一项研究将患有活动性和稳定性牙周炎个体的龈下样本与先前关于牙周特征的研究进行了比较。在定义疾病与健康状态的微生物群落中鉴定出了功能特征,患病组中与转运、蛋白水解、蛋白激酶C激活G蛋白偶联受体信号通路和抗生素反应相关的红色复合体基因上调,而与钴胺素(维生素B12)生物合成相关的基因下调。重要的是,该研究确定,多种未明确定义为假定牙周病原体的物种,包括轻型链球菌(Streptococcus mitis)、中间链球菌(Streptococcus intermedius)和细小韦荣球菌(Veillonella parvula),也对疾病进展有贡献。这些发现强调了微生物群落组成和功能失调在驱动牙周病发病机制中的作用(Yost et al., 2015)。
抗生素牙周炎作为一种菌群失调的复杂多微生物生物膜的特性,导致其治疗困难。更复杂的是,口腔微生物组是移动抗生素抗性基因的重要储存库,这些基因可以转移给病原微生物(Roberts and Mullany, 2010; Carr et al., 2020)。Rams等人的一项研究发现,74.2%的患者(n=400名患有慢性牙周炎的成年人)的牙周病原体对至少一种测试的抗生素(多西环素、阿莫西林、甲硝唑或克林霉素)具有抗性(Rams et al., 2013)。Sgolastra等人(2021)完成了对21项慢性牙周炎随机临床试验的系统综述,发现与单纯进行刮治和根面平整相比,刮治和根面平整联合阿莫西林(AMX)+甲硝唑(MTZ)在6个月和12个月时达到了最高的探诊深度减少和临床附着水平获得(Sgolastra et al., 2021)。尽管此类治疗已被证明更成功,但随着抗菌素耐药性发病率的上升,必须考虑使用广谱抗生素的全身性影响。越来越多的研究将微生物组的扰动与抗生素使用联系起来(Blaser, 2016; Faber et al., 2016; Mohajeri et al., 2018; Maier et al., 2021)。世界卫生组织(WHO)已将抗菌素耐药性列为人类面临的十大全球健康威胁之一(World Health Organization, 2014)。基于这些考虑,必须实施创新的靶向方法来对抗牙周炎。其中一种治疗方法是新型抗生素阿米西昔(amixicile),它通过抑制丙酮酸-铁氧还蛋白氧化还原酶(PFOR)来抑制与牙周炎相关的厌氧菌,包括牙龈卟啉单胞菌、福赛斯坦纳菌、齿垢密螺旋体和具核梭杆菌(Hutcherson et al., 2017; Gui et al., 2020)。阿米西昔靶向PFOR的辅因子而非酶本身,这降低了因突变而产生抗生素抗性的风险(Hutcherson et al., 2017)。此外,已发现阿米西昔能抑制口腔厌氧菌的生长,同时不影响耐氧菌(Hutcherson et al., 2017; Gui et al., 2020)。将靶向抗菌药物与支持恢复健康口腔微生物组的治疗方法相结合的多方面策略,可能会改善牙周炎患者的健康结果。
牙周病中的口腔病毒组口腔微生物群在牙周病进展中的作用主要集中在与细菌种类相关的菌群失调上。然而,由噬菌体、病毒和逆转录病毒组成的口腔病毒组在牙周炎口腔微生物群中的作用在很大程度上仍然有限。病毒已被认为是健康和疾病状态下口腔微生物群的组成部分(Ly et al., 2014),某些病毒,如EB病毒、单纯疱疹病毒和巨细胞病毒,已被牵涉到多种口腔病理中(Bilder et al., 2013; Kato et al., 2013; Contreras et al., 2014; Slots, 2015; Zhu et al., 2015; Lu et al., 2016; Gao et al., 2017; Naqvi et al., 2018; Slots, 2019)。Martínez等人(2021)全面概述了关于病毒在牙周病病因学中作用的研究发现,包括病毒通过与牙周病原体相互作用、病毒感染宿主细胞以及病毒介导的生物膜失调来加剧疾病。然而,相比之下,口腔病毒组在牙周炎中的重要性尚未完全阐明。采用包含牙龈卟啉单胞菌、具核梭杆菌、齿垢密螺旋体和福赛斯坦纳菌的接种物,在多微生物感染的小鼠模型中进行了为期8周的研究,以了解感染对牙周膜特性、牙槽骨丧失、宿主血清免疫谱和常驻口腔微生物群的影响(Gao et al., 2020)。在给予感染前(抗生素治疗后)以及感染后1、4和8周收集口腔拭子,以了解口腔微生物群随疾病进展随时间的变化。利用上颌骨和下颌骨标本进行宏基因组鸟枪法测序,以检查口腔微生物群对病原性接种物的响应扰动。对照组和感染组之间的细菌群落组成和多样性无显著差异(p=0.92)。然而,感染组和对照组之间检测到口腔病毒组的显著变化(p=0.04)。感染组中与骨丧失增加相关的病毒成员包括γ逆转录病毒(Gammaretrovirus)、猪C型肿瘤病毒(Porcine type-C oncovirus)、蝙蝠γ逆转录病毒(Bat Gammetrovirus)和金黄地鼠胞内A型颗粒H18(Golden hamster intracisternal A particle H18)。猪C型肿瘤病毒还与牙周膜间隙增加相关。关于免疫反应,发现长臂猿白血病病毒(Gibbon ape leukemia virus)与免疫基因Tnfsf 14之间存在弱关联(Gao et al., 2020)。病毒组在其他慢性疾病状态中的重要作用也已得到认识,其中一些疾病也与牙周炎相关,包括炎症性肠病、糖尿病和癌症(Santiago-Rodriguez and Hollister, 2019)。
口腔中存在的大多数病毒是噬菌体(Pride et al., 2012; Robles-Sikisaka et al., 2013),其中许多属于有尾噬菌体目(Caudovirus)的科,即长尾噬菌体科(Siphoviridae)、肌尾噬菌体科(Myoviridae)和短尾噬菌体科(Podoviridae)(Wichels et al., 1998; Sullivan et al., 2003)。与口腔微生物组的细菌组成部分一样,病毒组也受到环境因素的影响,并且在个体之间差异很大(Pride et al., 2012; Robles-Sikisaka et al., 2013; Abeles et al., 2014)。此外,口腔病毒已被证明能引发宿主免疫反应,从而暗示了其在宿主免疫与口腔微生物群之间相互影响中在牙周病发病机制中的作用(图1)(Duerkop and Hooper, 2013; Abeles et al., 2014)。Ly等人(2014)的一项研究试图定义健康与牙周炎中口腔病毒组的区分特征。从16名牙周健康或有轻度至显著牙周炎的受试者中收集唾液和口腔生物膜样本。唾液病毒组主要根据牙周病状态进行聚类。这在龈上和龈下生物膜样本中也得到了反映,其中显著牙周炎受试者的病毒组聚类在一起。对于龈下菌斑样本,与轻度牙周炎或健康状态的受试者相比,重度牙周病受试者中共享病毒组同源物的比例更高(p=0.002)。在牙周健康受试者与患病受试者之间,关于口腔生物地理位点也存在显著差异。在健康受试者中,长尾噬菌体科被鉴定为最丰富的病毒科。健康受试者每个口腔内位点的短尾噬菌体科丰度也相似,然而,肌尾噬菌体科的相对丰度随生物地理位点和疾病状态的变化而有很大差异。虽然与患病队列相比,健康个体唾液中肌尾噬菌体科的丰度显著更高,但在牙周炎队列的龈下菌斑中,其丰度也高于健康受试者。然而,在龈上菌斑中没有观察到病毒科的显著差异。总之,这些发现表明,由于肌尾噬菌体科丰度增加,龈下菌斑中的口腔病毒组发生了显著改变。在更高的分类水平上,属于厚壁菌门和变形菌门的病毒在唾液中最为丰富,其次是拟杆菌门和放线菌门。相反,与变形菌门和拟杆菌门相关的病毒在生物膜样本中最丰富。噬菌体是口腔中最丰富的病毒,作为不同微生物生态系统中细菌多样性的重要驱动因素,因此可能操纵牙周炎中细菌介导的各个方面(Willner et al., 2009; Reyes et al., 2010; Minot et al., 2011; Foulongne et al., 2012; Pride et al., 2012; Minot et al., 2013; Ly et al., 2014)。因此,更好地了解口腔病毒组对于其潜在的牙周病直接影响及其在细菌介导的疾病加剧中可能发挥的作用至关重要。
牙周免疫的必要性与陷阱龈上和龈下多微生物生物膜群落的持续累积会在牙周组织内引发持续的宿主免疫反应(Hajishengallis et al., 2020)。如果去除微生物生物膜,并且炎症仅限于牙龈上皮和结缔组织受累,则此炎症过程是可逆的。然而,如果生物膜持续累积并导致更深的牙周组织受累,例如牙龈沟加深、牙周膜破坏和牙槽骨丧失,则炎症过程变得不可逆,此时疾病从牙龈炎进展为牙周炎(Armitage, 2004)。这种持续的炎症因牙周病原体的过度生长而进一步加剧,这些病原体在炎症条件下得以繁盛,期间组织破坏的蛋白性副产物(即胶原蛋白分解产物、氨基酸、铁、血红素等)会强化病原体的过度生长(Hajishengallis, 2014; Herrero et al., 2018; Rosier et al., 2018)。牙周病的严重程度由炎症细胞浸润的复杂性来定义。Page和Schroeder模型描述了表征疾病进展的四个不同阶段:初始病变以中性粒细胞为主,早期病变以巨噬细胞和T细胞增多为特征,而后期形成的和晚期的病变则以B细胞和浆细胞参与为特征(Page and Schroeder, 1976)。尽管微生物刺激是疾病发生的必要条件,但宿主炎症反应是牙周组织破坏的主要驱动力(Hasturk and Kantarci, 2015; Hajishengallis and Korostoff, 2017)。
微生物-宿主炎症过程牙龈袋中病原体的存在会引发上皮细胞分泌趋化因子,将中性粒细胞从体循环招募到结合上皮(Bosshardt and Lang, 2005; Fujita et al., 2018)。中性粒细胞的保护性蛋白水解反应因此会破坏上皮,从而促进病原体更深地侵入上皮组织和固有层,加剧组织破坏和骨吸收(Bosshardt and Lang, 2005)。牙周病原体已进化出劫持和操纵宿主炎症反应的能力,既能促进炎症,又能逃避这些反应。细菌通过直接操纵参与屏障功能的宿主基因和/或蛋白质,以及通过涉及免疫调节反应的间接机制,来影响上皮屏障功能(Turner, 2009)。当口腔微生物组与宿主免疫反应之间的稳态通讯受到干扰时(无论是通过微生物还是炎症刺激),菌群失调就会持续存在,牙周炎的有害影响也会循环持续。牙周炎中的组织破坏是由TH17细胞以白细胞介素(IL)-6和IL-23依赖性方式的扩增所驱动的,这是由于微生物群落结构的变化所致(Dutzan et al., 2018)。
有害的微生物群落重塑主要归因于关键牙周病原体牙龈卟啉单胞菌的代表性增加和整合,该菌驱动细菌负荷增加、微生物群组成改变,并在特定病原体自由(SPF)小鼠中诱导显著的骨丧失。有趣的是,尽管发现它会增加细菌负荷,但牙龈卟啉单胞菌仅占总细菌数的0.01%。此外,牙龈卟啉单胞菌本身无法在无菌(GF)小鼠中驱动骨丧失,这表明其本身并非唯一导致牙周破坏的因素(Hajishengallis et al., 2011)。牙龈卟啉单胞菌还能引导在牙周病中观察到的重要炎症扰动,例如调节Toll样受体(TLR)-2和C5aR之间的相互影响。这种相互作用会破坏TLR-MyD88通路,并启动促炎性的TLR2-PI3K信号通路,该通路通过减少吞噬作用和增强牙龈卟啉单胞菌的细胞内生存来引发炎症(Maekawa et al., 2014; Makkawi et al., 2017)。
微生物-宿主组织破坏特征在牙周炎中,可以观察到细胞外基质的分解和牙周膜间隙的改变(Armitage, 2004)。最近,Malone等人描述了齿垢密螺旋体通过牙周膜细胞中的肌动蛋白重塑动力学对细胞屏障功能产生直接影响的机制(Malone et al., 2021)。免疫荧光染色显示,用齿垢密螺旋体攻击减少了肌动蛋白应力纤维的丰度,并通过Western印迹观察到的β-肌动蛋白表达下降30%加以补充。RNA测序证实了这些发现,即在齿垢密螺旋体攻击后,牙周膜细胞表现出肌动蛋白和细胞骨架相关通路的上调,包括Ras蛋白信号转导和小GTP酶介导的信号转导的调控。从这些基因中,鉴定出RASA4在齿垢密螺旋体攻击后显著上调。接下来研究了齿垢密螺旋体的效应蛋白dentilisin在肌动蛋白重组中的作用,其中纯化的dentilisin足以增强RASA4的上调。在齿垢密螺旋体攻击后,基质金属蛋白酶(MMP)-2的活化增加;因此,研究了齿垢密螺旋体介导的肌动蛋白动力学变化及其对牙周膜细胞中MMP-2活性的影响。齿垢密螺旋体显著增加了MMP-2活性,这种效应被聚合剂Jasplakinolide消除,而被解聚剂Latrunculin B增强,表明齿垢密螺旋体通过肌动蛋白解聚促进MMP-2表达(Malone et al., 2021)。
牙周病原体还通过上调宿主组织中的组织破坏基因来促进组织破坏。牙周膜成纤维细胞通过表达包括MMP在内的水解酶进行组织重塑,并且还参与产生促炎介质,如细胞因子和趋化因子。此外,牙周膜细胞调节模式识别受体和TLR的表达,这些受体有助于监测牙周组织中的微生物种类(Sun et al., 2010; Tang et al., 2011; Jönsson et al., 2011; Sokos et al., 2015; Zhang et al., 2015; Jiang et al., 2016)。未解决的TLR信号传导导致参与组织破坏的基因过度激活,例如那些编码MMP的基因(Li et al., 2011; Sapna et al., 2014; Sokos et al., 2015)。脂蛋白被认为是与TLR2刺激细菌配体相关的重要毒力因子(Sela et al., 1997; Wilson and Bernstein, 2016; Sobocińska et al., 2018)。牙周炎患者中齿垢密螺旋体水平升高伴随着牙周组织中MMP水平升高(Loesche, 1988; Ramseier et al., 2009; Ateia et al., 2018)。Ganther等人最近研究了齿垢密螺旋体通过其效应蛋白dentilisin介导的MMP表达。用齿垢密螺旋体攻击的牙周膜细胞在20个显著富集的生物学过程中,显示出参与细胞外基质受体、胶原降解和细胞外基质降解的基因表达增加(Ganther et al., 2021)。尽管不显著,但MMP-2和MMP-14在齿垢密螺旋体攻击后上调,这与先前证明它们参与牙周病的研究结果一致(Lint and Libert, 2007; Page-McCaw et al., 2007; Ateia et al., 2018)。MMP-2和MMP-14的上调是齿垢密螺旋体特有的,因为用革兰氏阴性共生菌细小韦荣球菌攻击不会导致这些MMP的上调。接下来研究了效应蛋白dentilisin对MMP调节的作用,其中用纯化的dentilisin攻击导致MMP上调。相反,用dentilisin缺陷的齿垢密螺旋体攻击不会诱导MMP活化。为了建立TLR2激活与牙周膜细胞中MMP基因调控的直接关联,进行了TLR2的shRNA敲减,并用纯化的dentilisin或齿垢密螺旋体攻击细胞。用纯化的dentilisin或齿垢密螺旋体处理后,MMP-2、-11、-14、-17和-28的表达显著增加。接下来研究了Myd88在TLR2激活中的作用,因为大多数TLR通过MyD88进行信号传导(Wang et al., 2017)。使用shRNA敲减MyD88。与对照样本相比,用齿垢密螺旋体或纯化的dentilisin处理的敲减细胞系未诱导MMP靶点上调。特异性蛋白-1(Sp-1)是与组织破坏和促炎症相关的TLR/MyD88的靶点。为了确定Sp1表达是否因牙周膜细胞中的齿垢密螺旋体而改变,用野生型齿垢密螺旋体或对照dentilisin突变体齿垢密螺旋体-CF522攻击细胞,然后使用针对Sp1的单克隆抗体进行Western blot分析。用野生型细胞处理增加了Sp1表达,而用齿垢密螺旋体-CF522攻击则未能增加。总之,这项研究将dentilisin与TLR2激活联系起来,并鉴定了可能在介导牙周病宿主炎症反应中发挥额外作用的潜在组织特异性诱导型MMP(Ganther et al., 2021)。
无辜的旁观者:细胞衰老微生物失调和宿主炎症反应的潜在机制不断发展,促进了对这些过程的更深入理解,并且牙周组织破坏发生的替代机制也持续被发现。被招募的中性粒细胞分泌促炎细胞因子和活性氧(ROS)以清除受影响组织中的病原体。宿主免疫通过进一步促进微生物失调,反而加剧了牙周病的严重程度(Ebersole et al., 2013; Cekici et al., 2014)。与此概念一致,新出现的证据表明,牙周组织的慢性炎症通过慢性暴露于炎症环境中的健康常驻细胞的细胞衰老,进一步促进炎症过程和组织破坏(Aquino-Martinez et al., 2020)。虽然ROS可以保护免受入侵细菌的侵害,但它们也可能对健康的宿主细胞造成伤害,从而诱导应激介导的DNA损伤(Barzilai and Yamamoto, 2004)。炎症过程产生的ROS会损伤常驻牙周细胞的细胞DNA。此外,暴露于细菌脂多糖(LPS)也会促进牙龈和牙槽骨细胞的DNA损伤(Cheng et al., 2015; Aquino-Martinez et al., 2020)。受损的DNA可以进行修复;然而,对基因组的慢性损伤会引起暴露细胞发生凋亡或衰老反应(Childs et al., 2014)。获得衰老表型的细胞过度表达促炎细胞因子(包括但不限于IL-6、IL-1β和IL-8)和蛋白水解酶(包括MMP-1、MMP-3、MMP-12和MMP-13)(Coppé et al., 2010; Aquino-Martinez et al., 2020; Levi et al., 2020)。这些细胞被称为具有衰老相关分泌表型(Coppé et al., 2010)。促炎信号、蛋白水解酶和ROS的分泌改变了牙周环境,加剧了作为牙周病标志的炎症细胞浸润和组织损伤。衰老细胞可能进一步促进牙周炎中的炎症正反馈循环,因为DNA损伤和慢性炎症可以驱动衰老诱导的炎症过程,而慢性炎症从而促进ROS的产生和应激介导的DNA损伤(Jurk et al., 2014; Mittal et al., 2014)。
四种主要机制可能与牙周病进展相关的衰老有关:革兰氏阴性病原体的持续攻击、慢性炎症、受损组织的持续修复以及细菌诱导的免疫抑制。持续暴露于革兰氏阴性病原体的LPS会在牙龈成纤维细胞中诱导遗传毒性效应(Cheng et al., 2015)。研究表明,持续暴露于牙龈卟啉单胞菌的LPS会导致牙槽骨细胞内出现由过早DNA损伤驱动的衰老(Aquino-Martinez et al., 2020)。此外,伴放线聚集杆菌分泌的细胞致死性扩张毒素会在人牙龈上皮细胞中诱导双链断裂,导致凋亡或细胞衰老(Guerra et al., 2011; DiRienzo, 2014; Grasso and Frisan, 2015)。慢性炎症通过持续产生ROS和氧化应激损害细胞DNA(Martindale and Holbrook, 2002; Van Houten et al., 2018)。由于LPS暴露,牙龈成纤维细胞中产生的ROS诱导了DNA损伤,表现为抗凋亡和促凋亡蛋白表达增加。在修复和/或再生的组织中也鉴定出了衰老细胞(Coppé et al., 2010; Campisi, 2013)。牙龈上皮持续的修复和更新能力,尽管作为对机械损伤和细菌攻击的细胞防御机制发挥作用,但也可能导致牙周组织破坏(Bulut et al., 2006; Ji et al., 2015)。支持这一假设的是,雷帕霉素(一种mTOR通路抑制剂)延迟了衰老特征的出现,并保留了健康牙龈成纤维细胞的有丝分裂潜能(Xia et al., 2017)。衰老细胞也会被宿主免疫系统识别以检测和清除受损细胞。然而,多种牙周病原体(包括牙龈卟啉单胞菌、伴放线聚集杆菌和福赛斯坦纳菌)的免疫抑制能力可能会促进衰老细胞的积累。关于细胞衰老在牙周病进展中作用的研究发现,可能有助于更好地理解慢性炎症在牙周炎中的作用,并通过抗衰老治疗策略开辟疾病预防的新途径(Aquino-Martinez et al., 2020)。
坚守阵地:稳态牙龈屏障防御尽管宿主炎症反应在牙龈疾病进展中发挥作用,但牙龈的屏障免疫至关重要,因为该部位容易受到常规咀嚼挑战、微生物参与以及饮食和空气传播抗原的攻击(Dutzan et al., 2016)。与其他生理屏障部位相比,牙龈的这些组织特异性信号导致牙周组织内产生独特的免疫反应。衬在牙龈内部的口腔上皮屏障特别容易受到细菌攻击。牙龈沟壁衬有非角化的沟上皮,该上皮向沟底逐渐变薄,在沟底处黏膜与牙齿的釉质表面相遇。在这个相互作用点,上皮过渡为结合上皮,该上皮特别脆弱,因为它逐渐变细至仅1-2层细胞的厚度。在这里,上皮通过半桥粒附着在牙齿表面,这种连接具有高度通透性(Dutzan et al., 2016)。在此部位,龈沟液流动并含有宿主免疫成分,包括血浆蛋白、细胞因子、免疫球蛋白和各种免疫细胞(Buclkacz and Carranza, 2012; Lamster, 1997)。然而,结合上皮保持了对损伤作出反应的再生能力(Nanci, 2017),这种再生能力反映了这个屏障部位是独特地适应以承受各种细菌、炎症和机械刺激的(Nanci, 2017)。
牙龈处免疫稳态的微生物组依赖性和非依赖性机制已被确定,其中微生物非依赖性机制在稳态免疫中占据主导地位(Dutzan et al., 2017)。通过结合上皮,中性粒细胞迁移进入牙周组织。在健康状态下,中性粒细胞构成了龈沟处大多数免疫细胞,占白细胞的95%(Dutzan et al., 2016; Rijkschroeff et al., 2016)。无菌小鼠中中性粒细胞的存在证明了中性粒细胞在牙龈中的监视作用是独立于微生物群的。中性粒细胞对于通过下调IL-23以响应微生物介导的炎症来消除免疫反应也至关重要(Serhan et al., 2008; Moutsopoulos et al., 2014; Ley, 2017; Moutsopoulos et al., 2017)。中性粒细胞对此类攻击的反应功能障碍(如通过影响粒细胞生成、中性粒细胞招募和外渗的各种单基因突变所证明,这些突变导致严重的牙周炎表型)强调了中性粒细胞对维持牙周健康的重要性。然而,中性粒细胞代表性增加以响应炎症是牙周炎中异常炎症相互强化的标志。因此,中性粒细胞的微妙平衡对于牙周免疫至关重要(Kantarci et al., 2003; Eskan et al., 2012; Billings et al., 2017)。
树突状细胞、巨噬细胞和单核细胞也构成了健康状态下的牙龈免疫网络(Hovav, 2014; Dutzan et al., 2016)。这些免疫细胞在维持牙龈屏障完整性和对细菌攻击的免疫调节中发挥作用(Steinmetz et al., 2016)。多种树突状细胞群存在于牙龈组织中,并在炎症期间增加(Jotwani et al., 2001; Jotwani and Cutler, 2003)。T细胞、B细胞和先天淋巴细胞也存在于健康的牙龈组织中。虽然先天淋巴细胞和B细胞在健康状态下的作用尚待完全阐明,但大量注意力已集中在牙龈中T细胞群的作用上(Dutzan et al., 2016; Dutzan and Abusleme, 2019)。T细胞群对于牙周健康和牙周病病理学至关重要。在健康状态下,具有记忆表型的CD4+ T细胞在牙龈组织中占主导地位(Dutzan et al., 2016)。CD4+和CD8+记忆T细胞均产生IL-1、IL-17和IFN-γ细胞因子。TH17细胞在宿主免疫稳态的微生物非依赖性机制中的作用已获得越来越多的关注。Dutzan等人发现,TH17细胞在牙龈组织中的代表性随着年龄增长而增加,且这种增加是以不依赖于微生物组的方式发生的(Dutzan et al., 2017; Dutzan et al., 2018)。这与其他屏障部位(如肠上皮衬里和皮肤)形成对比,在这些部位,TH17细胞的扩增依赖于微生物的存在(Ivanov et al., 2009; Naik et al., 2012)。咀嚼力造成的机械损伤导致牙龈组织中TH17扩增,从而证明了牙龈组织对这种独特的组织特异性信号产生了独特的免疫反应(Dutzan et al., 2017)。咀嚼挑战还以IL-6依赖的方式促进了先天屏障防御(Dutzan et al., 2017; Dutzan et al., 2018)。因此,TH17细胞在应对牙龈处出现的非微生物依赖性刺激(如机械损伤)时表现出保护作用。与此相对,IL-17+ TH17细胞的扩增在牙周炎和健康状态中都是特征,分别响应微生物和机械刺激(Dutzan and Abusleme, 2019; Takahashi et al., 2019)。在牙周健康与牙周疾病中,IL-17的细胞来源被区分开来:在稳态条件下,TCRγδ+ T细胞是IL-17的主要来源,而TH17细胞在疾病中构成占主导地位的IL-17+群体。与在健康状态下观察到的微生物非依赖性机制相反,实验性牙周炎中TH17的扩增依赖于微生物失调,以及IL-6和IL-23。有趣的是,16S rRNA测序并未揭示特定细菌候选物在驱动失调中的作用,因为TH17扩增是针对靶向特定细菌种群的多种抗生素方案诱导的整体微生物组变化而发生的(Dutzan et al., 2018)。
口腔健康在全身健康中的作用牙周病发病率和严重程度的增加与远离口腔的多种病理状况有关。迄今为止,与牙周病相关的全身性疾病状态中,最受关注的是心血管疾病、类风湿性关节炎和糖尿病(Hajishengallis and Chavakis, 2021)。各种全身性病理的口腔表现,例如克罗恩病,也已得到认识(Pittock et al., 2001)。然而,近年来,人们越来越认识到口腔健康在加剧甚至在某些情况下驱动全身性病理中的作用。远离口腔的其他病理状况,如阿尔茨海默病,因其与牙周健康的关联而获得了广泛关注。这些发现引发了人们对口腔健康与全身健康关联的更广泛认识。在此,我们讨论进一步的研究,这些研究证明了牙周病与其他全身性疾病之间新发现的关联,以及牙周炎在加剧远离口腔部位的多种病理状态中的作用。
阿尔茨海默病与认知功能障碍阿尔茨海默病的特征是从轻度认知障碍、记忆丧失、语言和沟通障碍,以及心理和行为障碍进展的神经退行性病变(Qiu et al., 2009)。患有阿尔茨海默病的患者通常表现出受损的牙周健康(Martande et al., 2014; Aragón et al., 2018; D’Alessandro et al., 2018),这表面上是由自我护理能力下降和护理人员对口腔卫生的忽视引起的。然而,越来越多的人认识到牙周病作为阿尔茨海默病潜在促成因素的可能影响,例如通过增加促炎介质(如C反应蛋白(CRP)、IL-6、IL-1β和TNF-α)的水平,这些介质可能有助于突触毒性β-淀粉样蛋白和神经原纤维缠结的沉积(Gaur and Agnihotri, 2015)。Hu等人(2021)的一项荟萃分析全面回顾了过去十年间关于牙周病作为阿尔茨海默病发展促成因素的相关研究。在162篇出版物中,有13项研究符合荟萃分析的标准。纳入的8项研究的汇总结果表明,与健康患者队列相比,牙周病患者患阿尔茨海默病的风险显著更高(Cestari et al., 2016; Chen et al., 2017; Choi et al., 2019; Tiisanoja et al., 2019; de Oliveira Araújo et al., 2021)。此外,牙周病还与轻度认知障碍(正常认知与痴呆之间的过渡阶段,常被视为阿尔茨海默病的主要早期临床表现)的发展相关联。虽然未发现轻度/中度牙周炎与阿尔茨海默病风险增加之间存在显著关联,但重度牙周病与之显著相关。
已确定牙周病可能导致阿尔茨海默病的三种主要机制如下:
1)外周促炎细胞因子增加,通过神经、体液和细胞机制全身性影响大脑(Schmidt et al., 2002; Holmes et al., 2003; Engelhart et al., 2004);
2)牙周细菌及相关分子通过血液和/或颅神经异位迁移至大脑;
3)软脑膜可能充当牙周病原体与脑内小胶质细胞之间的沟通方式(Hashioka et al., 2019)。
牙周病原体异位迁移至脑组织已通过阿尔茨海默病患者尸检标本中牙龈卟啉单胞菌及相关牙龈素以及密螺旋体属的存在得到证实(Riviere et al., 2002)。在小鼠中,口服牙龈卟啉单胞菌感染后,也观察到牙周病原体异位迁移至脑组织,表现为脑内病原体浸润以及已知构成阿尔茨海默病中淀粉样斑块的β1-42淀粉样蛋白水平增加。牙龈素具有切割tau蛋白的能力,提示牙龈卟啉单胞菌在tau蛋白磷酸化和随之而来的阿尔茨海默病病理中观察到的不溶性tau蛋白积累中的作用(Konig et al., 2016; Dominy et al., 2019)。支持这一点的是,在尸检标本中,牙龈素负荷与tau蛋白和泛素负荷相关。此外,与用野生型牙龈卟啉单胞菌处理的组相比,用牙龈素缺陷型牙龈卟啉单胞菌处理的小鼠未出现β1-42淀粉样蛋白增加。其他口腔来源的细菌也与阿尔茨海默病有关,包括直肠弯曲杆菌(Campylobacter rectus)和产黑色素普雷沃菌(Prevotella melaninogenica)(Beydoun et al., 2020)。此外,在省略感染的小鼠牙周炎模型中,仍观察到不溶性β-淀粉样蛋白水平升高和神经炎症增加,这进一步支持了其他口腔来源细菌在促进阿尔茨海默病中的作用(Kantarci et al., 2018; Kantarci et al., 2020; Hajishengallis and Chavakis, 2021)。
迄今为止,大多数研究仅在老年人群中描述了牙周病与阿尔茨海默病风险的关联。然而,牙周病状况对较年轻人群阿尔茨海默病风险的影响也是一个重要的关注点,因为阿尔茨海默病病理通常在较年轻人群中主要表现为轻度认知能力下降。此外,在较少有机会出现可能混淆研究结果的合并症的较年轻人群中,可以更明确地确立阿尔茨海默病与牙周病之间的关联。最重要的是,将牙周病确定为阿尔茨海默病发展的一个重要风险因素,可能为阿尔茨海默病提供额外的检测和干预机会(Hategan et al., 2021)。Hategan等人(2021)通过延迟回忆和即时记忆评估了60名患有慢性牙周炎、侵袭性牙周炎或无牙周病状况的年轻个体(<45岁)的情景记忆,测试采用雷伊听觉言语学习测试(RAVLT)。还使用了蒙特利尔认知评估测试(MOCA)、简易精神状态检查表(MMSE)和布拉格测试(Lam et al., 2013; Hategan et al., 2021)。牙周炎受试者的延迟和即时回忆得分显著较低,不同牙周病组之间的RAVLT回忆得分存在显著差异。此外,与慢性和健康队列相比,侵袭性牙周炎组的RAVLT延迟和即时回忆得分也较低。MOCA回忆得分也与之一致。唾液IL-1β和TNF-α也作为与牙周炎相关的促炎分子进行了评估。虽然TNF-α水平与任何认知测试均无显著关联,但IL-1β水平与雷伊即时回忆能力显著相关(Hategan et al., 2021)。这项研究最终表明,与患有侵袭性牙周病的年轻健康受试者相比,没有牙周病的年轻健康受试者具有更好的情景记忆和学习速度。
系统性红斑狼疮系统性红斑狼疮(SLE)和牙周病具有共同的致病因素,包括环境、遗传、免疫和微生物等方面的因素。此外,SLE的口腔表现,包括但不限于黏膜溃疡、口干、唾液分泌减少、盘状病变、唇炎和红斑样斑块,也已被注意到(Khatibi et al., 2012; Benli et al., 2021),这进一步支持了SLE与牙周病状况之间可能的联系。此外,SLE患者中牙周炎的患病率相当高,占所有SLE患者的60%至94%(Calderaro et al., 2016),并且与非SLE牙周炎个体相比,SLE患者表现出更严重的牙周病,具有更大的临床附着丧失和增加的探诊深度(Wang et al., 2015; Corrêa et al., 2017; Zhang et al., 2017)。牙周炎中的口腔失调可能引发SLE中观察到的异常炎症反应。相反,SLE中的遗传和环境风险因素可能有助于牙周组织中持续炎症的启动或维持。多项研究已确定了SLE可能通过免疫失调、组织破坏和龈下微生物群改变来加剧牙周病发病机制的机制。SLE诱导的牙周组织炎症变化可能促进失调的龈下微生物群。支持这一点的是,与患有牙周病的非SLE受试者相比,SLE/牙周病患者唾液中炎性细胞因子IL-6、IL-17A和IL-33增加(Bunte and Beikler, 2019)。有趣的是,SLE患者还表现出针对牙周病相关口腔细菌(如伴放线聚集杆菌、牙龈卟啉单胞菌和齿垢密螺旋体)的血清抗体升高。牙周病与SLE之间也存在遗传联系;与SLE相关的遗传变异,如Fcγ受体基因型PIIA、PIIIA和PIIIb,在同时患有SLE和牙周病的患者中更高。这一发现支持SLE与牙周炎之间的联系可能涉及Fcγ受体的多态性。此外,具有合并Fcγ受体风险等位基因的SLE患者与无该病的SLE患者相比,表现出更严重的牙周病(Kobayashi et al., 2007; Kobayashi et al., 2010)。越来越多的证据也表明牙周病在加剧SLE发病机制中的作用。与SLE诱导的牙周炎恶化相对应,牙周病原体可能导致牙周组织中TLR的过度免疫激活,从而促进全身性自身免疫(Getts et al., 2020)。与健康个体相比,SLE患者还表现出更高的细菌负荷和口腔病原体的相对丰度增加(Jensen et al., 1999; Sete et al., 2016; Corrêa et al., 2017)。此外,发现牙周治疗可以改善SLE患者对免疫抑制治疗的反应,从而支持牙周炎可能加剧SLE并因此作为一个潜在的可改变风险因素的观点(Fabbri et al., 2014)。
血液与牙周病相关的全身性炎症性疾病状态被假设是由于牙周病原体和/或牙周炎相关的炎性介质(如IL-1、IL-6、CRP和纤维蛋白原)迁移进入血流所致(Genco and Van Dyke, 2010; Bokhari et al., 2012; D’Aiuto et al., 2013; Schenkein et al., 2020)。牙周健康对全身炎症过程的影响通过局部治疗牙周炎可减轻全身炎症标志物而得以凸显(Tonetti, 2009; Bokhari et al., 2012; Türer et al., 2017; D’Aiuto et al., 2018; Schenkein et al., 2020)。牙周袋的表面积约为8-20平方厘米(Rosan and Lamont, 2000),可能作为牙周病原菌、其相关副产物以及牙周炎相关免疫介质进入体循环的直接途径(Hajishengallis and Chavakis, 2021)。全身性扰动,例如由牙周病原体引起的全身性菌血症,通过骨髓中的造血干细胞和祖细胞经Toll样受体和炎性细胞因子感知。结果,造血干细胞增加增殖和髓系分化,以增加中性粒细胞和单核细胞计数(Chavakis et al., 2019)。单核细胞前体的进一步分化导致骨髓中破骨细胞前体的生成及其随后在血流中的循环。支持这一点的是,牙周炎患者的外周血单核细胞计数更高,这些细胞更倾向于成为RANKL诱导的破骨细胞(Herrera et al., 2014)。通过F-氟代脱氧葡萄糖正电子发射断层扫描-计算机断层扫描的临床影像学也显示,牙周组织内的炎性代谢活动与增加的骨髓生成和动脉炎症相关(Ishai et al., 2019)。总之,这些发现提示牙周炎诱导的造血活性增加在远端部位炎症中发挥作用。
PCR和下一代测序技术已证实血液中存在细菌DNA,其中来自肠道、生殖道、皮肤和口腔的细菌是血源性细菌的可能来源(Nikkari et al., 2001; McLaughlin et al., 2002; Amar et al., 2013; Rajendhran et al., 2013; Païssé et al., 2016; Gosiewski et al., 2017)。侵入性口腔操作,如牙周治疗、刷牙、牙科就诊和口腔手术,与短暂性菌血症有关(Tomás et al., 2012)。此外,口腔细菌如伴放线聚集杆菌、牙龈卟啉单胞菌、齿垢密螺旋体、中间普雷沃菌(Prevotella intermedia)、福赛斯坦纳菌、变形链球菌(Streptococcus mutans)和血链球菌(Streptococcus sanguinis)已在心血管病变中被鉴定出来,并通常与心血管疾病相关(Ford et al., 2005; Kozarov et al., 2005; Gaetti-Jardim et al., 2009; Leishman et al., 2010; Rafferty et al., 2011; Armingohar et al., 2014)。大多数血源性细菌DNA含量主要被归为变形菌门(80-87%),其次是放线菌门和拟杆菌门,这表明血液中大多数细菌DNA来源于肠道微生物群(Païssé et al., 2016)。然而,这些研究仅考虑了总DNA,并未区分裂解的和完整的细菌细胞,因此未能反映血液中发现的活细菌群体(Whittle et al., 2019)。Emery等人(2021)最近采用MolYsis Complete5系统来仅鉴定牙周健康和牙周病队列血液中的完整细菌细胞。与通常鉴定的源自肠道的变形菌门相反,该研究另发现43-52%的血源性细菌来自口腔,变形菌门仅占低水平。厚壁菌门,包括链球菌属物种,占健康队列中鉴定出的所有细菌序列的近65%,在牙周炎中该数字仅略有增加。后续按降序排列的组别是放线菌门、拟杆菌门、梭杆菌门和螺旋体门,它们在健康和患病队列中的百分比相似。只有两个分类群在健康和患病队列之间显示出显著不同的水平,但两者仅占总微生物群的次要组成部分:糖细菌门(Saccharibacteria)在患病队列中不存在,而变形菌门、δ-变形菌纲(Deltaproteobacteria)和黏球菌目(Myxococcales)在健康队列中更高(Emery et al., 2021)。
炎症性肠病口腔与炎症性肠病的相关性通过肠外表现得以证明,例如克罗恩病可表现为颊黏膜、舌、唇、牙齿和牙周组织的病变(Muhvić-Urek et al., 2016)。重要的是,IBD的口腔受累发生率为0.5-20%(Pittock et al., 2001; Katz et al., 2003; Zbar et al., 2012; Skrzat et al., 2017)。此外,与健康队列相比,IBD患者中牙周炎的患病率和严重程度更高,这证明了肠道健康对口腔的作用(Habashneh et al., 2012; Vavricka et al., 2013)。然而,最近的证据也表明,这种关系本质上是双向的,牙周健康是肠道健康和IBD发病机制的重要因素。例如,在克罗恩病的小鼠模型中,小鼠自发发展为牙周炎症,且牙周炎的严重程度与回肠炎症呈正相关(Pietropaoli et al., 2014)。此外,口腔细菌如聚集杆菌属(Aggregatibacter)、弯曲杆菌属(Campylobacter)、肠杆菌科(Enterobacteria)、梭杆菌属(Fusobacterium)、孪生球菌属(Gemella)、奈瑟菌属(Neisseria)、巴斯德菌属(Pastruella)、消化链球菌属(Peptostreptococcus)和链球菌属(Streptococcus)物种在IBD队列的黏膜组织中富集(Dinakaran et al., 2019; Kitamoto et al., 2020)。牙周炎与IBD之间的免疫学联系也被假设,即牙龈组织中由牙周病原菌局部激活的免疫细胞可以迁移到肠道,并导致异常和加剧的炎症过程(Morton et al., 2014)。
Kitamoto等人(2020)的一项综合研究通过两种潜在机制研究了牙周病对IBD严重程度的作用:
1)口腔细菌在肠道中的异位定植;
2)口腔中引发的免疫细胞迁移至肠道。
通过葡聚糖硫酸钠处理诱导实验性结肠炎的小鼠,同时接受口腔结扎诱导的牙周炎,表现出加剧的肠道炎症,其特征是TH17和TH1特征增加。对口腔和肠道微生物组的检查显示,接受实验性牙周炎和结肠炎的小鼠表现出口腔菌群失调,口腔和肠道微生物群中肠杆菌科(如克雷伯菌属(Klebsiella)和肠杆菌属(Enterobacter)物种)的代表性更高。有趣的是,仅实验性结肠炎并未导致肠杆菌科丰度增加,而且,仅实验性牙周炎也未使这些物种在肠道中富集(Kitamoto et al., 2020)。这些发现与先前的研究一致,这些研究确定了牙周炎-结肠炎患者与无口腔受累的结肠炎患者相比具有独特的微生物特征,其中与IBD相关的牙周炎富集了革兰氏阴性杆菌,如弯曲杆菌属(Liu et al., 2018; Graves et al., 2019)。这些发现表明牙周病和结肠炎在加剧炎症性肠病方面具有协同效应,即健康的肠道微生物群可能抵抗牙周病原体的异位定植。
还探讨了牙周炎与IBD之间的微生物-免疫轴:IL-1β分泌升高与IBD和牙周炎均相关(Park et al., 2014; Seo et al., 2015)。用来自结扎诱导牙周炎小鼠的失调口腔微生物群定植的易患结肠炎无菌小鼠,与用健康口腔微生物群定植的无菌小鼠相比,显示出更高的IL-1β特征。进一步检查显示,产生IL-1β的细胞主要由炎性巨噬细胞组成。IL-1β也被确定为口腔病原体介导的肠道炎症中的一个重要因素,因为用IL-1受体拮抗剂治疗在很大程度上减轻了用牙周炎相关口腔微生物群定植的无菌小鼠的结肠炎。此外,证实了口腔病原共生菌(而非肠道病原共生菌)对肠道IL-1β分泌的重要性,从而表明结肠炎中IL-1β分泌可能归因于口腔病原体。还研究了免疫细胞从牙周组织向肠道的迁移。由于同时患有实验性牙周病和结肠炎的小鼠中TH17和TH1细胞显著富集,因此提出了此类T细胞从口腔黏膜迁移到肠道的可能机制。牙周炎诱导产生了口腔病原共生菌特异性的IL-17A+ TH17记忆T细胞,这些细胞在颈淋巴结中积累。将从结扎小鼠颈淋巴结分离的口腔T记忆细胞转移到由结扎诱导牙周炎小鼠的口腔细菌定植的无菌小鼠中。T记忆细胞的转移引发了结肠炎的发展以及结肠黏膜中口腔T记忆细胞的扩增,而用健康口腔微生物群定植的无菌小鼠在转移后未观察到这种情况(Kitamoto et al., 2020)。总之,这项研究确定了将牙周炎与IBD病理联系起来的微生物学和免疫学联系:在现有结肠炎中,口腔细菌反应性T细胞迁移至肠道,随后通过口腔病原体的异位定植激活这些口腔引发的T细胞。
口腔癌牙周病已通过微生物和免疫机制被牵涉到口腔鳞状细胞癌(OSCC)的加剧中。牙周炎特征性的口腔微生物群内病理性微生物变化导致假定牙周病原体(包括牙龈卟啉单胞菌、齿垢密螺旋体和福赛斯坦纳菌)的相对丰度增加,这些病原体出现在口腔生物膜发育的后期阶段。此类病原体丰度的增加与牙周病严重程度相关(Simonson et al., 1988; Yoshida et al., 2004)。口腔微生物群的病理性变化已与口腔癌相关联(Whitmore and Lamont, 2014),并且特定的微生物变化与头颈部鳞状细胞癌的原发性和转移性相关(图1)(Shin et al., 2017)。虽然已经提出了牙周炎期间口腔微生物群的病理性变化与OSCC之间的这种关联,但这些疾病状态协同作用的潜在机制在很大程度上仍未得到探索。Kamarajan等人(Kamarajan et al., 2020)最近通过测量特定牙周病原体(包括牙龈卟啉单胞菌、福赛斯坦纳菌和具核梭杆菌)对细胞迁移、侵袭、干性和肿瘤侵袭性的影响,研究了它们在OSCC癌变中的作用,并确定了这些生物体促进OSCC进展的可能机制。通过划痕迁移实验评估了牙周病原体对OSCC细胞迁移的影响,结果显示每种病原体均促进了细胞侵袭的增加。每种病原体还增加了OSCC细胞的肿瘤球形成能力。小鼠口底模型证实了体外发现,即注射了病原体攻击的OSCC细胞的小鼠与注射了无病原体OSCC细胞的小鼠相比,表现出增加的肿瘤负荷。由于整合素αV是OSCC迁移的核心,为了更好地理清牙周病原体在OSCC发病机制中的机制基础,还研究了每种病原体如何利用整合素αV来促进细胞迁移和干性增加。与对照组相比,用病原体攻击后,OSCC细胞中整合素αV显著上调。相反,在整合素αV表达受抑制后,OSCC细胞中病原体诱导的迁移被减弱。由于细胞迁移依赖于整合素与细胞外基质的结合,导致黏着斑激酶的募集,因此也研究了FAK在病原体诱导的细胞迁移中的作用。齿垢密螺旋体攻击以剂量依赖性方式增强了FAK磷酸化,而抑制FAK信号传导则减弱了病原体诱导的整合素αV表达和FAK磷酸化。还研究了TLR/MyD88与整合素/FAK信号通路的交叉点,其中抑制MyD88阻止了齿垢密螺旋体对FAK的磷酸化。通过研究特定细菌因子在OSCC中的作用,进一步探讨了其机制基础。来自齿垢密螺旋体的纯化脂寡糖以及来自牙龈卟啉单胞菌和具核梭杆菌的LPS能够促进OSCC迁移。有趣的是,来自共生菌种细小韦荣球菌的LPS无法诱导相同的效应(Kamarajan et al., 2020)。
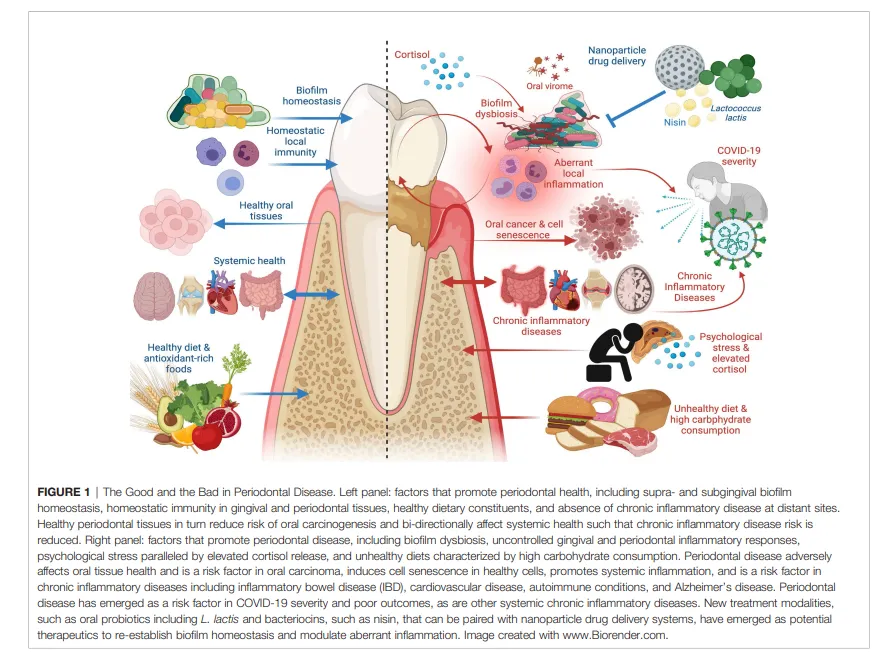
图 1 | 牙周病中的“好”与“坏”。左图:促进牙周健康的因素,包括龈上和龈下生物膜稳态、牙龈和牙周组织中的稳态免疫、健康的饮食成分,以及无远处部位的慢性炎症性疾病。健康的牙周组织反过来会降低口腔癌变的风险,并对全身健康产生双向影响,从而降低慢性炎症性疾病的风险。
右图:促进牙周病的因素,包括生物膜失调、不受控制的牙龈和牙周炎症反应、伴随皮质醇释放增加的心理压力,以及以高碳水化合物摄入为特征的不健康饮食。牙周病对口腔组织健康产生不利影响,是口腔癌的一个风险因素,会诱导健康细胞发生细胞衰老,促进全身性炎症,并且是包括炎症性肠病、心血管疾病、自身免疫性疾病和阿尔茨海默病在内的慢性炎症性疾病的风险因素。牙周病已成为增加COVID-19严重程度和导致不良结局的一个风险因素,如同其他全身性慢性炎症性疾病一样。新的治疗方式,例如口服益生菌(包括乳酸乳球菌)和细菌素(如乳链菌肽),可与纳米颗粒药物递送系统结合使用,已成为重建生物膜稳态和调节异常炎症的潜在疗法。
牙周炎引起的牙龈炎症过程会诱导牙周组织的环境改变,例如活性氧、挥发性硫化合物、乙醛、乳酸、乙酸、丁酸和异己酸水平升高(Karpiński, 2019),这些变化有可能通过增加宿主细胞DNA损伤来改变细胞行为和细胞外基质成分。这些变化促进细胞侵袭、增殖和转移性肿瘤细胞的播种。牙周炎严重程度与颊黏膜DNA损伤增加相关,表现为核芽形成增加和染色体不稳定性(Borba et al., 2019)。牙周病在OSCC加剧中的作用已在由4-硝基喹啉-1-氧化物致癌物诱导的OSCC小鼠模型中得到提示,其中与仅接受致癌物处理的无菌小鼠相比,同时口服引入牙周病原体感染的小鼠中癌性病变的大小和数量均增加(Stashenko et al., 2019)。牙周炎中的病原菌影响免疫调节网络,包括细胞因子、趋化因子和生长因子,这些可以减弱和中断免疫监视(Hajishengallis and Lambris, 2012)。这些机制不仅使病原菌能够在牙周组织中繁盛,而且还可能促进转移性肿瘤细胞的播种和/或促进原发性恶性病变(Elebyary et al., 2021)。例如,牙龈卟啉单胞菌也被证明通过激活STAT3来破坏免疫效能,从而导致免疫抑制性髓源性抑制细胞的产生,这些细胞有助于维持OSCC细胞增殖并促进其逃避免疫监视(Arjunan et al., 2018)。此外,牙周病原菌对免疫细胞群(如多形核中性粒细胞)的重编程和颠覆,形成了一个相互强化的循环,使牙龈炎症持续存在,同时促进病原体的过度生长,这也可能促进OSCC的发展。在牙周炎患者中观察到由多形核中性粒细胞产生的免疫抑制性IL-10细胞因子增加,并且这些中性粒细胞与受脂多糖刺激的调节性T细胞的相互作用诱导了IL-10的产生(Lewkowicz et al., 2016)。在OSCC患者中也观察到类似的IL-10+多形核中性粒细胞升高,从而揭示了牙周感染可能通过降低免疫调节过程来促进OSCC的可能联系。OSCC还与口腔中性粒细胞计数增加相关,这与较差的预后和较高的复发率相关(Shen et al., 2014)。
冠状病毒病-2019(COVID-19)COVID-19具有多种症状,范围从轻度表型(如发热、干咳、疲劳、味觉和/或嗅觉丧失)到更严重的症状(如呼吸困难、急性呼吸窘迫和多器官衰竭)(Sharma et al., 2016; Yang X. et al., 2020)。尽管大多数病例本质上是轻度的,但14%的确诊病例需要住院和氧气支持,5%需要重症监护室治疗,2%是致命的。严重症状的发展与过量的促炎细胞因子和全身组织破坏(称为细胞因子风暴综合征)有关(Yang Y. et al., 2020)。疾病死亡率与血清促炎介质(包括IL-6、CRP、D-二聚体和铁蛋白)水平升高呈正相关,这证明了高炎症反应与疾病严重程度之间的联系(Chen et al., 2020; Ruan et al., 2020)。此外,与全身性炎症相关的各种合并症,包括心血管疾病、肥胖和糖尿病,是COVID-19严重症状和不良预后的额外风险因素(Wu et al., 2020; Zhou et al., 2020)。牙周炎是一种慢性炎症性疾病,与全身性炎症反应和合并症相关,如前面章节所述。在Marouf等人(2021)的一项病例对照研究中,牙周状况与COVID-19严重程度一同进行了评估。病例被定义为诊断为COVID-19并出现并发症(包括重症监护室入院、通气支持和/或死亡)的患者。对照组被定义为未出现相应严重并发症的COVID-19患者。牙周状况通过放射影像学检测的骨丧失来定义,健康患者被定义为冠方三分之一牙根长度的骨丧失<15%或咬合翼片<2mm,牙周病患者被定义为骨丧失>冠方三分之一牙根长度的15%或咬合翼片>2mm。总共568名患者被纳入研究,其中40名经历了严重并发症。出现COVID-19并发症的患者中>80%患有牙周炎,相比之下,未出现并发症的患者中43%表现出一定程度的牙周病。在568名患者中,258名患有牙周炎,其中33名出现了COVID-19并发症。相比之下,310名无牙周炎的患者中仅有7名发展为严重的COVID-19并发症。在调整了糖尿病和高血压等合并症后,牙周炎对严重COVID-19并发症、死亡、ICU入院和通气需求的发生仍具有显著影响。致命的COVID-19结局与血液中检测到的炎性介质增加显著相关。患有牙周炎的COVID-19患者与无牙周炎的患者相比,具有更高的白细胞和CRP水平,这表明牙周炎通过全身性炎症加剧了COVID-19的严重程度(Marouf et al., 2021)。
关于牙周病如何加剧COVID-19严重程度,已提出了几种机制,包括牙周病原体的吸入导致下呼吸道中血管紧张素转换酶2(ACE2)表达增加和细胞因子增多(Takahashi et al., 2021),牙周病原体通过切割S糖蛋白诱导病毒毒力(Madapusi Balaji et al., 2020; Takahashi et al., 2021),以及口腔作为病毒储存库(Badran et al., 2020; Badran et al., 2020; Botros et al., 2020; Kheur et al., 2020; Madapusi Balaji et al., 2020),此外还有具有全身性后果的炎症反应通路增加(Sahni and Gupta, 2020)。SARS-CoV-2是COVID-19的致病因子,是一种空气传播的冠状病毒,通过说话、呼吸、咳嗽、打喷嚏以及其他涉及口腔的活动,经暴露于受感染的飞沫和气溶胶而传播(Ghinai et al., 2020; Pung et al., 2020; Hamner et al., 2020)。SARS-CoV-2利用ACE2和TMPRSS宿主受体进入宿主细胞(Hoffmann et al., 2020; Zang et al., 2020)。表达这些受体的细胞类型在全身广泛分布(Singh et al., 2020; Sungnak et al., 2020; Brann et al., 2020)。COVID-19的口腔表现,包括味觉丧失,在约50%的病例中出现临床症状。尽管如此,很少有研究确定该病毒直接在口腔组织中复制的能力,这对于理解口腔在病毒传播给其他人以及通过唾液传播到胃肠道中的作用可能非常重要。Huang等人(Huang et al., 2021)最近鉴定了牙龈和唾液腺内的34个独特细胞亚群,这些亚群携带SARS-CoV-2病毒进入因子,其中感染在口腔内不同部位是非均匀的,这与口腔的异质性一致。单细胞RNA测序和荧光原位杂交验证了ACE2和TMPRSS2在唾液腺和牙龈黏膜中的表达。在颊黏膜、舌腹/舌背、软腭和腭/舌扁桃体中也鉴定到了表达,与基底区室相比,在这些部位观察到基底上层表达增加。唾液部分,包括无细胞部分(来自受感染的唾液腺)和细胞部分(来自受感染的黏膜脱落),也在无症状和有症状个体中进行了测试并得到确认,突显了呼出的唾液飞沫可能有助于传播感染的重要性。此外,感知到的味觉和嗅觉丧失与唾液SARS-CoV-2 RNA水平呈正相关(Huang et al., 2021)。
牙周病病因学中的其他参与者-饮食在牙周病中的作用饮食对龋病进展的影响已得到充分证实。然而,其在牙周病病理学中的作用却相对被忽视。与牙周炎风险增加相关的主要饮食因素包括加工碳水化合物、低纤维摄入、饱和脂肪和高蛋白摄入(图1)(Woelber and Tennert, 2020)。微量营养素缺乏,如维生素C、维生素D、维生素B、维生素A、镁、钙、铁、锌、钾、铜、锰和硒缺乏,也与牙周病的发病率和严重程度相关(Dommisch et al., 2018)。目前关于牙周病发病率的研究结果在很大程度上是相关性的,并侧重于牙周病的临床参数,很少关注其机制基础。此外,不同研究者的发现存在差异。Alhassani等人(2021)采用饮食模式分析,研究了健康专业人员随访研究参与者在24年期间的主要饮食模式与牙周病发病率之间的关联。该研究包括51,529名男性受试者,他们在1986年完成了问卷(当时年龄为40-75岁),并持续每四年通过食物频率问卷提供饮食习惯信息(基线时患有牙周炎的受试者未被纳入)。在整个研究过程中,每两年观察到3,738例新发牙周炎病例。然而,未观察到西方饮食(高脂肪、低纤维、加工碳水化合物)或谨慎饮食(全谷物、水果、蔬菜)与牙周病发病率之间存在显著关系,但牙周炎在肥胖个体中确实随着西方饮食的消费而显著增加。Jauhiainen等人(2020)进行的一项为期11年的随访研究发现,在240名个体中,不良饮食(由波罗的海饮食评分和推荐芬兰饮食评分确定)与中年人牙周袋加深的发展相关。RFD和BFD中的健康饮食包括水果、蔬菜、较高的白肉和鱼类消费、纤维谷物(黑麦、燕麦、大麦)以及不饱和脂肪酸与饱和脂肪酸比例较高的饮食。负面成分包括盐、蔗糖、红肉消费和酒精摄入(Alhassani et al., 2021)。Woelber等人(2019)研究了抗炎饮食对牙龈炎患者的影响。实验组采用低加工碳水化合物和动物蛋白、富含omega-3脂肪酸、维生素C、维生素D、抗氧化剂、植物硝酸盐和纤维的抗炎饮食,而对照组不改变西方饮食习惯。在实验期间,两组均停止齿间清洁四周。研究期后的临床和血清学参数以及龈下微生物组分析表明,与对照组相比,实验组的牙龈出血显著减少(约40%)。然而,两组之间在血清学炎症参数(TNF-α、IL-6、高敏C反应蛋白)方面未观察到显著差异。此外,未发现龈下微生物群发生显著变化(Woelber et al., 2019)。然而,未研究实验组和对照组微生物群的代谢能力。该研究的一个主要局限性可能部分归因于实验周期较短。
高碳水化合物消费在龋病中是公认的风险因素(Moye et al., 2014; Wang et al., 2019)。最近的研究也已确定增加碳水化合物消费是牙周病的风险因素,从而支持了龋病和牙周病的综合假说(Nyvad and Takahashi, 2020)。这些发现与农业整合度和饮食影响较低的社会中口腔疾病负担较低(Crittenden and Schnorr, 2017; Crittenden et al., 2017),以及在新石器时代革命时期口腔疾病发病率出现(与谷物消费增加并行)的情况一致(Adler et al., 2016)。Hamasaki等人发现高碳水化合物、低脂肪饮食与牙周病发病率之间存在显著关联。利用来自2005年日本国民健康与营养调查、生活状况综合调查和牙科疾病调查的大数据集(共包含3,043名个体),发现牙周病发病率与来自脂肪的总热量百分比之间存在显著关联。在晚期牙周病组中,来自脂肪的热量百分比显著较低,并且低脂肪、高碳水化合物饮食与牙周病发病率相关(Hamasaki et al., 2017)。这些发现与先前的研究一致,这些研究发现胆固醇水平较高的受试者(Izumi et al., 2009)以及omega-3脂肪酸摄入量较高的受试者(Iwasaki et al., 2010)牙周病发病率较低。Moreira等人(2021)的一项研究还发现,青少年中糖摄入量增加与牙周病之间存在正相关。世界卫生组织建议将糖摄入量限制在每日总能量的10%以下,以降低非传染性疾病的风险(WHO, 2021)。因此,研究了糖摄入量>每日能量10%与青少年牙周病状况之间的关联。在2,515名18-19岁青少年中,他们完成了食物频率问卷(过去12个月内106种食物的频率和份量)以及牙周临床检查(6颗牙齿的可见菌斑指数、探诊出血、牙周探诊深度、临床附着水平),34.35%的受试者每日糖摄入量>10%,2.31%的受试者糖消费量>总能量摄入的20%。在调整了社会人口学因素和吸烟/饮酒情况后,每日糖摄入量>10%与受牙周病影响的牙齿数量增加相关(p=0.011)(Moreira et al., 2021)。糖/碳水化合物摄入量增加与牙周病发病率较高之间的这种关联可以通过高血糖和晚期糖基化终末产物诱导的全身性炎症来解释(Aragno and Mastrocola, 2017; Nyvad and Takahashi, 2020)。增加的糖摄入量可能在口腔生物膜内局部起作用,驱动氧化应激和微生物失调,从而导致牙周炎。这一假设与龈上和龈下生物膜发育的体外发现一致,其中龈下生物膜的生长在很大程度上依赖于解糖的龈上物种的预先定植和相应的胞外多糖合成(Thurnheer et al., 2016)。鉴于牙周病发病率与碳水化合物消费之间的关联,以及以谷物消费增加为特征的历史时期口腔疾病负担增加的事实,以及口腔龈下生物膜的多物种性质,这些发现值得未来进行研究,以更好地理解碳水化合物消费在牙周病中的全身和/或局部影响。
心理压力在牙周病中的新意义宿主的环境扰动(如饮食和生活方式)同样具有改变宿主-微生物组稳态的能力。持续的心理压力已被认为是多种慢性疾病(包括糖尿病和类风湿性关节炎)的病因学风险因素(McCray and Agarwal, 2011; Marcovecchio and Chiarelli, 2012)。压力激活中枢神经系统和下丘脑,导致促肾上腺皮质激素释放激素和精氨酸加压素的释放。这进一步刺激垂体释放促肾上腺皮质激素,导致肾上腺皮质产生皮质醇。这一过程统称为下丘脑-垂体-肾上腺轴(Breivik et al., 2000)。皮质醇是与压力反应相关的主要激素。值得注意的是,在牙周炎患者中,唾液和血清中的皮质醇水平升高,其水平与疾病严重程度呈正相关,并且牙周炎患者龈沟液中的皮质醇水平更高(Ishisaka et al., 2008; Rai et al., 2011)。此外,已证明糖皮质激素(包括皮质醇)会下调口腔中的免疫功能,这可能损害对牙周病原体的免疫反应(Genco and Van Dyke, 2010)。Duran-Pinedo等人(2018)最近的研究确定了皮质醇产生对口腔生物膜样本扰动的直接作用,该作用与牙周炎患者队列的牙周病严重程度一致。体外用皮质醇处理牙周炎患者的牙菌斑样本,以研究其对口腔微生物群的直接影响,同时避免全身性内分泌效应可能带来的混杂因素。转录组学分析揭示了梭杆菌门水平的显著变化。随后进行了基因本体论分析,以更好地了解口腔微生物组对皮质醇处理的基因表达谱。在变化的表达谱中,蛋白水解、寡肽转运、铁代谢和鞭毛组装在皮质醇处理组中富集(Duran-Pinedo et al., 2018)。这些基因谱与牙周病中口腔微生物群的活动一致(Duran-Pinedo et al., 2014; Yost et al., 2015)。重要的是,即使在不存在宿主细胞的情况下,皮质醇处理组中与宿主免疫反应相关的基因也被上调。与其他存在的门相比,梭杆菌门的转录活性增加更为显著。然而,大多数微生物群落都表现出其表达谱的转变,这表明更大比例的物种共同上调了假定的毒力因子。其中,链球菌属在毒力因子上调方面产生的变化最大。在研究皮质醇对最初鉴定为活性更高的生物体纯培养物的影响时,观察到Leptotrichia goodfellowii和具核梭杆菌的转录组谱均发生转变。具核梭杆菌显示出与牙周炎相关的上调生物过程,包括蛋白水解、钴胺素生物合成和铁转运,在L. goodfellowii中也观察到了这些过程。两种生物体还显示出与脂质A生物合成、DNA复制或翻译、铁获取和肽酶活性相关的基因上调(Duran-Pinedo et al., 2018)。总之,这项研究介绍了心理压力相关激素对口腔微生物群扰动的新的直接作用,这种扰动与体内牙周炎中观察到的转录变化平行。
心理压力已被证明通过抑制宿主免疫反应来延迟伤口愈合(Bosch et al., 2007; Vegas et al., 2012)。因此,Zhao等人(2012)研究了心理压力对牙周炎伤口愈合的影响。牙周愈合由多种生长因子介导,包括碱性成纤维细胞生长因子,其被表征为牙周膜再生的重要因子(Murakami et al., 1999; Lalani et al., 2005; Katayama et al., 2006),并且在正常伤口愈合中通过细胞增殖、分化和血管生成发挥作用(Gospodarowicz, 1974)。因此,研究者测试了心理压力对牙周伤口愈合中bFGF表达下调的影响。通过在上颌第二磨牙周围放置丝线结扎,在大鼠中诱导实验性牙周炎,并在1、2或4周后移除结扎线。移除结扎线后,在愈合过程中对大鼠施加慢性不可预见的轻度压力(包括湿垫料24小时、禁食12小时、光暗周期颠倒、冷水或热水中游泳5分钟以及1小时束缚应激)。结扎线移除后基线时的仅牙周炎组和牙周炎-压力组均表现出炎症浸润、显著的牙槽骨丧失和临床附着丧失。仅牙周炎组小鼠在移除结扎线后的四周内表现出自发的软组织愈合和牙槽骨重塑。相反,牙周炎-压力组的愈合过程显著延迟,与仅牙周炎组相比,在第2周和第4周时具有显著更严重的炎症浸润、牙槽骨丧失和附着丧失(p<0.05)。移除结扎线后,与基线相比,仅牙周炎组在第1、2和4周时IL-1β和TNF-α减少。然而,牙周炎-压力组在移除结扎线后IL-1β未显著降低。TNF-α确实降低了;然而,其水平仍高于仅牙周炎组。移除结扎线4周后,仅牙周炎组大鼠的bFGF表达恢复,与此相反,牙周炎-压力组中,心理压力延迟了bFGF表达的恢复(Zhao et al., 2012)。因此,心理压力不仅对微生物组产生直接影响,而且还可能通过加剧炎症和阻止牙周组织愈合来延续疾病发病机制。
奶酪的力量:乳链菌肽和纳米颗粒对抗牙周炎目前牙龈炎和牙周炎的治疗方法包括正确的口腔卫生习惯、刮治和根面平整,其治疗目标是减少牙周袋深度和改善临床附着水平(Claffey et al., 2004; Goodson et al., 2012)。抗生素治疗已被用作机械治疗的辅助治疗方式,以帮助清除非手术治疗后可能残留的龈下病原体(Barca et al., 2015)。然而,抗生素治疗并非没有副作用,例如胃肠道副作用、肠道微生物群的改变以及耐抗生素细菌菌株的出现(Kapoor et al., 2012; Ramirez et al., 2020)。益生菌(定义为当以足够剂量施用时可能为宿主带来健康益处的活微生物培养物)已作为非手术牙周治疗的辅助治疗方式获得越来越多的认可(Teughels et al., 2008; Morelli and Capurso, 2012)。牙周治疗中使用的益生菌包括含有活菌罗伊氏乳杆菌(Lactobacillus reuteri)、唾液乳杆菌(Lactobacillus salivarius)的片剂、含有干酪乳杆菌(Lactobacillus casei)的益生菌饮料、含有罗伊氏乳杆菌的口香糖以及含有不同剂量口腔链球菌(Streptococcus oralis)、乳房链球菌(Streptococcus uberis)和鼠链球菌(Streptococcus rattus)的漱口水,用于治疗不同程度的牙龈炎症和牙周炎(Nguyen et al., 2020)。乳链菌肽是一种由某些革兰氏阳性菌(如乳球菌属(Lactococcus)和链球菌属(Streptococcus)物种)产生的抗菌肽,对多种革兰氏阳性和革兰氏阴性细菌具有杀菌作用(Shin et al., 2015)。如今,乳链菌肽被美国食品药品监督管理局认定为生物安全的食品防腐剂,并被用作加工奶酪的一种成分(de Arauz et al., 2009)。产乳链菌肽的细菌作为治疗口腔和全身性疾病(范围从胃肠道疾病到各种癌症)的潜在治疗方式,已受到越来越多的关注。将高纯度乳链菌肽应用于含有牙龈卟啉单胞菌、中间普雷沃菌、伴放线聚集杆菌、齿垢密螺旋体和粪肠球菌(Enterococcus faecalis)的唾液来源生物膜,可抑制病原菌的生长,且抑制作用以剂量依赖性方式增加(Shin et al., 2015)。
乳链菌肽的益处不仅体现在其杀灭病原体的能力上,还体现在其对宿主缺乏有害副作用。虽然乳链菌肽已被证明能诱导病原体杀灭,但高剂量的乳链菌肽应用并未对人源口腔细胞的活力和增殖产生毒性作用(Shin et al., 2015)。另一个有趣的发现在于乳链菌肽似乎具有选择性杀灭能力。例如,产乳链菌肽的乳酸乳球菌(L. lactis)益生菌以及纯化的乳链菌肽,在应用于掺有牙周病原体的口腔生物膜时,可以降低牙周病原体的水平,同时保留共生菌种(Radaic et al., 2020)。Radaic等人(2020)发现,用产乳链菌肽的乳酸乳球菌或纯化的乳链菌肽处理,能够在体外抑制致病性口腔生物膜的生长,其中乳链菌肽能够显著抑制和破坏生物膜的形成、结构和活力。对掺有牙周病原体并进行益生菌处理的生物膜进行16S rRNA测序表明,产乳链菌肽的乳酸乳球菌能够将微生物多样性指数恢复到对照水平,表明乳链菌肽可以选择性地靶向牙周病原体。在物种水平上,产乳链菌肽的乳酸乳球菌和纯化的乳链菌肽处理成功抑制了病原体(包括福赛斯坦纳菌和具核梭杆菌)的生长,同时增加了共生菌种(如黄色奈瑟菌(Neisseria flava)和乳酸乳球菌(L. lactis))的比例(Radaic et al., 2020)。乳链菌肽与牙周病原体减少相关的这些发现反映在牙周病进展的临床参数改善上,例如产乳链菌肽的乳酸乳球菌在牙周病小鼠模型中抑制牙槽骨丧失的能力(Nguyen et al., 2020)。乳链菌肽的益处已被证明超越牙周病。Kamarajan等人(2020)发现,在OSCC小鼠模型中,乳链菌肽能够减少口腔肿瘤发生并延长荷瘤小鼠的寿命。此外,在给予乳链菌肽后,由牙周病原体加剧的小鼠口腔肿瘤发生得以消除,即乳链菌肽处理后,病原体增强的癌细胞迁移、侵袭、肿瘤球形成和体内口腔肿瘤发生均减少。对其潜在机制的研究揭示,乳链菌肽能够通过下调整合素αV表达和FAK磷酸化来抑制齿垢密螺旋体介导的口腔癌发生(Kamarajan et al., 2020)。
虽然细菌素已成为牙周炎的新型辅助疗法,但也注意到了这种方法的缺点。革兰氏阳性菌通过细胞壁修饰、膜脂磷脂修饰、细菌素酶促失活(Zhou et al., 2014)产生的细菌素抗性,革兰氏阴性菌外膜的抗性,以及细菌素对蛋白酶(如蛋白酶K和胃蛋白酶)的敏感性(Prudêncio et al., 2015; Ansari et al., 2018),都影响了细菌素相关疗法的疗效。纳米药物递送系统可以通过三种主要机制帮助细菌素递送,包括:
1)改善药代动力学,例如改变溶解度、电荷和稳定性,这些共同可能增加保质期、生物利用度和杀菌半衰期。
2)纳米药物递送系统还可以通过保护细菌素免受耐药细菌产生的降解酶的影响(Zhang et al., 2010; Arthur et al., 2014; Fahim et al., 2016),并通过允许它们克服微生物耐药机制(例如通过破坏细菌细胞膜和细胞壁、损害细菌质子外排泵或在细菌中诱导氧化应激)来提高细菌素对抗细菌耐药性的功效(Baptista et al., 2018)。
3)纳米药物递送系统还可以通过细胞外或细胞内机制直接将细菌素递送至病变组织(Anselmo and Mitragotri, 2016)。
基于乳链菌肽的细菌素疗法在牙周炎中受到越来越多的关注。然而,乳链菌肽的使用受到一些因素的限制,包括结构不稳定以及出现对其作用耐受和/或耐药的细菌(Salmaso et al., 2004; Zhou et al., 2014; Randall et al., 2018)。例如,乳链菌肽抗性基因/蛋白通过切割羊毛硫氨酸-28和丝氨酸-29之间的肽键使乳链菌肽失活,导致截短的乳链菌肽,其膜亲和力、成孔能力降低,杀菌能力降低100倍(Khosa et al., 2013; Field et al., 2015)。乳链菌肽还对环境因素(如pH和温度)敏感(Zhou et al., 2014)。纳米药物递送系统已被用于通过保护乳链菌肽免受酶降解、环境因素影响并降低细菌耐药性来提高其功效。例如,研究表明,当与纳米药物递送系统结合使用时,乳链菌肽的抗菌效果增强,这表明纳米药物递送系统允许将乳链菌肽直接递送至作用部位(Zhou et al., 2014)。此外,将纳米药物递送系统应用于乳链菌肽可实现细菌素的持续释放,从而增加长期功效和作用。例如,接种后,乳链菌肽/纳米药物递送系统复合物保持活性长达50天,而单独游离的乳链菌肽仅能保持7天。因此,纳米药物递送系统可以作为药物储库(Fahim et al., 2016),其中包封的乳链菌肽通过扩散、细菌降解和聚合物溶蚀随时间缓慢持续释放(Chopra et al., 2014; Alishahi, 2014; de Abreu et al., 2016)。Radaic等人2020年的初步研究已发现,乳链菌肽/纳米药物递送系统增强了细菌素破坏口腔生物膜、抑制牙周病原体生长和降低口腔癌细胞活力的功效。因此,纳米药物递送系统与细菌素联合使用可能作为牙周炎中清除牙周病原体的新型治疗方式。
牙周免疫细胞响应细菌病原体攻击而产生的活性氧通过诱导氧化损伤,从而干扰细胞周期进程并诱导组织损伤,促进了牙周病的发病机制(Hirschfeld et al., 2017; Kanzaki et al., 2017; Liu et al., 2017)。Bao等人(2018)最近研究了聚多巴胺作为抗氧化防御平台在氧气应激诱导的牙周病中清除ROS的作用,使用了纳米颗粒。牙周炎小鼠模型表明,聚多巴胺纳米颗粒成功清除了ROS并减少了牙周炎症。此外,注意到几乎没有长期毒性,这与聚多巴胺的高生物相容性和生物降解性一致。研究了聚多巴胺纳米颗粒清除羟基自由基和超氧自由基的能力,其中羟基自由基的清除通过荧光2-羟基对苯二甲酸的存在来测量。在聚多巴胺纳米颗粒存在下,观察到荧光减弱,表明聚多巴胺纳米颗粒可以以浓度依赖性方式清除羟基自由基。在聚多巴胺纳米颗粒浓度为0.125 mg/mL时,几乎所有的羟基自由基都被清除。超氧自由基清除通过NBT光还原的抑制率来测量,其中随着超氧自由基的增加,出现强吸收信号。当将聚多巴胺纳米颗粒添加到系统中时,吸收光谱显著降低,当聚多巴胺纳米颗粒以0.1 mg/mL的浓度施用时,超氧自由基被完全从系统中清除。还研究了聚多巴胺纳米颗粒清除细胞内ROS的能力,其中使用Cu2+修饰的聚多巴胺纳米颗粒作为探针来确定HGE细胞的摄取动力学。摄取效率取决于孵育期长度,在12小时时高于50%。此外,在0.1 mg/mL的共孵育浓度下,聚多巴胺纳米颗粒处理使细胞内ROS的产生减少了80%(Bao et al., 2018)。总之,这些数据证明了纳米颗粒系统在促进细菌素递送和细菌杀灭方面的新的意义,此外还能减轻炎症并促进牙周病的恢复。
结语龈上和龈下生物膜失调与牙龈持续炎症相结合,是牙周病发生和进展的基石(Hajishengallis and Lambris, 2012)。假定的牙周病原体对于引发疾病和促进宿主炎症至关重要,同时通过免疫颠覆和组织操纵继续延续疾病(Maekawa et al., 2014; Hajishengallis, 2015; Malone et al., 2021)。各种模型的出现进一步强调了口腔共生菌和病原共生菌在通过介导与关键病原体(如牙龈卟啉单胞菌、福赛斯坦纳菌、伴放线聚集杆菌和齿垢密螺旋体)的复杂相互作用来促进牙周病中的关键作用(Marsh, 1994; Socransky et al., 1998; Hajishengallis et al., 2011; Suzuki et al., 2013)。此外,对非细菌微生物(包括构成口腔微生物群的各种病毒和噬菌体)在疾病进展中作用的新认识正成为一个研究热点(Pride et al., 2012; Gao et al., 2020)。
观察表明,口腔病毒组在牙周病中发生显著变化(Gao et al., 2020),从而提示了病毒物种在疾病进展中可能操纵细菌和宿主过程的潜在机制。影响微生物失调和牙周炎症的因素已超出了单纯缺乏口腔卫生的范畴,现在还包括宿主环境因素,如心理压力和饮食(Rai et al., 2011; Duran-Pinedo et al., 2018; Woelber et al., 2019; Woelber and Tennert, 2020; Aral et al., 2020)。心理压力和不良饮食可能通过促进宿主炎症来加剧牙周病。然而,体外研究表明,压力激素皮质醇可直接影响微生物失调和病原体过度生长,从而证明了压力影响微生物群落的直接作用(Duran-Pinedo et al., 2018)。牙周免疫学的新概念引入了细胞衰老在促进炎症过程中的作用,并确定了牙龈中独特的、与其他屏障部位不同的免疫反应(Dutzan et al., 2017; Dutzan et al., 2018; Aquino-Martinez et al., 2020; Aquino-Martinez et al., 2020)。其他慢性炎症性疾病(如IBD、心血管疾病和自身免疫性疾病)的存在也已被认为是可能促进牙周病发病机制的合并症(Hajishengallis and Chavakis, 2021)。远处病理状态的口腔表现已被广泛认识,并在各种IBD的临床表现中尤其突出(Lankarani et al., 2013; Benli et al., 2021)。
然而,口腔病理和疾病在促进全身炎症状况中的新作用揭示了一个新概念,即口腔疾病的相互影响的全身表现。这一点尤其通过最近关于牙周病与阿尔茨海默病之间联系的研究发现得到强调,其中在尸检标本的脑组织中鉴定出了牙周病原体(Chen et al., 2017; Dominy et al., 2019)。与此一致,越来越多的证据支持牙周病在加剧COVID-19严重程度和结局中的作用,如同其他慢性炎症性疾病一样(Botros et al., 2020; Sahni and Gupta, 2020; Huang et al., 2021)。关于疾病病因学的新发现,以及传统非手术和抗生素治疗之外的新型治疗方式,正在不断涌现。益生菌,如产乳链菌肽的乳酸乳球菌,不仅破坏病原体过度生长,而且不对共生微生物物种产生不利影响(Radaic et al., 2020)。纯化的乳链菌肽在牙周病相关生物膜中也具有这种效果,并且不会对宿主细胞产生有害影响(Shin et al., 2015; Radaic et al., 2020)。纳米药物递送系统的整合进一步增强了益生元乳链菌肽给药的效果,使得病变组织被直接靶向,同时消除了潜在和不可避免的缺陷(Bao et al., 2018; Radaic et al., 2020)。总之,这些发现令人兴奋地将新概念整合到现有的牙周病发病机制模型中,进一步强调了口腔健康对全身健康的作用,并随着对新疗法的不断构想,持续推动我们对疾病认识的进步。

















声明:本文翻译自国外病例展示,仅供口腔专业人士进行技术交流,仅代表医生个人观点,不构成任何医疗建议,如有翻译错误之处敬请指正。
END

微信公众号:chi-xue-tang
扫码关注 获得更多精彩
本公司对外合作联系:18361831107
投稿邮箱:chixuetang@163.com


