抗体靶向疗法涵盖广泛的生物制剂,二十年来已发展为一种灵活且强大的治疗模式。这类疗法利用抗体将治疗药物精准递送至靶细胞,同时尽可能减少对健康细胞的损伤。

抗体药物偶联物(antibody-drug conjugates, ADCs)是抗体靶向疗法中研究最为深入的形式。2000年,吉妥珠单抗奥唑米星(gemtuzumab ozogamicin,商品名为Mylotarg)成为首个获美国FDA批准的ADC药物[1,2]。截至2024年年底,全球已有15种ADC药物被批准用于癌症治疗,超过200家公司正在开发ADC[3],预计到2033年其全球市场规模将达到250亿美元[4]。
继ADC之后,其他基于抗体的新分子形式不断涌现,如递送核酸的抗体-寡核苷酸偶联物(antibody-oligonucleotide conjugates, AOCs)和诱导靶蛋白降解的降解剂-抗体偶联物(degrader-antibody conjugates, DACs)。这些新分子不仅将适应症从癌症向更多疾病领域延伸,还提供了细胞毒性之外的全新作用机制[5,6]。抗体靶向疗法的核心优势在于其三元结构—抗体、连接子(linker)和有效载荷(payload),这三个部分共同构成了三重精准调控点。
抗体靶向疗法的开发是一个复杂的多步骤过程。不断扩展的技术手段和在发现与开发各阶段可供选择的策略,既为该过程提供了助力,也增加了难度。本白皮书概述了ADC、DAC和AOC的开发流程,并重点探讨了研究这些药物时所面临的独特挑战。
抗体靶向疗法的特点和分类
单克隆抗体、连接子与载荷的特定组合取决于靶点及作用机制。
抗体靶向疗法主要包含三种结构要素:
单克隆抗体(monoclonal antibody, mAb):用于将疗法递送至靶细胞;
连接子:将有效载荷连接到抗体;
有效载荷:如毒素、小干扰RNA(small interfering RNA, siRNA)或降解剂,在靶细胞内释放后发挥治疗作用。
1
抗体偶联药物(ADC)
科学家们开发ADC的初衷是确保高效的细胞毒性药物能够精准靶向癌细胞,同时最大限度减少对其他细胞类型的影响。通过将药物与mAb偶联,该疗法能够选择性地靶向癌细胞(图1)。药物随抗体内吞进入细胞后释放,进而诱导细胞死亡。
目前,以微管抑制剂(auristatins和maytansinoids)为代表的细胞毒性分子在ADC市场占据主导地位[7]。然而,这类细胞毒性药物本身选择性有限,且ADC的整体毒性通常高于AOC和DAC。因此,即使采用高选择性的递送机制,脱靶毒性仍是ADC临床应用中的一个重要挑战。
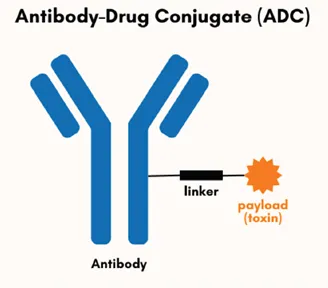
图1.抗体偶联药物结构
2
抗体-寡核苷酸偶联物(AOC)
AOC由siRNA或反义寡核苷酸(antisense oligonucleotide, ASO)与单抗偶联组成,其通过抗体介导的内吞作用进入靶细胞并释放有效载荷(图2)。这些分子能够与靶RNA特异性结合,导致信使RNA(messenger ribonucleic acid, mRNA)降解、外显子包含或排除、调控基因表达或改变前体mRNA剪接 [8]。
由于寡核苷酸序列可高度定制化,AOC既可通过抗体实现细胞特异性递送,又能通过寡核苷酸序列实现分子层面的作用特异性,从而具备双重靶向能力。目前,未偶联的siRNA、ASO和磷酰二酰胺吗啉寡聚物(phosphorodiamidate morpholino oligomers, PMO)等已获批用于治疗多种疾病,如心血管、神经肌肉和中枢神经系统疾病。
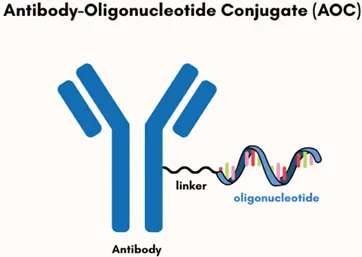
图2.抗体-寡核苷酸偶联物
AOC的独特之处在于,其兼具治疗与诊断的双重功能,因为同一单克隆抗体既能用于对病变细胞进行成像,又能选择性递送治疗药物。
3
降解剂-抗体偶联物(DAC)
DAC由单克隆抗体与双功能分子偶联而成,该抗体负责将双功能分子精准递送至特定细胞(图3)。双功能分子能够同时结合两种蛋白质,在DAC中,其主要功能是实现靶向蛋白的降解。这类分子包含两种配体:一种可与待降解的靶蛋白结合,另一种则招募细胞内降解机制的相关组分。
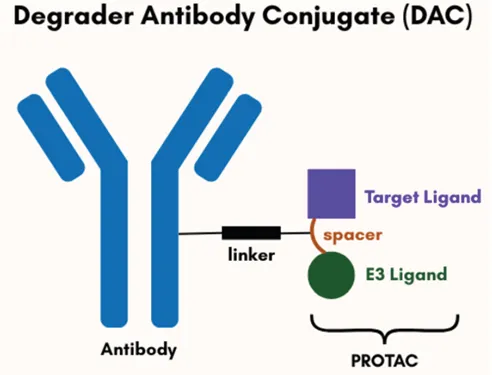
图3.降解剂-抗体偶联物
目前已有多种类型的降解剂可用于构建DAC,包括:
蛋白降解靶向嵌合体(proteolysis-targeting chimeras, PROTACs),将靶蛋白募集至E3泛素连接酶附近。随后E3连接酶可为靶蛋白添加泛素化标记,从而引导其降解(图4)[9]。
溶酶体靶向嵌合体(lysosome-targeting chimeras, LYTACs),可将靶向表面蛋白递送至溶酶体靶向受体,进而使其被内吞并降解[10]。
自噬靶向嵌合体(autophagy-targeting chimeras, AUTACs),通过将靶蛋白结合到鸟嘌呤衍生物标签,进而招募自噬机制实现对靶蛋白的降解[11]。
DAC在癌症、中枢神经系统疾病、罕见病及炎症性疾病等多种疾病治疗领域中展现出广泛的应用潜力。
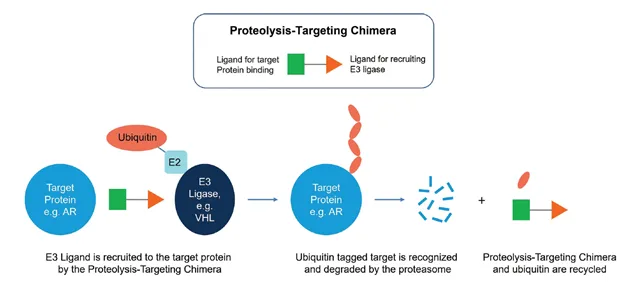
图4.PROTAC作用机制
抗体靶向疗法的研发挑战及策略
尽管各类抗体靶向疗法面临各自独特的挑战,但ADC、AOC以及DAC的开发遵循着共同的流程,包括:设计治疗性分子的各个组成部分,将其通过连接子进行偶联,进而对分子及其生物学效应进行表征与优化。研发流程中每个环节的选择都可能影响分子的脱靶效应、有效载荷释放、内化效率、稳定性及耐药性。
1
单克隆抗体的识别与工程化改造
在抗体靶向疗法中,理想的单克隆抗体应能以高亲和力特异性结合靶细胞,并最大程度地避免与非靶细胞结合。该抗体需在血液中具备较长的半衰期,并能有效促进靶细胞对药物的摄取。一旦确定候选抗体,可进一步通过工程化改造来优化这些特性。
抗体偶联药物的脱靶效应,即有效载荷作用于非靶细胞,是此类疗法面临的关键挑战之一。使用对靶细胞具有高特异性的单克隆抗体,有助于缓解这一问题。尽管这类精准药物设计上具有高度选择性,但脱靶效应仍无法完全避免。其原因包括:抗体可能与非靶细胞发生非特异性结合;有效载荷可能在循环系统中提前释放;或有效载荷在靶细胞内释放后,扩散至邻近的非靶细胞并产生毒性。
2
有效载荷的设计
3
连接子的选择
可裂解型:该连接子能够通过多种细胞机制释放有效载荷,包括在靶细胞内上调的机制。例如,溶酶体蛋白酶敏感型连接子可被组织蛋白酶B等酶切割,而该酶在癌细胞中常过表达[15]。可裂解连接子在循环系统中需保持稳定,以避免有效载荷过早释放。除此之外,酸敏感型连接子能在低pH环境,如炎症细胞中实现更具选择性的裂解。 不可裂解型:该连接子仅在抗体于溶酶体内降解后释放有效载荷,因此脱靶风险较低。常见的有马来酰亚胺己酰基(maleimidocaproyl)和马来酰亚胺甲基环己烷-1-羧酸酯(maleimidomethyl cyclohexane-1-carboxylate) [16]。
4
偶联与表征
非定点偶联方法:将有效载荷非特异性地连接到抗体表面的任意的氨基酸残基上,早期ADC药物开发多采用此路径。这种方法操作简单、产率较高,但所得产物为异质性混合物,均一性和稳定性较差,可能对疗效产生负面影响。 定点偶联方法:通过基因工程、酶催化反应或在特定官能团上进行选择性化学偶联,将有效载荷精确连接到抗体上预设的位点。这类方法的优势在于能获得组成均一、DAR明确的治疗分子。然而,使用定点偶联合成抗体靶向疗法难度较大,产率通常较低,且每个分子上可用的偶联位点数量有限。
5
体外功能与稳定性研究

蛋白质印迹法与酶联免疫吸附实验(enzyme-linked immunosorbent assays, ELISA):定量检测目标蛋白的降解水平; 泛素化实验:评估蛋白降解过程中的泛素标记状态; FACS:分析降解剂-抗体偶联物的细胞内吞效率; 细胞活力检测:明确蛋白降解所引发的生物学效应。
6
体内药效与PK/PD
结语
ADC、AOC和DAC等新分子正持续拓展靶向疗法的技术边界。抗体靶向药物的开发涵盖复杂且多环节的工作流程,其中存在大量可优化节点,以应对脱靶效应、有效载荷释放及稳定性等挑战。
推进此类药物的开发,离不开值得信赖且经验丰富的合作伙伴。药明康德作为一体化、端到端的CRDMO,为抗体靶向疗法的全研发周期提供支持。其服务涵盖靶点识别与验证、先导化合物发现与优化、定制化连接子合成、先进偶联与分析技术、体外功能与生物物理性质评价,以及用于PK/PD药效评估的体内肿瘤模型等前沿服务。
参考文献(上下滑动查看更多)
1. Virginia Metrangolo and Lars H. Engelholm, “Antibody-Drug Conjugates: The Dynamic Evolution from Conventional to Next-Generation Constructs,” Cancers 16, no 2 (Jan. 2024): 447, https://doi.org/10.3390/cancers16020447.
2. Ruili Wang et al., “Antibody-Drug Conjugates (ADCs): Current and Future Biopharmaceuticals, J. Hematol. Oncol. 18, no. 51 (April 2025), https://doi.org/10.1186/s13045-025-01704-3.
3. “200+ Pharma Companies Vie for the Top Spot in the Expanding Antibody-Drug Conjugate Oncology Market,” PR Newswire, Oct. 17, 2024, https:// www.prnewswire.com/news-releases/200-pharma-companies-vie-for-thetop-spot-in-the-expanding-antibody-drug-conjugate-oncology-market--delveinsight 302278759.html.
4. Antibody Drug Conjugates Market Size is Expected to Reach USD 25.38 Billion by 2033, Growing at a CAGR of 8.84%: Straits Research,” GlobalNewswire, Jan. 22, 2025, https://www.globenewswire.com/newsrelease/
2025/01/22/3013689/0/en/Antibody-Drug-Conjugates-Market-
Size-is-Expected-to-Reach-USD-25-38-Billion-by-2033-Growing-at-a-CAGRof-8-84-Straits-Research.html.
5. Jinlan Jiao et al., “Overcoming Limitations and Advancing the Therapeutic Potential of Antibody-Oligonucleotide Conjugates (AOCs): Current Status and Future Perspectives,” Pharmacol. Res. 209 (Nov. 2024): 107469, https:// doi.org/10.1016/j.phrs.2024.107469.
6. Ki Bum Hong and Hongchan An, “Degrader-Antibody Conjugates: Emerging New Modality,” J. Med. Chem. 66, no. 1 (Jan. 12, 2023): 140–48, https://doi.org/10.1021/acs.jmedchem.2c01791.
7. Dan-Yun Ruan, Hao-Xiang Wu, and Qi Meng, “Development of Antibody-Drug Conjugates in Cancer: Overview and Prospects,” Cancer Commun. 44, no. 1 (Jan. 2024): 3–22. https://doi.org/10.1002/cac2.12517.
8. Barbora Malecova et al., “Targeted Tissue Delivery of RNA Therapeutics Using Antibody-Oligonucleotide Conjugates (AOCs), Nucleic Acids Res. 51, no. 12 (July 7, 2023): 5901–10, https://doi.org/10.1093/nar/gkad415.
9. Kyli Berkley et al., “Journey of PROTAC: From Bench to Clinical Trial and Beyond,” Biochemistry 64, no. 3 (Feb. 4, 2025): 563–80, https://doi.org/10.1021/acs.biochem.4c00577.
10. Bhavana Ramadas, Pritam Kumar Pain, and Debasish Manna, “LYTACs: An Emerging Tool for the Degradation of Non-Cytosolic Proteins,” ChemMedChem 16, no. 19 (Oct. 6, 2021): 2951–53, https://doi.org/10.1002/cmdc.202100393.
11. Daiki Takahashi et al., “Second-Generation AUTACs for Targeted Autophagic Degradation,” J. Med. Chem. 66, no. 17 (Sept. 14, 2023): 12342–72, https://doi.org/10.1021/acs.jmedchem.3c00861.
12. Syed Saqib Ali Zaidi et al., “Engineering siRNA Therapeutics: Challenges and Strategies,” J. Nanobiotechnol. 21, no. 1, 381 (2023), https://doi.org/10.1186/s12951-023-02147-z.DOI: 10.1186/s12951-023-02147-z
13. Priyanka Mangla, Quentin Vicentini, and Annabelle Biscans, “Therapeutic Oligonucleotides: An Outlook on Chemical Strategies to Improve Endosomal Trafficking,” Cells 12, no. 18 (Sept. 11, 2023): 2253, https://doi.org/10.3390/cells12182253.
14. Bowen Xiao et al., “Development, Opportunities, and Challenges of siRNA Nucleic Acid Drugs,” Mol. Ther.—Nucleic Acids 36, no. 1 (March 11, 2025): 102437, https://doi.org/10.1016/j.omtn.2024.102437.
15. Vera S. Eragova et al., “Smart Delivery Systems Responsive to Cathepsin B Activity for Cancer Treatment,” Pharmaceutics 15, no. 7 (June 29, 2023): 1848, https://doi.org/10.3390/pharmaceutics15071848.
16. Nareshkumar Jain et al., “Current ADC Linker Chemistry,” Pharm. Res. 32, no. 11 (March 11, 2025): 3526–40, https://doi.org/10.1007/s11095-015-1657-7.
17. Janet M. Sasso et al., “The Evolving Landscape of Antibody-Drug Conjugates: In Depth Analysis of Recent Research Progress,” Bioconjugate Chem. 34, no. 11 (Nov. 15, 2023): 1951–2000, https://doi.org/10.1021/acs. bioconjchem.3c00374.
18. Mahmood et al., “Clinical Pharmacology of Antibody-Drug Conjugates,” Antibodies. 10, no. 2 (May 21, 2021): 20, https://doi.org/10.3390/antib10020020

如您对本篇文章推介的相关业务感兴趣
请长按扫描上方二维码联系我们


