康方全方位新药研究开发平台ACE平台,涵盖了药物靶点验证、抗体发现与临床前研究、CMC生产工艺开发和符合GMP要求的规模化生产,全面覆盖抗体蛋白、新型细胞治疗、核酸药物(siRNA/mRNA) 等方向。

Tertrabody双抗/多抗平台:Tetrabody技术是康方生物自主开发的、用于设计及生产创新四价双特异性抗体的专有技术。该技术克服了由于双特异性抗体的高分子量导致的低效表达水平、双特异性抗体的结构异质引起的工艺开发障碍、以及由于双特异性抗体缺乏稳定性而导致的药物不可成药性等CMC难题。
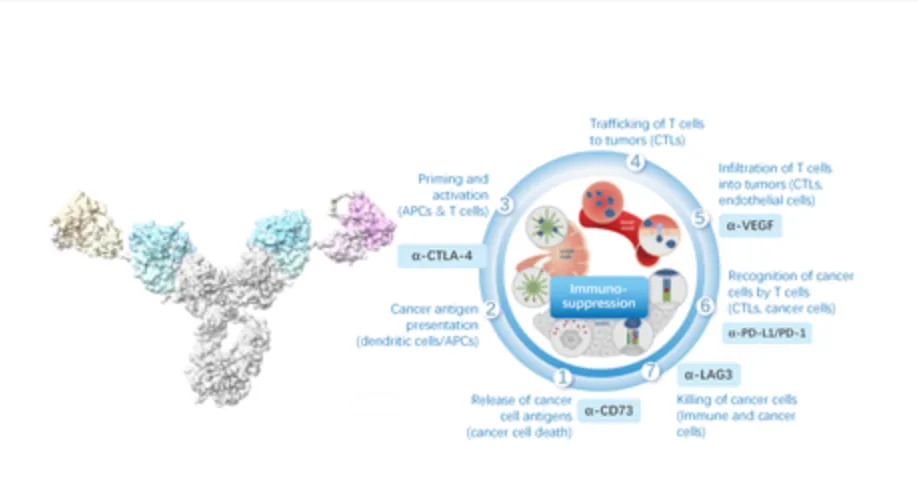
抗体偶联 Dual-Shield ADC 平台:凭借在多特异性抗体领域的领先优势,康方自主开发了独有的抗体偶联药物(ADC)技术平台,已研发了多个具有领先性的第三代ADC和双抗ADC产品。
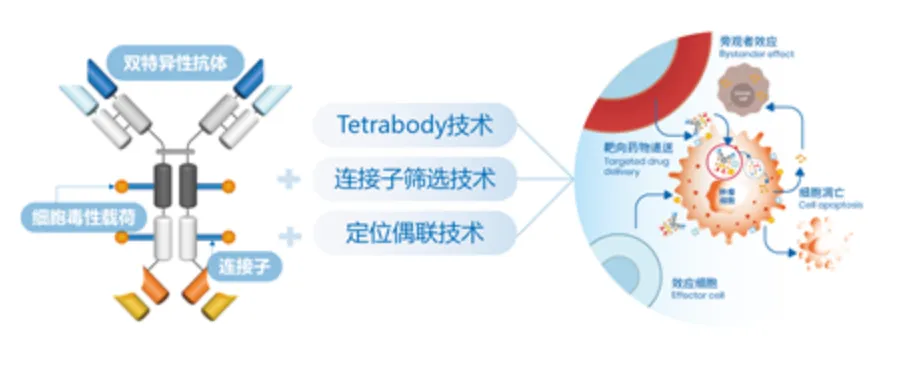
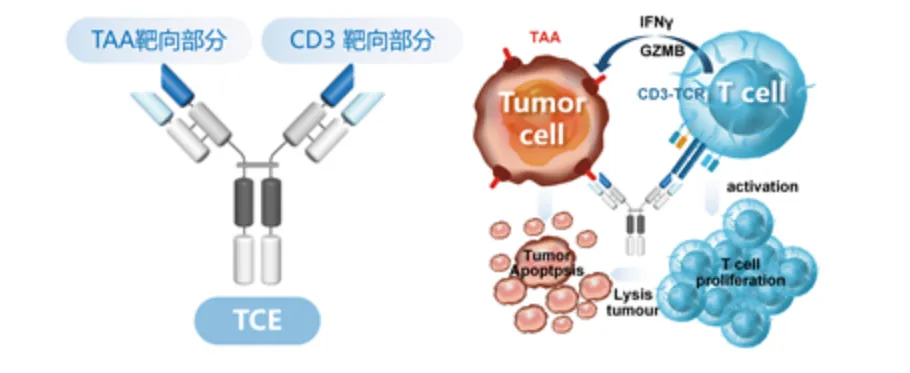
T细胞衔接器 Dual-Lock TCE 技术平台:康方自主开发了独有的减毒增效抗体T细胞衔接器技术平台,已有多个管线在研,并快速向临床推进中 。
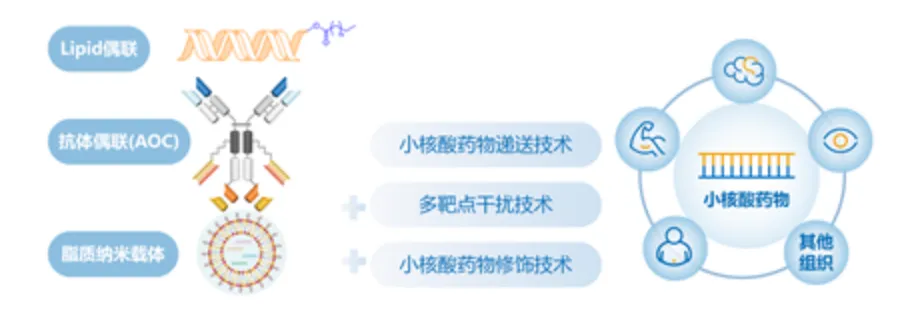
Tissue-Smart siRNA 平台:康方自主开发了多个肝外递送siRNA技术平台,已有多个创新性siRNA药物管线,布局多个治疗领域 。
细胞治疗技术平台:紧扣生物科技前沿,康方打造全新的CARL-NK细胞治疗药物开发平台,以现有创新技术为基础,实现NK细胞多维度的基因工程优化突破。
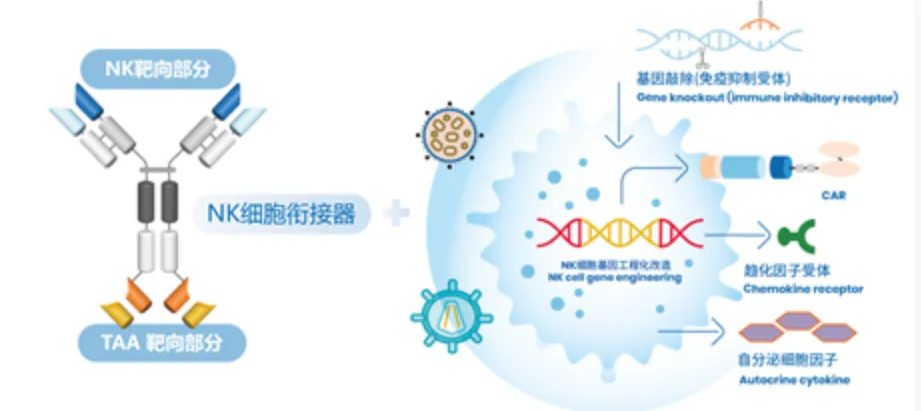
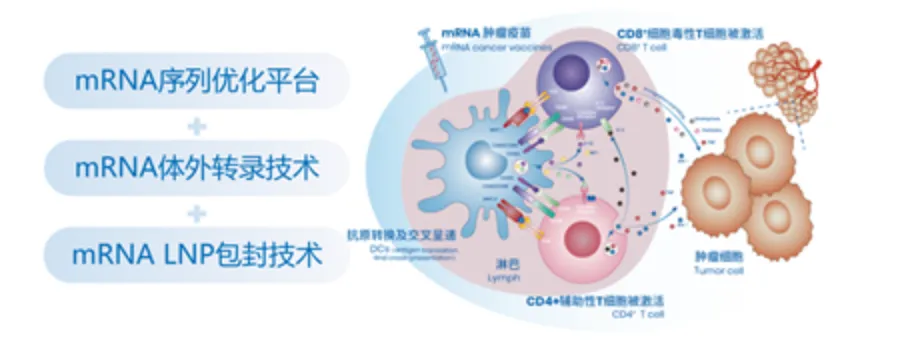
Flex-Nano mRNA 平台:抢占生物医药高地,康方开发了从mRNA序列设计到递送系统的完整链条技术平台,正在开发mRNA肿瘤治疗性疫苗和基因治疗产品管线,具有全球先发优势。
依达方®(PD-1/VEGF双抗,依沃西单抗注射液)
康方生物自主研发的全球首创PD-1/VEGF双特异性肿瘤免疫治疗药物,于2024年5月获得中国国家药品监督管理局批准上市,是全球首个获批上市的“肿瘤免疫+抗血管生成“协同抗肿瘤机制的双特异性抗体新药。
2024年5月,依沃西获批用于经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗进展的EGFR突变的局部晚期或转移性非鳞非小细胞肺癌(nsq-NSCLC)。2025年4月,依沃西一线治疗PD-L1表达阳性的晚期非小细胞肺癌的适应症在获批上市,该项适应症的III临床HARMONi-2研究中,依沃西头对头“药王”帕博利珠单抗获得决定性胜出阳性结果,成为全球首个在头对头III期临床研究中证明疗效显著优于“药王”的药物;该项适应症的获批为患者提供了全新更优的“去化疗”选择。
开坦尼®(PD-1/CTLA-4双抗,卡度尼利单抗注射液)
公司自主研发的全球首创PD-1/CTLA-4双特异性肿瘤免疫治疗药物,于2022年6月获得中国国家药品监督管理局批准上市,是世界上第一个肿瘤免疫治疗双抗新药,也是中国的第一个双特异性抗体新药。
卡度尼利已获批3项适应症:2022年6月29日,卡度尼利获得批准用于既往接受含铂化疗治疗失败的复发或转移性宫颈癌患者的治疗;2024年9月,卡度尼利联合方案用于局部晚期不可切除或转移性胃或胃食管结合部(G/GEJ)腺癌患者一线治疗适应症获批;2025年5月,卡度尼利加含铂化疗联合/不联合贝伐珠单抗一线治疗持续、复发或转移性宫颈癌的适应症获批。
安尼可 ®(PD-1单抗,派安普利单抗注射液)
目前全球唯一采用IgG1亚型并进行Fc段改造的新型差异化PD-1单抗,能够更有效增强免疫治疗疗效,且减少不良反应。
目前,派安普利5项适应症均已经获得批准并上市销售:联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌、联合方案一线治疗晚期肝细胞癌、治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤,以及一线治疗和二线后治疗转移性鼻咽癌。
伊喜宁®(PCSK9单抗,伊努西单抗注射液)
公司自主开发创新的PCSK9单克隆抗体新药,于2024年9月获批上市,主要用于治疗原发型高胆固醇血症和混合型高脂血症,包括杂合子家族性高胆固醇血症 (HeFH) 及同时患有动脉粥样硬化性心血管疾病的高胆固醇血症,成为公司非肿瘤领域的首个获批产品。
爱达罗®(IL-12/IL-23单抗,依若奇单抗注射液)
公司自主研发的新型人源化IL-12/IL-23单克隆抗体新药,获得国家“重大新药创制”科技重大专项课题支持,主要用于治疗银屑病、溃疡性结肠炎和其他自身免疫性疾病。
【免责声明】本文信息来源于上市公司公告等公开资料,不保证真实、准确、完整,不代表本人立场及任何投资建议。
【作者简介】厦门大学硕士,医学、法学复合背景,保荐代表人,注册会计师,律师,10+年投行经验,某券商在职员工。


