CAR-T细胞疗法作为一种新的治疗方式,为癌症患者提供了突破性的疗效及治愈潜力。自2017年首款CAR-T细胞疗法产品获批以来,全球CAR-T细胞疗法市场一直在强劲增长。随著全球癌症发病率上升,更多适应证的CAR-T细胞疗法获批,生产技术及能力提升,以及CAR-T细胞产品在更多市场可及,预计全球CAR-T细胞疗法市场将进一步增长。截至2025年6月,有七款CAR-T细胞产品获得美国FDA批准,以及七款CAR-T细胞产品获得中国NMPA批准。然而,全球癌症患者仍有大量未被满足的医疗需求,需要更好更多的创新CAR-T细胞产品,尤其是用于治疗实体瘤的创新CAR-T细胞产品。公司凭借赛恺泽®及舒瑞基奥仑赛注射液等管线产品以及CycloCAR®、THANK-uCAR®、THANK-u Plus™、LADAR™及CARcelerate®等创新技术平台,致力于开发创新疗法以满足该等未被满足的医疗需求。

赛恺泽®(泽沃基奥仑赛注射液)是一种用于治疗复发或难治性多发性骨髓瘤的全人抗自体BCMA CAR-T细胞产品,其融合了具有低免疫原性和较高稳定性的全人源BCMA特异性单链可变片段(scFv)的CAR结构,在没有肿瘤相关靶点的情况下,可降低CAR-T细胞的自我激活,克服了T细胞耗竭的问题。。国家药品监督管理局于2024年2月23日批准赛恺泽®新药上市申请,用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
2023年1月,科济药业及华东医药(杭州)有限公司就在中国大陆地区商业化赛恺泽®的独家权利签订协议。已收取首付款2亿元人民币和监管里程碑付款人民币7500万元。根据协议条款,科济药业还有权获得最高不超过 10.25亿元人民币的注册及销售里程碑付款。科济继续负责赛恺泽®在中国大陆地区的开发、注册及生产。在商业化落地方面,华东医药已组建独立专业、全方位的商业化团队全面推广赛恺泽®,已利用中国多层次保险体系,提高患者可及性。
舒瑞基奥仑赛注射液是一种全球潜在同类首创的、靶向Claudin18.2蛋白的自体CAR-T细胞产品。舒瑞基奥仑赛注射液用于治疗Claudin18.2阳性实体瘤,主要治疗胃癌和胰腺癌。Claudin18.2在一系列实体瘤中表达,包括G/GEJA、PC、结直肠癌、肺癌和卵巢癌。科济药业是全球范围内率先成功识别、验证并报告Claudin18.2作为实体瘤相关抗原及CAR-T细胞疗法的可行靶点。科济药业针对舒瑞基奥仑赛注射液开发了一种受专利保护的创新性清淋预处理方案,该方案的特点是在包括环磷酰胺和氟达拉滨的传统清淋方案基础上加入低剂量的白蛋白结合型紫杉醇。
2025年6月,中国NMPA的CDE已受理舒瑞基奥仑赛注射液的NDA,用于治疗Claudin18.2表达阳性、至少二线治疗失败的晚期胃癌。2025年5月及3月,CDE向舒瑞基奥仑赛注射液分别授予优先审评及突破性治疗药物品种认定。
科济药业还利用专有THANK-uCAR®平台推进差异化的通用型CAR-T细胞产品。科济药业最近开发的THANK-u Plus™平台,作为THANK-uCAR®通用型CAR-T技术的升级版,以克服NKG2A表达水平对疗效可能的影响。
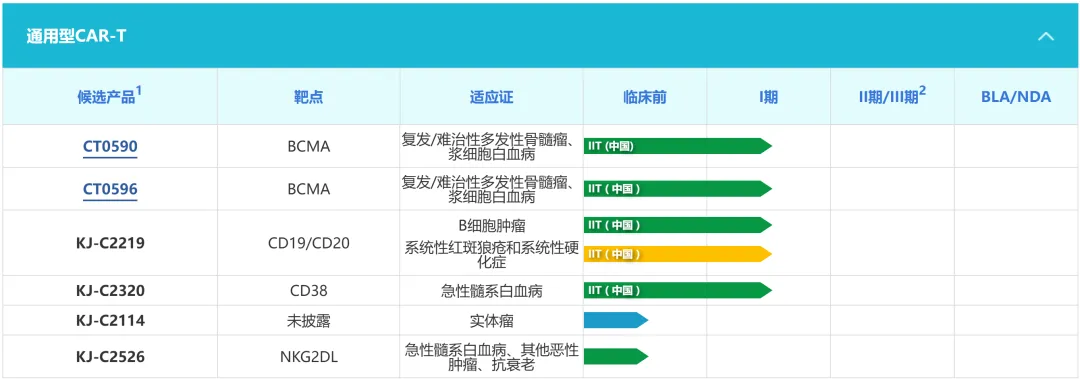
CT0590是一种利用THANK-uCAR®技术靶向BCMA的通用型CAR-T细胞候选产品。在中国已经启动一项研究者发起的临床试验,旨在评估CT0590治疗复发或难治性多发性骨髓瘤的安全性和疗效。CT0590 IIT概念验证研究结果已于2024年12月在第66届ASH年会上进行展示,标题为「CT0590:一种靶向BCMA和NKG2A的三重基因敲除异体CAR-T细胞疗法在复发/难治性多发性骨髓瘤患者中的首次人体研究」。
CT0596是一种利用THANK-u Plus™技术靶向BCMA的通用型CAR-T细胞候选产品。一项研究者发起的临床试验已在中国启动,旨在评估CT0596治疗复发或难治性多发性骨髓瘤及复发或难治性浆细胞白血病的安全性和疗效。截至2025年5月6 日,此项临床研究已经完成8例至少经过三线治疗后的复发或难治性多发性骨髓瘤患者的细胞输注,所用清淋方案为FC方案(氟达拉滨22.5-30 mg/m2,环磷酰胺为350-500 mg/m2)。已完成首次第4周疗效评估的五名患者中,其中3名 (60%)达到sCR/CR,4名(80%)达到骨髓微小残留病(MRD)阴性。所有sCR/CR患者均在持续缓解中,包括已完成第4个月访视的首名患者。无剂量限制性毒性(DLT)、3级及以上的细胞因子释放综合征(CRS)、免疫细胞 治疗相关神经毒性综合征(ICANS)或移植物抗宿主病(GvHD)。根据初步安全性及疗效数据,CT0596用于R/R MM患者总体耐受性良好,在所有预设剂量组都观察到了CAR-T细胞的扩增,并出现了令人鼓舞的疗效信号。


