
关注康薪KANGLIFE,获取更多IVD及临床法规最新资讯

康薪咨询
KANGLIFE CONSULTING
中国医药研发外包(CRO)行业政策汇总及解读,改革制度助力行业发展提速
01
CRO政策发展历程

中国国民经济规划医药研发外包(CRO)政策的演变
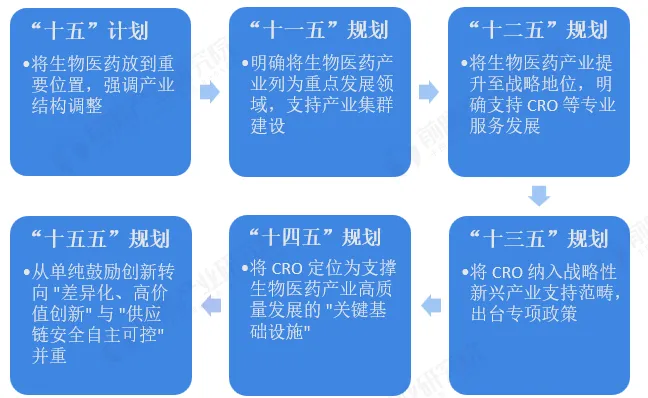
(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)
02
国家层面CRO政策汇总及解读

截至2025年11月国家层面有关CRO行业的政策重点内容解读 (一)
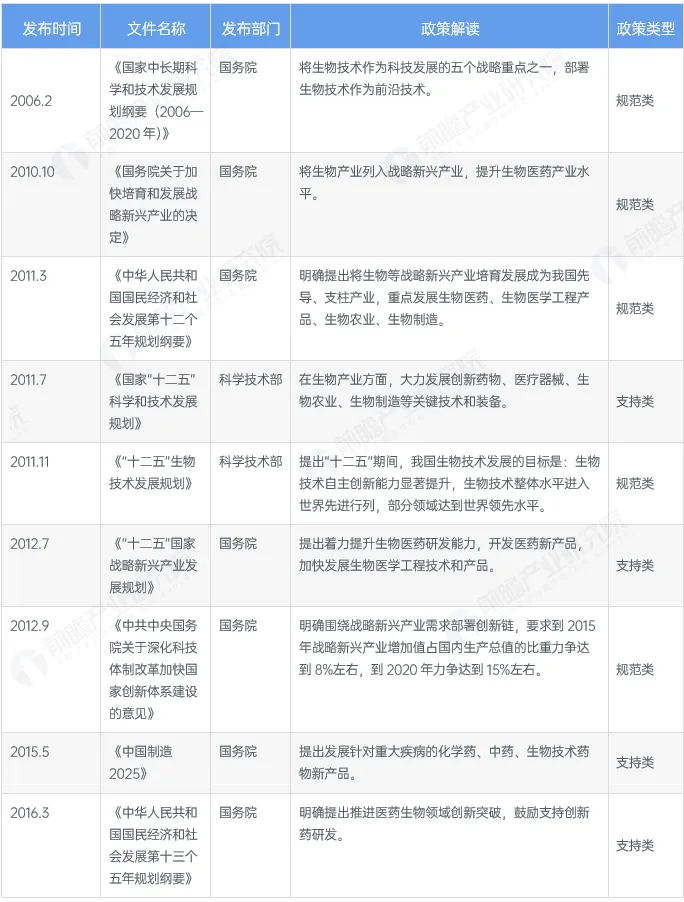
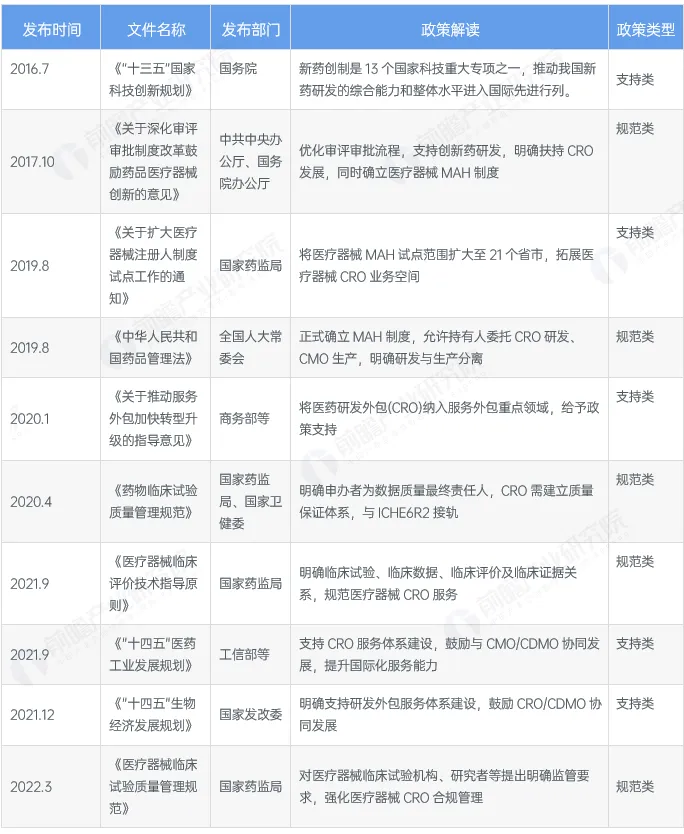
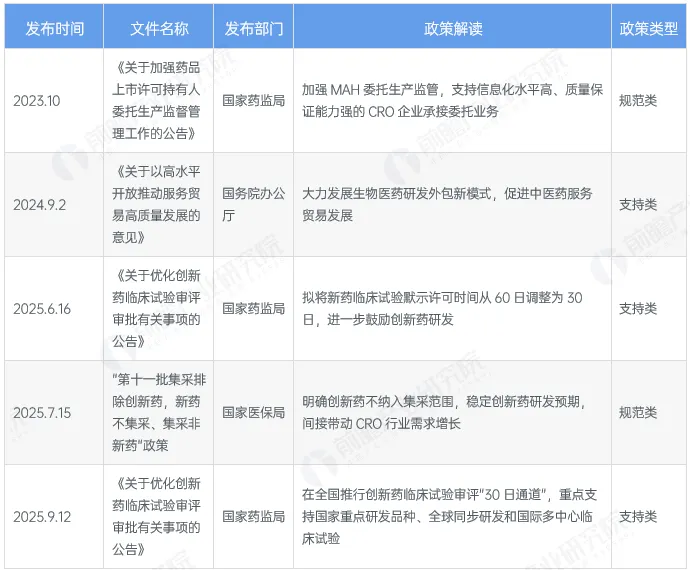
(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)

中国药品审评审批制度改革政策汇总及解读

(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)

《国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》政策内容解读
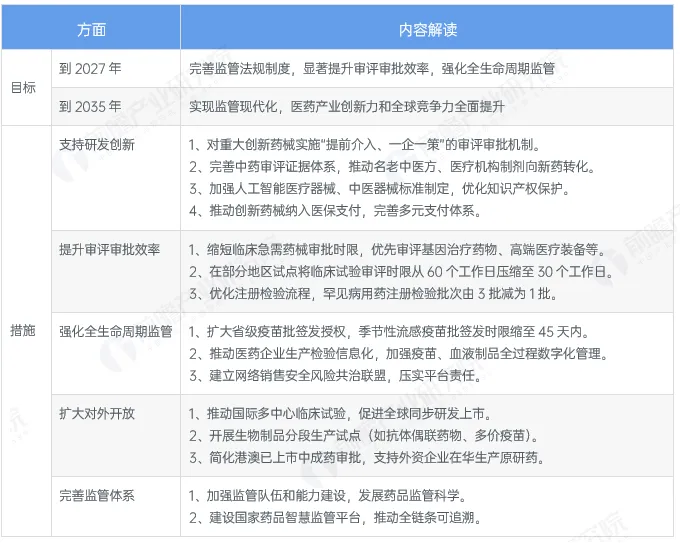
(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)

03
省市层面CRO政策汇总及解读

截至2025年11月各省市层面有关CRO行业政策重点内容解读 (一)
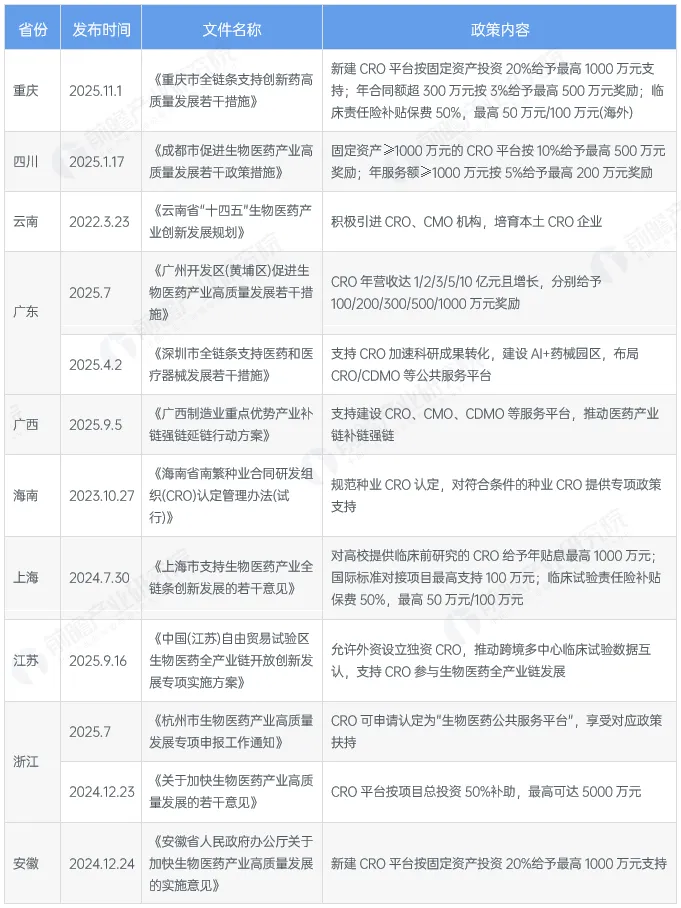
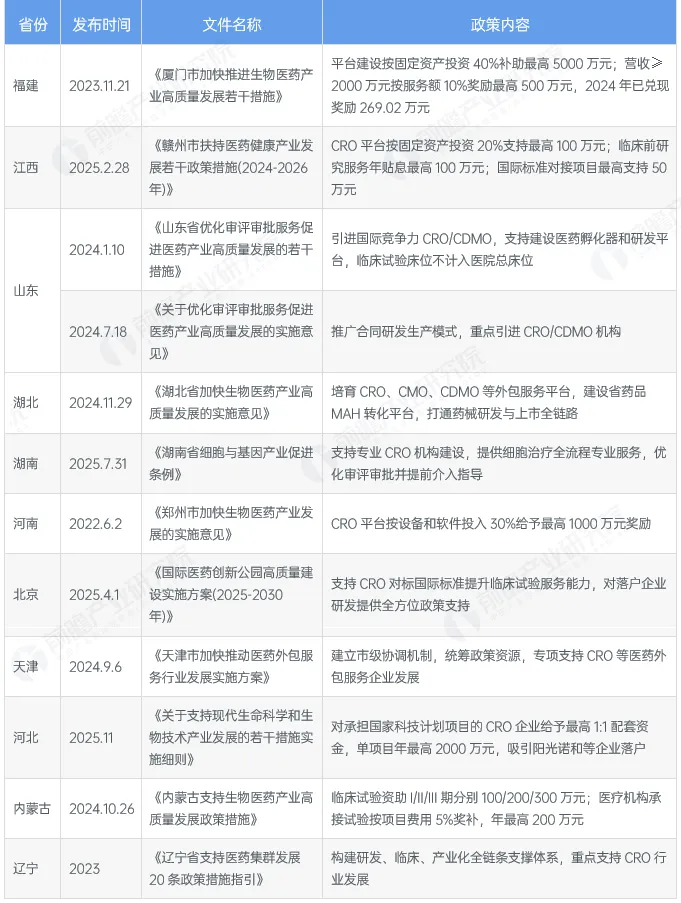
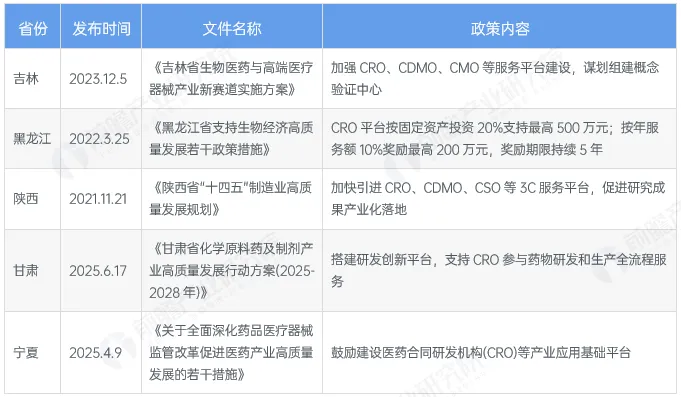
(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)

中国部分省份关于CRO产业的目标布局
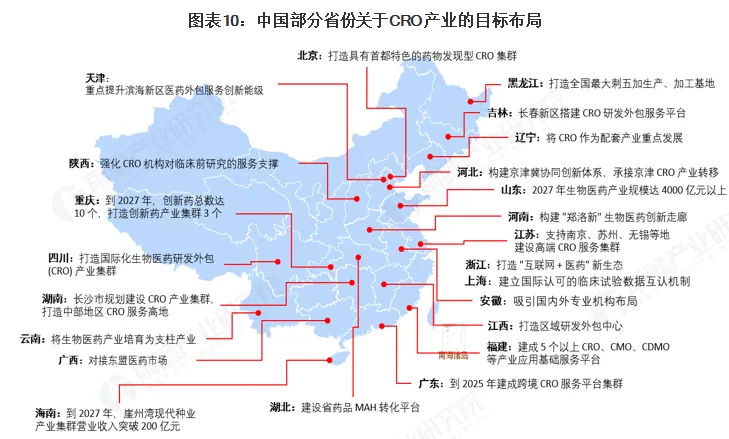
(*数据来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》)
总结
当前,我国CRO行业正呈现"全球化布局加速、行业集中度提升"的发展趋势,在国家"十四五"生物经济发展规划、创新药临床试验快速审批通道及地方对CRO直接贴息支持等政策大力扶持下,CRO通过专业化服务帮助医疗器械企业大幅缩短研发周期、有效降低研发成本,助力企业高效应对法规差异、加速海外注册等,已成为医疗器械制造商突破技术壁垒、加速产品上市的核心战略伙伴和产业新基建。
康薪咨询全球化合规一站式服务
康薪咨询自成立以来,致力于为医疗器械及IVD企业提供全生命周期合规服务,助力本土企业高效突破国际法规壁垒、实现全球化布局:
临床试验服务:依托欧洲、泰国等地战略合作实验室与医院,提供临床前性能验证、临床试验、上市后评估等全链条临床服务
国际法规注册:覆盖欧盟IVDR/MDR、中国NMPA、美国FDA、英国MHRA、澳大利亚TGA、日本PMDA、韩国MFDS、新加坡HSA、泰国TFDA、马来西亚MDA、沙特SFDA、阿联酋MOHAP、巴西ANVISA、墨西哥COFEPRIS等全球主要市场的技术文件辅导与申报;
质量管理体系:ISO 13485、MDSAP等国际质量体系搭建与认证支持;
出海战略支持:当地授权代表服务、出海战略规划及合规人才培养等
*资料来源:前瞻产业研究院《2025年中国医药研发外包(CRO)行业政策汇总及解读》
*声明:本文章报告内容均为转载,仅用于分享,如涉及版权等问题,请随时与我们取得联系,我们将于第一时间进行修正,谢谢。
康薪咨询团队可承接欧洲多国、泰国、中国等多国医疗器械及IVD器械注册要求的临床实验研究项目(可出具伦理批件),可为IVD企业提供全生命周期的解决方案服务。
康薪KANGLIFE
业务范围
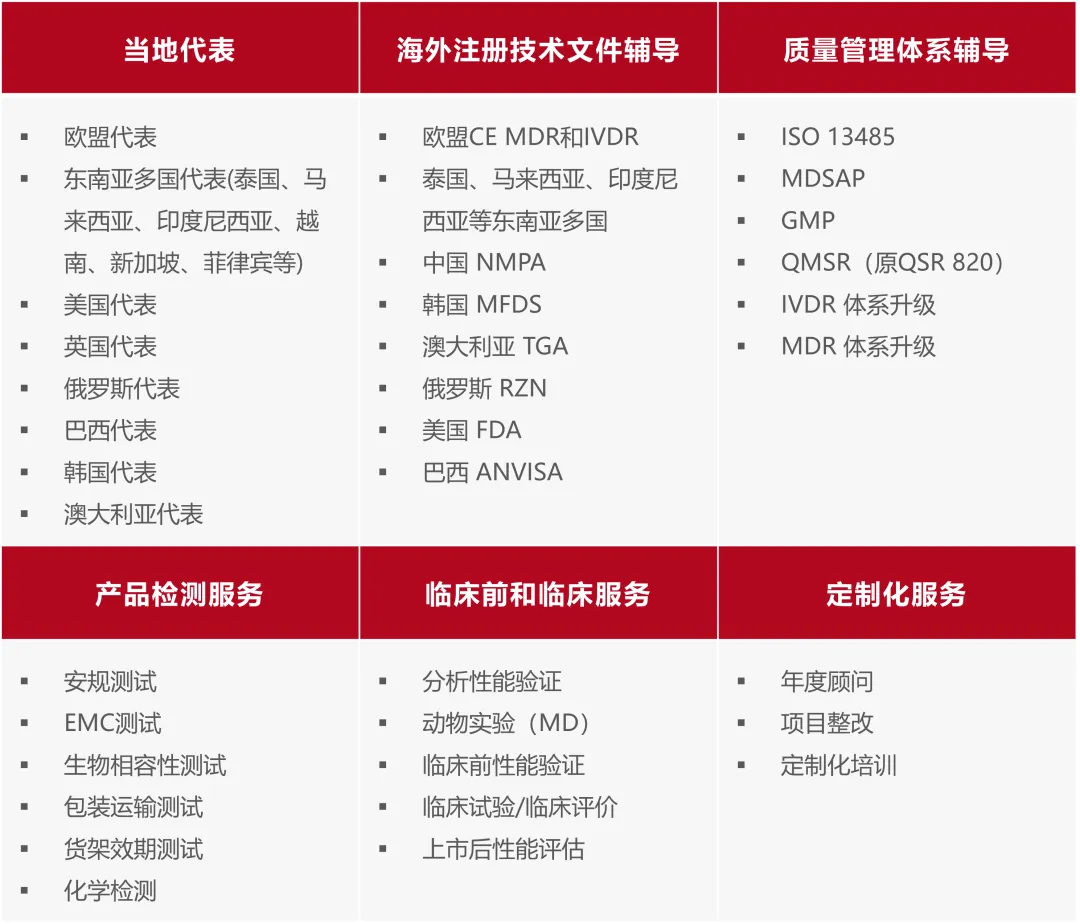
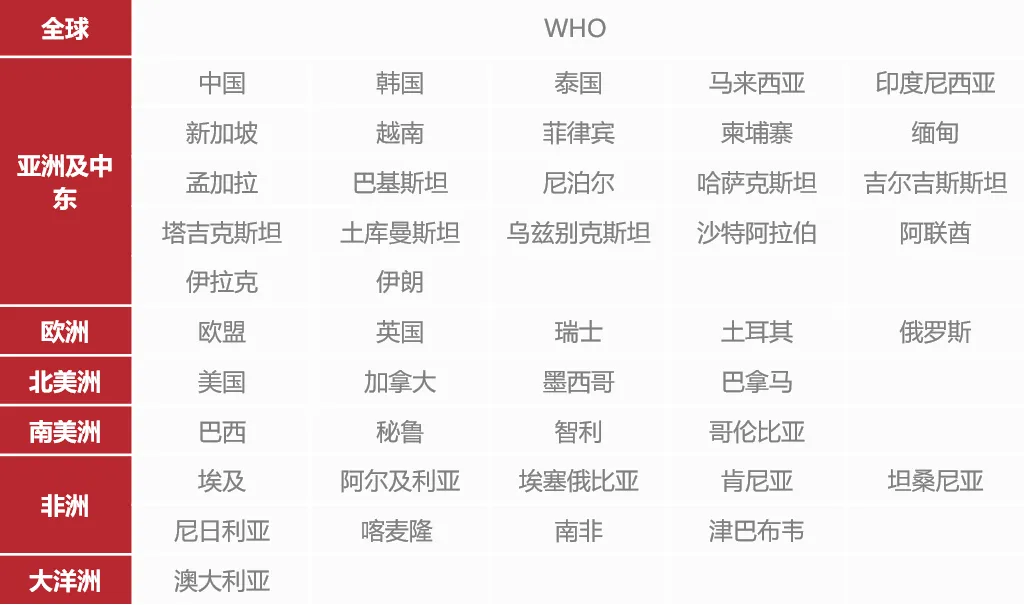
注册服务支持区域
临床实验室资源

关于康薪咨询
ABOUT KANGLIFE
| 专业特色:
协同企业,共同定制出海战略服务。
| 核心文化:
协助国内外优秀体外诊断及医疗器械企业实现战略发展、培养合规人才,携手共筑中国企业出海愿景。
康薪咨询成立以来已与数百家企业强强联合,协同高效合作,提供定制化服务,成功获得多个欧美和东南亚市场准入资质。
推荐阅读
业务咨询
CONTACT US

华北区咨询顾问
Harold Hua

华东区咨询顾问
Joyce Hua

华南区咨询顾问
Fitter Cao


关注康薪咨询
Follow KANGLIFE
点击下方”阅读原文“,即刻与我们取得进一步联系!


