
Journal Club 09/30/2025
1958年,英国科学家弗朗西斯·克里克提出生命的“中心法则”,并于1970年修正,揭示遗传信息DNA如何转录成mRNA最后翻译为蛋白质的流动路线[1]。1990年起,人类基因组计划 (HGP) 的启动实施,成功解析人类遗传密码的30亿个DNA碱基对和大约25000个基因,开启研究遗传信息如何决定生物功能的新纪元。面对这30亿个碱基对,科学家们还并不能完整地理解基因组,关键在于缺少精准空间和时间的信息。作为一类将分子分析与空间分辨成像相结合的前沿技术,时空组学能够在完整组织架构中同时获取基因表达、蛋白质丰度、代谢物分布等高维分子数据,并保留其准确的空间坐标。
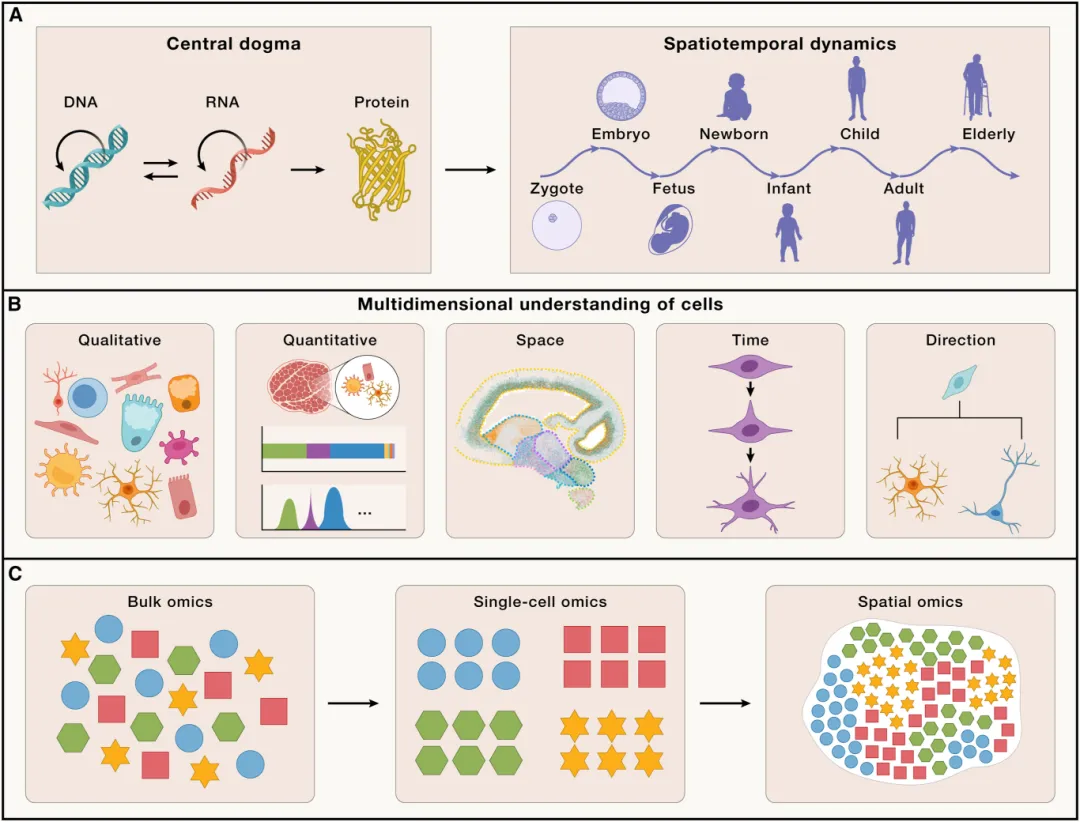
图1. 细胞的多维测量。来源:Liu L, Chen A, Li Y, Mulder J, Heyn H, Xu X. Spatiotemporal omics for biology and medicine. Cell. 2024;187(17):4488-4519
技术革新:从静态测序到动态时空解析
传统单细胞转录组测序的原理是将组织细胞打散制备为单细胞悬液进行检测和分析,提供的是基因的平均表达水平,丢失了细胞与细胞相互作用、细胞的时空关系,这可能会掩盖真实的细胞比例和细胞亚群的特异性。时空组学能够在完整组织架构中同时获取基因表达、蛋白质丰度、代谢物分布等高维分子数据,并保留其空间坐标信息,本质在于能够在精确的空间坐标下对分子 (DNA、RNA、蛋白质等) 组成、定位、细胞-细胞相互作用和空间动力学进行全面测绘。
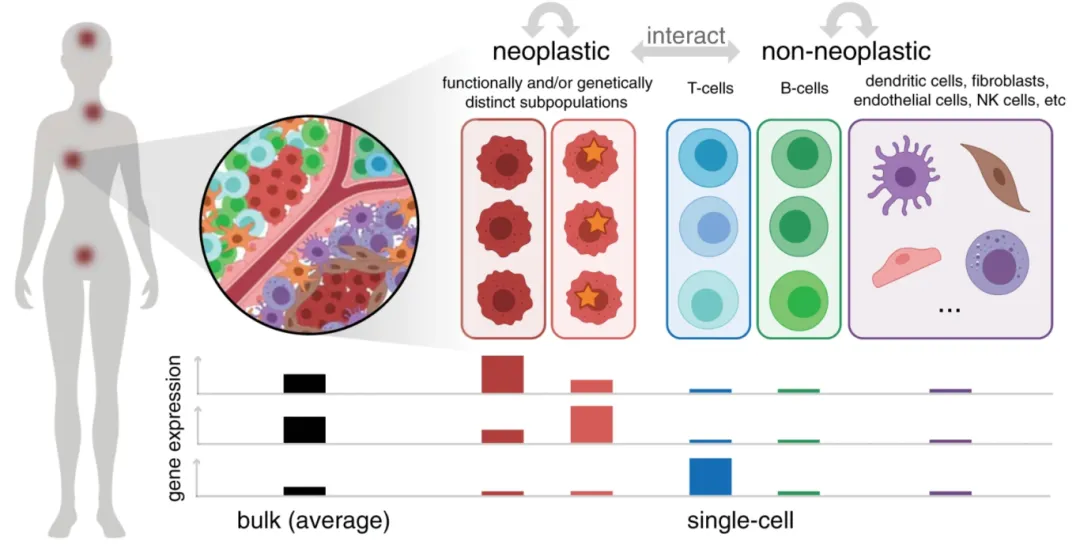
图2. 癌症可能表现为空间上不同的多个肿瘤,由功能或遗传上不同的肿瘤亚群以及相互作用影响临床结果的多种非肿瘤细胞类型和状态组成。来自:Fan J, Slowikowski K, Zhang F. Single-cell transcriptomics in cancer: computational challenges and opportunities. Exp Mol Med. 2020;52(9):1452-1465
时空组学根据所分析的分子层次,可将其分为空间转录组学、空间蛋白质组学、空间代谢组学等多个领域。根据方法的原理,主要分为基于原位捕获的方法 (如10x Visium、华大Stereo-seq) 和基于原位成像的方法 (如MERFISH、CODEX/PhenoCycler)。
作为最早的空间转录检测技术,荧光原位杂交 (FISH) 使我们能够在细胞内直接观察到RNA或DNA的布局,它通常使用多个带有荧光标记的短单链寡核苷酸探针,特异性地结合到靶RNA分子上[2]。最后通过荧光显微镜,每个结合的探针荧光信号被检测为一个亮点信号,从而定量分析RNA的丰度和单个细胞中的位置。早期空间转录检测技术虽然在检测通量和灵敏度上存在局限,但已经能够为免疫学研究提供有价值的信息。
1998年首次报道的单分子荧光原位杂交 (smFISH) 技术使每个mRNA分子都可以被可视化为一个荧光斑点,使得单分子水平对转录本进行定量和定位成为可能。Oroboros smFISH (OsmFISH) 通过荧光成像记录每轮中多个转录本的空间位置,图像采集后洗脱探针进行下一轮荧光杂交,靶标的数量由荧光通道的数量和杂交周期的数量决定[3]。通过这种方法,OsmFISH可以同时检测33个转录本的表达。现代时空转录组学技术,如多重纠错荧光原位杂交FISH (MERFISH, Multiplexed Error-Robust Fluorescence In Situ Hybridization) 和连续/顺序荧光原位杂交FISH (seqFISH, sequential fluorescence in situ hybridization),在原有的测序技术上采用组合条形码和顺序成像策略,使用具有容错编码方案的组合标记方法实现在单细胞中同时鉴定数千种RNA的空间定位信息。
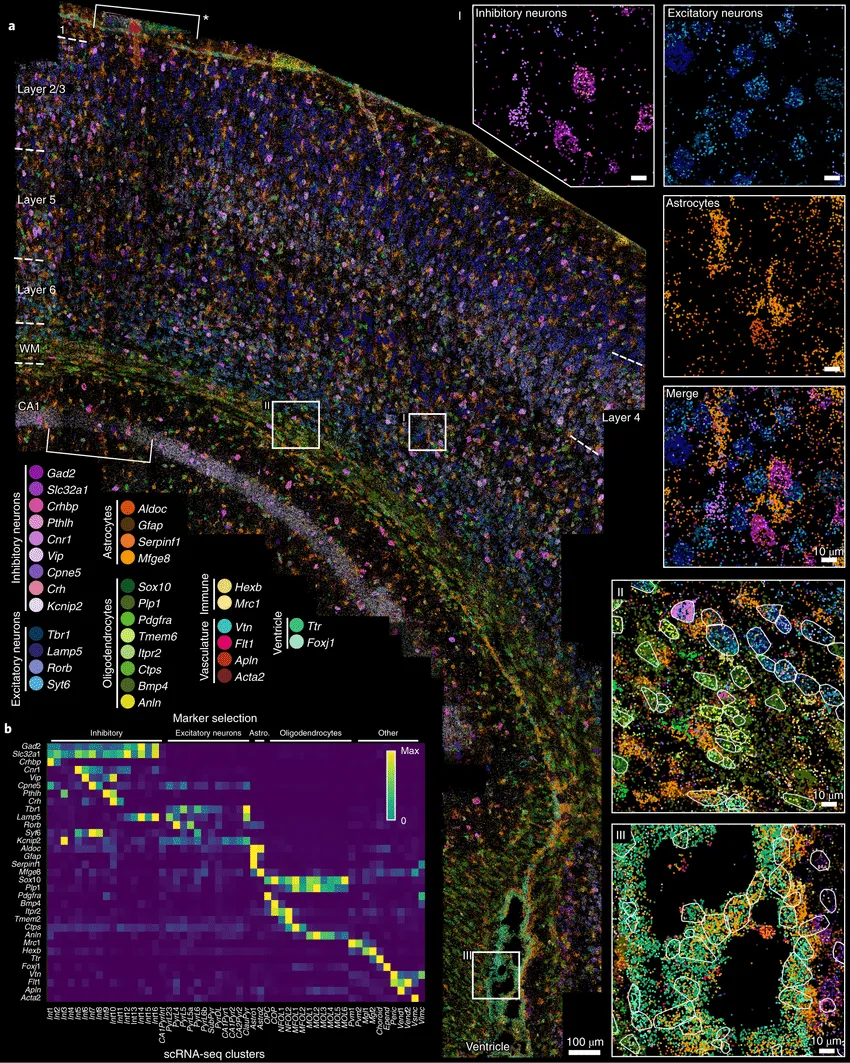
图3. osmFISH揭示了小鼠体感皮层中基因的空间表达。来自:Codeluppi, Simone et al. Spatial organization of the somatosensory cortex revealed by osmFISH. Nat Methods. 2018;15(11):932-935
原位成像的另一种方法是原位测序 (ISS),在细胞内原位读取目标核酸的特定序列实现多个基因的同时检测。
传统原位测序 (ISS)是通过滚环扩增(RCA)产生包含大量拷贝目标序列的克隆扩增滚环产物 (RCP),然后通过连接RCP读取目标序列[4]。第一代ISS的主要缺点是检测效率低,主要是由于原位反转录形成cDNA的效率低所致。空间分辨转录扩增 (STARMAP) 使用双引物形成DNA纳米球和水凝胶组织化学的方法绕过反转录步骤,将可检测的基因数量增加到1000个,从而显著提高检测效率[7]。通过这些原位成像技术,已经初步认识到免疫细胞在组织中的非随机分布、细胞间相互作用的空间约束性以及免疫微环境的区域特性。
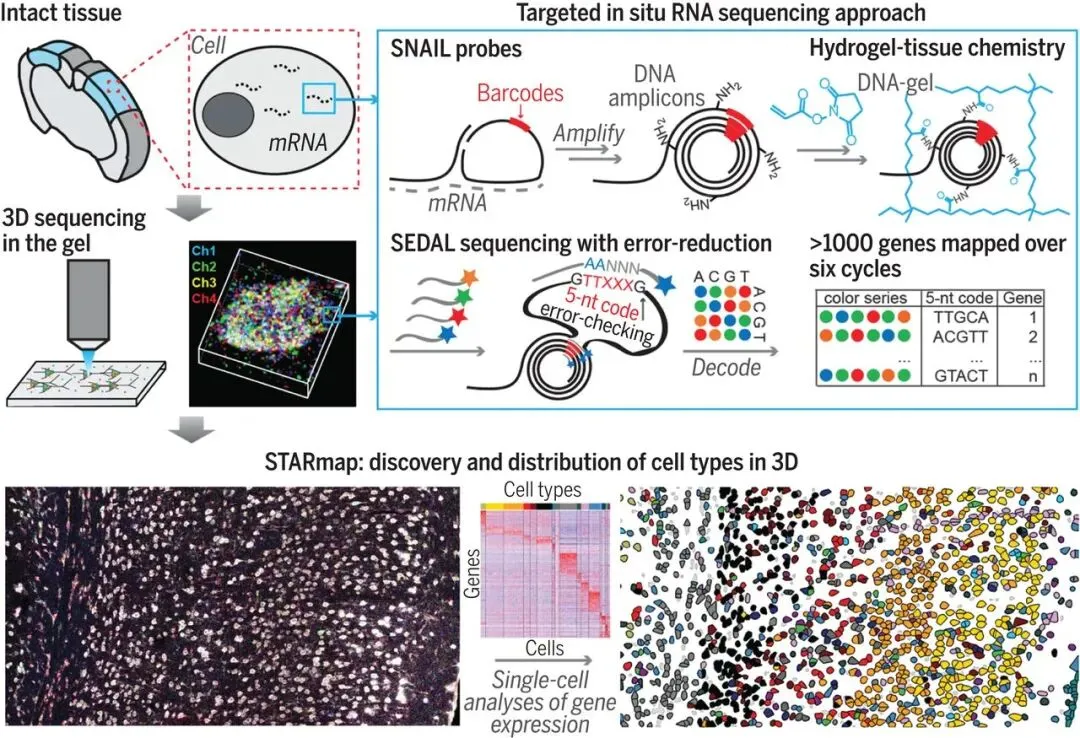
图4. 用于 3D 转录组成像和分子细胞分型的 STARmap技术。来自:Wang X, Allen WE, Wright MA, et al. Three-dimensional intact-tissue sequencing of single-cell transcriptional states. Science. 2018;361(6400):eaat5691
基于测序的空间转录学的本质在于捕捉和标记具有空间位置信息的分子。
第一代空间转录组学技术通过物理切割组织蜡块获得细胞团的空间位置信息,如基于组织切片的Tomo-seq[5]和基于显微镜的Geo-seq[6]。这些组学技术通过在预设位置对组织物理分割后进行单独的转录测序,然后基于空间信息进行3D结构组装,但受限于物理切割的精细程度。第二代空间转录技术-NICE-Seq和ZipSeq,使用光敏基团来预先修饰捕获探针,同时使用“空间条形码技术”检测RNA分子,在一定程度上提高了分辨率。
2016年是空间转录组学发展的一个重要里程碑,瑞典皇家理工学院的Joakim Lundeberg团队开发了首个基于原位捕获RNA的空间转录组学方法[8]。这项技术的核心创新在于使用带有空间条形码的捕获探针,当组织切片放置在玻片上时,组织中的mRNA被原位捕获并通过条形码记录其空间位置,随后进行高通量测序。这种方法首次实现了在全转录组范围内保留基因表达的空间信息,标志着空间转录组学时代的到来。
在空间转录组技术领域,10x Genomics和华大 (BGI) 两家公司是重要参与者。10x Genomics的Visium空间转录组学技术,通过使用预先带有独特空间条形码 (Spatial Barcode) 的寡核苷酸探针阵列玻片,将探针与mRNA结合连接形成完整探针序列,再经过透化等过程,最终构建成完整的文库。核心在于每个探针都携带着独特的空间条形码和唯一分子标识符 (UMI),标记每一条mRNA分子的“地理位置”。 Visium的出现降低了空间转录组学的技术门槛,使其迅速在免疫学领域得到应用,特别是在肿瘤免疫微环境、自身免疫疾病和免疫器官发育等研究中发挥重要作用。此外,10xGenomics还提供Xenium平台,这是一种基于原位成像的方法,通过反复的探针杂交和成像,能以更高的灵敏度和亚细胞分辨率对数百个靶基因进行精准定位。
华大 (BGI)自主研发的Stereo-cell技术,核心在于高密度DNA纳米球 (DNB) 阵列通过静电吸附捕获细胞,实现原位动态测序,捕捉基因转录活性变化,并保留空间位置及时序变化信息[9]。这些技术使免疫学研究进入了空间解析的新时代。利用这些高分辨率空间转录组技术,研究人员开始深入探索免疫细胞在组织中的三维空间、细胞间通信网络以及微环境特异性调控。
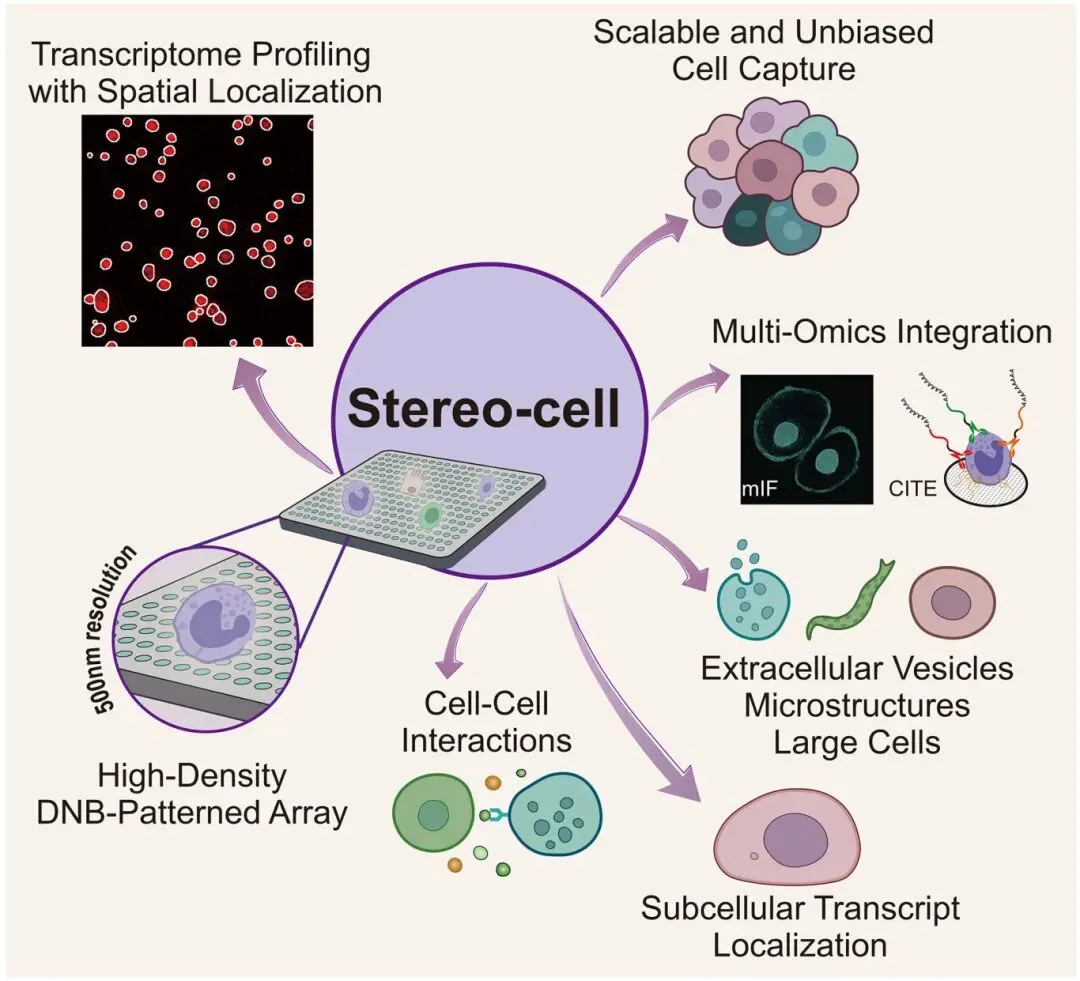
图5. Stereo- cell:一种单细胞多模态平台。来自:Liao S, Zhou X, Liu C, et al. Stereo-cell: Spatial enhanced-resolution single-cell sequencing with high-density DNA nanoball-patterned arrays. Science. 2025; 389(6762):eadr0475
时空组学如何重塑免疫学研究
时空组学就像一个强大的“生命GPS系统”,能精确定位和追踪免疫细胞在时间和空间上的动态变化,助力揭示免疫应答时空动态背后的机制。其中肿瘤免疫微环境是一个高度复杂的生态系统,免疫细胞、肿瘤细胞和基质细胞通过精密的相互作用共同影响肿瘤的进展和治疗响应。时空组学技术使我们能够从空间维度重新审视这一系统,揭示了许多先前传统测序技术没有发现的免疫学效应及其机制。
肿瘤微环境的时空异质性,是指构成肿瘤的细胞 (如癌细胞、免疫细胞、成纤维细胞等) 及其周围的支持结构在空间位置和时间进程上呈现出的复杂且动态的不均一性。
在空间维度上,同一肿瘤内部不同区域 (如核心区、边缘区、侵袭前沿) 的细胞组成、血管分布、免疫细胞浸润程度和细胞外基质状态都存在显著差异,形成各具特色的“生态位”。在时间维度上,随着肿瘤进展或受到治疗 (如化疗、免疫治疗) 的影响,其微环境的组成和功能状态会发生动态演变。这种时空异质性是导致免疫治疗响应不一、出现获得性耐药以及预后判断复杂化的根本原因之一,也是当前精准医疗需要攻克的核心难题。
2024年3月,比利时大学的Diether Lambrechts团队在Immunity在线发表“CD4+ T cell activation distinguishes response to anti-PD-L1+anti-CTLA4 therapy from anti-PD-L1 monotherapy”论文,首先通过10X Visium空间转录组学发现,单药 (抗 PD‑L1) 治疗主要引起肿瘤细胞内CD8+ T 细胞扩增;而联合疗法 (抗 PD‑L1+抗 CTLA4) 则同时扩增 CD4+ 和 CD8+ T细胞,并且这些 CD4+ T细胞呈现活化的Th1表型。随后通过空间蛋白组学技术,发现扩增的CD4+与 CD8+ T细胞在肿瘤组织中共定位,并且被表达T细胞归巢因子的树突状细胞或产生抗体的浆细胞所围绕。这些发现为抗PD-L1、抗PD-L1和抗CTLA4联合治疗的机制提供了新的见解[15]。
2025年,四川大学李为民教授团队在Advanced Science在线发表“SLPI+ AT2-Like Cells Orchestrate Lung Adenocarcinoma Invasion via Wnt Pathway Activation and Stromal Crosstalk in a Spatially Defined Margin Niche”论文。研究人员利用时空组学技术发现肿瘤组织中免疫细胞表现出明显的空间分布现象。通过整合空间转录组与单细胞RNA测序数据发现一种表达分泌性白细胞蛋白酶抑制剂 (SLPI) 的AT2样细胞亚群特异性定位在肿瘤侵袭边缘,驱动肺腺癌从微浸润 (MIA) 向浸润 (IA) 状态转变[10]。其机制在于该细胞亚群通过上调Dickkopf-1m (DKK1) 增强肿瘤细胞干性和上皮-间质转化 (EMT),同时与表达MRC1的组织驻留巨噬细胞 (RTM-TAMs) 和癌症相关肌成纤维细胞 (myo-CAFs) 协同形成促肿瘤生态位。这些发现揭示了肿瘤侵袭前沿的特定细胞组成、空间结构和功能交互,为理解肿瘤进展机制提供了新的视角。
NK细胞作为固有免疫系统的重要组成部分,已被证明是早期肝细胞癌(HCC)的潜在预后指标之一。以往研究表明肿瘤组织内NK细胞活性和浸润增加与患者生存率密切相关。然而,NK细胞在肿瘤内的空间分布规律及其对预后的影响的机制尚未阐释。
2025年4月,中国科学技术大学的孙成教授、刘连新教授与Joe Yeong教授合作在Nature在线发表“Spatial immune scoring system predicts hepatocellular carcinoma recurrence”论文。研究人员首先对17名HCC患者进行空间转录组技术分析,发现NK细胞主要在未复发患者肿瘤侵袭前沿显著富集。对NK细胞富集区域进行全转录组分析,发现这些NK细胞中特异性表达5个关键基因 (SPON2、ZFP3612、ZFP36、VIMHLA-DRB1)。通过单细胞RNA测序分析,发现SPON2+ NK细胞具有更高的IFN-γ、穿孔素等效应分子的表达。 最后通过3D生物打印模型证明SPON2+ NK能够有效地迁移到肿瘤细胞区域,并具有更强的IFN-γ分泌和细胞毒性。该研究通过体内外实验证明SPON2在增强NK细胞浸润和IFNγ分泌中发挥的关键作用,为早期HCC治疗决策提供依据[20]。
结直肠癌 (CRC) 是全球癌症死亡率最高的恶性肿瘤之一,生存率低且肿瘤异质性复杂。传统免疫学方法难以全面破译肿瘤微环境中细胞间的动态相互作用,缺少高分辨、高精度的空间转录组信息。2025年6月,四川大学李为民教授团队在Nature Genetics在线发表“High-definition spatial transcriptomic profiling of immune cell populations in colorectal cancer”论文。通过对5例人CRC样本进行Visium HD空间转录组技术分析,发现肿瘤边界区域存在SELENOP+ 和SPP1+ 两种不同基因表达谱的巨噬细胞亚群,功能分析显示SELENOP+ 巨噬细胞显著富集的信号通路包括TNF-κB和凋亡途径,而SPP1+ 巨噬细胞则上调胆固醇稳态和KRAS信号通路。通过对包埋组织采用2μm数据分割技术分析,发现肿瘤相关成纤维细胞和巨噬细胞是与肿瘤细胞互作最多的细胞亚群,配体-受体对分析发现SPP1+ 巨噬细胞通过CD44与肿瘤细胞相互作用。在肿瘤微环境中,SELENOP+巨噬细胞 (通过B2M–KLRD1轴) 与CD8+ T细胞相互作用,抑制其细胞毒性功能,从而导致免疫监视减弱以及免疫系统的逃逸。该研究免疫细胞群体的空间定位为CRC生物学提供了新认知,提示空间分布各异的巨噬细胞亚群可能成为治疗靶点[16]。
除此之外,时空组学研究还有助于揭示肿瘤微环境中免疫抑制机制的空间特性。2025年,复旦大学华克勤教授团队在Molecular Cancer在线发表“Integrated multi-omics identifies a CD54+ iCAF-ITGAL+ macrophage niche driving immunosuppression via CXCL8-PDL1 axis in cervical cancer”论文。通过单细胞RNA测序联合空间多组学分析,发现了一类在宫颈癌 (CC) 中富集的CD54+ 炎症性癌症相关成纤维细胞 (iCAFs),该细胞亚群与ITGAL+ 巨噬细胞在空间上共定位,并促进免疫抑制微环境的形成[11]。机制上,CD54+ iCAFs通过分泌CCL2将ITGAL+ 巨噬细胞极化为M2样表型,同时通过直接接触的CD54–ITGAL依赖性信号和可溶性CCL2介导的巨噬细胞重编程,激活巨噬细胞自分泌CXCL8和随后的PD-L1上调,最终抑制CD8+ T细胞功能。
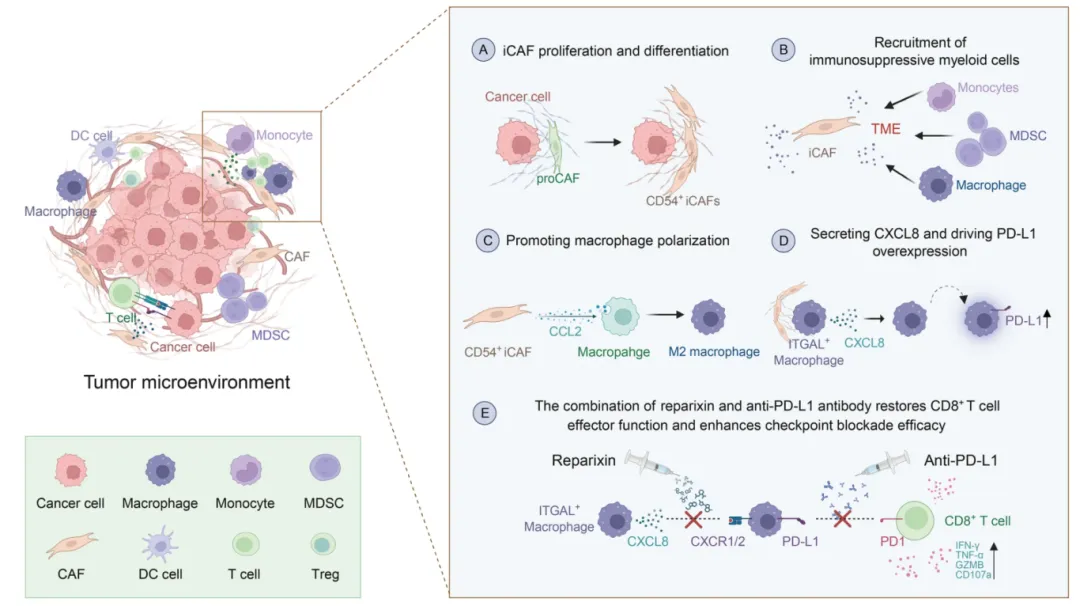
图6. D54 iCAFs-ITGAL巨噬细胞通过CXCL8-PD-L1机制驱动免疫抑制。来自:Chen F, Bai G, Liu Q, et al. Integrated multi-omics identifies a CD54+ iCAF-ITGAL+ macrophage niche driving immunosuppression via CXCL8-PDL1 axis in cervical cancer. Mol Cancer. 2025;24(1):262
2024年9月,复旦大学王红阳院士/陈磊团队在Nature Cancer在线发表“Spatial single-cell protein landscape reveals vimentinhigh macrophages as immune-suppressive in the microenvironment of hepatocellular carcinoma”论文。利用包含36种抗体的CODEX技术对401例HCC样本进行空间单细胞蛋白图谱分析,发现高表达波形蛋白 (Vimentin) 巨噬细胞的免疫抑制作用[12]。研究人员发现vimentinhigh巨噬细胞与调节性T细胞 (Treg) 在肿瘤组织中存在空间共定位现象,并通过增加白细胞介素-1β分泌,增强Treg细胞的免疫抑制活性促进肿瘤进展。
2024年8月,荷兰癌症研究所的Leila Akkari团队在Cell在线发表“Macrophage-mediated myelin recycling fuels brain cancer malignancy” 论文。通过单细胞和空间多组学分析,深度解析了胶质母细胞瘤的肿瘤微环境 (TME) 异质性,并鉴定出一种肿瘤相关巨噬细胞 (TAM) 亚群——脂质负载巨噬细胞 (lipid-laden macrophage, LLM),该亚群通过吞噬来自神经细胞的髓磷脂 (myelin) 转化为脂质积累表型,并与间充质样肿瘤细胞共定位在肿瘤缺氧区域。脂质负载巨噬细胞通过LXR/Abca1依赖性机制将髓鞘来源的脂质转移到高代谢需求的间质样胶质母细胞瘤中,从而促进肿瘤细胞的增殖和复发[17]。
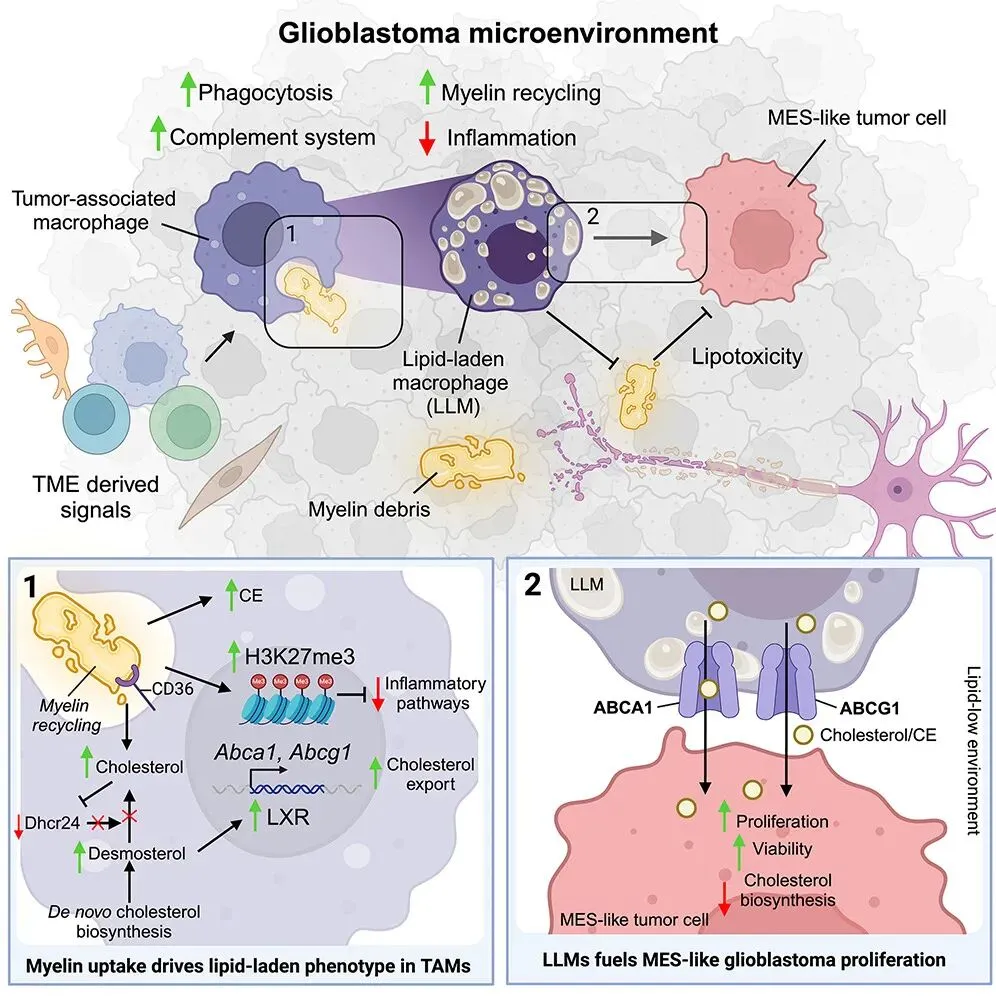
图7. 巨噬细胞介导的髓鞘再循环促进脑癌恶性进展。来自:Kloosterman DJ, Erbani J, Boon M, et al. Macrophage-mediated myelin recycling fuels brain cancer malignancy. Cell. 2024;187(19):5336-5356.e30
三级淋巴结构 (TLS) 是在慢性炎症部位的非淋巴组织中发育的异位淋巴器官,可以增强局部免疫反应,并与患者的预后密切相关,也是近年来肿瘤免疫研究的热点。成熟的TLS是组织最紧密的异位淋巴结构,具有富含T细胞的区域和包含生发中心的B细胞区域。以往的研究表明肿瘤内TLS密度与宿主免疫力和较长的生存期密切相关。2025年4月,中山大学匡铭/刘石平研究团队在Cancer Cell在线发表“Spatial transcriptomics reveals tryptophan metabolism restricting maturation of intratumoral tertiary lymphoid structures”论文。利用时空组学Stereo-seq技术,首次绘制出肝细胞癌中三级淋巴结构的全景发育图谱。发现肝癌细胞通过调控色氨酸代谢,显著影响TLS的成熟[13]。小鼠肝癌模型中发现:低色氨酸饮食不仅显著提升成熟TLS的密度,还与抗PD-1免疫治疗产生协同效应有效减小肿瘤体积。将传统的“不成熟TLS”进一步划分为“趋向成熟型”和“偏离成熟型”,并明确在免疫应答和预后的不同作用,揭示了免疫代谢调控在免疫应答中发挥的关键作用,也为联合代谢干预和免疫治疗提供了理论依据。
时空组学技术不仅重塑了我们对肿瘤微环境的理解,还为免疫细胞的功能调控和发育分化提供了新的见解,通过揭示免疫细胞在组织中的三维空间组织、迁移轨迹和细胞间通信网络。
2025年1月,国家儿童医学中心/北京市儿科研究所倪鑫/桂晋刚教授团队在Cancer Research在线发表“Spatial and Single Cell Analyses Reveal Heterogeneity of DNAM-1 Receptor-Ligand Interactions that Instructs Intratumoral γδT-Cell Activity”论文。通过空间转录组学与单细胞转录组测序 (scRNA-seq) 联合应用,发现肿瘤细胞表面CD112和CD155的表达存在明显的空间异质性,并与肿瘤细胞分化状态及代谢特征显著相关[14]。空间代谢组学进一步揭示CD112/CD155比值与神经元代谢通路活性的空间分布存在正相关性,机制研究表明,肿瘤细胞上的CD155通过与γδT细胞直接接触,诱导DNAM-1受体泛素化降解。解释了肿瘤浸润γδT细胞功能受损的机制,也为调控CD155-DNAM-1轴增强γδT细胞抗肿瘤活性提供了理论依据。
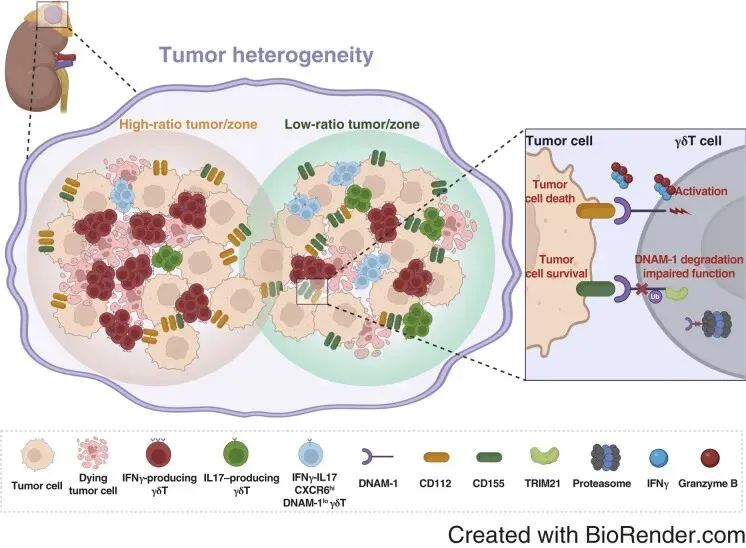
图8. 空间和单细胞转录组联合分析揭示了指示瘤内γδT细胞活性的DNAM-1受体-配体相互作用的异质性。来自:Wang X, Wang H, Lu Z, et al. Spatial and Single-Cell Analyses Reveal Heterogeneity of DNAM-1 Receptor-Ligand Interactions That Instructs Intratumoral γδT-cell Activity. Cancer Res. 2025;85(2):277-298
2024年9月,斯坦福大学的Dean W. Felsher和Renumathy Dhanasekaran团队在Nature Cancer在线发表“Spatial analysis reveals targetable macrophage-mediated mechanisms of immune evasion in hepatocellular carcinoma minimal residual disease”论文。首先通过单细胞高通量细胞成像技术,发现特殊的空间微环境结构:表达PD-L1的M2型巨噬细胞与具有干细胞特性的肿瘤细胞发生相互作用,且与患者预后不良密切相关。空间转录组分析表明,巨噬细胞分泌的TGFβ1在维持具有干细胞特性的残留肿瘤细胞中发挥关键作用,阻断PD-L1和TGFβ信号可清除免疫抑制性巨噬细胞,同时招募活化CD8+ T细胞,最终清除肿瘤细胞。该研究首次揭示肝细胞癌微小残留病变 (MRD) 中免疫逃逸的空间调控机制[18]。
2025年10月,慕尼黑工业大学Mikael Simons和Janos Groh团队在Immunity在线发表“Single-cell spatial transcriptomic profiling defines a pathogenic inflammatory niche in chronic active multiple sclerosis lesions”论文。通过单核RNA测序联合高通量空间转录组,成功构建并绘制了慢性活动性多发性硬化 (MS) 病灶的单细胞空间图谱。空间转录组数据分析显示,慢性活动性MS病灶内CD8+ 组织驻留记忆T细胞与GPNMB+小胶质细胞的相互作用构成致病炎症生态位。其机制是病灶内的CD8+ T细胞通过分泌IFN-γ促进小胶质细胞对髓鞘来源胆固醇的储存,并抑制其外排导致脂质蓄积和炎症状态持续,提升小胶质细胞胆固醇外排可能具有成为进展期多发硬化治疗的策略[19]。
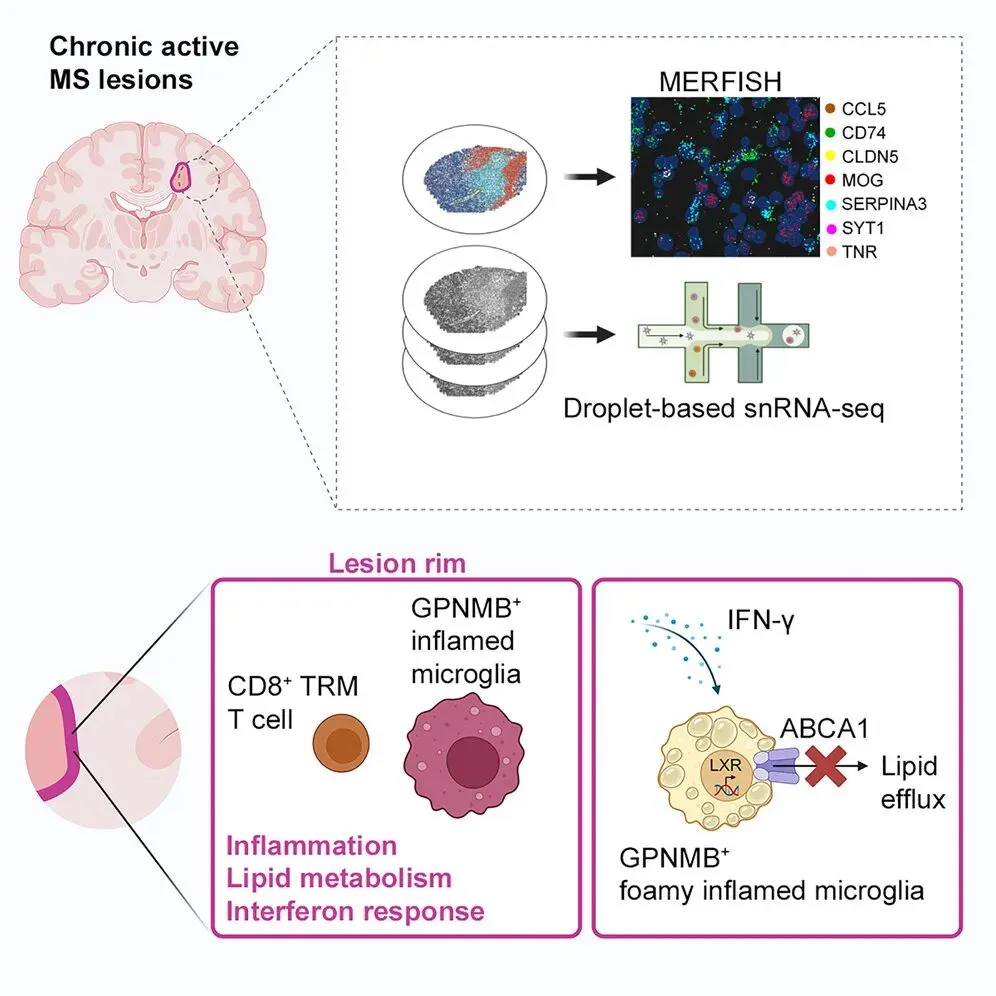
图9. 单细胞空间转录组学分析揭示慢性活动性多发性硬化病灶中的致病性炎症微环境。来自:Feng R, Spieth L, Liu L, et al. Single-cell spatial transcriptomic profiling defines a pathogenic inflammatory niche in chronic active multiple sclerosis lesions. Immunity. 2025;58(12):2989-3005.e10

时空组学推动免疫学研究方式的转变——从静态描述到动态解析,从二维观察到四维(空间+时间)建模,从单一分子层次到多组学整合。时空组学技术的不断成熟和普及有助于更加精细追踪免疫细胞在时空维度上的动态变化,同时空间组学技术的出现使得在分子、细胞和组织水平上同时研究疾病成为可能,整合这些层次的信息将增强我们对疾病进展机制的理解。
本推文封面图来源:Spatiotemporal transcriptomic atlas of mouse organogenesis using DNA nanoball-patterned arrays - ScienceDirect
参考文献:
1. Crick F. Central dogma of molecular biology. Nature. 1970;227(5258):561-563
2.Lécuyer E, Yoshida H, Parthasarathy N, et al. Global analysis of mRNA localization reveals a prominent role in organizing cellular architecture and function. Cell. 2007;131(1):174-187
3. Codeluppi S, Borm LE, Zeisel A, et al. Spatial organization of the somatosensory cortex revealed by osmFISH. Nat Methods. 2018;15(11):932-935
4. Ke R, Mignardi M, Pacureanu A, et al. In situ sequencing for RNA analysis in preserved tissue and cells. Nat Methods. 2013;10(9):857-860
5. Junker JP, Noël ES, Guryev V, et al. Genome-wide RNA Tomography in the zebrafish embryo. Cell. 2014;159(3):662-675
6. Peng G, Suo S, Chen J, et al. Spatial Transcriptome for the Molecular Annotation of Lineage Fates and Cell Identity in Mid-gastrula Mouse Embryo. Dev Cell. 2020;55(6):802-804
7. Wang X, Allen WE, Wright MA, et al. Three-dimensional intact-tissue sequencing of single-cell transcriptional states. Science. 2018;361(6400):eaat5691
8. Ståhl PL, Salmén F, Vickovic S, et al. Visualization and analysis of gene expression in tissue sections by spatial transcriptomics. Science. 2016;353(6294):78-82
9.Liao S, Zhou X, Liu C, et al. Stereo-cell: Spatial enhanced-resolution single-cell sequencing with high-density DNA nanoball-patterned arrays. Science. 2025;389(6762):eadr0475
10. Wang Z, Zhu G, Tang P, et al. SLPI⁺ AT2-Like Cells Orchestrate Lung Adenocarcinoma Invasion via Wnt Pathway Activation and Stromal Crosstalk in a Spatially Defined Margin Niche. Adv Sci (Weinh). 2025 Nov 11:e16580.
11. Chen F, Bai G, Liu Q, et al. Integrated multi-omics identifies a CD54+ iCAF-ITGAL+ macrophage niche driving immunosuppression via CXCL8-PDL1 axis in cervical cancer. Mol Cancer. 2025;24(1):262
12. Qiu X, Zhou T, Li S, et al. Spatial single-cell protein landscape reveals vimentinhigh macrophages as immune-suppressive in the microenvironment of hepatocellular carcinoma. Nat Cancer. 2024;5(10):1557-1578
13.Tang Z, Bai Y, Fang Q, et al. Spatial transcriptomics reveals tryptophan metabolism restricting maturation of intratumoral tertiary lymphoid structures. Cancer Cell. 2025;43(6):1025-1044.e14
14. Wang X, Wang H, Lu Z, et al. Spatial and Single-Cell Analyses Reveal Heterogeneity of DNAM-1 Receptor-Ligand Interactions That Instructs Intratumoral γδT-cell Activity. Cancer Res. 2025;85(2):277-298
15. Franken A, Bila M, Mechels A, et al. CD4+ T cell activation distinguishes response to anti-PD-L1+anti-CTLA4 therapy from anti-PD-L1 monotherapy. Immunity. 2024;57(3):541-558.e7
16.Oliveira MF, Romero JP, Chung M, et al. High-definition spatial transcriptomic profiling of immune cell populations in colorectal cancer. Nat Genet. 2025;57(6):1512-1523
17.Kloosterman DJ, Erbani J, Boon M, et al. Macrophage-mediated myelin recycling fuels brain cancer malignancy. Cell. 2024;187(19):5336-5356.e30
18. Lemaitre L, Adeniji N, Suresh A, et al. Spatial analysis reveals targetable macrophage-mediated mechanisms of immune evasion in hepatocellular carcinoma minimal residual disease. Nat Cancer. 2024;5(10):1534-1556
19. Feng R, Spieth L, Liu L, et al. Single-cell spatial transcriptomic profiling defines a pathogenic inflammatory niche in chronic active multiple sclerosis lesions. Immunity. 2025;58(12):2989-3005.e10
20. Jia G, He P, Dai T, et al. Spatial immune scoring system predicts hepatocellular carcinoma recurrence. Nature. 2025;640(8060):1031-1041
撰稿/田恒瑞
编辑/koala
文献精读【Science】肠道肥大细胞来源的白三烯介导对摄入抗原的过敏反应
文献精读【Nature】RNA的N-糖基化赋予其免疫逃逸促进稳态下胞葬
免疫学杰出学者系列专题(四十五)——Frederick W. Alt
免疫学杰出学者系列专题(四十四)——Ruslan Medzhitov




