1. 核心观点
· 行业拐点:随着液体活检技术发展,循环游离RNA (cell-free RNA, cfRNA)正在成为肿瘤微小残留病灶检测(Minimal Residual Disease, MRD)和疗效动态监测的新支点。最新研究表明,与传统的循环肿瘤DNA (ctDNA) 检测相比,cfRNA标志物在术后复发预警等场景中显示出更高的检测灵敏度。这一趋势标志行业拐点:cfRNA有望在MRD检测和治疗监测中后来居上,提供比ctDNA更及时敏感的肿瘤动态信号。
· 技术壁垒:cfRNA检测面临“痕量+噪音”双重挑战:血浆中cfRNA含量极低且背景噪音信号丰富(如核糖体RNA占比高),增加了信号提取难度。此外,cfRNA分子易被降解,稳定性远逊于ctDNA。为克服这些壁垒,行业正探索超高灵敏痕量检测结合AI大模型的方案:一方面通过富集稀有片段、去除背景干扰提高检测下限;另一方面运用Transformer等深度学习模型对海量cfRNA数据去噪建模,放大肿瘤复发微弱信号。技术突破的关键在于如何提升对复发信号的敏感性和准确性。
· 商业路径:在商业化落地上,行业公司普遍采用“三步走”策略:(1) 科研服务(B2B)阶段率先切入,通过与医药研发机构合作提供cfRNA检测服务来验证技术、积累数据;(2) LDT模式(实验室自建检测,Laboratory Developed Test)落地医院术后随访和疗效评估场景,以检测服务形式迅速进入临床;(3) IVD产品(体外诊断试剂)申报注册,推出标准化检测试剂盒,瞄准更大规模的术后复发监测和疗效动态评估市场。此路径先易后难:先利用LDT灵活性满足临床需求,再以IVD规范化放大规模,实现商业化成长。
2. 行业深度拆解
2.1 cfRNA vs ctDNA:疗效监测中的异同– Comparing cfRNA and ctDNA in Treatment Monitoring
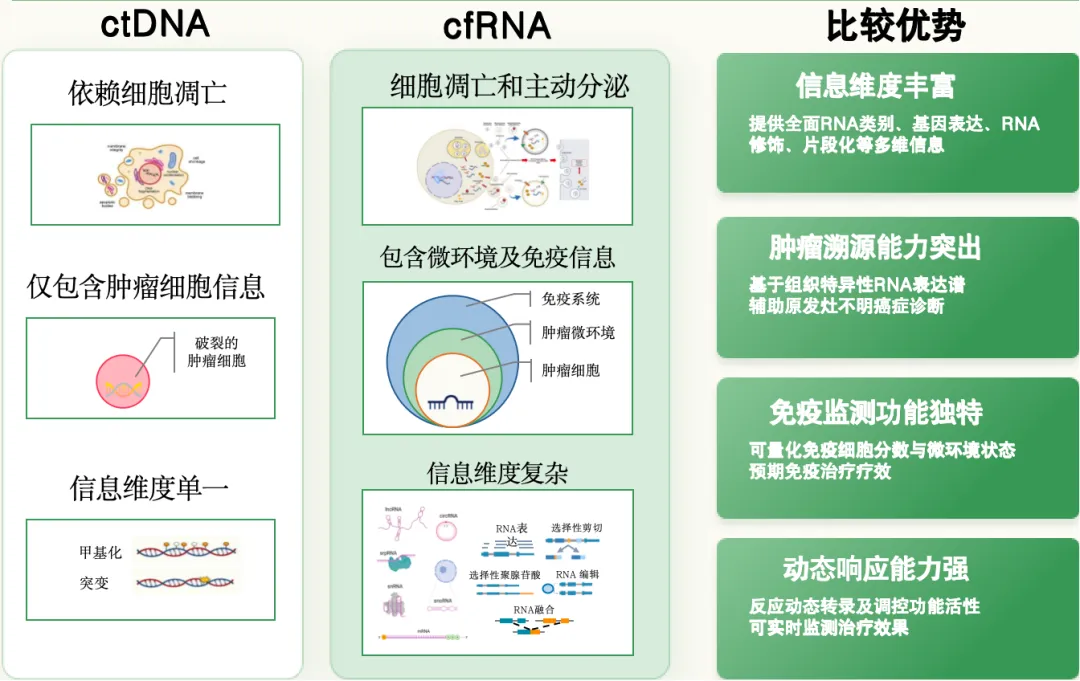
在肿瘤治疗监测和复发检测中,cfRNA与ctDNA各有特点:
· ctDNA(循环肿瘤DNA):ctDNA源自肿瘤细胞裂解后释放的基因片段,具有相对稳定、检测技术成熟的优势,目前已广泛用于MRD检测和复发监测。例如典型的ctDNAMRD产品会针对患者肿瘤特异突变进行个性化检测,从而在术后发现分子残留或微小复发灶。然而,ctDNA信号依赖肿瘤细胞释放,在肿瘤负荷很低或“Non-shedder”肿瘤(不易脱落DNA的肿瘤)中,ctDNA往往难以检出。临床数据显示早期患者ctDNA阳性率偏低,如I期患者ctDNA检出率可能只有30-50%,治疗过程中ctDNA水平快速下降也会降低对疗效响应的监测灵敏度。因此,仅依赖ctDNA可能出现假阴性,无法及时捕捉部分患者的残存病灶。
· cfRNA(游离RNA):cfRNA是血液中循环的信使RNA及非编码RNA片段,可实时反映肿瘤基因表达和机体反应状态。相较ctDNA,cfRNA在肿瘤相关信号检测上展现出更高的灵敏度:清华大学等的多组学研究发现,血浆中cfRNA对癌基因变异的检出敏感性是ctDNA的3倍,意味着使用cfRNA标志物可以检测到更多早期癌症患者。此外,cfRNA还能捕捉免疫应答和肿瘤微环境信号:患者血浆中的cfRNA表达谱可揭示肿瘤相关免疫通路的异常变化(如免疫抑制信号),这些基于cfRNA的免疫指标与肿瘤大小、分期等临床状态高度相关,可作为肿瘤动态监测的潜在标志物。换言之,cfRNA提供了“肿瘤+宿主”双重信息:既有肿瘤自身的转录变化,也反映机体对肿瘤的反应,从而在疗效评估和复发预测中更全面。其不足在于:RNA分子稳定性差,血浆中易降解,需要更高要求的前处理和存储;且正常组织来源的背景cfRNA丰富,需要高效噪音过滤技术。总体来看,cfRNA在实时性和敏感性上胜出一筹, 为术后监测提供了有力补充,而ctDNA在可靠性和特异性(如突变溯源肿瘤)上仍具价值,未来二者可能互为补充、融合应用。
2.2 cfRNA的独特优势:动态转录与免疫信号– Advantages of cfRNA: Dynamic Transcription & Immune SignalscfRNA之所以在治疗监测中表现突出,源于其独特的生物学信息内涵:
·实时反映动态转录变化:ctDNA主要提供基因突变等静态遗传信息,而cfRNA代表了肿瘤和相关细胞当下的基因表达活动。尤其在治疗干预下,肿瘤细胞可能进入休眠或发生表型转化,DNA突变不变但RNA表达显著改变。cfRNA可及时捕捉这些转录组水平的波动。例如有研究利用cfRNA检测发现,当肺癌患者对靶向药产生耐药时,血浆cfRNA中出现了反映组织学转化(如小细胞肺癌转化)的基因表达信号,以及耐药相关通路的变化。这些信息是ctDNA突变检测所无法提供的。因此cfRNA有助于疗效监测:通过监测肿瘤相关基因的表达上调/下调,及时判断患者对疗法的响应和耐药趋势。
· 揭示免疫应答和微环境:肿瘤的发展和复发不仅取决于肿瘤细胞本身,也与机体免疫系统和肿瘤微环境密切相关。cfRNA谱中包含大量免疫细胞来源的转录本。例如,有研究通过cfRNA计算外周免疫细胞分数和肿瘤微环境分数,能够有效预测肿瘤分期、肿瘤大小等指标。又如在消化道肿瘤患者中,血浆cfRNA揭示了特定免疫通路被抑制的证据,提示免疫系统受肿瘤影响的动态变化。这些免疫信号对于评估治疗有效性(如免疫治疗的反应)和预测复发具有重要意义——ctDNA因缺乏这方面信息而存在盲区。因此,cfRNA的加入让液体活检从单纯检测“肿瘤有没有”升级为监测“肿瘤怎么样,身体怎么样”,更全面地反映患者状态。正因如此,业内观点认为复发监测将成为液体活检的重要增长领域,其潜在市场空间仅次于癌症早筛。
2.3 海外布局:先锋公司动态– Overseas Players and Their Progress欧美多家前沿公司已布局“AI+液体活检”赛道,将cfRNA纳入肿瘤监测体系,在MRD及疗效评估方向取得积极进展:
· Freenome:美国液体活检独角兽,公司平台采用多组学(包含cfDNA、cfRNA、蛋白等)结合机器学习进行早期癌症检测和疗效监测。Freenome最初聚焦结直肠癌早筛(与ExactSciences达成独家协议合作商业化其血检产品),但其技术平台延展性强,也用于与制药企业合作开展MRD检测和治疗反应预测等项目。例如Freenome与多家药企合作,通过其cfRNA等多组学数据帮助发现治疗反应生物标志物、监测新药临床试验患者的分子残留病灶。公司已累计融资超过10亿美元,估值数十亿美元,体现资本市场对多组学+AI模式的认可。
· Grail:液体活检领军者,由Illumina孵化,凭借ctDNA甲基化检测的Galleri多癌早筛闻名。尽管Grail当前产品侧重于无症状人群的早期筛查,但其技术同样适用于术后复发监控。Grail近期宣布与安进、阿斯利康等制药公司合作,利用其甲基化平台试验MRD监测和复发检测的新方法。发布数据亦显示,针对复发/难治患者的甲基化检测方案癌症检出率可达92%。这表明大型液体活检平台正在延伸应用场景,从早筛拓展到术后随访、辅助治疗决策等精准医疗领域。Grail于2021年被Illumina以约80亿美元收购(后因监管问题正寻求剥离),其高估值也为行业树立了标杆。
· Exai Bio:致力于cfRNA技术的初创公司,以发现“孤儿非编码RNA (orphan non-coding RNA, 即oncRNA)”为特色,即健康个体不存在、肿瘤特有的一类小片段RNA。Exai开发了无需个体化设计的通用RNA测序检测平台,可敏感、快速且低成本地检测这些oncRNA。在乳腺癌新辅助治疗试验中,他们证明了oncRNA的动态变化能够反映治疗响应:治疗后血液中oncRNA的清除情况与残存病灶和预后显著相关。值得一提的是,Exai还构建了多模态Transformer模型Exai-1对cfRNA进行深度学习分析,将序列和表达信息融合以提升信号质量、降低技术噪声。该模型在8339个样本上预训练(累计3060亿token),能够生成高保真合成cfRNA数据增强小样本训练,提高罕见癌症检测的AUC约0.1。Exai目前融资总额逾1亿美元,在2025年发布的Exai-1成为业界首个cfRNA领域的大型生成式基础模型,标志着AI+cfRNA融合的技术前沿。
· Biostate AI:成立于美国的新锐公司,由麻省理工等背景的科学家创立,核心理念是“RNA是被低估的实时健康生物标志物,可以通过AI赋能释放价值”。Biostate AI开发低成本RNA测序和AI分析平台,为药物研发和临床提供决策支持,例如用于指导黑色素瘤等的治疗方案选择。公司已获得1200万美元A轮融资,并在中、美、印三地布局数据合作:与中国金匙基因(Kindstar)成立合资公司获取本土临床数据,与麻省总医院合作开发AI模型监测黑色素瘤疗效。这类公司通过扩大全球RNA数据集建立算法优势,强调RNA测序结合AI在指导个性化治疗、预测疗效上的巨大潜力。Biostate等的进展也验证了投资机构对“RNA+AI”赛道商业价值的信心。
3. 技术挑战与突破
3.1 cfRNA检测的技术挑战虽然cfRNA在肿瘤监测中前景诱人,但技术上存在多重挑战,需要克服方可实现可靠检测和解读:
· 稳定性差:cfRNA分子很脆弱,极易被血浆中的核酸酶降解。与相对稳定的DNA相比,RNA从样本采集、处理到储存的全过程中都可能发生降解,导致信号丢失。这要求在前处理时严格控制样本质量、尽快进行低温保存和提取,并开发专门的试剂减少RNA降解风险。稳定性问题限制了cfRNA检测的一致性,是首先需解决的基础难题。
· 背景噪音高:健康组织正常代谢也会释放大量cfRNA进入血液,尤其核糖体RNA (rRNA)等高度丰度的背景分子占据测序读数的大部分。此外,线粒体RNA、YRNA、tRNA等碎片在血浆中广泛存在。这些非肿瘤来源的RNA噪音淹没了稀有的肿瘤信号。解决之道是去除富集背景:例如通过探针捕获并耗减rRNA、mtRNA序列,从而腾出测序深度用于分析更有意义的转录本。这一思路在DETECTOR-seq等方案中已有验证,通过定制引物在建库时就剔除大宗噪音序列,实现对有用cfRNA的更高测序效率。
·片段化和低丰度:血浆cfRNA长度短且浓度极低。大部分cfRNA片段可能只有几十上百个核苷酸,无法像细胞RNA那样提供完整的转录本信息。此外,每毫升血浆中有用的肿瘤cfRNA拷贝数可能微乎其微(检测下限需求可达0.05%以下变异丰度)。因此需要超高灵敏度的建库和扩增技术,以及高深度测序支持。例如RARE-seq通过随机引物扩增结合亲和富集,极大提高了低浓度cfRNA的检测成功率,其灵敏度比传统全转录组测序提高约50倍。为了捕获片段化信息,新技术也要求极低起始RNA输入量(如<1mL血清)且依然保持鲁棒,这方面如DETECTOR-seq已做到仅100微升血浆建库的高灵敏度检测。总之,如何从海量极短序列中发现蛛丝马迹,是cfRNA检测的核心挑战。
3.2 技术突破:超敏检测方法针对上述挑战,近年研究提出多项创新技术,大幅提升了cfRNA检测的灵敏度和可靠性:
· RARE-seq– Random priming & Affinity Capture for cfRNA: 由斯坦福大学团队开发的超灵敏cfRNA测序方案。RARE-seq通过随机引物对cfRNA片段进行充分扩增,并使用特定探针富集“稀有表达基因 (Rare Abundance Genes)”的转录本,以提高肿瘤来源RNA的检出率。同时引入血小板去卷积算法减少假信号干扰。验证显示,RARE-seq相较传统RNA测序对肿瘤cfRNA的检出灵敏度提升约50倍,检测最低可至0.05%变异频率。在临床试验中,RARE-seq成功检测出早期肺癌患者血浆中的肿瘤转录信号,其对I期非小细胞肺癌的检出率达30%,并且整体上优于同步进行的ctDNA检测。此外,它还能在EGFR突变肺癌耐药患者中捕获组织学转化的RNA信号,实现ctDNA检测无法覆盖的生物标志物。RARE-seq的出现被视为cfRNA液体活检的“拐点”——首次证明了通过方法学创新,cfRNA可用于与ctDNA媲美甚至更胜一筹的肿瘤检测。
· DETECTOR-seq– Depletion-assisted Multiplexed cfRNA Sequencing: 清华大学团队开发的低成本cfRNA测序方法。该技术的核心是在文库构建中引入特异性引导RNA探针,批量去除血浆中高丰度的无信息RNA序列(如rRNA、线粒体RNA碎片)。同时采用早期条形码引入策略,实现多个样本平行建库以降低成本和起始量需求。DETECTOR-seq应用于全血浆cfRNA vs 胞外囊泡cfRNA的对比研究,结果展示出血浆和外泌体中的cfRNA谱有显著差异:血浆cfRNA富含环状RNA、YRNA等小片段及病毒RNA,而外泌体cfRNA富集mRNA和信号识别颗粒RNA等。功能分析亦发现,血浆cfRNA偏重于剪接体和体液免疫通路信号,外泌体cfRNA则富集转录活性、细胞迁移和抗原受体等信号。更重要的是,两者均能区分癌症患者与健康人,并且血浆中检出的微生物cfRNA对特定癌种有分类潜力。DETECTOR-seq的意义在于,它提供了一种高效噪音过滤+多重并行的方案,使在低起始量样本中开展全转录组cfRNA分析成为可能。这为未来大规模cfRNA组学研究和应用奠定基础。
(注:除上述两种,近来也有其他方法如MIT开发的Terlinsky方法等探索提高cfRNA测序效率,但RARE-seq和DETECTOR-seq是当前文献报道中较具代表性的两项突破,分别侧重于灵敏度和宽覆盖度。)
4. 市场规模与商业模式
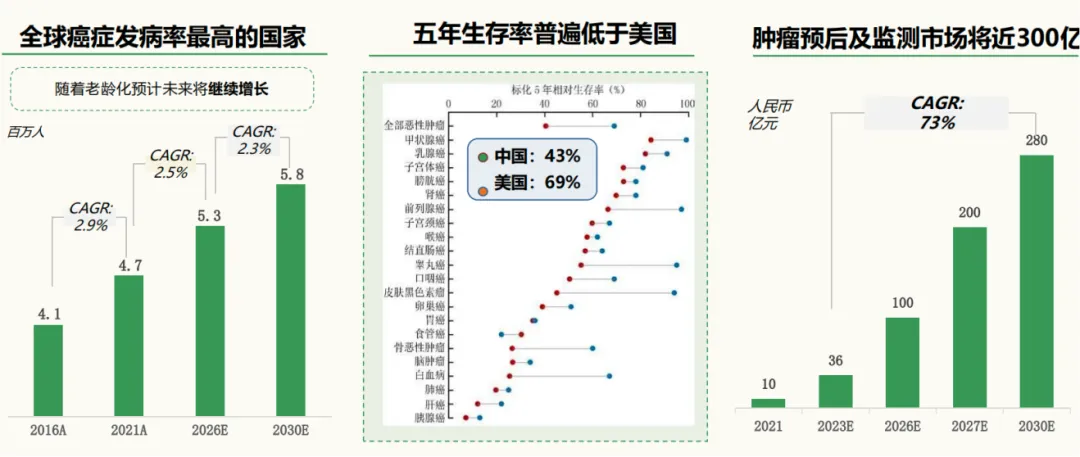
4.1 肿瘤监测与复发预测市场:规模与增长随着癌症生存者人数增加和精准治疗理念普及,肿瘤治疗监测与复发预测正崛起为体外诊断领域增速最快的细分市场之一。相较于泛人群的癌症早筛,术后复发监测有更明确的目标人群和临床需求:全球范围每年数百万肿瘤患者接受根治性治疗后进入随访期,仅美国就估计有超过300万名实体瘤患者符合MRD检测适应证。这些患者在术后5年内面临较高复发风险,因此存在定期检测的强需求。MRD液体活检可以比传统影像提前数月乃至两年发现分子复发征兆, 为临床决策(如是否加强辅助治疗)提供依据。这一价值已逐步获得认可:例如美国CMS在2025年批准了ExactSciences公司Oncodetect™ ctDNA MRD检测对II-III期结直肠癌患者的医保覆盖,期限长达5年。这表明复发监测正从科研走向标准临床管理。
从市场测算看,复发监测的潜在市场空间可观。行业分析普遍认为,在液体活检多场景中,市场空间大小排序为:癌症早筛 > 复发监测 > 治疗伴随诊断。虽然当前早筛吸引了更多关注,但复发监测由于靶向高风险已患人群,预期渗透率和付费意愿更高,增长确定性强。在中国,目前已经有2000-3000万的带瘤生存人群,考虑每年新发肿瘤病例超400万,大约60%有治愈或缓解后进入监测阶段,假设其中一半采用每年2-4次液体活检MRD检测,每次收费数千元,则国内术后监测市场未来有望达到千亿级人民币规模。再加上肿瘤疗效动态评估(如免疫治疗过程中用液体活检评估肿瘤反应)的需求兴起,整个“癌症治疗全程管理”市场被进一步打开。在资本逻辑上,复发监测被视为液体活检商业化的优先路径——技术更易落地、临床需求迫切、付费方(医院/医保)接受度高。近期国内政策也释放积极信号:监管层面开始认可以LDT形式开展高通量基因检测服务,在保证质量前提下鼓励创新产品进入临床。例如已有肿瘤基因检测公司将自研MRD测序方案在医院通过LDT开展性能验证。可以预见,未来3-5年内,肿瘤复发监测将逐步从顶尖医院试点走向更广泛应用,市场规模呈加速扩张态势。
4.2 商业模式:LDT先行与IVD转化鉴于目前技术和监管环境,肿瘤MRD/监测产品的商业落地一般遵循“LDT先行,IVD跟进”的模式:
· 科研服务/B2B阶段:首先通过与制药公司、科研机构合作,以服务形式切入。比如为新药临床试验提供MRD检测服务、为医院课题提供cfRNA测序分析。这一阶段公司主要收入来自项目服务费,同时借机获取宝贵的样本和临床数据,验证技术性能。科研服务模式轻资产、强验证,既锤炼技术又建立口碑,为下一步临床产品化奠定基础。
· LDT模式临床落地:在技术成熟和初步验证后,公司会选择特定应用场景以实验室自建检测的方式推出服务。对于MRD/复发监测而言,最佳切入点是术后随访:如结直肠癌术后每3个月一次血检,用于早期发现分子复发;或肺癌靶向治疗过程中每月一次检测,动态评估疗效。公司可以在自有经认证的实验室开展检测(类似美国的CLIA实验室模式),直接对接医院科室或患者提供检测服务。目前中国对于NGS检测的监管逐步放开,顶尖医院实验室在条件许可下也可引入经过验证的LDT项目。LDT模式相对IVD上市周期短,可快速响应临床需求。院内示范效应有助于推动更多医院采纳LDT服务。通过LDT积累的大量真实世界数据,也将为将来申报注册提供有力证据。需要注意的是,LDT模式下公司需建立健全的质量管理体系,确保检测可靠性和合规性,这是获取医生和监管部门信任的关键。
· IVD产品注册:长远来看,为了规模化占领市场,公司需将检测方案开发成标准化体外诊断产品。这意味着要将复杂的测序+AI流程打包成试剂盒或配套软件,经国家药品监督管理局(NMPA)审批上市。一旦获批,医院检验科可直接采购试剂,在院内开展检测,无需依赖公司中心实验室,从而实现大范围铺开。这一步挑战较大:监管审批需大规模临床试验数据支持,周期长且投入高。但其回报是确立了进入常规临床的正式资质,尤其有望进入医保支付体系,迅速放量。目前国内尚无cfRNA相关IVD获批,ctDNAMRD产品也在注册初期,因而数全基因等创新企业选择了循序渐进策略,先在科研和LDT阶段证明价值,再择机启动IVD注册申报。值得一提的是,公司规划在MRD产品成熟后,进一步拓展多癌种早筛 (Multi-Cancer Early Detection, MCED)领域,将cfRNA+AI技术应用于健康人群的癌症早期筛查。这是一个潜在更为庞大的远景市场(2035年中国多癌早筛市场预计达522亿元)。短期内,早筛项目仍处于验证阶段,真正实现商业回报尚需时日。相比之下,术后监测和疗效评估无疑是更贴近临床刚需、也更能快速转化收益的应用。
5. 国内外典型公司与估值水平
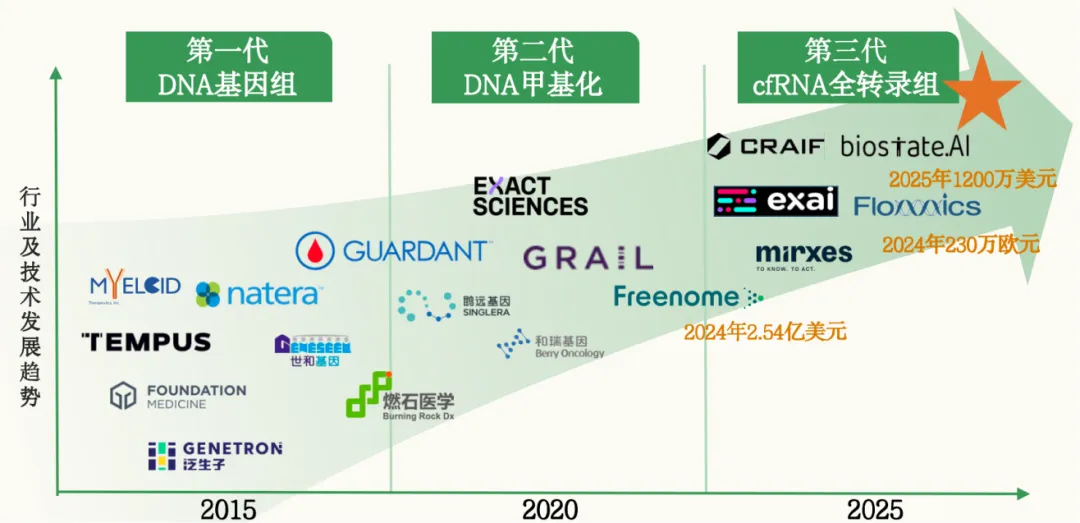
国外代表公司:
·Freenome:【美国,成立2014】“AI+多组学”早筛及MRD领域领先者。截至2023年底累计融资超$1.2B,美股二级市场对其估值预期已达数十亿美元量级。Freenome目前产品管线以早期筛查为主(其多癌种早筛血检已与ExactSciences达成独家授权合作),但同时通过与MerckKGaA等合作布局术后MRD检测。参考其最新融资(2023年$300M+),投资人给予Freenome高估值,主要基于其海量样本数据和顶尖AI能力。
· Grail:【美国,成立2016】液体活检龙头,2021年以~$8B被Illumina收购(相当于其投入研发成本数倍)。Grail以ctDNA甲基化的Galleri测试闻名,目前尚未推出MRD产品,但与大型药企合作探索术后复发监测方案。作为行业先驱,Grail的高估值来自其先发优势和庞大临床试验数据。
· Exai Bio:【美国,成立2021】cfRNA液体活检新秀,公司估值在近期融资后约为$300-400M区间(累计融资约$100M+)。Exai以技术取胜:其发现的oncRNA生物标志物及Exai-1基础模型均属业内创举。目前Exai尚处于产品验证和临床前研究阶段,但已在2022年ESMO发布多癌种早检数据(敏感度87%,特异性95%),并计划开展MRD应用。Exai的进展证明了纯RNA标志物路径的可行性,也给投资人讲述了新的故事。
· Biostate AI:【美国,成立2023】强调RNA测序赋能精准医疗的新兴企业。该公司A轮融资$12M,投后估值估计<$50M,但其“全球联盟”扩张速度快,与中印伙伴合作拓展数据来源。Biostate业务模式偏向科研服务和合作开发(如与医院联合培养本地化AI模型)。Biostate的低估值一方面因为成立时间短、业绩兑现尚需时间,另一方面也反映出纯服务型模式的天花板。
国内代表公司:
· 数全基因:作为国内少数深耕cfRNA的企业,数全基因在技术路线中融合了上述最新进展,构建了独有的“cfRNA超敏建库 + AI大模型”架构,用于MRD检测与复发预测:
Ø极致痕量cfRNA捕获:数全基因开发了标准化的样本预处理和文库构建流程,专门优化用于血浆cfRNA。通过片段化富集策略,提高对短片段RNA的捕获效率;并借鉴RARE-seq/DETECTOR-seq思路,在建库时加入背景去除和目标富集步骤,比如耗减rRNA等高背景序列,富集肿瘤相关稀有转录本。该流程使得在一管血(~5-10mL)中即可稳定检出pg级别的肿瘤cfRNA信号,为后续分析奠定了基础。据公司披露,其创新工艺使早期肿瘤信号检出率提升显著,相比传统ctDNA检测早期敏感性提高约50%,对部分癌种的组织来源判断准确率增加20%,同时测序成本降低约75%(得益于无需个体定制靶标,流程高通量自动化)。这些改进使低成本、高通量的cfRNA常规检测成为可能,大幅提高了方案的商业可行性。
ØAI大模型赋能动态分析:在数据分析端,数全基因采用了前沿Transformer深度学习模型对cfRNA信号进行训练。模型以海量真实世界cfRNA测序数据为基础进行预训练,结合了RNA序列特征和表达矩阵等多模态输入(类似Exai-1模型思路)。通过自注意力机制,模型能有效去噪,挖掘出癌症信号与正常变异模式的细微差异,提高检测特异度。同时,大模型引入变分推断和对抗训练,以学习cfRNA复杂的上下文关联,使之具备生成高保synthetic cfRNA数据的能力,可用于扩充小样本训练集。这一点对于稀有癌种、少量随访病例的建模尤为关键,能提升模型对不同癌种、不同行为学背景的泛化能力。据悉,数全基因已建立国内最大的cfRNA深度测序数据库之一,涵盖数千份患者和健康体检者样本。在此基础上训练的Transformer模型,目前可实现三大功能:①癌症信号检测:判别血浆中是否存在异常肿瘤RNA谱;②组织来源溯踪:基于特征模式判断信号可能来自的肿瘤类型/器官;③复发风险评估:结合患者术后随访多次检测的序列变化,输出未来6-12个月内复发概率的预测。模型通过多任务学习同时优化上述目标,在测试集上取得了AUC 0.95以上的性能,达到2025年Nature等顶尖研究报道的国际先进水平。借助这一AI平台,原本微弱紊乱的cfRNA信号被提炼整合为有临床意义的指标,使肿瘤“全程动态追踪”成为可能。特别地,在MRD应用中,数全基因方案已实现比传统影像学提前约6-12个月预警复发的效果(内部试点数据),为肿瘤患者争取宝贵的干预时间窗口。
其他公司:
一些本土NGS公司(燃石、泛生子等)布局了ctDNAMRD检测,但尚未涉足cfRNA技术。从估值参考看,国内上市的泛生子(Nasdaq:GTH)等公司市值曾一度达数十亿元人民币水平。