本报告/资料下载领取方式详见文末


(一)生物技术制药快速发展
1953年,DNA双螺旋结构的发现揭开了生命科学划时代的一页,此后的20年中科学家们又研究出了一系列与DNA有关的新发现,为分子生物学和遗传学的建立和发展奠定了基础,尤其包括限制性内切酶等工具酶的发现与应用,推动了重组DNA技术的快速发展。1974年,美国的Boyer和Cohen首次在实验室中实现了基因转移,为基因工程开启了通向现实的大门。1978年,基因泰克的科学家宣布在大肠杆菌中成功表达人胰岛素,1982年,礼来获得基因泰克授权的重组人胰岛素获FDA批准上市,成为首个基因工程药物,开启了生物技术制药的序幕,从此使用超过60年的动物提取胰岛素逐步退出市场。此后,重组人生长激素以及各种重组人细胞因子类药物相继上市,极大弥补了当时已有治疗方式在安全性和产量上的不足。20世纪90年代后随着基因工程、细胞工程、酶工程、蛋白质工程和发酵工程技术的快速发展,生物技术制药大规模产业化,并进入了高速发展期。
(二)重组蛋白质药物是生物技术药物发展的主要方向和必然趋势
与合成药物不同,生物技术药物的活性药物成分主要是重组蛋白和核酸。目前,绝大多数商业化的生物技术药物以重组蛋白为其活性药物成分。
重组蛋白药物是指采用DNA重组技术,对编码目的蛋白的基因通过载体(质粒等)导入适当的宿主细胞中,从而在宿主细胞中表达目的蛋白,之后经提取、纯化等技术制备具有生物活性的蛋白制剂,可用于疾病的治疗、预防和诊断。
1982年FDA批准礼来的重组胰岛素产品(Humulin,中文名优泌林)是全球第一个重组蛋白药物;1992年中国预防医学科学院病毒学研究所与上海生物制品研究所联合研发的注射用重组人干扰素α-1b获得国家一类新药证书,是我国第一个获得国家批准的重组蛋白药物。
随着DNA重组技术在制药领域的广泛应用,生物制品由早期的从动物组织或血浆中提取制备逐步被重组DNA技术生产所替代。从血液中制备的干扰素、凝血因子等均逐步被基因工程产品所取代,目前仅有少量的生物制品包括人血清白蛋白、抗胰蛋白酶和丙种球蛋白等因技术难度较高还暂未被基因工程产品所取代,但随着生物技术的进一步发展,基因工程生产的重组产品取代从组织或血浆制备的生物制品是必然趋势。
(三)重组蛋白药物制备的表达体系和基本过程
重组蛋白药物制备的表达体系是利用细胞作为蛋白生产车间来生产目的蛋白,各类表达体系和系统可统称为生物反应器。重组蛋白表达体系(生物反应器)按照宿主细胞不同可以分为原核表达体系与真核表达体系,原核表达体系主要以大肠杆菌为主;真核表达体系采用真核细胞表达,主要包括酵母细胞、杆状病毒-昆虫细胞、哺乳动物细胞等;同时,重组蛋白表达体系(生物反应器)又可细分为微生物表达体系(生物反应器)、动物表达体系(生物反应器)和植物表达体系(生物反应器),其详情如下:
1、微生物表达体系(生物反应器)
微生物表达体系主要分为细菌表达系统和酵母表达系统。
① 细菌表达系统
细菌表达系统是应用广泛,较为成熟,亦是相对最简单的蛋白表达系统。细菌表达系统中使用最多、最常见的是大肠杆菌表达系统,主要适合表达非糖基化蛋白和(或)高级结构比较简单的蛋白质。大肠杆菌表达系统除了可以用于生产重组蛋白以外,还可以生产一些其他类型的化合物用作药物。
② 酵母表达系统
用于重组蛋白表达的酵母表达系统包括巴斯德毕赤酵母、汉逊酵母、酿酒酵母、粟酒裂殖酵母、乳酸克鲁维酵母和博伊丁假丝酵母等。目前,药物开发中使用较多的有巴斯德毕赤酵母、汉逊酵母和酿酒酵母等。
2、动物表达体系(生物反应器)
动物表达体系通常分为哺乳动物细胞表达系统、昆虫细胞表达系统和动物表达系统。
① 哺乳动物细胞表达系统
哺乳动物细胞表达系统是目前重组蛋白药物研发和生产中使用最多的表达系统。目前可用的哺乳动物细胞表达系统包括中国仓鼠卵巢细胞(CHO)、啮齿类动物细胞系(如NS0、BHK和Sp2/0等)和人细胞系(如HEK293、PER、C6、HT-1080和CAP等)。其中,中国仓鼠卵巢细胞(CHO)是重组蛋白药物生产的主要选择。
② 昆虫细胞表达系统
昆虫细胞表达系统介于细菌表达系统和哺乳动物表达系统之间。截至目前尚未有采用该表达系统生产的人用重组蛋白药物上市。
③ 动物表达系统
动物表达系统是将外源目的基因以一定方式导入动物基因组,构建基因工程动物,通过基因工程动物的某种组织或体液表达目的蛋白。目前应用最普遍的是哺乳动物的乳腺生物反应器,常用于制备乳腺生物反应器的动物主要有小鼠、兔、猪、绵羊、山羊和牛等。rEVO Biologics(旧称:GTC Biotherapeutics)公司的ATryn(α-antithrombin)于2006年在欧盟获批上市,于2009年在美国获批上市,是第一个上市的动物生物反应器表达制备的人用药物,其是一种抗凝血药,其活性药物成分重组人α-抗凝血酶是在山羊的乳腺中产生的。
3、植物表达体系(生物反应器)
① 叶片表达系统
叶片表达系统包括两种体系,即生物总量表达系统(Biomass)和叶绿体表达系统。生物总量表达系统常用烟草、生菜等植物叶片来进行表达,通过农杆菌介导将目的基因导入叶片,瞬时表达获得大量重组蛋白。美国的Icon Genetics公司2014年利用烟草叶片生产的实验性新药曾治愈了在利比亚感染埃博拉病毒的两位患者,但该药物并未获批上市。叶绿体表达系统是通过叶绿体基因组来合成重组蛋白,叶绿体是植物细胞中具有自主遗传信息的重要细胞器,叶绿体表达系统需要利用叶绿体转化技术将目的基因导入细胞叶绿体中,并经过多代纯化和富集,获得稳定工程叶绿体用于表达。
② 植物悬浮细胞表达系统
植物悬浮细胞表达系统是指将外源基因导入植物细胞中,经诱导愈伤组织后,进行植物细胞悬浮培养,实现植物来源生物医药产品的规模化生产的系统。2012年5月,美国FDA批准辉瑞公司的ELELYSO™上市,ELELYSO™注射液作为酶替代疗法用于I型戈谢病的治疗。ELELYSO™是全球首个植物悬浮细胞表达系统制备的人用药物,其表达载体为经基因修饰的胡萝卜植物根系悬浮细胞。
③ 种子(或果实)表达系统
植物种子生物反应器是利用禾本科植物的胚乳细胞作为生物反应器,采用组织特异性启动子使得目的基因在胚乳细胞中特异性转录、翻译并大量积累储存。
植物种子生物反应器构建的一般详细技术路径为:将介导目的基因表达的胚乳特异性表达盒构建到农杆菌Ti质粒中,将重组质粒转染农杆菌,通过农杆菌感染植物愈伤组织,并在含有选择压力的培养基上进行筛选,利用植物细胞全能型的特性,经过诱导、分化和再生获得完整植株,在植物开花成熟后,筛选胚乳细胞高表达目的蛋白的单株,经过2-3代选育,获得稳定遗传的纯合株系和品系。
综上,上述每个系统用于重组蛋白药物制备都有各自的优缺点。因此,需要根据目标重组蛋白药物的特点选择合适的表达系统。
重组蛋白药物制备表达系统优缺点对比情况
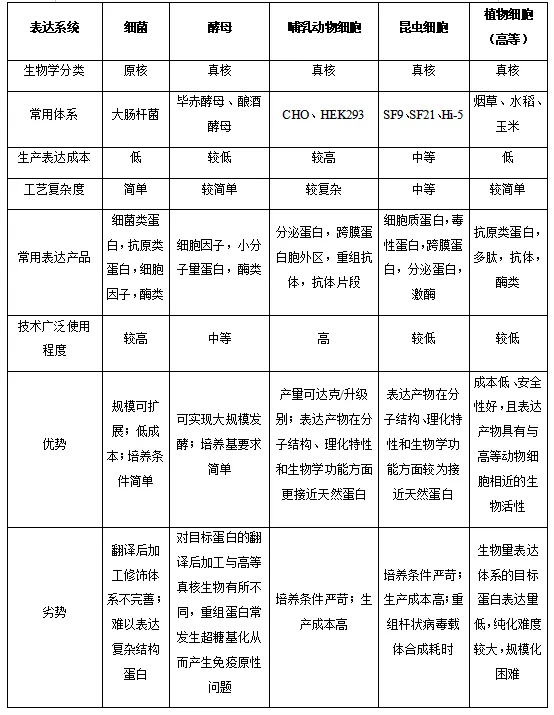
资料来源:文献研究、弗若斯特沙利文分析。
(四)植物表达体系发展历程
1958至1959年,Reinert和Steward分别由胡萝卜细胞诱导形成了胚状体,并获得了再生植株,证明了植物细胞的全能性,植物细胞工程技术实现了突破。1960年,英国科学家Cocking建立了植物原生质体培养和体细胞杂交技术;1980年Davey等用Ti质粒转化原生质体成功;1983年,Zambryski等用农杆菌介导法获得了世界上首例基因工程植物;1987年,Sanford等发明了基因枪法。
20世纪90年代,植物遗传转化技术陆续取得重大突破,农杆菌介导法先后在玉米、水稻、大麦、小麦上实现了高效转化。
以植物表达体系生产药用重组蛋白在国际上又称植物分子医药(Molecular Pharming,MP),相对于目前现有的微生物表达体系和动物表达体系,植物表达体系具有成本低、安全性好和规模化容易的优势,但早期以烟草叶片为主的叶片生物量表达系统存在表达量低、纯化工艺复杂、规模化困难等技术门槛,阻碍了植物表达体系的进一步发展。植物表达体系的发展历程如下:
1、技术萌芽期与期望膨胀期,1989-2005年
1989年,Hiatt等人首次报道了利用烟草生产重组抗体,植物分子医药的概念随之诞生。此后的一段时间,该领域迅猛发展,针对不同的植物,包括陆生植物(烟草、水稻、小麦等)、水生植物、苔藓等的概念验证研究层出不穷。繁多的植物表达系统意味着不同的蛋白产品可以选择最适宜的表达系统来生产,植物表达体系相比于动物表达体系而言具有诸多优势:如成本更低、产量更大;植物瞬时表达系统相比于基于发酵的大肠杆菌表达系统和酵母表达系统等而言,产能放大的周期更短。此外,目前无任何证据表明植物病毒可与人或动物共患,因此,植物作为蛋白药物的表达系统也具有更好的安全性。
植物表达体系根据其目的蛋白的用途不同,可分为重组药用蛋白和重组非药用蛋白。重组药用蛋白的研究旨在利用植物表达体系生产药用蛋白,如抗体、疫苗、血液制品、酶等,而非药用蛋白研究旨在生产工业用酶和实验试剂等。
非药用蛋白分支方面,美国公司ProdiGene在20世纪90年代后期因其开发和商业化水解酶方面的开创性工作,使得利用植物表达体系生产工业蛋白相比药用蛋白率先实现商业化。与此同时,加拿大公司SemBioSys Genetics、美国公司Ventria Bioscience、冰岛公司ORF Genetics利用红花、水稻、大麦生产的化妆品原料和科研试剂也成功实现商业化。另一方面,药用分支领域蓬勃发展,据Twyman等人报道,2005年,植物分子医药领域至少有50家企业正在推动其相关技术的商业化进程,其中大多数都专注于医药领域。
2、泡沫破裂谷底期,约2005-2010年
植物表达体系及植物分子医药在2005年至2010年经历了泡沫破裂谷底期,具体原因如下:
① 企业对植物分子医药具有较高的预期,而发展产业化遇到技术瓶颈
相较于利用动物或微生物细胞表达系统生产药用重组蛋白,植物表达体系具有生产成本低、可生产结构复杂的蛋白、便于贮藏和运输以及安全性较高等优势,这使得企业对植物分子医药产生了较高的预期。然而,发展产业化遇到了诸多技术瓶颈,例如:以叶片为生物反应器的生物总量表达系统中存在规模化生产与下游技术的GMP符合性等问题,这些技术瓶颈影响了植物分子医药的规模化生产,进一步影响了植物分子医药的产业化。
② 植物分子医药下游环节的高成本,对其商业化发展造成了困难
以植物细胞作为生物反应器生产药用重组蛋白的核心优势在于成本低廉,但这仅指种植植物的生产成本。然而通常种植成本仅构成其总成本的有限部分,植物分子医药的主要成本体现在纯化工艺上。以叶片生物量表达系统为例,由于表达量低、叶片宿主细胞蛋白近万种等问题,导致纯化工艺非常复杂,故而相比于低成本的“上游”环节,“下游”环节中建立GMP/cGMP、提取纯化表达产物、产品质量控制等成本很大。植物分子医药下游环节所需要的高成本,对植物分子医药的商业化发展造成了一定困难。
③ 基因工程部分技术和资金链问题尚未解决,导致其发展受挫
由于药物开发周期长,投资大,风险高等特点,植物生物反应器技术在产量、纯化工艺和规模化等方面尚处于早期阶段,与产业化相关的技术亟待突破;此外,由于从事植物分子医药的企业以科学家为主,对医药研发周期和资金需求估计不足,叠加公众的科学认知和市场接受度等社会因素以及植物分子医药产业化政策发展滞后和资本市场当时尚未成熟等原因,导致植物分子医药研发公司容易出现资金链问题,导致植物分子医药的发展受挫。
④ 国际上植物分子医药药物评审的法规滞后或尚未建立,新技术体系受到法规障碍
由于工业界已习惯于使用大肠杆菌、酵母及哺乳动物细胞表达体系,即使植物表达体系在安全、成本、规模化和环保等方面具有优势,仍然难以撼动已有几十年应用历史并广泛使用的微生物及哺乳动物细胞表达体系。工业界不愿意尝试这一新兴的、尚无完善监管审评制度和质量体系的技术。
综上,植物分子医药领域在经历了技术萌芽期和期望膨胀期后,随着研究和商业化的失败,处于泡沫破裂谷底期。
3、稳步爬升复苏期,约2010年-至今
经历了低谷期后,部分幸存的植物分子医药企业重新开始发展。在2012年辉瑞与以色列的Protalix合作开发治疗戈谢病的药物ELELYSO™获得FDA批准上市,在技术体系和审批法规方面获得了突破,给植物分子医药领域注入一剂“强心针”,植物分子医药进入复苏阶段。
4、植物表达体系的商业化
高等植物属于真核生物,其表达系统具有翻译后的加工修饰体系,表达的外源蛋白更接近于天然蛋白,表达产物具有与高等动物细胞相近的生物活性。同时植物表达体系具有成本低、安全性好的优势。植物生物反应器已经在药用辅料、体外诊断试剂、培养基、高级食品添加剂、科研试剂等多个领域实现商业化应用,植物生物反应器表达系统制备的重组蛋白药物也于近年来陆续进入临床试验阶段。
(一)(重组)人血清白蛋白药品
1、人血清白蛋白的功能和用途
人血清白蛋白(Human Serum Albumin,HSA)是血液或血浆中主要蛋白成分,由肝脏细胞生产,占血浆总蛋白的60%,对维持血浆渗透压、保持血管内外液体平衡具有重要的作用;正常人体内的血清白蛋白浓度维持在一定范围内,低于正常水平会导致低白蛋白血症,是许多常见临床疾病的并发症。
人血清白蛋白有多重生理功能,包括:①维持血浆胶体渗透压,保持血管内外液体平衡;②运输、结合和转运体内多种离子、脂质及代谢产物;③维持毛细血管通透性、抗炎、抗氧化以及调节凝血功能等。
人血清白蛋白的主要用途包括:①药品用途,主要用来改善低白蛋白血症,应用人血清白蛋白的部分主要场景包括:肝硬化低白蛋白血症、严重脓毒症、恶性腹水、透析内低血压。②药用辅料用途,人血清白蛋白在疫苗和细胞治疗药品中作为药物稳定剂或保护剂以稳定或保护其有效成分,防止其降解或失去活性;人血清白蛋白作为药物载体,与药物偶联后可控制药物释放速度,延长药物的体内半衰期,实现药物长效化;还可以用作其他药用辅料,如注射用紫杉醇(白蛋白结合型)以人血清白蛋白为辅料制备。根据《药品注册管理办法》,人血清白蛋白作为药用辅料需要获得CDE关联审评通过。③科研用途,主要包括细胞培养基、血浆基质对照封闭剂和酶保护剂等。
2、人血清白蛋白药物的制备
① 生化提取
目前,绝大多数国内外企业从血浆中分离纯化人血清白蛋白采用低温乙醇法。低温乙醇法是以混合血浆为原料,通过逐级降低酸度(从pH7.0降到pH4.0)、提高乙醇浓度(从0%升到40%)、降低温度(从2°C降到-2°C)的方式,使得各种蛋白在不同分离条件下分步从溶液中析出,并通过离心或者过滤的方法获得各目标组分。以此方法从血浆中得到人血清白蛋白原液后,经超滤、配制、巴氏灭活、除菌过滤分装等处理,可得到人血清白蛋白成品。
② 生物技术制备
由于市场需求量大,单靠人血浆提取人血清白蛋白难以满足市场的需求。近年来,国内外学者正积极开发研究采用基因工程技术生产重组人白蛋白替代血浆提取pHSA的技术。
尽管生化提取法来源广泛,但其普遍存在产量低、纯化难、成本高、可能存在传播血源性疾病的潜在风险等问题。相较而言,重组人白蛋白纯度高、免疫原性低、过敏反应少且能进行规模化生产。因此,蛋白药物的生产方式呈现出以生物技术制备取代生化提取的趋势。上述两种制备方法的原理与各自优劣势比较如下:
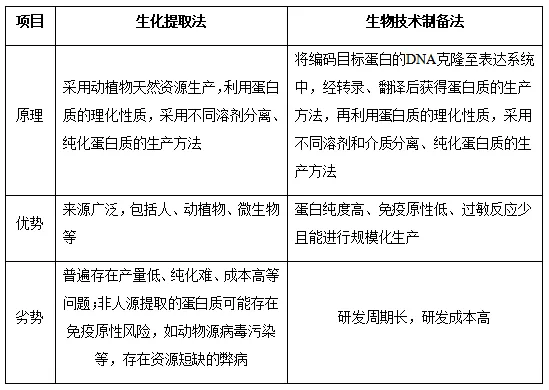
自1981年以来,国际上试图生产重组人白蛋白替代血浆提取,但在技术上一直没有获得突破。主要原因是:①人血清白蛋白在临床上使用剂量高、用量大(10g至20g级别),对重组人白蛋白的安全性和成本要求极高,重组人白蛋白技术不仅要求纯度高(>99.9999%),且要求宿主细胞杂质安全性好;②由于市场需求量大,对规模化生产和环保要求也非常高。在形成上百吨人白蛋白产能规模的同时,在经济上也要求重组人白蛋白生产成本低,且对环境影响小。
2007年,日本田边三菱制药株式会社研发的通过毕赤酵母表达体系生产的重组人血清白蛋白Medway获批上市,但是由于其试验数据涉嫌造假,于2009年撤市。除此之外,其它公司的产品,如赛多利斯集团(Albumedix公司)、Ventria Bioscience的重组人白蛋白均只可用作药用辅料或科研试剂。
中国采用生物技术制备重组人白蛋白的研究正在快速发展,其中:2024年4月和2025年3月,安睿特由酵母表达的重组人白蛋白药品分别在俄罗斯和吉尔吉斯斯坦实现注册上市,重组人白蛋白的技术路径已被初步印证;国内市场中安睿特及普罗吉由酵母表达和禾元生物由水稻胚乳细胞表达的重组人白蛋白药品均已经完成了III期临床试验,其中禾元生物HY1001已率先于2025年7月顺利获批上市;健通生物由酵母表达的重组人白蛋白药品处于Ia期临床试验;海正药业、华北制药和禾元生物药用辅料级别的重组人白蛋白已经完成NMPA或FDA的药用辅料登记。
1、中国人血清白蛋白的市场需求
① 临床药品需求
人血清白蛋白药品的临床需求量十分可观,2016年至2021年,我国人血清白蛋白药品的批签发量逐年上升,但受限于原料来源、生产方式与监管机制等问题,相比于临床上的用药需求而言,我国人血清白蛋白市场仍存在较大缺口。
2020年中国人血清白蛋白治疗药物市场规模达到258亿元人民币,2030年市场规模预计570亿元人民币。截至2025年8月31日,我国仅禾元生物的重组人白蛋白药品实现获批上市,市场上主要为通过血浆提取得到的人血清白蛋白药品。目前,在国内尚有三款重组人白蛋白药品处于临床试验阶段。随着重组人白蛋白药品的上市,重组人白蛋白药品凭借其产量大、疗效好、安全性佳、成本低的优势,我国人血清白蛋白治疗药物市场的临床需求缺口将得到填补,进口依赖的现象也将得到改善,故人血清白蛋白治疗药物市场的规模将相应快速增长。
② 药用辅料、科研试剂需求
非药用白蛋白产品包括药用辅料、培养基级别等的人血清白蛋白产品。其中,人血清白蛋白作为药用辅料是理想的药物载体、保护剂,且可以作为药物长效化的有效手段,预计将随着蛋白药物、疫苗、细胞和基因治疗以及长效化药物产品等市场的快速发展而需求量上升,由此驱动,药用辅料的人血清白蛋白市场将稳步增长。在培养基应用方面,人血清白蛋白是许多无血清细胞培养系统的重要成分之一,由于其不含有动物源成分,可减少动物源病毒传播和污染的潜在风险,加之良好的产品均一性、批间一致性和规模效应带来的成本优势,预计培养基级别的人血清白蛋白需求量将稳步提升。
2020年,中国非药用人血清白蛋白(药用辅料、科研试剂)市场规模达25亿元人民币,预计2025年达到56亿元人民币,复合年均增长率为17.8%,2030年市场规模预计90亿元人民币,2025年至2030年复合年均增长率为10.0%。
2、中国人血清白蛋白的供给及市场竞争
(1)人血清白蛋白药品的供给及市场竞争
① 血浆来源人血清白蛋白(pHSA)市场
2016年至2021年,我国人血清白蛋白批签发量稳步增长,从2016年的400.0吨增长至2021年的645.2吨。按产地拆分,进口产品批签发量占比约60%,呈现出严重依赖进口的情况。2020年我国国产人血清白蛋白的批签发量与2019年基本持平,国产占比略有下降。2021年我国国产人血清白蛋白批签发量较2019年及2020年得到大幅提升,国产占比也有所增加。
中国人血清白蛋白药品市场中,排名前四的均为境外企业。2021年,这四家境外企业生产的人血清白蛋白批签发量占整体市场的60.8%,进口依赖较为严重。国产企业中,天坛生物为最大的人血清白蛋白药品生产企业,但仅占据了7.3%的市场份额。
国内人血清白蛋白药品平均中标价多年来一直维持在380元(50ml:10g规格)左右,主要原因如下:①中国人血清白蛋白市场长期处于供不应求的状态,2001年后国家无新批血制品生产企业,目前国内仅有约30家企业具有血制品生产资质,且新建单采血浆站门槛较高,血浆供给端的短缺导致人血清白蛋白药品存在较大的市场缺口。②国产血液制品主要采用院外销售模式,院外市场销售占比在一半左右,价格受带量采购政策的影响较小。2022年1月19日,广东11省联盟公布了276个带量采购品种。从《广东联盟双氯芬酸等药品集中带量采购(第二批)拟中选/备选结果公示表》中可以看出人血清白蛋白药品的价格依旧维持在380元(50ml:10g规格)左右。
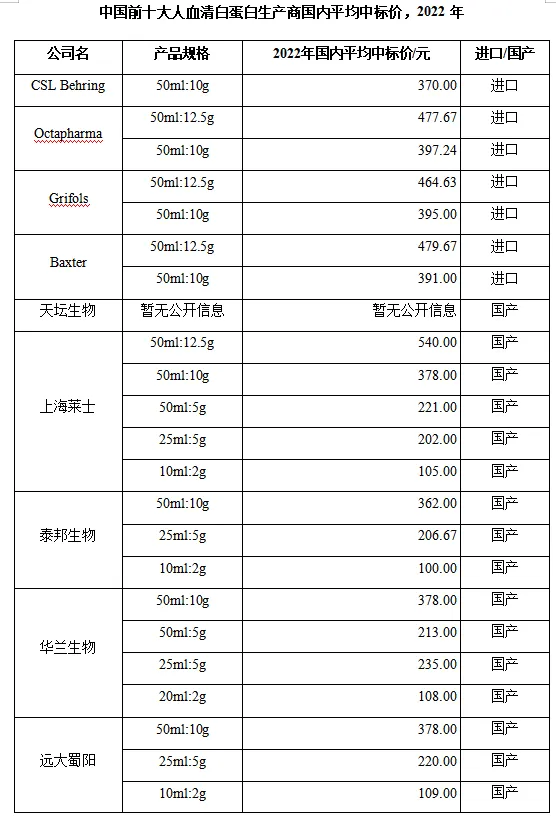
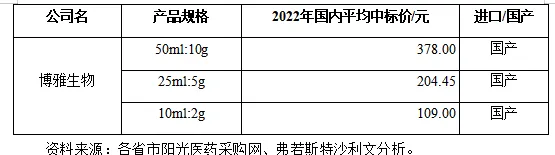
① 重组人白蛋白药品市场
截至2025年8月31日,全球市场仅禾元生物的重组人白蛋白药品于2025年7月在中国实现获批上市以及安睿特的重组人白蛋白药品于2024年4月和2025年3月分别在俄罗斯和吉尔吉斯斯坦实现注册上市。日本田边三菱制药株式会社通过毕赤酵母表达系统生产的重组人白蛋白药物Medway于2007年在日本批准上市,但是由于该药物试验数据涉嫌造假,已于2009年撤市。目前,全球市场上主要为通过血浆提取得到的人血清白蛋白药品。
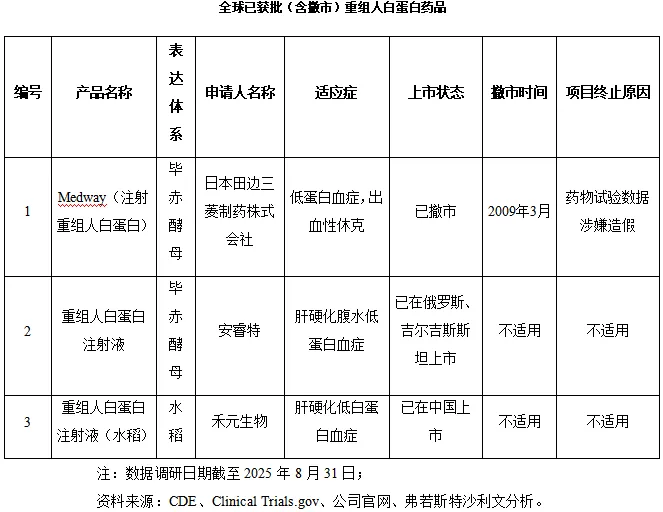
在研药品方面,全球范围内在研的重组人白蛋白药品数量极少,具体情况如下:
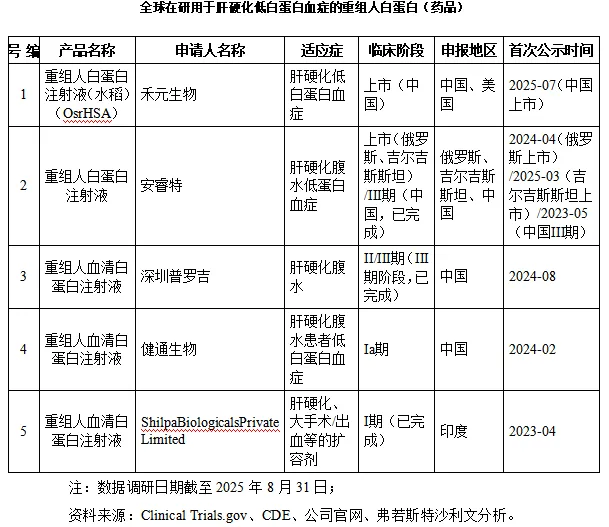
(2)药用辅料、科研试剂的重组人白蛋白供给及市场竞争
截至2025年8月31日,有5家企业的重组人白蛋白作为药用辅料完成了NMPA和/或FDA的登记,具体情况如下:
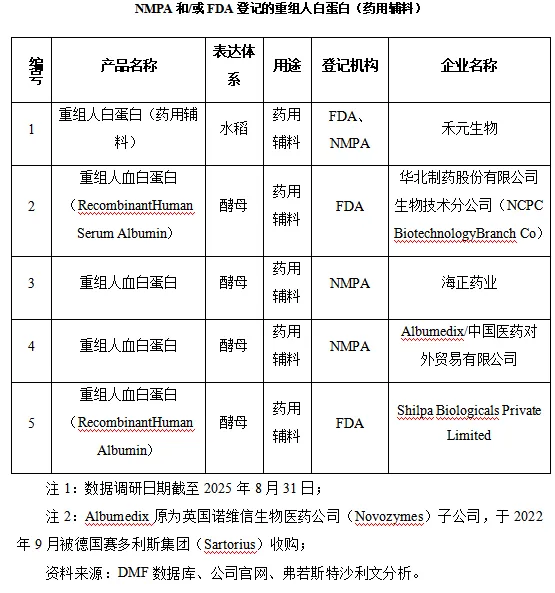
进一步药用辅料的临床试验和关联审评方面,截至2025年8月31日,上述登记产品中,Albumedix公司的产品Recombumin已应用于美国默克(Merck)公司的麻腮风三联疫苗以及诸多在研药品的生产当中。国内生产的重组人白蛋白作为药用辅料进入临床阶段的为华北制药通过酵母表达系统生产的重组人白蛋白。华北制药于2011年启动重组人白蛋白在中国健康受试者中的耐受性和安全性研究的临床试验。临床总结显示其生产的重组人白蛋白对中国健康受试者安全性和耐受性达到预期目标。进一步其重组人白蛋白产品作为药用辅料与辽宁成大生物股份有限公司的狂犬疫苗组合开展了III期临床试验,根据CDE公开信息,试验目前仍在进行中。
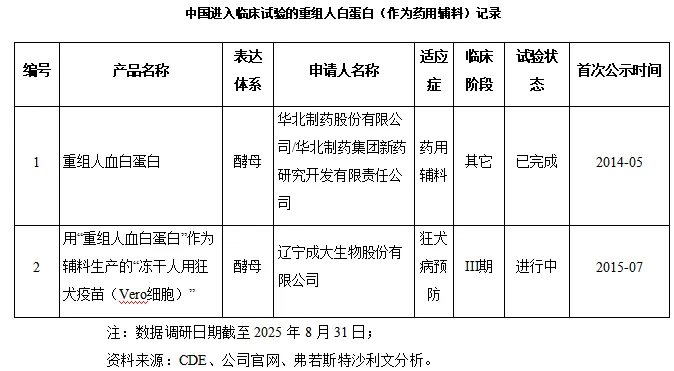
除了作为药品或者药用辅料,用于科研试剂及其他方面的重组人白蛋白商业化市场中,全球较为成熟且有一定市场认可度的主要生产方包括禾元生物、Ventria Bioscience、赛多利斯集团(Albumedix公司)等公司。
《中国生物技术制药行业深度分析报告(政策法规、发展现状、未来趋势、竞争格局)》原文WORD版:请回复“报告239”免费下载。


