线粒体研究报告:昼夜节律性 REV-ERBs 通过抑制 E4bp4 激活 NAMPT 依赖性的 NAD+ 生物合成并维持心脏功能
Nature Cardiovascular Research:昼夜节律性 REV-ERBs 通过抑制 E4bp4 激活 NAMPT 依赖性的 NAD+ 生物合成并维持心脏功能出处:Dierickx P, Zhu K, Carpenter BJ, et al. Circadian REV-ERBs repress E4bp4 to activate NAMPT-dependent NAD+biosynthesis and sustain cardiac function. Nat Cardiovasc Res. 2022;1(1):45-58.
作者介绍:
心脏是一个高度代谢活跃的器官,利用多种能量来源来满足其 ATP 生成需求。昼夜进食-禁食周期会导致底物可利用性的波动,而这种波动与活动期增加的能量需求共同决定了心脏代谢需要具有节律性。核受体 REV-ERBα 和 REV-ERBβ 是分子昼夜节律钟中至关重要的抑制性组分,也是代谢的重要调控因子。为探究其在心脏中的作用,我们构建了心肌细胞特异性双敲除 Rev-erbs 的小鼠,该模型因扩张型心肌病而过早死亡。在明显病理改变出现之前,Rev-erbs 的缺失即显著下调脂肪酸氧化相关基因,这一效应由转录抑制因子 E4BP4 的诱导所介导,而 E4BP4 是心脏 REV-ERBs 的直接靶点。E4BP4 通过远端顺式调控元件直接控制 Nampt 及其生物合成产物 NAD+ 的昼夜节律性表达。因此,REV-ERB 介导的 E4BP4 抑制对于维持补救途径中的 Nampt 表达和 NAD+ 生成是必需的。综上,这些结果突出表明,昼夜节律性 REV-ERBs 对心脏基因表达、代谢稳态及心脏功能具有不可或缺的作用。
大多数生物都会表现出昼夜交替的活动期与静息期,因此其生物学功能需要在不同燃料来源之间进行切换。在哺乳动物中,底物选择具有组织特异性,因此某些器官主要依赖葡萄糖供能(如脑),而另一些器官,如肝脏和心脏,则主要依赖脂肪酸。燃料利用不仅取决于营养物质的可用性,还取决于机体所处的生理背景。¹ 许多生命活动都可观察到时间依赖性的昼夜节律,体内振荡过程由昼夜节律钟驱动,使机体能够预先适应如明暗变化和食物摄入等节律性刺激。² 昼夜节律钟紊乱可导致多种代谢缺陷,如高血糖、低胰岛素血症、糖尿病和血脂异常,以及睡眠缺陷、再生能力受损和癌症易感性增加。³ 因此,理解昼夜节律钟对器官特异性组织稳态的精确作用具有极其重要的意义。若干心血管参数,如心率和血压,会在一天内发生波动,并在清醒期早期达到峰值。⁴˒⁵ 心脏中许多受昼夜节律调控的过程由心肌细胞昼夜节律钟所支配。⁶ 其分子基础依赖于一个转录/翻译反馈环路,该环路包含若干核心节律因子,如 BMAL1、CLOCK 以及 REV-ERBα 和 REV-ERBβ。它们的节律性功能可形成组织特异性的节律钟控制基因(clock-controlled gene, CCG)表达程序,从而维持正常的细胞生理功能。³˒⁷ Nicotinamide phosphoribosyltransferase(烟酰胺磷酸核糖转移酶,Nampt)是 NAD+ 补救途径中的限速酶,即为这样一种 CCG,已被证实受 BMAL1:CLOCK 异二聚体的直接调控。⁷˒⁸ NAD+ 不仅在氧化代谢和生物能量学中发挥核心作用,还可作为辅助因子参与能够生成信号中间体或改变翻译后修饰的反应(例如 ADP-核糖基化或 sirtuins 介导的去乙酰化)。⁹ 通过在全身水平敲除 Clock 或 Bmal1,¹⁰ 以及在心脏中特异性敲除这些基因,均会导致代谢紊乱、¹¹ 心室心律失常¹² 和扩张型心肌病。¹¹˒¹³REV-ERB 核受体是核心节律钟负反馈支路中的关键因子,并已被认为是心外组织中连接昼夜节律与代谢的重要机制纽带。¹⁴˒¹⁵ 由于其缺乏核受体经典的激活结构域,REV-ERBs 通过招募 Nuclear Receptor CoRepressor(NCoR)和 Histone Deacetylase 3(HDAC3)而发挥强效且持续性的转录抑制作用。¹⁶ 后者可促进增强子处组蛋白去乙酰化,从而有助于抑制靶基因转录。目前,REV-ERBs 在健康心脏中如何调控基因转录仍知之甚少,但已有多项研究表明,REV-ERB 激动剂可影响心脏转录组、心肌肥厚和心脏功能,甚至在心肌梗死后亦然。¹⁷⁻¹⁹ 尽管这些研究所使用的化合物已被证明存在部分不依赖 REV-ERB 的效应,²⁰ 但这仍然凸显了研究 REV-ERBs 的作用及其靶基因的重要性,从而更好地理解其在生理条件下体内如何调控心脏功能。在本研究中,我们报道了一种在心肌细胞中同时删除两个 Rev-erbs 的小鼠模型(CM-RevDKO 小鼠),其会发生随年龄出现的扩张型心肌病,并导致过早死亡。我们提供的证据表明,在缺乏 REV-ERBs 的情况下,一方面由于一组基因被直接去抑制(即被激活),另一方面由于转录抑制因子上调而使另一组基因受到抑制,心脏无法满足其高能量生成需求,最终导致心力衰竭逐渐发生。在心外组织中,已有研究报道昼夜节律钟可通过 BMAL1:CLOCK 介导的 Nampt 昼夜节律性转录激活来促进 NAD+ 水平的周期性变化。我们发现,除受节律钟通路正调控支路调节外,REV-ERBs 对维持正常 Nampt 表达同样至关重要。尽管 Bmal1 表达增加,但 REV-ERBs 缺失仍会因 E4BP4 上调而导致 Nampt 显著受抑;E4BP4 可直接结合 Nampt 上游的顺式调控元件。与 E4BP4 的主导作用一致,我们显示,在 Bmal1 KO 心脏中,Nampt 的抑制可被额外的 E4bp4 KO 所阻止,从而证明 E4BP4 介导的 Nampt 下调在昼夜节律通路中具有因果作用。总之,我们表明,昼夜节律性 REV-ERBs 对建立控制心脏代谢的转录程序是不可或缺的,而该程序失调会导致扩张型心肌病和过早死亡。心肌细胞特异性耗竭 REV-ERBs 可导致致死性扩张型心肌病
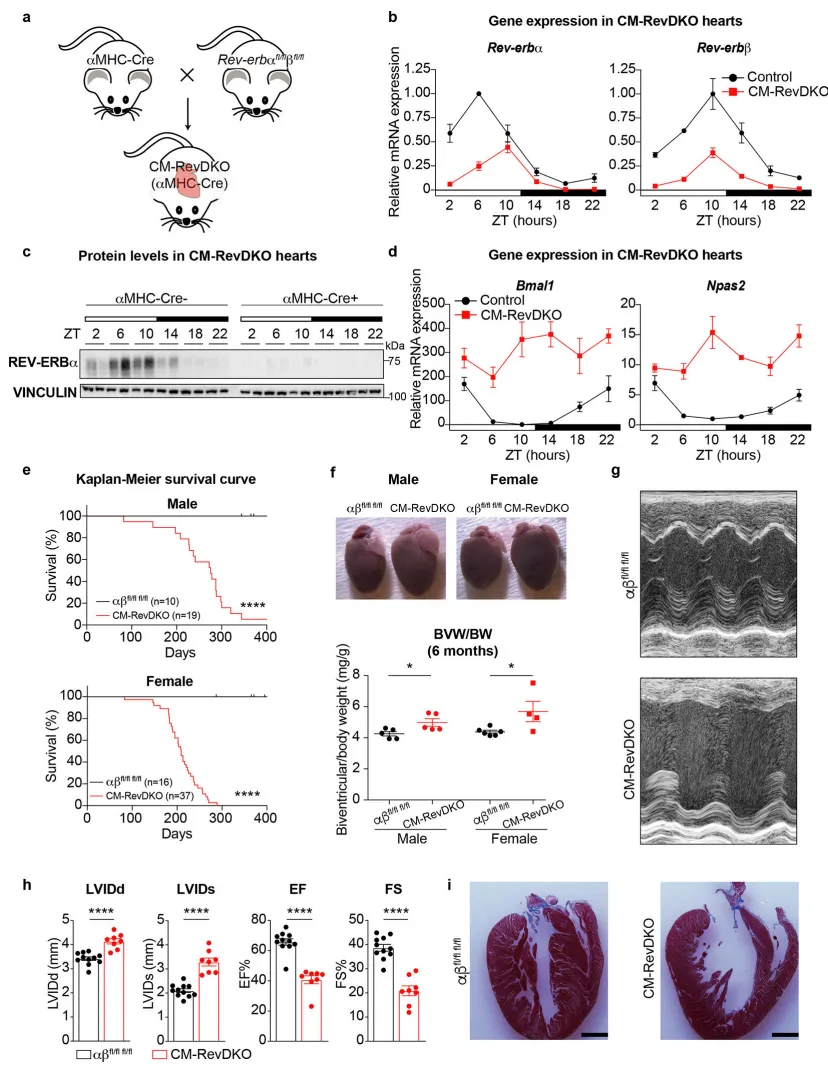
为探究核受体 REV-ERBα 和 REV-ERBβ 在心脏中的作用,我们将条件性 Rev-erbαfl/fl/βfl/fl 小鼠²⁰与心肌细胞特异性 Cre 删除鼠(αMHC-Cre²¹,C57BL/6 背景)杂交,构建了心肌细胞特异性 Rev-erbα/β 双敲除(CM-RevDKO)小鼠(图 1a)。在整个 24 小时昼夜节律周期内,CM-RevDKO 小鼠心脏中 Rev-erbα 和 β 的 mRNA 表达均降低(图 1b),且 CM-RevDKO 心脏中 REV-ERBα 蛋白水平持续降低(图 1c)。与此一致,经典 REV-ERB 靶基因 Bmal1 和 Npas2 在 CM-RevDKO 心脏中的表达显著升高(图 1d),BMAL1 蛋白水平亦持续维持在较高水平(扩展数据图 1a)。另一方面,Per2 mRNA 的节律性水平未受影响(扩展数据图 1b)。值得注意的是,与 2 月龄 floxed 对照小鼠相比,6 月龄 floxed 对照小鼠中 Rev-erb mRNA 水平的昼夜差异减弱(扩展数据图 1c)。
虽然 CM-RevDKO 小鼠出生时符合预期的孟德尔分离比(扩展数据图 2a),但无论雄性还是雌性小鼠,其寿命均明显缩短,并在约 6–9 月龄时死亡率增加(图 1e)。CM-RevDKO 小鼠表现出正常的昼夜节律行为、摄食量和体重(扩展数据图 2b,c,d)。此外,6 月龄小鼠的葡萄糖耐量试验和胰岛素耐量试验结果也正常(扩展数据图 2e,f)。然而,与 WT 小鼠相比,CM-RevDKO 雄性和雌性小鼠在 6 月龄时的心脏重量均增加(图 1f),而 2 月龄时无此现象(扩展数据图 2g),提示心肌细胞特异性 Rev-erb 缺失会随时间推移引起心脏增大。与双心室重量增加一致,6 月龄 CM-RevDKO 小鼠的心肌细胞横截面积也增大(扩展数据图 2h)。这一结果与近期一项报道相一致,该研究描述了 REV-ERB 激活对新生大鼠心室肌细胞肥大的保护作用。¹⁹ 超声心动图显示,6 月龄时左心室(LV)收缩末期和舒张末期内径显著增加,同时伴有 LV 射血分数、LV 缩短分数降低(图 1g,h),以及其他反映心肌病性病理重构的超声异常,而这些变化仅见于较老龄小鼠(扩展数据图 2i,j)。H&E 和三色染色显示 CM-RevDKO 心脏发生扩张,但未见纤维化征象(图 1i,扩展数据图 2k)。此外,我们也未在 CM-RevDKO 或对照心脏中检测到明显细胞死亡(扩展数据图 2l)。综上,心肌细胞中 REV-ERBs 的缺失在结构和功能层面均造成重大影响,最终导致扩张型心肌病所致的过早死亡。Fig. 1 心肌细胞特异性 Rev-erbα/β 双敲除导致致死性扩张型心肌病a,CM-RevDKO 小鼠构建示意图。b,在 24 小时昼夜周期内对照组与 CM-RevDKO 小鼠心脏中 Rev-erbα 和 β 的 mRNA 表达。c,对照组与 CM-RevDKO 小鼠心脏中 REV-ERBα 蛋白水平。d,CM-RevDKO 心脏中 Bmal1 和 Npas2 的 mRNA 表达。e,对照组与 CM-RevDKO 小鼠的生存曲线。f,不同年龄阶段小鼠的心脏重量。g,h,超声心动图评估左心室结构与功能参数。i,对照组与 CM-RevDKO 心脏的 H&E 及 Masson 三色染色。CM-RevDKO 扰乱代谢性转录程序并引起线粒体缺陷
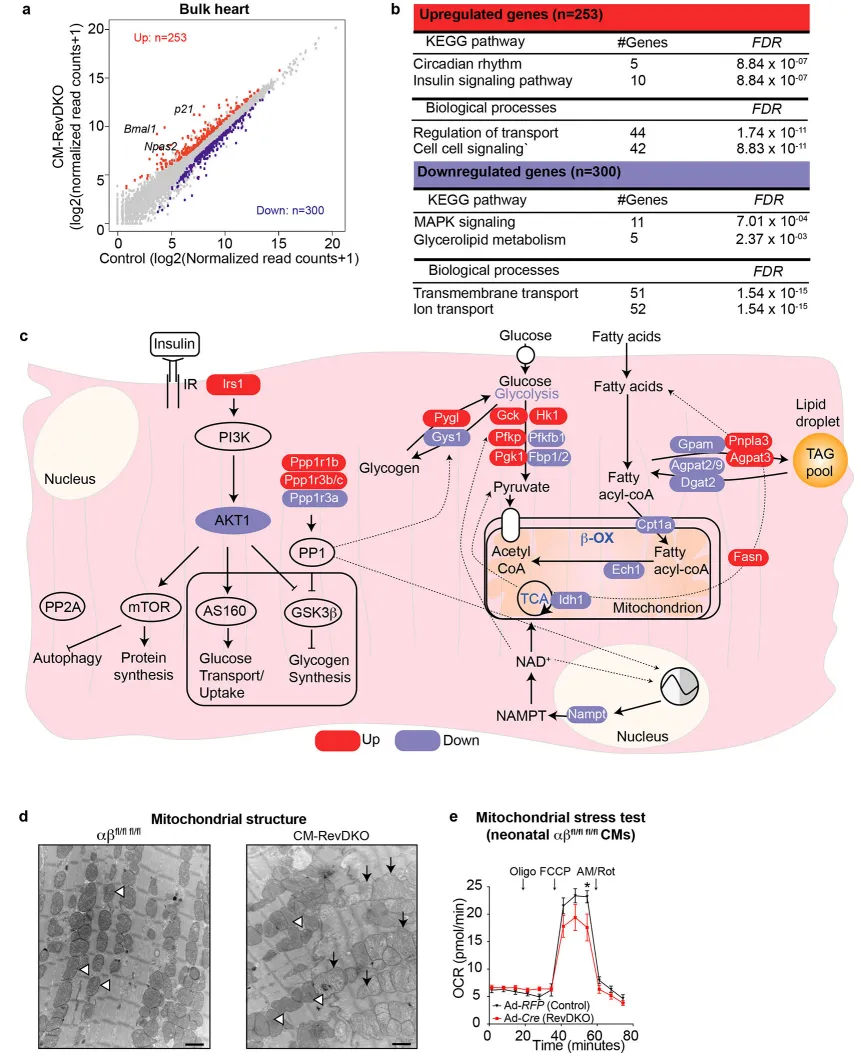
为阐明心肌细胞中双重敲除 Rev-erbs 后导致年龄依赖性心力衰竭的分子机制,我们在 2 月龄时进行了转录组分析(即心肌病发生前阶段)。在 ZT10 时点分离心脏,此时 WT 心脏中 Rev-erbα 和 β 表达较高,而 Bmal1 表达处于谷底值(扩展数据图 3a)。我们共检测到 553 个差异表达基因(log2 倍数变化(FC)> 0.58,Adj. P < 0.05),其中 253 个在 CM-RevDKO 心脏中上调,300 个下调(图 2a 和补充表 1)。将这些基因(n=553)与肝脏中 Rev-erbs 敲除后 ZT10 时点差异表达的转录本²²(n=762,log2 倍数变化(FC)> 0.58,Adj. P < 0.05)进行比较显示,心脏中的 REV-ERB 靶基因总体上不同于肝脏中的靶基因(扩展数据图 3b),这与既有观点一致,即除核心节律因子外,REV-ERBs 以组织特异性方式调控基因表达。²³ 事实上,Bmal1、Clock 和 Npas2 等经典昼夜节律调控因子在 CM-RevDKO 心脏和肝细胞特异性 RevDKO 肝脏中均发生去抑制(扩展数据图 3b)。相反,若干参与心肌细胞基本功能的关键心脏基因(如参与代谢、信号传导及离子通道功能的 p21、Slc41a3 和 Fhit)在 REV-ERB 缺失后发生失调,并经 qRT-PCR 验证(扩展数据图 3c)。与既往发表的心脏昼夜节律基因表达数据²⁴ 重叠分析显示,CM-RevDKO 心脏中约 31% 的差异表达基因在 WT 心脏中呈节律性表达。此外,上调和下调基因的峰相位分别主要与 Rev-erbs 的表达呈反相和同相聚集(扩展数据图 3d)。这提示 REV-ERB 在一天中的静息期通常抑制这些上调基因,而下调基因很可能并非 REV-ERB 的直接靶点。
为进一步探究 CM-RevDKO 心脏中上调和下调基因的功能,我们进行了 GO 和 KEGG 通路分析。上调基因富集于昼夜节律、胰岛素信号以及转运和细胞间信号调控等条目,而下调基因则主要与 MAPK 信号、甘油脂代谢以及跨膜转运和离子转运有关(图 2b)。这些数据提示,心脏中双重缺失 Rev-erbs 会导致关键心脏氧化代谢过程的转录失调。的确,在 CM-RevDKO 心脏中,胰岛素信号通路中的若干成分——这是已知受心脏节律钟调控的过程之一¹¹˒²⁵——如 Irs1(上调)、Pde3a(上调)、Akt1(下调)均发生差异表达;此外,胰岛素下游靶向通路也发生改变,如糖原储存相关基因 Pygl(上调)以及调控这些蛋白活性的信号通路成分 Ppp1r3a(下调)、Ppp1r1b(上调)和 Ppp1r3b/c(上调)(图 2c)。我们通过 qRT-PCR 和 Western blot 验证了 DARPP-32(由 Ppp1r1b 编码)水平的显著升高,DARPP-32 是蛋白磷酸酶 1(PP1)活性的重要调节因子(扩展数据图 4a,b)。由于 PP1 是心脏中重要的磷酸酶,也是多条关键心脏信号通路的重要调控者,而其功能失调已被认为与心脏功能障碍有关,²⁶ 因此其在 CM-RevDKO 心脏中的失调可能促成这些小鼠年龄依赖性的致死表型。我们还注意到,脂质氧化基因主要呈下调。这些代谢基因涵盖了线粒体脂肪酸摄取相关基因(转运体 Cpt1a)、主要心脏 β-氧化基因如 Acads/l、Hadha 和 Ech1(均下调,FC > 1.25),以及胆固醇代谢相关基因 Ces1d 和 Nceh1(图 2c)。此外,对 6 月龄 CM-RevDKO 心脏进行电子显微镜观察发现,许多心肌细胞线粒体体积增大,并伴有异常嵴结构,提示肿胀(图 2d 和扩展数据图 4c)。而 2 月龄 CM-RevDKO 心肌细胞的线粒体则较对照心脏显著更小(扩展数据图 4d)。不过,线粒体 DNA 含量未见差异(扩展数据图 4e)。另外,在以棕榈酸供能的线粒体应激实验中,我们观察到线粒体功能受损(图 2e)。这些结果表明,REV-ERBs 是线粒体能量代谢和脂肪酸氧化(FAO)基因的关键调控因子,而其失调将导致 DCM 和过早死亡。Fig. 2 CM-RevDKO 扰乱代谢性转录程序并导致线粒体功能异常a,CM-RevDKO 与对照组心脏差异表达基因分析。b,上调和下调基因的 GO 与 KEGG 通路富集分析。c,胰岛素信号通路及脂质代谢相关基因的表达变化。d,电子显微镜观察心肌细胞线粒体结构。e,以棕榈酸为底物的线粒体应激实验(氧耗率)。REV-ERBs 可通过直接抑制心脏中的 E4bp4 介导基因激活
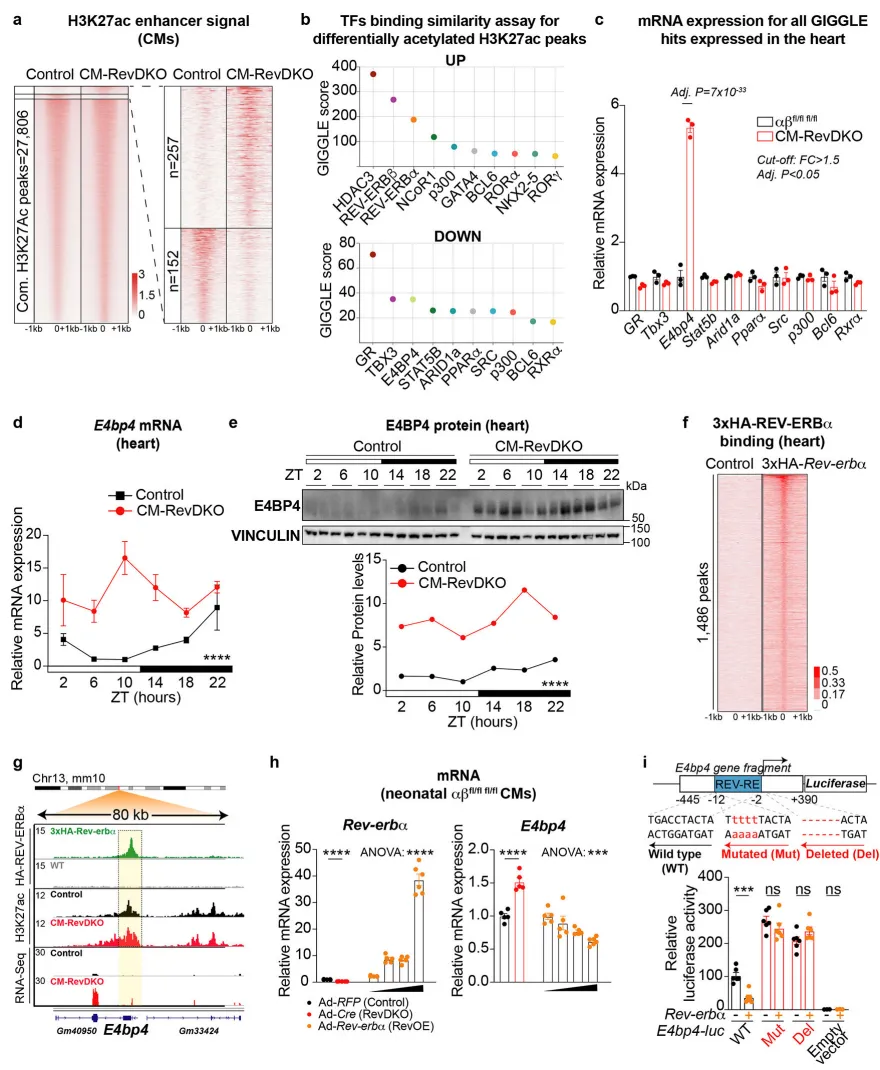
已知 REV-ERBs 通过结合增强子和启动子等顺式调控元件(CREs)发挥作用,从而抑制转录。²³ 为识别 REV-ERB 反应性调控区域,以解释直接上调的基因以及在 CM-RevDKO 心脏中可能参与间接基因下调的潜在调控位点,我们对活性增强子标记 H3K27ac 进行了 Cut&Run 分析。²⁷ H3K27ac 是活性增强子的标志。²⁸˒²⁹ 由于下调基因不太可能是 REV-ERB 的直接靶点,我们选择在分离的心肌细胞中而非整个心脏组织中进行对照组和 CM-RevDKO 小鼠的 Cut&Run,以提高特异性,并寻找可能参与下调 CREs 的转录因子结合位点(图 3a)。随后将 H3K27ac 的变化与 RNA-Seq 数据通过 Integrated Analysis of Motif Activity and Gene Expression(IMAGE)³⁰ 进行整合,结果显示包括 REV-ERBs、ARNTL、NPAS2、CLOCK、NKX2-5 和 E4BP4(亦称 NFIL3)在内的多种转录因子(补充表 2)可能是 REV-ERB 依赖性 mRNA 和增强子活性变化的驱动因子。此外,我们还利用 CistromeDB³¹ 进行了结合相似性分析,将 H3K27ac 发生变化的区域与已发表的心脏、骨骼肌和肝脏 ChIP-Seq 实验中的 cistrome 进行匹配。如预期所示,该分析表明,在 REV-ERBs 缺失后变为活跃的 H3K27ac 位点上,REV-ERBα 及其已知互作因子如 REV-ERBβ、HDAC3 和 NCoR1 的结合均呈富集(图 3b),支持 REV-ERBs 直接参与靶基因去抑制。相反,在 CM-RevDKO 心肌细胞中下调至少 2 倍的差异富集 H3K27ac 区域中,结合相似性分析显示 GR、TBX3、E4BP4 等因子的富集(图 3b)。
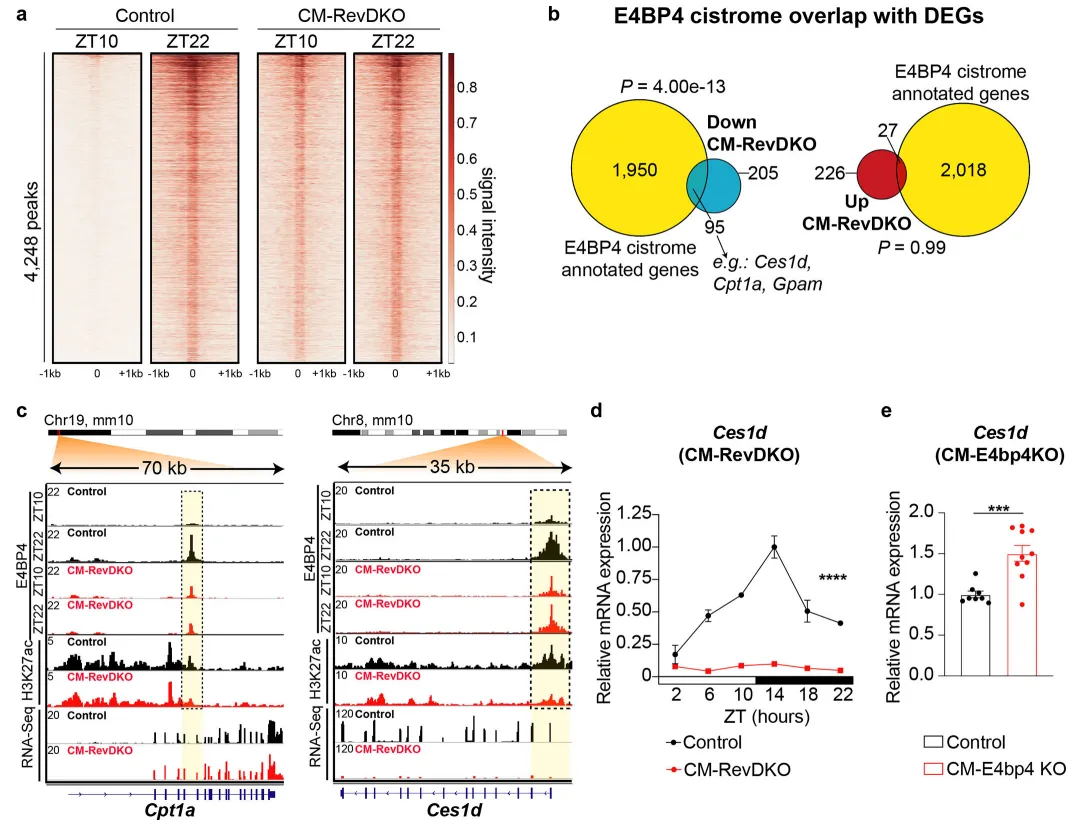
为了确定这些因子中哪些最有可能直接参与本文所述下调差异表达基因(DEGs)的抑制,我们考察了它们在 Rev-erb DKO 后是否发生差异表达(FC ≥ 1.5,Adj. P < 0.05)。结果发现,E4BP4 变化最为显著,其表达上调约 6 倍。虽然 GR 略有下降(下降,FC < 1.4;图 3c),但 CM-RevDKO 下调基因与已发表的心脏特异性 GR KO 心脏失调基因数据³² 几乎无重叠(扩展数据图 5a)。因此,我们将研究重点转向 E4bp4,并观察到该基因在整个昼夜周期内无论在 mRNA 水平还是蛋白水平均持续处于去抑制状态(图 3d,e)。为验证 REV-ERBs 在心脏中对 E4bp4 的特异性调控,我们在 3xHA-Rev-erbα 小鼠模型中采用抗 HA 抗体于 ZT10 进行 REV-ERBα ChIP-Seq,并以无 HA 敲入的 WT 小鼠作为对照。结果在 3 个样本中鉴定出 1,486 个高置信度峰值,且生物学重复之间相关性较高(Pearson correlation > 0.85;图 3f 和扩展数据图 5b)。其中,9% 的 REV-ERB 峰位于启动子,51% 位于内含子区域,35% 位于基因间区(扩展数据图 5c)。基序搜索证实其在已知结合基序如 RORE 和 RevDR2 处富集。与此一致,H3K27ac 信号升高 2 倍的增强子也呈现类似基序(扩展数据图 5d)。将注释后的高置信度峰与 CM-RevDKO DEGs 进行重叠分析显示,上调基因附近显著富集 REV-ERB 结合,而下调基因则无此现象(扩展数据图 5e)。带有 REV-ERBα 结合且调控活性发生变化的 DEG 示例既包括经典节律钟靶基因,如 Bmal1 和 Cry1(扩展数据图 5f,g),也包括重要心脏调控因子,如缺血/再灌注损伤调节因子 p21 以及编码细胞外糖蛋白 Fibrillin 2 的 Fbn2(扩展数据图 5h)。重要的是,我们发现 REV-ERBα 可结合心脏中 E4bp4 启动子(图 3g),提示 REV-ERB 可直接抑制 E4bp4 表达。事实上,采用不同腺病毒滴度过表达 Rev-erbα 可导致 E4bp4 呈剂量依赖性受抑(图 3h)。为进一步验证 REV-ERB 对 E4bp4 的功能性转录调控,我们构建了 E4bp4-luciferase(E4bp4-luc)报告载体,其中包含 E4bp4 启动子区段(相对于转录起始位点的 −445,+390),并带有一个鉴定出的潜在 REV-ERB 反应元件(REV-RE)。瞬时转染实验显示,Rev-erbα 过表达可抑制该 WT E4bp4-luc 构建体(图 3i,扩展数据图 5i)。而当 REV-RE 被突变或删除后,这种抑制作用消失(图 3i)。这些结果表明,REV-ERB 通过结合 E4bp4 启动子近端区域中鉴定出的 REV-RE,直接抑制 E4bp4 表达。综上,REV-ERBs 缺失会导致一组基因发生去抑制,其中包括转录抑制因子 E4bp4。Rev-erb DKO 后,E4bp4 持续高表达,并可能促成其靶基因在失去抑制性 REV-ERBs 的背景下反常地下调。Fig. 3 REV-ERBs 通过直接抑制 E4bp4 参与基因调控a,H3K27ac Cut&Run 分析流程示意图。b,H3K27ac 变化区域的转录因子结合相似性分析。c,潜在转录因子的表达变化。d,e,E4bp4 在昼夜周期中的 mRNA 与蛋白表达。f,REV-ERBα ChIP-Seq 结果。g,REV-ERBα 在 E4bp4 启动子区域的结合。h,Rev-erbα 过表达对 E4bp4 的抑制作用。i,E4bp4 启动子荧光素酶报告实验验证 REV-ERB 依赖性调控。为探究 CM-RevDKO 介导的 E4bp4 去抑制是否参与基因下调,我们在对照组和 CM-RevDKO 心脏中于 ZT10 和 ZT22 进行了 E4BP4 ChIP-Seq。对照组 ZT22 心脏峰值的已知基序和 de novo 基序搜索均显示 NFIL3 为最显著富集的基序(扩展数据图 6a),验证了 ChIP-Seq 数据质量。在对照心脏中共观察到 3,087 个结合位点,其中约 28% 注释于启动子区域,约 25% 位于基因间区,约 43% 位于内含子区域(扩展数据图 6b)。与对照心脏中所见的节律性 E4BP4 结合不同,在 CM-RevDKO 中染色质结合的节律性消失,表现为 ZT10 和 ZT22 时点均持续结合于 CREs(图 4a)。事实上,对照心脏 ZT22 时点的 E4BP4 结合位点中,大多数(2,187/3,384)在 CM-RevDKO 后于 ZT22 和 ZT10 两个时点均可检测到结合(扩展数据图 6c),说明 CM-RevDKO 心脏并未获得新的 E4BP4 结合位点,而是使 E4BP4 持续结合于那些通常仅在暗相期间占据的位点。
将这些数据与 CM-RevDKO 心脏中的 DEGs 进行交叉分析后发现,下调转录本附近更富集 E4BP4 结合(图 4b),这与 E4BP4 的转录抑制作用一致。多种在 CM-RevDKO 心脏中受抑的重要代谢基因,其调控区域在缺乏 REV-ERBs 时 H3K27ac 水平下降,并与心脏中的 E4BP4 结合共定位。例如,调控长链脂肪酸进入线粒体并参与后续 β-氧化的 Cpt1a(Carnithine O-palmitoyltransferase)、脂肪酶 Ces1d(carboxylesterase 1d),以及参与心脏中三酰甘油合成的两个关键酶 Gpam(Glycerol-3-phosphate acyltransferase 1, mitochondrial)和 Dgat2(Diacylglycerol O-acyltransferase 2),均呈现这一模式(图 4c,扩展数据图 6d)。此外,Ces1d mRNA 在整个昼夜周期内均下调(图 4d),这与 E4BP4 持续高表达相一致。在心肌细胞特异性 E4bp4 敲除心脏中,Ces1d mRNA 水平升高(图 4e),从而验证该基因是 E4BP4 的直接靶基因。因此,我们得出结论:REV-ERBs 在心脏中的作用,部分是通过解除对另一种抑制因子(E4BP4)的抑制而间接实现的,进而导致多个下游基因的转录活性下降。REV-ERBs 可在转录水平抑制 Bmal1。¹⁶˒³³ 同时,其自身表达又受 BMAL1 介导的激活。³⁴ 这突显了分子节律钟不同支路之间复杂的调控关系。此前报道的一种心肌细胞特异性 Bmal1 敲除(CBK)小鼠同样表现出严重的心脏缺陷。¹¹ 重要的是,由于上述两种节律因子之间的相互作用,Bmal1 KO 会导致 Rev-erb 下调。³⁵ 因此,CBK 小鼠和本研究模型可能共享一部分基因表达改变,且预期主要表现为上调,因为在两种模型中 REV-ERB 的抑制功能均缺失。反过来,Rev-erb DKO 会导致 BMAL1 持续存在(图 1d,扩展数据图 1a),因此也可能存在一类基因在 CBK 中下调而在 CM-RevDKO 中上调。我们对此进行了分析,确实发现,在 CM-RevDKO 心脏中上调的 253 个基因中,有 105 个在 CBK 心脏中也上调;而在这 253 个基因中,仅有 10 个在 CBK 中下调(扩展数据图 6e)。这提示,上调的转录变化可能是 REV-ERB 缺失的结果,而非 BMAL1 在 CBK 中缺失或在 CM-RevDKO 中增加所致。事实上,其中约 25% 的基因在心脏中具有 REV-ERBα 结合位点(扩展数据图 6f)。在 CM-RevDKO 心脏中下调的 300 个基因中,有 121 个在 CBK 心脏中也下调(扩展数据图 6g)。鉴于强效抑制因子 E4BP4 在 Bmal1 和 Rev-erb 敲除模型中均上调,我们将这两种转录因子敲除心脏的转录组数据与 E4BP4 ChIP-Seq 数据进行了比较。在 Bmal1 和 Rev-erbα/β 敲除心脏中共同下调的基因中,约 45% 在附近具有 E4BP4 结合(扩展数据图 6h)。这些差异富集基因之间的重叠提示,REV-ERBs 缺失及其导致的 E4BP4 持续高表达共同促成了两种模型中观察到的表型。事实上,由于 Bmal1 缺失会显著下调 REV-ERBs,¹¹ 这提示 Bmal1 KO 可通过下调 REV-ERBs 而间接影响 E4BP4。Fig. 4 E4bp4 去抑制介导脂质代谢基因的下调a,对照组与 CM-RevDKO 心脏中 E4BP4 染色质结合节律变化。b,E4BP4 结合与差异表达基因的关联分析。c,脂质代谢关键基因调控区域的 H3K27ac 变化及 E4BP4 结合。d,Ces1d 在昼夜周期中的 mRNA 表达。e,心肌细胞特异性 E4bp4 敲除对 Ces1d 表达的影响。REV-ERB 通过 E4BP4 介导的 Nampt 抑制调控心脏 NAD+ 生物合成
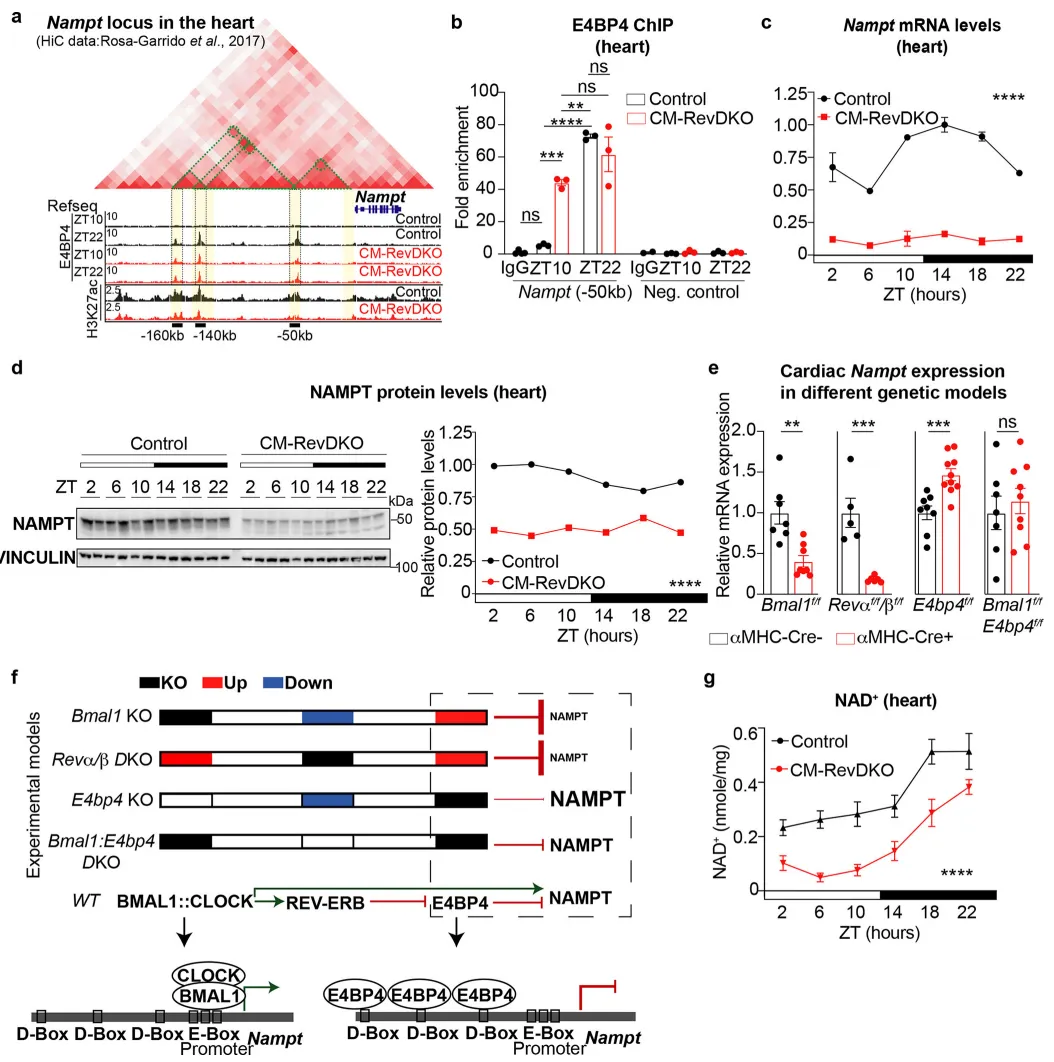
鉴于我们的结果提示 E4BP4 具有重要作用,我们进一步探讨该因子如何影响心脏代谢。E4BP4 在人类病变心脏中呈过表达状态³⁶,其果蝇同源蛋白 Vrille 随年龄增长而升高,且其过表达可通过线粒体功能障碍引起心脏扩张³⁷。与此一致,在 CM-RevDKO 心脏中,多种线粒体代谢关键因子如 Pgc1-α/β、Naprt1 和 Nampt 在 ZT10 时点显著下调(扩展数据图 7a)。由于 NAMPT 是 NAD+ 补救途径中的限速酶,而 NAD+ 可通过直接作用(例如结合代谢酶或作为代谢反应底物)及间接作用(例如作为多种翻译后修饰的辅因子)调控代谢³⁸,因此我们推测 REV-ERBs 通过 E4BP4 对 Nampt 的转录调控在 NAD+ 稳态中发挥关键作用。在心肌细胞中,Nampt 启动子上游增强子区域的 H3K27ac 水平下降,这些增强子在对照心脏中呈昼夜节律性结合,而在 CM-RevDKO 心脏中则表现为持续的 E4BP4 结合(图 5a)。将这些数据与既往发表的小鼠心脏 HiC 数据³⁹ 结合分析显示,这些潜在增强子与 Nampt 启动子之间存在染色质环状结构(图 5a),提示这些 CREs 可直接调控心脏中 Nampt 的基因表达。此外,在这 3 个增强子中均发现了 D-box 基序(TTAYGTAA),这是 E4BP4 的经典结合序列⁴⁰。在最靠近 Nampt 启动子的 CREs(距启动子上游 50 kb)处进行的 E4BP4 ChIP-qPCR 显示,与对照组仅在 ZT22 结合不同,CM-RevDKO 心脏在 ZT10 和 ZT22 均存在 E4BP4 结合(图 5b)。这些表观遗传学改变导致 NAMPT 的 mRNA 和蛋白水平均在整个昼夜周期内持续受到抑制(图 5c,d)。传统观点认为,Nampt 的昼夜节律性表达主要归因于 BMAL1:CLOCK 介导的转录调控,而敲除 Clock 或 Bmal1 会显著降低 Nampt 及 NAD+ 水平⁷˒⁸˒⁴¹。由于在心肌细胞特异性 Bmal1 和 Rev-erbα/β 敲除心脏中均观察到 Nampt 下调和 E4BP4 上调,我们推测 E4BP4 是 Nampt 抑制的主要驱动因素。因此,我们比较了心肌细胞特异性 Bmal1、Rev-erbα/β、E4bp4 单敲除以及 Bmal1/E4bp4 双敲除小鼠中 Nampt、Bmal1、Rev-erbα/β 和 E4bp4 的 mRNA 水平(扩展数据图 7b)。结果显示,Bmal1 和 Rev-erbα/β 单敲除均导致 Nampt 水平下降,而 E4bp4 敲除心脏则表现为 Nampt 表达升高(图 5e)。更为关键的是,Bmal1/E4bp4 双敲除并未表现出 Nampt 下调,提示在 Bmal1 单敲除模型中,E4BP4 是 Nampt 抑制所必需的(图 5e,f)。蛋白水平的结果与此一致,即 Bmal1 敲除心脏中 NAMPT 降低,而额外敲除 E4bp4 可部分恢复其表达(扩展数据图 7c)。综上,这些结果表明,REV-ERB–E4BP4 抑制轴在调控 Nampt 昼夜节律性表达中具有主导且必不可少的作用。
为进一步探究 NAMPT 失调对 NAD+ 的影响,我们比较了 CM-RevDKO 与对照心脏中的 NAD+ 水平,结果发现,在整个昼夜周期的各个时间点,CM-RevDKO 心脏中的 NAD+ 水平均显著降低(图 5g)。尽管 24 小时内持续下降具有统计学意义,但我们仍观察到心脏中 NAD+ 存在一定的节律性波动。类似现象也见于 Bmal1 敲除肝脏,即 NAD+ 水平整体降低但仍保留一定节律性⁴²。由于 CM-RevDKO 小鼠并不存在全身性节律紊乱,残余 NAMPT 蛋白活性及底物供应可能共同维持了 NAD+ 的残余节律性。然而,我们的结果表明,在缺乏 REV-ERBs 的情况下,E4BP4 持续介导的 Nampt 抑制会导致整个 24 小时周期内 NAD+ 水平降低。
Fig. 5 REV-ERB–E4BP4 轴调控 Nampt 表达及 NAD+ 生物合成a,Nampt 上游增强子区域的 H3K27ac 与 E4BP4 结合及染色质环结构。b,E4BP4 在 Nampt 上游 CREs 的结合(ChIP-qPCR)。c,d,Nampt 的 mRNA 与蛋白表达。e,f,不同基因敲除模型中 Nampt 表达变化。g,CM-RevDKO 与对照组心脏中 NAD+ 水平的昼夜变化。
心脏疾病与代谢紊乱的高度相关性凸显了理解心脏能量代谢在不断变化的外界刺激下如何维持的重要性。本研究揭示了昼夜节律性 REV-ERB 核受体在心脏代谢过程中作为关键转录调控因子的核心作用。长期缺失 REV-ERBs 会导致扩张型心肌病并缩短寿命。此前研究已表明,心肌细胞特异性缺失核心节律因子 Bmal1 和 Clock 亦可引起心脏病理改变¹³˒⁴³⁻⁴⁶。尽管 CBK 与 CM-RevDKO 模型在许多失调基因上存在重叠(扩展数据图 6e,f,g,h),但两者之间仍存在大量差异,提示不同节律因子失调在疾病发生中的作用具有复杂性。这也强调了通过比较不同节律通路敲除模型以深入理解导致心脏表型的转录调控网络的重要性。对不同心肌细胞特异性敲除模型之间表型差异的深入比较,将有助于阐明不同失调基因集对表型的具体贡献。
在 Rev-erbα/β 双敲除 后,多个心脏基因如电压门控/离子通道(例如 Kcne1 和 Slc41a3)发生去抑制。此外,诸如编码 DARPP-32 的 Ppp1r1b 等基因,可能同时与核心节律钟及代谢调控相关(图 2)。未来研究仍需进一步解析这些不同基因对整体表型的具体贡献。
此外,我们发现转录抑制因子 E4bp4 是 REV-ERBα 的直接靶基因,在 CM-RevDKO 心脏中持续处于去抑制状态。E4bp4 在整个昼夜周期内的持续表达使其在 ZT22 和 ZT10 均占据其结合位点,而非仅在 ZT22 占据。在 ZT22 时,DKO 心脏中 E4BP4 结合略有下降,这可能与竞争性转录因子失调有关。下调基因在心脏表型中的作用体现在多种关键代谢基因(如 Cpt1a、Ces1d 和 Gpam)表达下降(图 4c,扩展数据图 6d)。此外,本研究还揭示,在 CM-RevDKO 心脏中,NAMPT 的显著下调是通过 E4BP4 在 Nampt 转录起始位点上游 160–50 kb 的 3 个顺式调控元件上的持续结合和抑制实现的。与此同时,心脏 NAD+ 水平在整个昼夜周期内均降低。然而,尽管 NAMPT 的 mRNA 和蛋白水平均持续降低,我们仍观察到 NAD+ 水平存在一定的残余节律性。由于 CM-RevDKO 小鼠仍保持节律性活动和摄食模式,因此系统性节律信号(如食物摄入)、其他 NAD+ 生物合成途径(de novo/犬尿氨酸途径或 Preiss–Handler 途径)或残余 NAMPT 蛋白均可能参与维持这种残余节律。这些结果表明,心脏 NAD+ 水平下降以及代谢基因表达受损共同促进了年龄相关的扩张型心肌病发生及过早死亡(图 6)。
我们发现,CM-RevDKO 心脏中下调的相当一部分基因在 CBK 心脏中同样下调。由于这些基因富集 E4BP4 结合位点,这提示 E4BP4 在 CBK 心脏中也可能参与基因抑制。我们进一步发现,在 CBK 心脏中 Nampt 下调可通过额外敲除 E4bp4 得到恢复。由此可见,E4BP4 是昼夜节律性 Nampt 调控的关键介导因子,并提示 REV-ERB–E4BP4 抑制轴在 Nampt 的昼夜节律性转录调控中比既往描述的 BMAL1:CLOCK 激活轴⁷˒⁸ 更具主导作用。在肝细胞特异性 Rev-erb 敲除模型中²²,同样观察到 Nampt 下调和 E4bp4 去抑制。鉴于 Nampt 在 Clock 和 Bmal1 敲除肝脏中也呈下调⁷˒⁸˒⁴²,并与上游 CREs 存在相互作用⁴⁷,这提示 E4BP4 介导的 Nampt 抑制并非心脏特异性机制,而可能在更广泛的组织中参与节律性 Nampt 表达的调控。
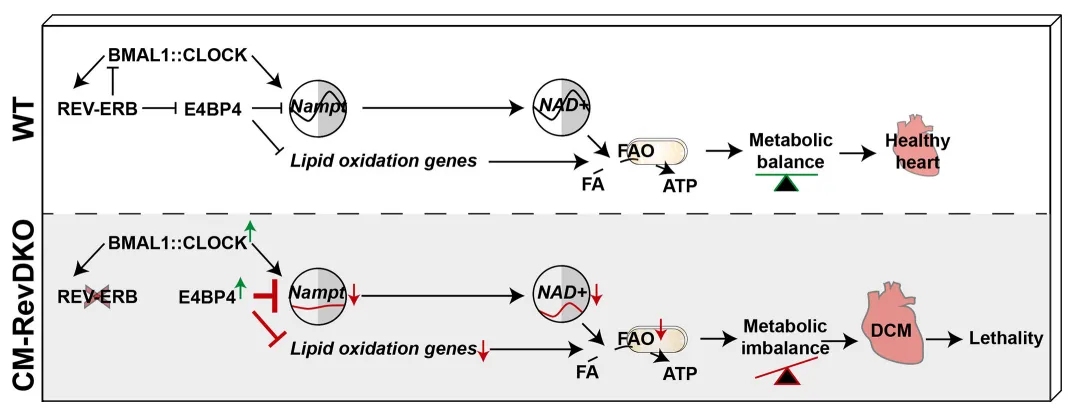
Fig. 6 REV-ERB–E4BP4–NAMPT 轴调控心脏代谢的机制示意图
示意 REV-ERBs 通过抑制 E4bp4 维持 Nampt 表达和 NAD+ 生物合成,从而支持心脏代谢稳态;当 REV-ERBs 缺失时,E4BP4 持续高表达,抑制 Nampt,降低 NAD+ 水平,最终导致代谢紊乱和扩张型心肌病。
在人类病变心脏中已观察到 E4BP4 过表达以及 NAMPT 和 NAD+ 水平下降³⁶˒⁴¹˒⁴⁸,这些现象进一步强调了阐明多种节律因子与心脏代谢之间联系的重要性,从而为后续研究下游效应分子提供依据。这对于明确哪些(靶)基因在心脏病理中起主要作用至关重要。鉴于增强 NAD+ 代谢在对抗心血管疾病及衰老相关疾病中的潜在价值,靶向 REV-ERB–E4BP4–NAMPT 轴可能为未来治疗提供新的思路。