
本文作者:Dr. Sonia Quintas, MD, MSc, Theresa Veira, MSN, MBA, Pora Kuperman, MPH, PhD。
偏头痛是一种高患病率的神经系统疾病,全球患病人数逾11亿,位列第二大致残原因。偏头痛绝非单纯的疼痛综合征,而是一种复杂的神经系统疾病,其病理过程涉及神经生理状态的改变及脑网络的进行性演变。偏头痛的慢性化(即由发作性偏头痛转为慢性偏头痛,年转化率约3%1)与中枢及外周神经系统的进行性持续敏化、兴奋性改变及适应性不良的神经可塑性相关。该过程进一步揭示了偏头痛的发病机制涉及三叉神经血管系统功能障碍、感觉处理增强及皮层抑制功能异常。
偏头痛疼痛的独特性在于其按明确阶段演进(前驱期—先兆期—头痛期—头痛后期),这充分表明偏头痛并非单一的疼痛事件,而是一个多阶段的神经病理过程。
深入理解病程分期及诱发因素的作用,是阐明偏头痛疼痛有别于其他类型疼痛的关键:偏头痛并非单纯对外界刺激或组织损伤的被动反应,而是大脑短暂进入易损状态所致的结果。
偏头痛的另一核心特征是与诱发因素密切相关,且诱因存在显著的个体内及个体间差异,甚至在同一患者的不同时期亦会动态变化。诱发因素并非以简单的方式直接导致偏头痛发作,而是与已处于高敏状态的大脑产生交互作用。偏头痛常伴发抑郁、焦虑、药物过度使用及睡眠障碍等共病,这些因素可调节疾病进展,并影响患者对干预措施的治疗应答。这种固有的异质性会干扰临床试验的疗效与安全性评价,提示研究设计需纳入精细的表型分析与纵向随访,以充分评估共病对偏头痛疾病转归的潜在影响。
主动式安慰剂效应管理
研究表明,随着时间推移,偏头痛预防性临床试验中的安慰剂反应率显著升高2,而药物效应保持稳定,导致整体治疗效果下降。此外,跨疾病领域观察发现,新型药物或疗法的安慰剂反应率通常更高3。基于此,2021年一项关于偏头痛预防性药物治疗的系统综述4指出,42%的试验未能使主要终点达到统计学显著性。进一步分析表明,上述差异主要源于试验成功率的显著分化:安慰剂反应率低于20%的研究与安慰剂反应率超过30%的研究之间,试验成功率相差达60%(见表1)。
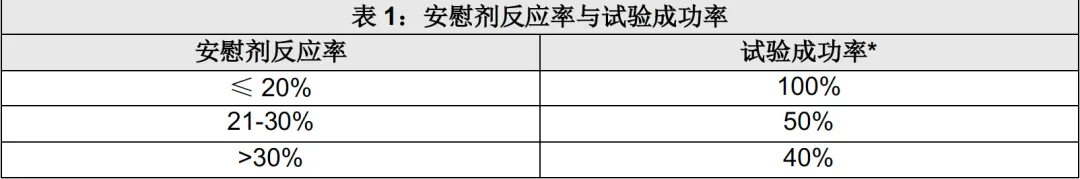
* 成功指主要终点充分达到统计学显著性水平
注:本表改编自Vollert等4,展示安慰剂反应率与达到主要终点成功率之间的关系。
研究表明,随着时间推需指出的是,由于患者报告结局(Patient-ReportedOutcomes,PRO)具有主观性,尤其在偏头痛等疼痛性疾病中,安慰剂反应较难完全规避。因此,深入探究任何可能减弱(或控制)安慰剂效应的潜在因素至关重要。其中一个潜在因素是患者辨识与报告自身症状及疼痛的能力5。具体而言,若患者未能掌握疼痛与症状的正确报告方法,其安慰剂反应率往往更高,且药物与安慰剂组间的疗效差异会被进一步缩小6。若该现象源于期望偏倚7(即对治疗获益的预期激活了大脑奖赏机制),一种建议的应对策略是通过“安慰剂反应降低培训”8来适度管理患者预期,或采用“安慰剂对照提醒话术”9,以提示患者识别可能诱发安慰剂反应的相关因素。此外,给药途径或临床环境等其他因素也可能促成“情境效应”10。针对上述效应,研究者可借此契机调控安慰剂效应的影响,重点关注患者预期,以及其与医务人员、研究场景及文化背景之间的交互作用移。
安慰剂对照提醒话术中的核心内容将首先载入知情同意书,于知情同意阶段向受试者说明。此后,在每次随访或医患互动中均沿用相同表述,以确保受试者与临床研究团队之间始终保持一致、中立的沟通基调。该话术的核心要素涵盖:保持中立语气、阐明安慰剂分配可能性、重申盲态原则、鼓励客观准确报告,以及最大限度降低报告偏倚。
通过对所有研究中心实施标准化培训,Medpace致力于削弱可能不成比例地诱发高安慰剂反应的中心特异性因素。然而,若高安慰剂反应的根本原因在于受试者报告失准,则可采用专项方法11对受试者进行培训,以提升其疼痛评估的准确性。另一项降低安慰剂反应的措施是设置安慰剂导入期,尽管该策略的临床有效性目前仍存在争议12。同时,亦有建议在安慰剂导入期基础上联合设置疼痛评分导入期,旨在评估受试者规范填写疼痛日记的依从性,并观察其日间疼痛波动特征。
此外,实施持续性数据动态监查,主动筛查临床数据中因疼痛评分前后矛盾等离群值所引发的质量问题,亦是进一步控制安慰剂反应的补充策略。在Medpace,我们的团队具备丰富的关键数据统计学分析经验,可有效识别呈现非典型数据特征的受试者与研究中心。这依托于我们的ClinTrak®系统,该系统可跨多个内外数据源整合海量数据,并通过集中监查模式,支持研究团队对实时数据进行可视化呈现、深度解读与交互分析,从而精准识别趋势、离群值及其他关键关注点,为快速实施风险干预及制定前瞻性试验策略提供数据支撑。
面向偏头痛人群的合规化临床实施
与成人偏头痛类似,该病亦是儿童及青少年各年龄段致残的首要原因之一,其患病率随年龄增长而攀升,从幼儿期的3%升至青春期的8%~23%13,14。然而,儿童偏头痛的临床表型与成人存在显著差异,且这种差异绝非仅限于学术探讨范畴,而是直接关乎疾病诊断、治疗应答以及临床试验的受试者筛选与入组。从诊断角度来看,儿童偏头痛发作通常持续时间较短,疼痛部位多为双侧,常伴显著的胃肠道症状,且晕动症15与眩晕的发生率更高。 低龄患者往往难以准确描述疼痛性质或伴随症状,在此背景下,儿童头痛绘画为解读这一独特的临床表达方式提供了极具价值的窗口16。
在药物干预方面,现有治疗方案多基于成人研究数据外推。然而,在成人中证实有效且经剂量调整后用于儿童的药物,其临床疗效未必理想。鉴于儿童在脑发育成熟度、受体表达、药代动力学特征及中枢疼痛处理机制等方面存在差异,成人患者中观察到的疗效与耐受性数据不能直接外推至儿童17,18,19,20。此外,与成人患者相似,儿童及青少年偏头痛群体同样表现出强烈的安慰剂效应,安慰剂组患者的发作频率与疼痛强度均呈现显著下降21,22。为此,国际头痛协会(IHS)已发布专项指导原则,旨在为儿童及青少年偏头痛临床试验的设计与实施提供规范参考。核心建议包括:入组年龄范围需确保合理的年龄分层设计,且试验应设置不少于28天的基线观察期,随后进行至少12周的治疗期23。
从临床研发的角度来看,这些差异会带来关键影响:若直接套用基于成人偏头痛定义的入选标准,可能会无意中将确患偏头痛的儿童排除在试验之外;同时,成人导向的研究终点与患者报告结局(PRO)可能对儿科人群缺乏足够的灵敏度。引入契合儿童发育阶段的诊断工具(如视觉量表或叙事性评估方法),并将研究终点调整为贴合儿科临床特征的指标,将有助于提升试验的科学性与成功率。
全球医疗卫生体系正加速向以患者为中心的照护(Patient-CenteredCare,PCC)模式转型24,而纳入患者报告结局测量工具(Patient-ReportedOutcomeMeasures,PROM)被广泛视为推动这一转型的有效路径25,26,27。在针对儿科人群开展研究时,必须充分考量不同年龄段儿童对健康概念的理解差异及其词汇表达的年龄特征。现有证据表明,若PROM量表的设计能充分适配儿童的词汇水平、认知发育及阅读能力,8岁以上患儿即可提供可靠的数据报告28,29。总体而言,在儿科临床环境(含临床试验)的PCC实践中,家庭成员或照护者通常被视为患儿医疗照护的主要执行者。鉴于此,儿科患者自我报告结局与照护者代报结局之间的一致性证据往往较为薄弱30,31,32。例如,多项研究证实,家长普遍倾向于低估患儿因疼痛导致的功能障碍程度33,34。因此,只要条件允许,儿科偏头痛临床试验应尽可能同步纳入患儿自评与照护者代报的PROM,以期获取最全面的病情信息并提升数据报告的准确性。例如,可要求家长采用0~10疼痛程度数字评估量表(NumericalPainScale,NPS)评估患儿疼痛;而对于年仅4岁的儿童35 ,若提供专为儿科人群设计的修订版面部表情疼痛量表(Faces Pain Scale-Revised,FPS-R)36,则能获得更为可靠的评估结果。此外,成人临床试验中常用的传统终点指标(如2小时疼痛完全缓解率)可能无法充分反映对儿童具有实际意义的临床获益,因为儿童的疾病负担往往更多表现为缺课、日常活动参与度下降或情绪困扰。
偏头痛临床研发的关键趋势
长期以来,偏头痛临床试验多依赖相对单一的终点指标,如每月偏头痛/头痛天数的减少或发作期疼痛强度的降低。尽管上述指标仍具参考价值,但偏头痛复杂的病理生理机制表明,它们仅能部分反映疾病的真实负担。现代医学已将偏头痛视为一种具有累积效应的疾病状态,其影响远超单次发作本身;因此,治疗目标应从单纯的发作期缓解,转向干预并改变疾病本身的自然病程37。鉴于此,临床研究终点正日益向更能体现“实质性整体疾病控制”的指标倾斜,而非仅关注孤立的症状改善。感觉症状评估、残疾评分及生活质量量表等工具,有助于全面捕捉偏头痛对患者日常起居、工作效能、睡眠质量及情绪健康的真实世界影响。
国际头痛协会(International Headache Society,IHS)近期发布的一份立场声明38提出,应提高偏头痛预防性治疗“成功”的判定标准,并将治疗结局划分为四个等级:
偏头痛完全缓解
理想控制
适度控制
控制不足
例如,既往通常将每月偏头痛天数减少≥50%作为判定受试者治疗有效的标准;但对于难治性偏头痛患者,每月发作天数减少≥30%即被认为具有临床显著意义。此类终点指标更便于非专科医师与监管机构解读,且与患者渴望恢复正常生活的核心诉求高度契合。
数字化疼痛追踪工具已成为推动这一转变的关键赋能技术。凭借其实时记录能力,该类工具可精准捕捉患者带病生活的日常真实状态,在有效降低回忆偏倚的同时,更准确地刻画偏头痛的波动特征。此类工具可全面记录头痛发作频次、持续时间、伴随症状、功能受损程度、用药情况及恢复模式,从而勾勒出更为详尽的疾病负担图谱
通过系统化采集高质量的患者报告数据,临床试验得以与现代偏头痛控制及预防理念深度接轨。研究者在摆脱对受试者记忆依赖的同时,可深入分析疗效反应的稳定性、发作间期残留症状,乃至疾病进展的早期预警信号等动态模式。借由上述机制,数字化工具有效弥合了前沿科学标准与可规模化临床执行之间的鸿沟,确保研究终点既具备坚实的科学严谨性,又切实反映患者的核心获益。
偏头痛神经科学的突破性进展重塑了该疾病的理论认知框架,尤其是确立了“反复发作可引发疼痛信号处理机制与大脑兴奋性发生持久性改变”这一核心观点。现代临床试验设计日益融入“偏头痛疾病活动呈连续谱分布”的病理生理学理念。该视角指导研究者在试验运营决策中,充分纳入基线疾病分期、疾病进展风险因素及发作间期症状等关键变量。
将上述认知融入试验方案设计,有助于优化受试者入选标准、延长随访周期,并采用能动态反映疾病稳定性演变的时间依赖性结局指标。如今的研究设计已具备更充分的能力,以评估干预措施是否不仅能缓解临床症状,更能实质性地改变疾病的潜在进程。
结论:偏头痛药物研发的战略性CRO合作伙伴
随着偏头痛研究的不断深入,临床试验面临的挑战日益凸显:研究终点标准不断提高,试验设计也愈发复杂。应对偏头痛临床表型的高度变异性,已成为当前临床研究的核心难题之一。偏头痛患者群体呈现显著异质性,在疾病严重程度、共病情况、既往用药史及症状特征等方面差异巨大。若缺乏严谨的试验规划与精细化执行,此类变异性极易掩盖真实的治疗效应,导致研究结果难以准确解读。
凭借在偏头痛领域的深耕经验,专业CRO能够将疾病特异性试验设计与患者管理专长深度融合,助力实现受试者筛选标准的统一、数字化追踪工具的规范化应用,以及患者报告结局(PRO)的高质量采集。这一专业化运营能力,可确保不断演进的研究终点在各研究中心得以精准、一致地评估。通过有效降低数据噪声、提升整体数据质量,以Medpace为代表的专业CRO可显著增强疗效信号检测能力,从而更清晰地将真实的治疗获益从背景变异中剥离出来。
依托全程深度参与各项研究的资深内部神经科专家团队,助力攻克复杂疑难疾病。我们的神经科学医师在疼痛领域临床研发方面经验丰富,可为试验方案设计与规划提供战略指导,负责运营团队培训、与主要研究者高效协作、提供全程医学监查,并可根据申办方需求支持与监管机构的沟通会议。
全方位临床开发服务
Medpace是一家以科学为导向、提供全方位服务的全球临床合同研究组织(CRO),为生物技术、制药和医疗器械行业提供I-IV期临床开发服务。Medpace的使命是在全球范围内利用我们跨治疗领域的深厚医学经验,通过高度科学和规范的操作方法,安全有效地促进治疗药物开发。
参考文献
Torres-Ferrús M, Ursitti F, Alpuente A, Brunello F, Chiappino D, de Vries T, Di Marco S, Ferlisi S, Guerritore L, Gonzalez-Garcia N, Gonzalez-Martinez A, Khutorov D, Kritsilis M, Kyrou A, Makeeva T, Minguez-Olaondo A, Pilati L, Serrien A, Tsurkalenko O, Van den Abbeele D, van Hoogstraten WS, Lampl C; School of Advanced Studies of European Headache Federation (EHF-SAS). From transformation to chronification of migraine: pathophysiological and clinical aspects. J Headache Pain. 2020 Apr 29;21(1):42. doi: 10.1186/s10194-020-01111-8. PMID: 32349653; PMCID: PMC7189559.
The temporal trend of placebo response in migraine prevention from 1990 to 2021: a systematic literature review and meta‑analysis with regression. Tepper et al. 2023
Doherty M, Dieppe P (2009) The “placebo” response in osteoarthritis and its implications for clinical practice. Osteoarthritis Cartilage 17(10):1255–1262. https://doi.org/10.1016/j.joca.2009.03.023
Vollert J, Cook NR, Kaptchuk TJ, Sehra ST, Tobias DK, Hall KT (2020) Assessment of Placebo Response in Objective and Subjective Outcome Measures in Rheumatoid Arthritis Clinical Trials. JAMA Netw Open 3(9):e2013196. https://doi.org/10.1001/jamanetworkopen.2020.13196
Evans K, Romero H, Spierings EL, Katz N (2021) The relation between the placebo response, observed treatment effect, and failure to meet primary endpoint: A systematic review of clinical trials of preventative pharmacological migraine treatments. Cephalalgia 41(2):247–255.
Sanders AE, Slade GD, Fillingim RB, Ohrbach R, Arbes SJ Jr, Tchivileva IE (2020) Effect of Treatment Expectation on Placebo Response and Analgesic Efficacy: A Secondary Aim in a Randomized Clinical Trial. JAMA Netw Open 3(4):e202907–e202907. https://doi.org/10.1001/jaman etworkopen.2020.2907
Zimbroff D. Patient and rater education of expectations in clinical trials (PREECT). J Clin Psychopharmacol 2001; 21: 251–252.
Placebo response mitigation with a participant-focused psychoeducational procedure: a randomized, single-blind, all placebo study in major depressive and psychotic disorders Cohen et al 2021
Forbes RB, McCarron M, Cardwell CR (2020) Efficacy and Contextual (Placebo) Effects of CGRP Antibodies for Migraine: Systematic Review and Meta-analysis. Headache 60(8):1542–1557. https://doi.org/10.1111/ head.13907
Treister R, Lawal OD, Shecter JD, et al. Accurate pain reporting training diminishes the placebo response: Results from a randomised, double-blind, crossover trial. PLoS One 2018; 13: 1–12.
Abu-Arafeh I, Razak S, Sivaraman B, Graham C. Prevalence of headache and migraine in children and adolescents: a systematic review of population-based studies. Dev Med Child Neurol. 2010;52(12):1088-1097. doi:10.1111/j.1469-8749.2010.03793.xPubMedGoogle ScholarCrossref
Stewart WF, Lipton RB, Celentano DD, Reed ML. Prevalence of migraine headache in the United States: relation to age, income, race, and other sociodemographic factors. JAMA. 1992;267(1):64-69. doi:10.1001/jama.1992.03480010072027
Kroon Van Diest AM, Ernst MM, Slater S, Powers SW. Similarities and Differences Between Migraine in Children and Adults: Presentation, Disability, and Response to Treatment. Curr Pain Headache Rep. 2017 Oct 25;21(12):48. doi: 10.1007/s11916-017-0648-2. PMID: 29071512; PMCID: PMC5885754.
Ferro F, Gaspari C, Manfrè G, Cernigliaro F, D'Agnano D, Panzica R, Correnti E, Ruta MR, Marchese F, Pitino R, Capizzi M, Santangelo G, Versace A, Sciruicchio V, Raieli V. Children's Headache Through Drawings: A Narrative Review and a Portrait Gallery. Life (Basel). 2025 Jun 23;15(7):996. doi: 10.3390/life15070996. PMID: 40724499; PMCID: PMC12298764.
El-Chammas K, Keyes J, Thompson N, Vijayakumar J, Becher D, Jackson JL. Pharmacologic treatment of pediatric headaches: a meta-analysis. JAMA Pediatr. 2013;167(3):250-258. doi:10.1001/jamapediatrics.2013.508ArticlePubMedGoogle ScholarCrossref
Le K, Yu D, Wang J, Ali AI, Guo Y. Is topiramate effective for migraine prevention in patients less than 18 years of age? a meta-analysis of randomized controlled trials. J Headache Pain. 2017;18(1):69. doi:10.1186/s10194-017-0776-4PubMedGoogle ScholarCrossref
Shamliyan TA, Kane RL, Ramakrishnan R, et al. Migraine in children: preventive pharmacologic treatments. https://www.ncbi.nlm.nih.gov/books/N
Powers, S.W.; Coffey, C.S.; Chamberlin, L.A.; Ecklund, D.J.; Klingner, E.A.; Yankey, J.W.; Korbee, L.L.; Porter, L.L.; Hershey, A.D. Trial of Amitriptyline, Topiramate, and Placebo for Pediatric Migraine. N. Engl. J. Med. 2017, 376, 115–124. [Google Scholar] [CrossRef] [Green Version]
Faria, V.; Linnman, C.; Lebel, A.; Borsook, D. Harnessing the placebo effect in pediatric migraine clinic. J. Pediatr. 2014, 165, 659–665. [Google Scholar] [CrossRef] [PubMed] [Green Version]
Lewis, D.W.; Winner, P.; Wasiewski, W. The placebo responder rate in children and adolescents. Headache 2005, 45, 232–239. [olume=45&pages=232%E2%80%93239&doi=10.1111/j.1526-4610.2005.05050.x"Google Scholar] [CrossRef]
Pablos-Mendez A, Barr RG and Shea S. Run-in periods in randomized trials: Implications for the application of results in clinical practice. JAMA 1998; 279: 222–225
Abu-Arafeh, I.; Hershey, A.D.; Diener, H.C.; Tassorelli, C. Guidelines of the International Headache Society for controlled trials of preventive treatment of migraine in children and adolescents, 1st edition. Cephalalgia 2019, 39, 803–816
Santana MJ, Manalili K, Jolley RJ, Zelinsky S, Quan H, Lu M. How to practice person-centred care: a conceptual framework. Health Expect. (2018) 21:429–40. doi: 10.1111/hex.12640
Olde Rikkert MGM, van der Wees PJ, Schoon Y, Westert GP. Using patient reported outcomes measures to promote integrated care. Int J Integr Care. (2018) 18:8. doi: 10.5334/ijic.3961
Ovretveit J, Zubkoff L, Nelson EC, Frampton S, Knudsen JL, Zimlichman E. Using patient-reported outcome measurement to improve patient care. Int J Qual Health Care. (2017) 29:874–9. doi: 10.1093/intqhc/mzx108
Black N. Patient reported outcome measures could help transform healthcare. BMJ. (2013) 346:f167. doi: 10.1136/bmj.f167
Riley AW. Evidence that school-age children can self-report on their health. Ambul Pediatr. (2004) 4(4 Suppl):371–6. doi: 10.1367/A03-178R.1
Haverman L, Limperg PF, Young NL, Grootenhuis MA, Klaassen RJ. Paediatric health-related quality of life: what is it and why should we measure it? Arch Dis Child. (2017) 102:393–400. doi: 10.1136/archdischild-2015-310068
Brunner HI, Klein-Gitelman MS, Miller MJ, Trombley M, Baldwin N, Kress A, et al. Health of children with chronic arthritis: relationship of different measures and the quality of parent proxy reporting. Arthritis Rheum. (2004) 51:763–73. doi: 10.1002/art.20689
Zhou H, Roberts P, Horgan L. Association between self-report pain ratings of child and parent, child and nurse and parent and nurse dyads: meta-analysis. J Adv Nurs. (2008) 63:334–42. doi: 10.1111/j.1365-2648.2008.04694.x
Bevans KB, Riley AW, Moon J, Forrest CB. Conceptual and methodological advances in child-reported outcomes measurement. Expert Rev Pharmacoecon Outcomes Res. (2010) 10:385–96. doi: 10.1586/erp.10.52
Coons SJ, Gwaltney CJ, Hays RD, Lundy JJ, Sloan JA, Revicki DA, et al. Recommendations on evidence needed to support measurement equivalence between electronic and paper-based patient-reported outcome (PRO) measures: ISPOR ePRO Good Research Practices Task Force report. Value Health. (2009) 12:419–29. doi: 10.1111/j.1524-4733.2008.00470.x
Chambers CT, Reid GJ, Craig KD, McGrath PJ, Finley GA (1998) Agreement between child and parent reports of pain. Clin J Pain 14(4):336–342 20.
Vetter TR, Bridgewater CL, Ascherman LI, Madan-Swain A, McGwin GL (2014) Patient versus parental perceptions about pain and disability in children and adolescents with a variety of chronic pain conditions. Pain Res Manage 19(1):7–14
Tomlinson D, von Baeyer CL, Stinson JN, Sung L (2010) A systematic review of faces scales for the self-report of pain intensity in children. Pediatrics e1168–98
Hicks CL, von Baeyer CL, Spafford PA, van Korlaar I, Goodenough B (2001) The faces Pain Scale–Revised: toward a common metric in pediatric pain measurement. Pain 93(2):173–183
Pozo-Rosich P, Caronna E, Sacco S, Peres MFP, Ashina S, Özge A, Ahmed F, Velez-Jimenez MK, Jenkins B, Wang SJ, Schwedt TJ, Sakai F, Levin M, Burstein R, Terwindt GM, Tassorelli C. Early treatment in migraine - A call to shift prevention from attacks to disease progression: A position statement from the International Headache Society. Cephalalgia. 2025 Oct;45(10):3331024251387721. doi: 10.1177/03331024251387721. Epub 2025 Oct 24. PMID: 41134822.
Sacco S, Ashina M, Diener HC, Haghdoost F, Lee MJ, Monteith TS, Jenkins B, Peres MFP, Pozo-Rosich P, Ornello R, Puledda F, Sakai F, Schwedt TJ, Terwindt G, Vaghi G, Wang SJ, Ahmed F, Tassorelli C. Setting higher standards for migraine prevention: A position statement of the International Headache Society. Cephalalgia. 2025 Feb;45(2):3331024251320608.doi:10.1177/03331024251320608. PMID: 39980456.
关于Medpace
作为一家业务足迹遍布44个国家/地区、拥有6,200名员工的全球性合同研究组织(CRO),Medpace对于在全球范围内设计和开展I-IV期临床试验拥有丰富的经验。我们的医疗、监管和运营专家掌握了丰富的资源,无论您身处哪个国家/地区,我们都能帮助您推进研发进程。自2004年Medpace在亚太地区开展业务以来,我们能够利用全球化的资源和因地制宜的经验,将当地的语言、文化和法规要求融入到对药物开发项目的设计和实施中。Medpace的使命是在全球范围内利用我们跨治疗领域的深厚医学经验,通过高度科学和规范的操作方法,安全有效地促进治疗药物开发。



