在药品批发企业的日常质量管理中,委托第三方机构对冷库、冷藏车、保温箱等冷链设备进行验证,已是一项常见且必要的质量活动。这类委托验证不仅能够有效弥补企业质量管理人员在验证专业能力上的短板,更有助于提升整体质量保障水平。然而,随着监管要求的持续趋严,冷链验证早已不再是"有报告即可"的形式流程。验证报告作为该项工作的最终交付成果,其质量直接关乎验证活动的真实性与有效性,亦成为飞行检查与内部审核中重点核查的对象。
但在实际操作中,不少质量管理人员面对一份内容繁复、数据庞杂的第三方验证报告,往往感到无从着手,难以精准识别报告中可能存在的缺项、漏项,甚至数据失真等深层问题。一旦审核流于表面,验证便丧失了其质量保障的根本意义,反而可能为企业埋下重大的合规风险隐患。
那么,质量负责人如何才能系统、精准地审阅一份第三方验证报告,使其真正成为企业合规运营的"护身符"?本文基于一线质量管理的实操经验,梳理出一套全流程、无盲区的审核指南,旨在助力各位同仁严把报告质量关,牢牢守住冷链管理的合规底线。
基础信息是验证报告的"身份标识",是确保报告真实有效的前提。一些机构直接用其他企业的报告直接进行修改,会存在基本信息与实际不符的情形,所以需对基本信息进行认真审核,一旦出现不符,报告即判定为不合格,需退回重做,从源头上阻断风险。
- 核对主体信息一致性:
报告中的企业名称、仓库地址,冷库位置、冷藏车的信息等必须与实际完全一致。 - 核对验证范围匹配性:
报告中所列的验证时间、范围、类型(如使用前验证、定期再验证),需与验证方案及实际作业情况严格对应。 - 核对设备信息完整性:
设备的名称、型号、编号、容积、冷藏车车牌号、冷库安装位置及库区布局图等信息,必须与现场实物、设备台账及档案记录逐一吻合。 - 核对过程资料齐全性:
验证、审核、批准人员的签字必须齐全。 验证相关的培训记录、签到表应完整归档。 现场布点、设备全景、作业过程等照片资料应清晰可辨,反映真实情况。 验证过程的原始记录如开门验证时间及数据记录等必须齐全,与采集到的数据相符。
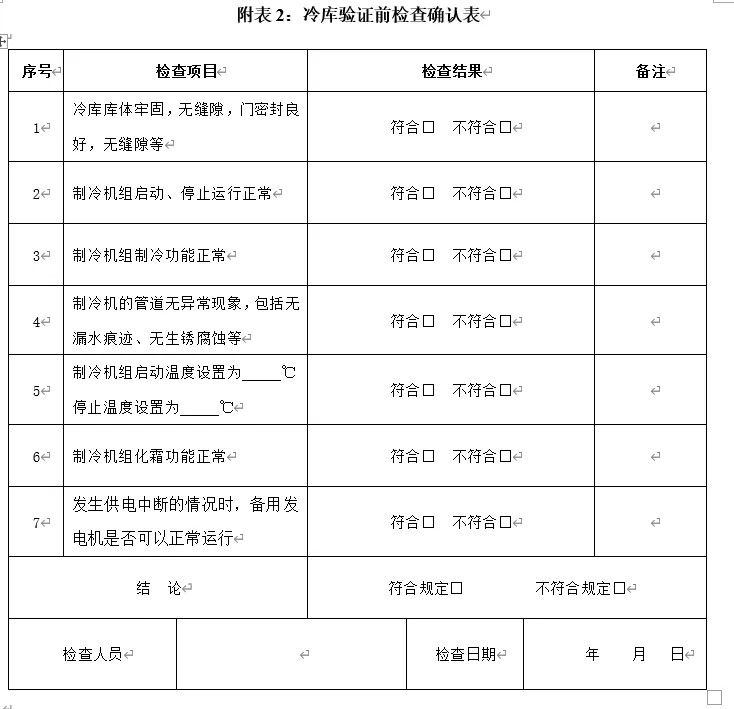
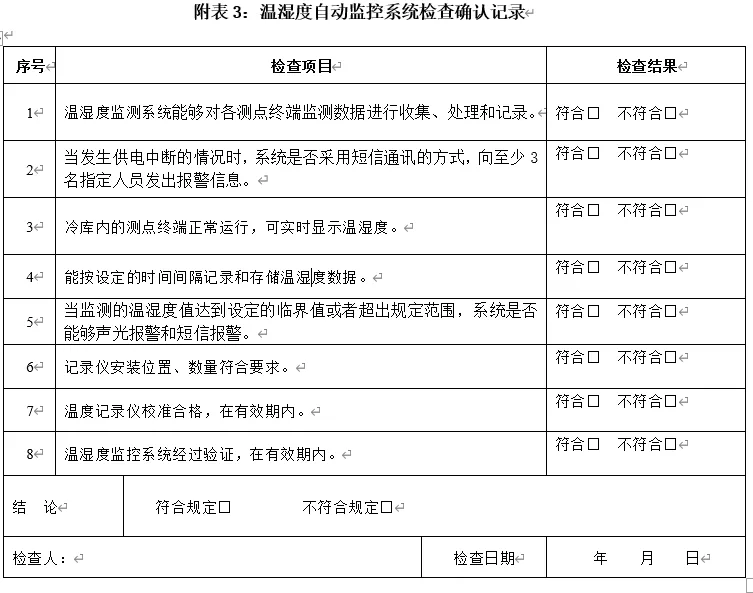
(验证过程的原始记录表格)
在确认基础信息无误后,应聚焦于验证项目本身的合规性。依据《药品经营质量管理规范》附录5《验证管理》的规定,验证项目必须全面覆盖,不得有任何删减。
- 必验项目全覆盖:
核对报告是否完整包含了以下核心内容:
温度分布特性验证 温控设备运行参数及性能验证 温度监测系统测点终端准确性验证 开门作业对温度分布影响验证 断电状况下保温时限验证 极端外部环境条件下的保温效果验证 问题列举:

- 验证工况区分清晰:
空载验证与满载验证应根据方案分别实施,其数据和结论应分别记录、分别分析,不得混淆替代。 - 数据采集过程符合方案:
数据采集的时间与频次需满足GSP要求,与方案设定一致。 布点的数量、位置(高度、平面分布)须严格按图施工,尤其应覆盖门口、角落、出风口等关键风险点位。
数据分析是验证报告的核心,也是识别数据是否真实、可靠的关键。此环节需对各项数据进行独立、严谨的审视。
- 逐项独立分析:
要求报告必须对验证项目进行独立的、而非合并的数据分析,每个项目都应有明确的图表和数据汇总表格。 - 数据资料形式规范:
温度分布曲线图、数据汇总表、布点位置示意图、关键作业过程记录图等资料应齐全、规范、清晰。 - 关键参数分析完整:
对于开门时长、开门方式、断电后的保温时长、极端环境下的温度变化趋势等关键参数,应有完整的记录与合理的分析。
问题列举:
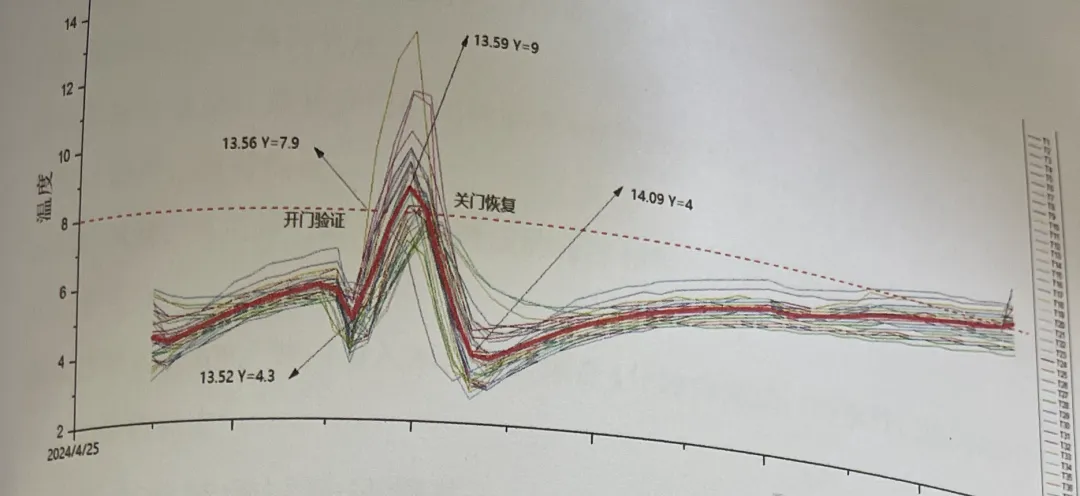
(开门验证操作不合理) - 数据逻辑自洽:
审阅原始数据与趋势图时,应关注数据波动是否平滑、有无异常跳变或篡改痕迹,判断其是否符合冷链设备运行的物理规律。
验证的最终目的是输出可操作的指导。结论必须明确有力,偏差处理必须形成闭环。
- 结论规范且有据可依:
验证结论不应模糊不清,所有定性判断都需有相应的数据作为支撑。结论应能直接转化为设备操作规范、日常监控标准或风险防控措施。 - 验证结论具有可操作性:
如冷库开门时长、保温箱蓄冷剂的释冷时长等,有具体的量化指标,有可操作性。 - 偏差处理实现闭环管理:
验证过程中出现的任何温度超标、布点不合理等偏差,均应被完整记录。 偏差报告需包含:问题描述、原因分析、风险评估、采取的纠正措施、措施有效性复核及预防性改进建议。 确认所有偏差均已处理完毕,无未关闭的风险项。 问题列举: 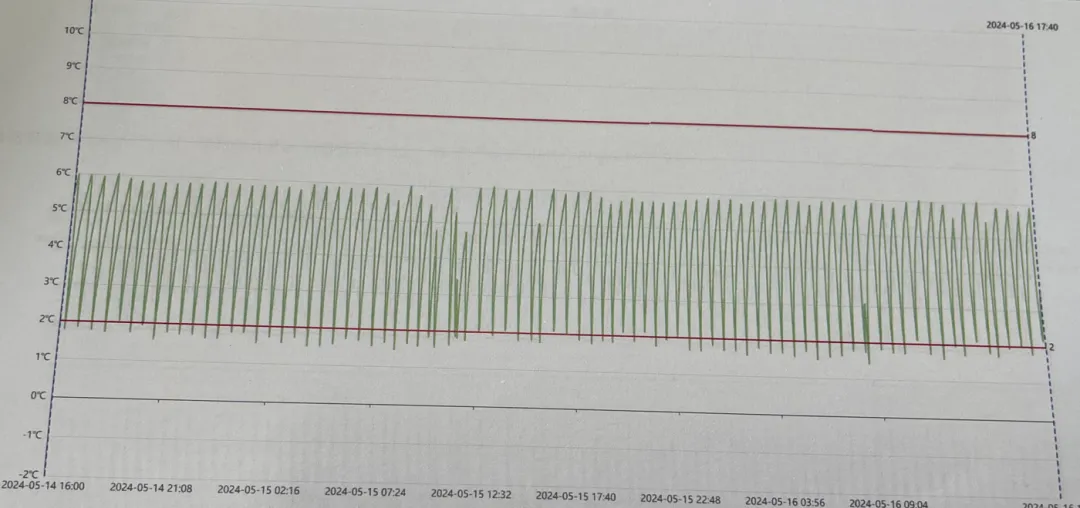
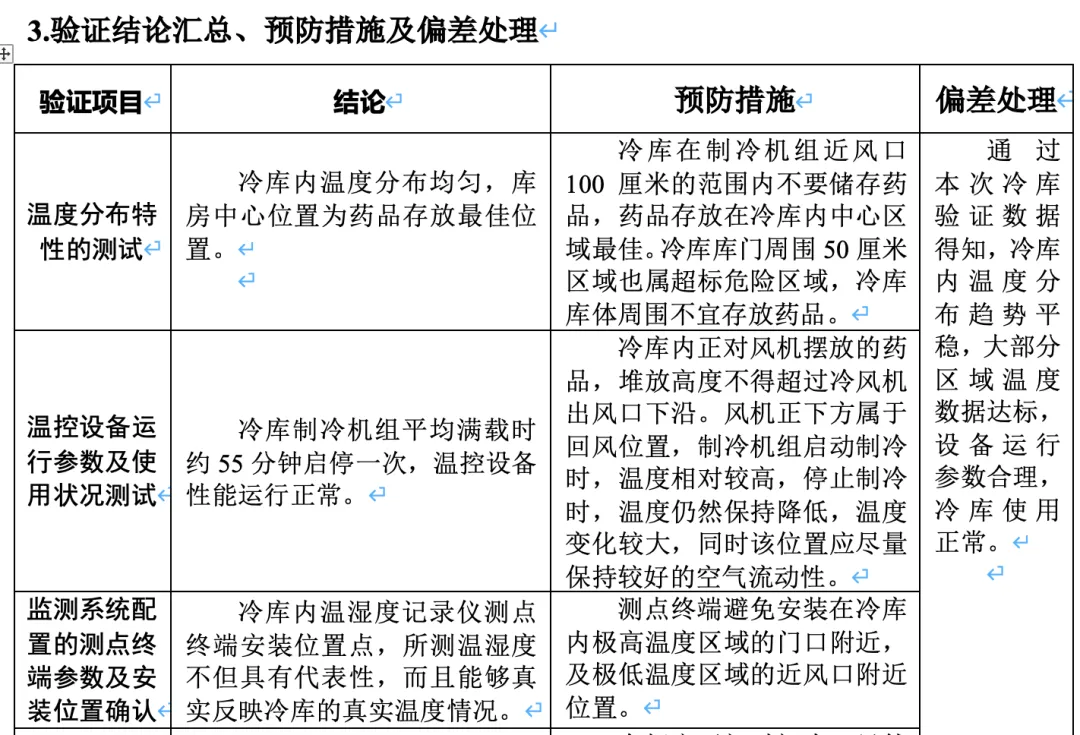
(验证数据发生低温,未做偏差分析和处理)
验证数据的可信度,建立在测量设备本身准确的基础上。此项审核是确保数据可追溯性的底线。
校准证书应由具备资质的法定计量检定机构出具。 确认校准证书在有效期内。 校准点位应完全覆盖验证过程中所使用的全部温度记录仪及布点位置。 校准证书编号、记录仪机身编号、验证报告中所列设备编号必须一一对应,杜绝套用、错用。 问题列举: 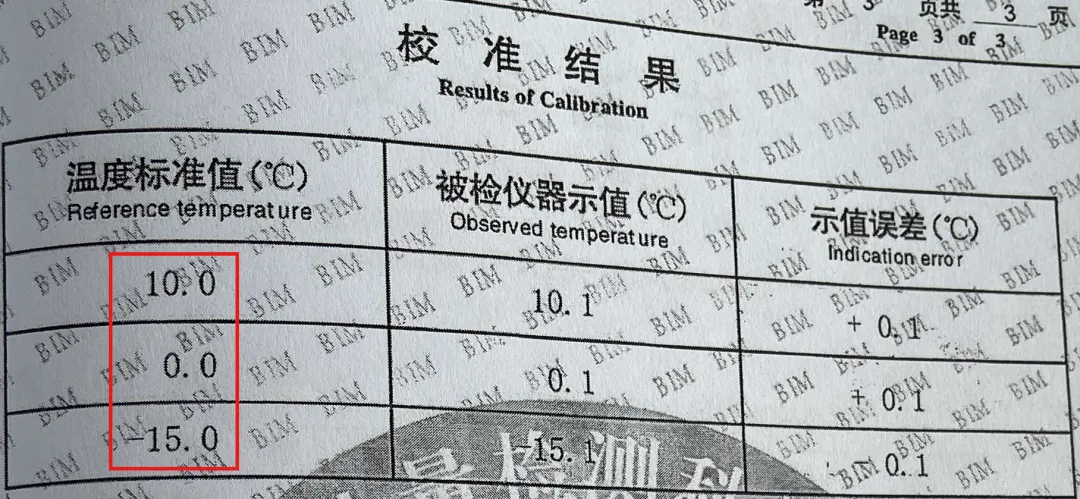
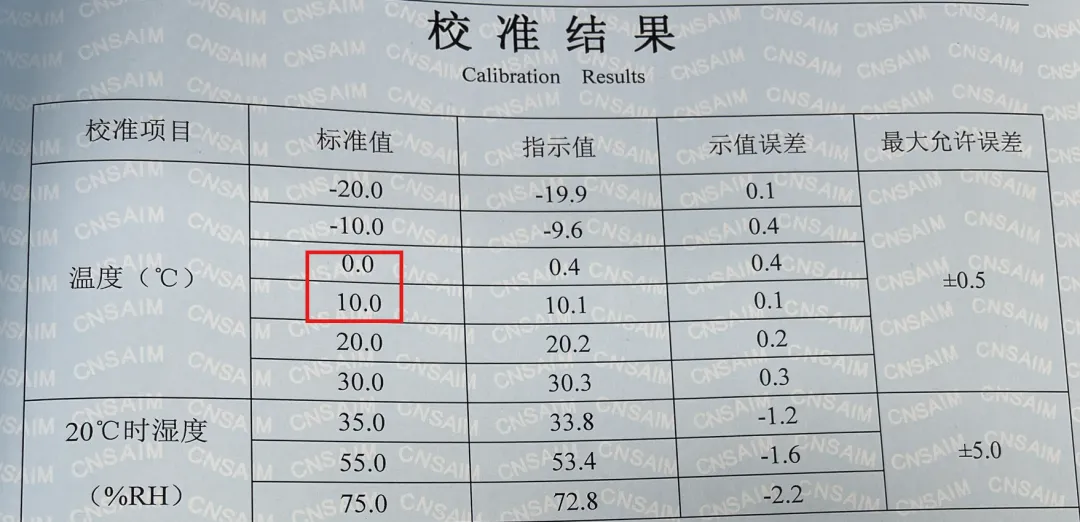
(温度标准值未包含2-8℃)
完成对报告文本的审核并非终点。验证结果必须融入企业的日常质量管理体系,方能实现其最大价值。
- 文件体系同步修订:
检查是否已依据验证结论,对相关的操作规程(SOP)、设备维护保养规程、质量管理制度等文件进行了修订,并保留修订记录。 - 专项培训执行到位:
确认是否针对验证结果和新的操作要求,对仓储、运输、养护、质管等岗位人员开展了专项培训,培训档案(课件、签到、考核)应完整。 - 验证档案闭环管理:
确保验证方案、报告、原始数据、校准证书、偏差处理记录、培训记录、文件修订记录等全套资料已统一归档,便于随时备查,形成完整的管理闭环。
第三方冷链设备验证报告的审核,是一项严谨、细致、专业性极强的工作,直接关系到企业的合规经营与药品质量安全。作为质量管理人员,我们应秉持"不删减要点、不简化流程、不遗漏内容"的原则,从基础信息到结果应用,逐项审核、严格把关。
只有将验证工作的成果真正内化为企业的质量管控能力,才能让每一次验证都物有所值,为企业冷链药品的质量安全筑起一道坚不可摧的防火墙。
你在审核验证报告中遇到哪些问题?留言区讨论吧!
感谢您关注质量思维,质量思维是一个分享质量管理心得、体会,分享优秀管理经验和管理工具的平台,旨在打造一个质量管理人员共同学习的平台、畅所欲言的平台。
欢迎您加入质量思维,并向我们投稿,稿件内容形式不限,转载须注明出处!投稿邮箱:maxfei2006@outlook.com
欢迎来到质量思维




