一、背景:偏差管理现实困境
偏差(Deviation)是指偏离已批准的程序、规定标准或工艺参数的任何情况,涵盖生产、检验、储存、运输等各环节。《药品生产质量管理规范》(GMP)明确要求企业必须建立完善的偏差管理体系,对偏差进行及时识别、记录、调查、评估和纠正。
然而,现实中许多药品生产企业的偏差数量异常偏低,大量真实偏差未被有效收集和上报。WHO 对我国企业的现场检查中,"偏差处理与 CAPA"是所有缺陷类别中出现频次最高的问题。偏差收集不足,不是生产做得好,而是管理体系存在系统性缺陷的信号。
二、无法收集偏差的六大根本原因
原因一:【认知层面】对"偏差"的定义和边界认识模糊
偏差识别的前提是员工清楚"什么是偏差",但实践中普遍存在以下问题:
根本分析:企业的偏差管理 SOP 对偏差的定义往往过于原则性,未给出清晰的判断标准和典型示例,导致一线人员无法准确识别。
原因二:【文化层面】惩罚性质量文化导致偏差被隐瞒
这是实践中最隐蔽却最普遍的原因。
"我国大部分药品生产企业不愿意暴露企业在质量管理方面存在的欠缺即偏差,对生产中出现的偏差并不准确记录在案,反而故意隐瞒。"——《药品生产偏差的现状及解决对策》
惩罚性文化的具体表现:
管理层将偏差数量多少视为绩效评价指标,偏差越少"越好" 发现偏差的员工被批评甚至受到处分,而非被鼓励 班组、车间之间相互竞争"零偏差",形成隐瞒的集体行为 员工担心上报偏差会"连累整批产品被召回"或"影响出货" 管理层追求"零偏差"KPI,向基层员工施压,导致系统性瞒报
后果:偏差管理从质量改进工具沦为合规应付工具,"应付检查"而非真正管理。
原因三:【制度层面】偏差报告流程设计存在缺陷
即便员工有意上报,制度缺陷也可能让偏差在流程中"消失":
1、报告流程繁琐,缺乏便捷性
纸质表单填写复杂,流转环节多,员工倾向于放弃上报 没有快速预报机制,紧急情况下缺乏即时上报手段 跨部门传递程序不清晰,偏差记录在部门间传递过程中丢失
2、职责分工不明确
未明确"谁有权利/义务发起偏差报告" 生产人员认为偏差上报是 QA 的职责,QA 等待生产人员主动报告,互相推诿 偏差发现与记录的时限要求(如24小时内)未在 SOP 中明确规定或执行不严
3、偏差分级标准不合理
分级定义模糊,员工担心"小事"被评为"重大偏差"而选择不报 分级标准缺乏风险导向,不能正确引导识别行为 部分企业将分级权力过度集中,现场人员无权启动偏差调查
原因四:【人员层面】培训不足与人员能力缺失
偏差收集的核心是"识别能力",而识别能力来源于有效培训。
培训现状问题:
特别值得注意的是:当一个偏差是在记录复核时才被发现(而非现场即时识别),说明一线人员的偏差识别能力存在严重不足,需要重新评估培训有效性。
原因五:【技术层面】文件体系和信息化支撑不足
偏差的有效收集离不开健全的文件基础设施:
文件体系缺失导致的问题:
SOP 中未涵盖所有需要上报的异常类型(如停电、设备高级别报警、物料短缺应急处置等) 批生产记录设计不合理,未内置偏差识别触发点 文件版本控制混乱,员工不知道当前标准是什么,无法判断"偏离了什么"
信息化管理缺失带来的问题:
纸质偏差记录容易丢失、难以追溯、统计分析困难 没有电子质量管理系统(eQMS),偏差无法在各部门间实时共享 无法自动触发偏差流程(如在线监控数据超限应自动生成偏差报告) 偏差趋势分析缺失,无法通过数据驱动发现系统性偏差
原因六:【管理层面】质量部门监督力度不足与体系割裂
现场监督缺位:
QA 现场检查频率不足,无法及时发现生产中的隐性偏差 QA 人员数量不够,对所有生产区域覆盖不全 生产压力大时,QA 放松监管,实质上默许了偏差的"自我消化"
质量体系割裂:
偏差管理与变更控制、CAPA、产品质量回顾(APR)未形成联动机制 实验室异常(OOS)与生产偏差管理两条线互不衔接,造成信息孤岛 跨部门协作不畅,生产、质量、设备、物料部门各自为政,偏差信息无法汇聚
绩效导向扭曲:
部分企业将"偏差数量少"作为质量绩效优秀的标志,而非关注偏差调查的深度和 CAPA 的有效性 年度产品回顾中偏差分析流于形式,失去持续改进的驱动力
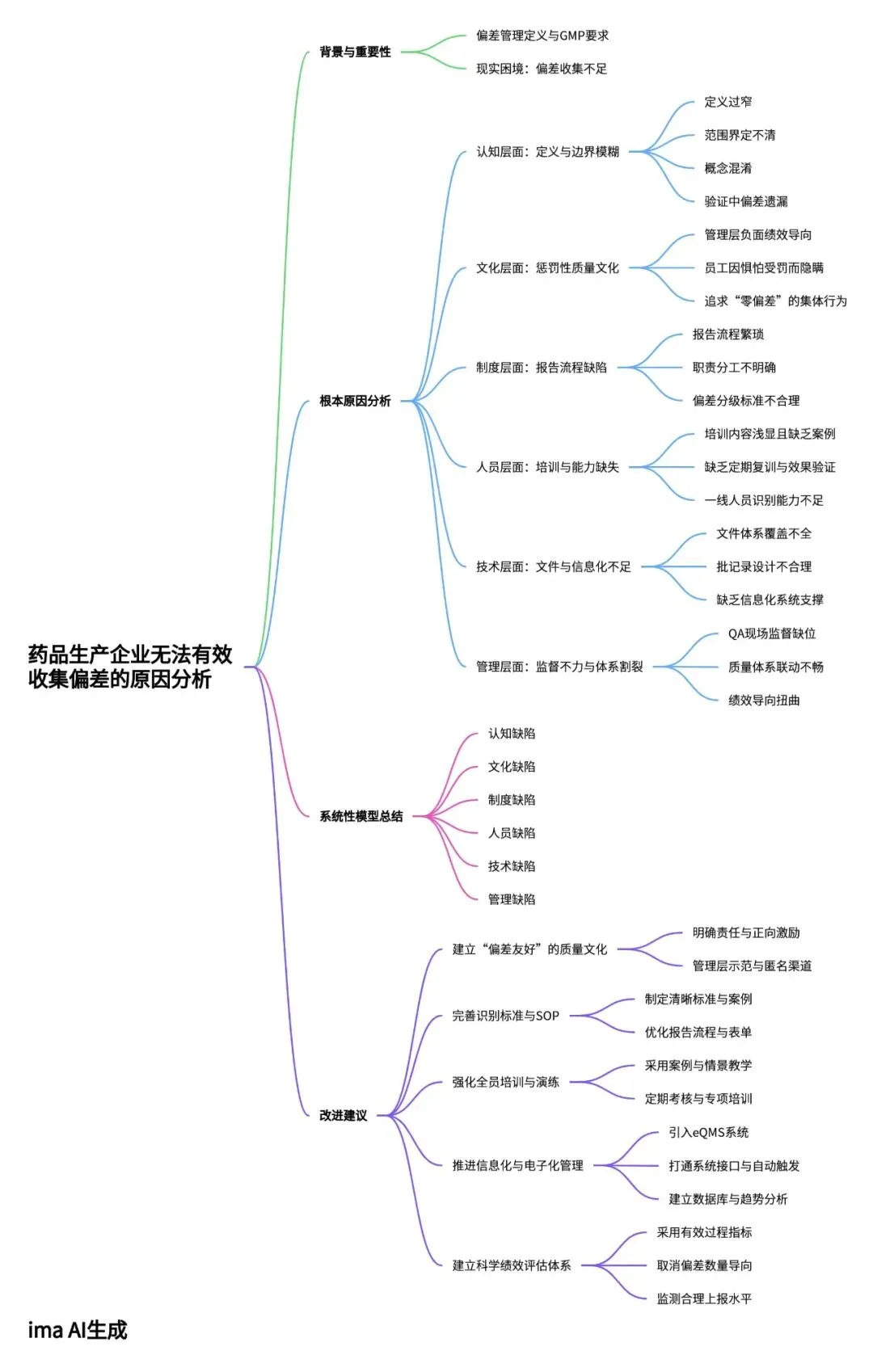
四、改进建议
1. 建立"偏差友好"的质量文化
2. 完善偏差识别标准和 SOP
3. 强化全员培训与实战演练
4. 推进信息化和电子化管理
5. 建立科学的绩效评估体系
《药品生产质量管理规范》(2010年修订版),中国卫生部令第79号 胡俊等,《WHO 对我国部分药品生产企业现场检查偏差管理相关缺陷分析》,《中国食品药品监管》2024年第1期 郑文科、张磊,《偏差流程要点分析和偏差处理成熟度的考量》,制药技术 2024年 东曜药业,《浅谈制药企业中的偏差处理》,搜狐健康 2024年 DDReg Pharma,《Deviation Management in Pharma: Regulatory Expectations and Best Practices》,2025年 辛格迪,《MAH必读:药品偏差管理流程中的常见缺陷与应对策略》,2024年 韩文连,《药品生产偏差的现状及解决对策》 国家药品监督管理局,《药品生产现场检查风险评定指导原则》


