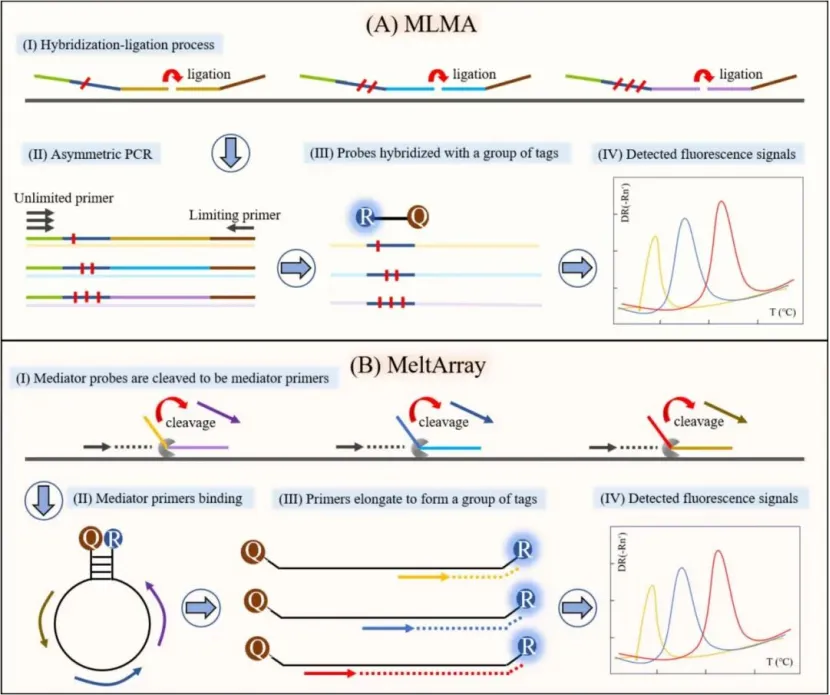
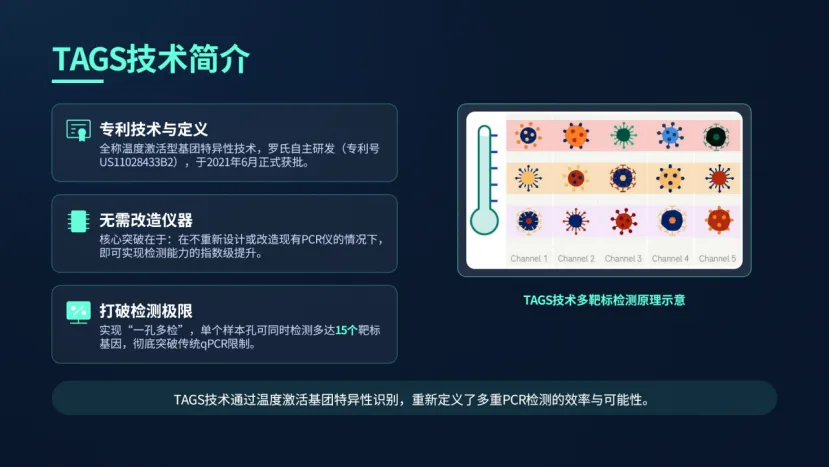
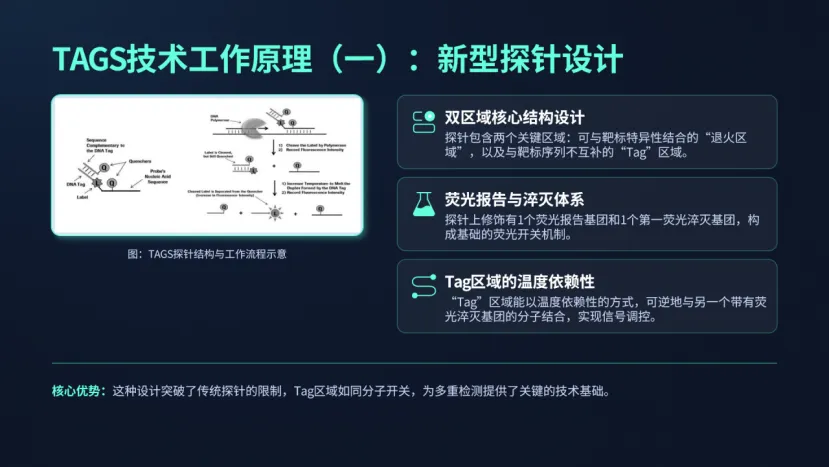
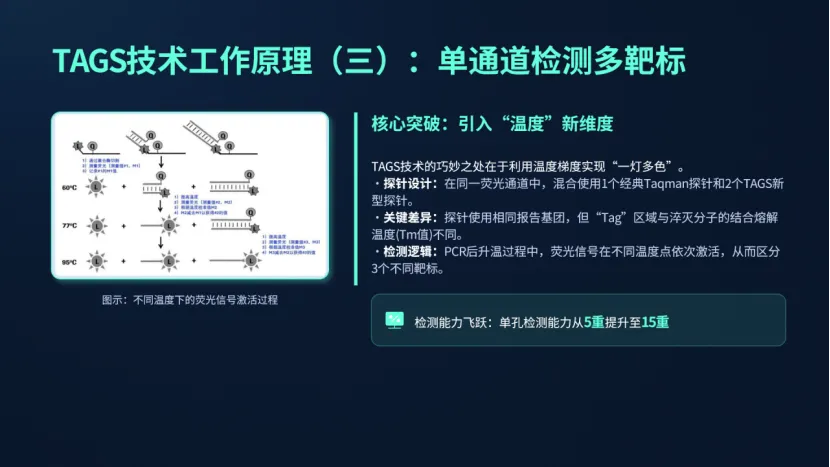
一、TAGS技术:多重检测的底层技术突破

二、RT-qPCR定量分析的数学逻辑革新:2-CT法的技术原理与验证




在LIVAK和SCHMITTGEN的原始低离散度数据中,2-ΔΔCT法的对照组归一化均值为1.02,偏离理论值1,而2-CT法的对照组归一化均值严格为1,实现了精准归一化。 在秀丽隐杆线虫镉暴露的高离散度实验数据中,2-ΔΔCT法计算得到的irg-6基因表达上调倍数为7.125倍,2-CT法的计算结果为4.124倍,两者偏差高达70%;同时两种方法的统计学P值存在数量级差异(2-ΔΔCT法P=0.0002,2-CT法P=0.0015),数据离散程度越高,2-ΔΔCT法的偏差越显著。 该方法具备极强的通用性:当PCR扩增效率E<100%时,仅需将公式中的底数2替换为

三、qPCR-熔解曲线分析的技术深化与多重检测拓展

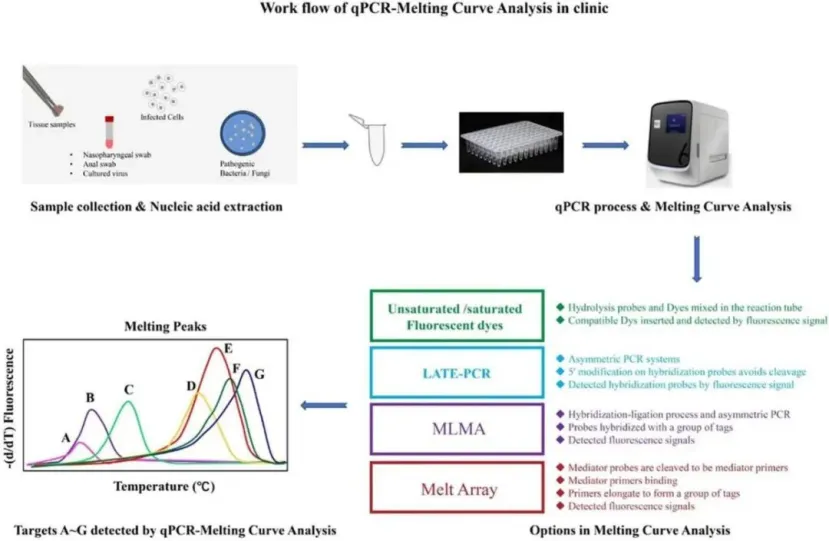
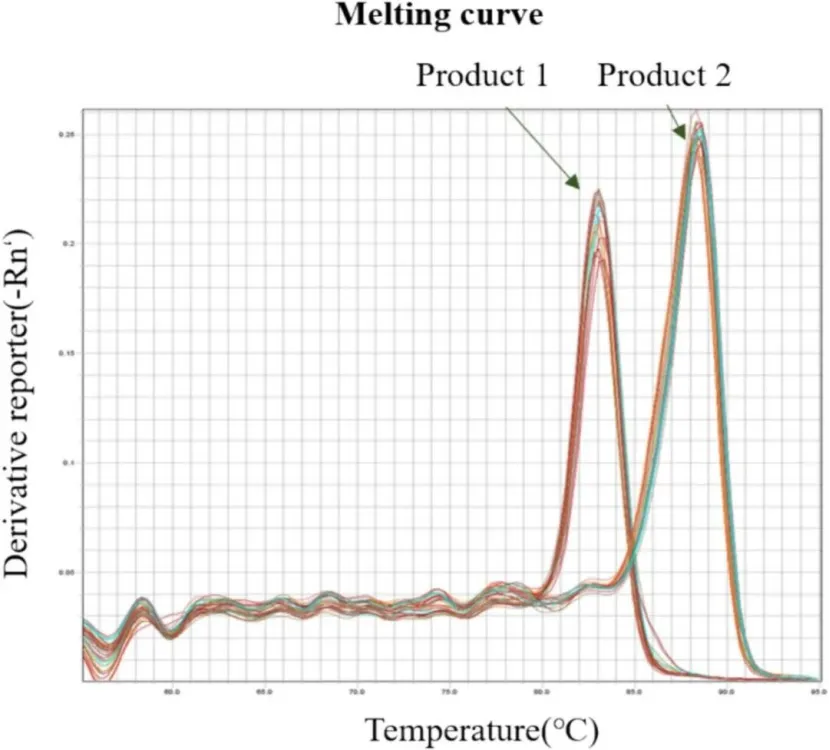
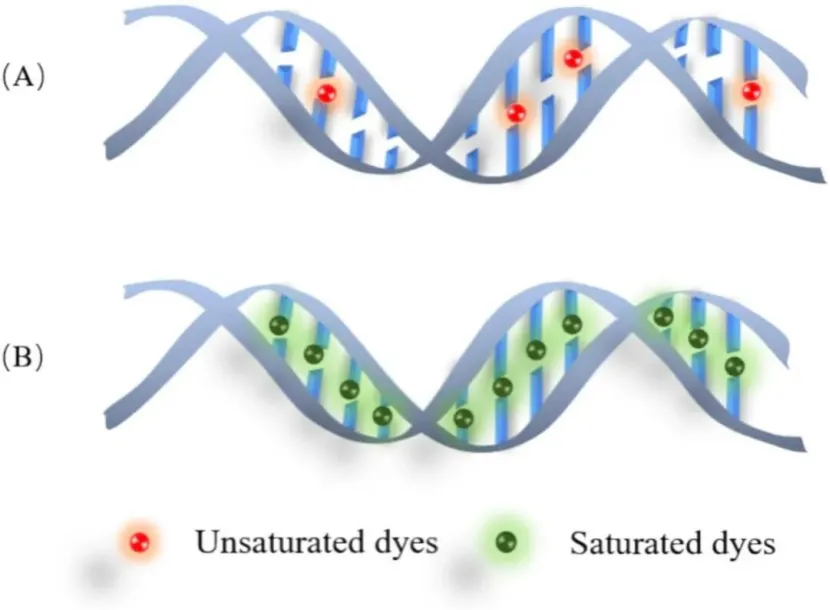
非饱和染料(如SYBR Green I):通过带正电的结构插入双链DNA的小沟中产生荧光,但其不会占据所有的DNA结合位点,当温度升高、DNA部分解链时,游离的染料会重新结合到未完全解链的DNA位点上,导致荧光信号变化与DNA解链过程不同步,Tm值检测偏差较大,无法区分单碱基差异的核酸序列。 饱和染料(如Eva Green、LC Green、SYTO 9):可100%占据双链DNA的所有结合位点,DNA解链过程中不会发生染料的重排,荧光信号的下降与DNA解链程度完全同步,信号分辨率显著提升,以此为基础的高分辨率熔解(HRM)技术,可实现单核苷酸多态性(SNP)、甲基化修饰的精准检测。
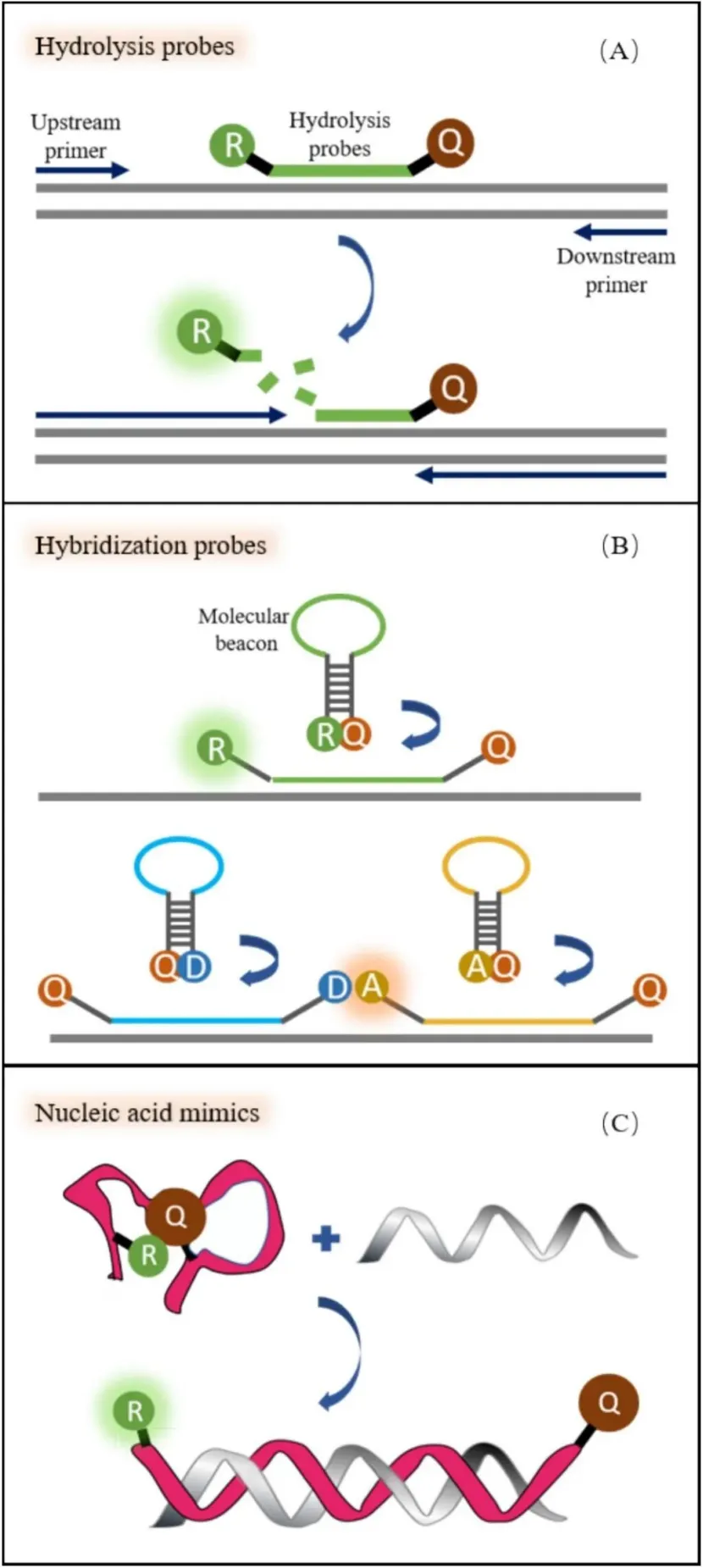
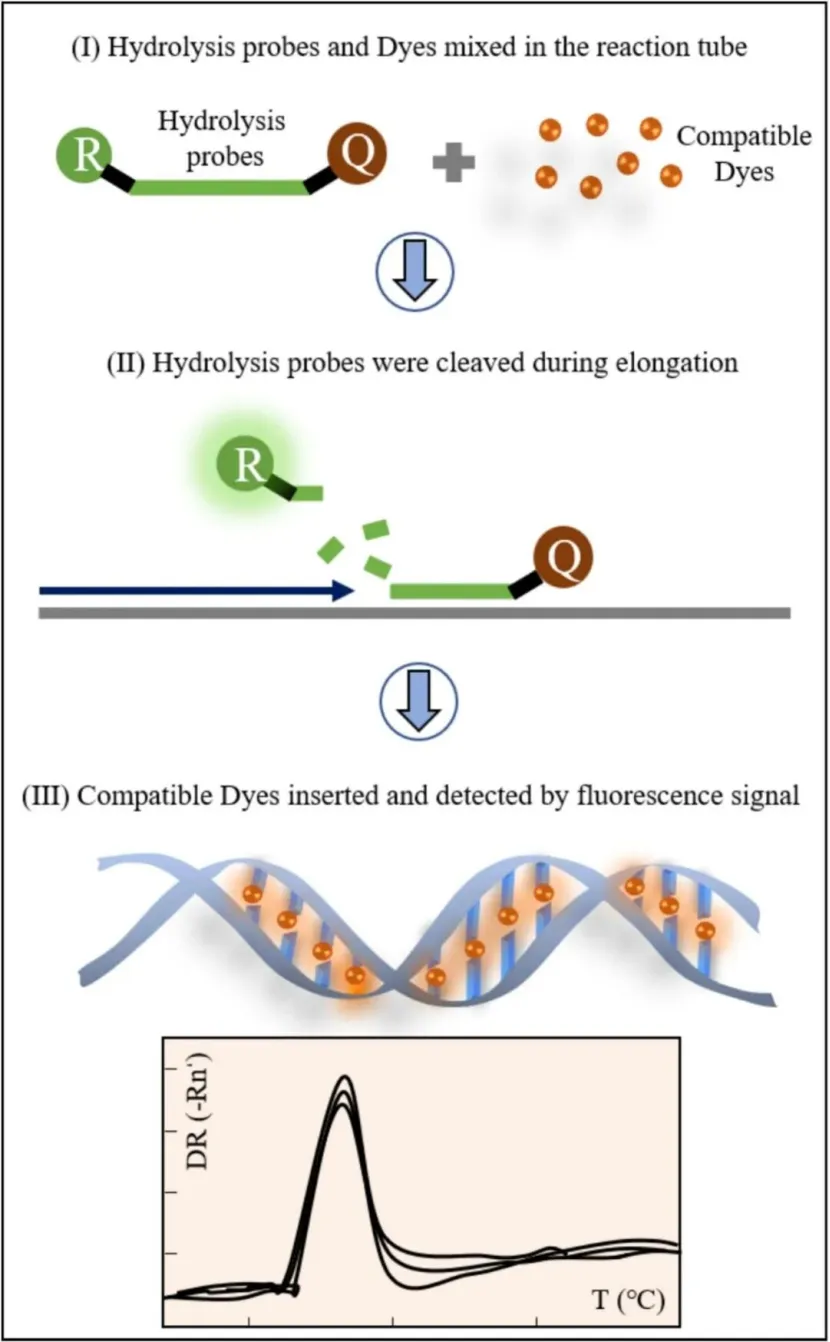
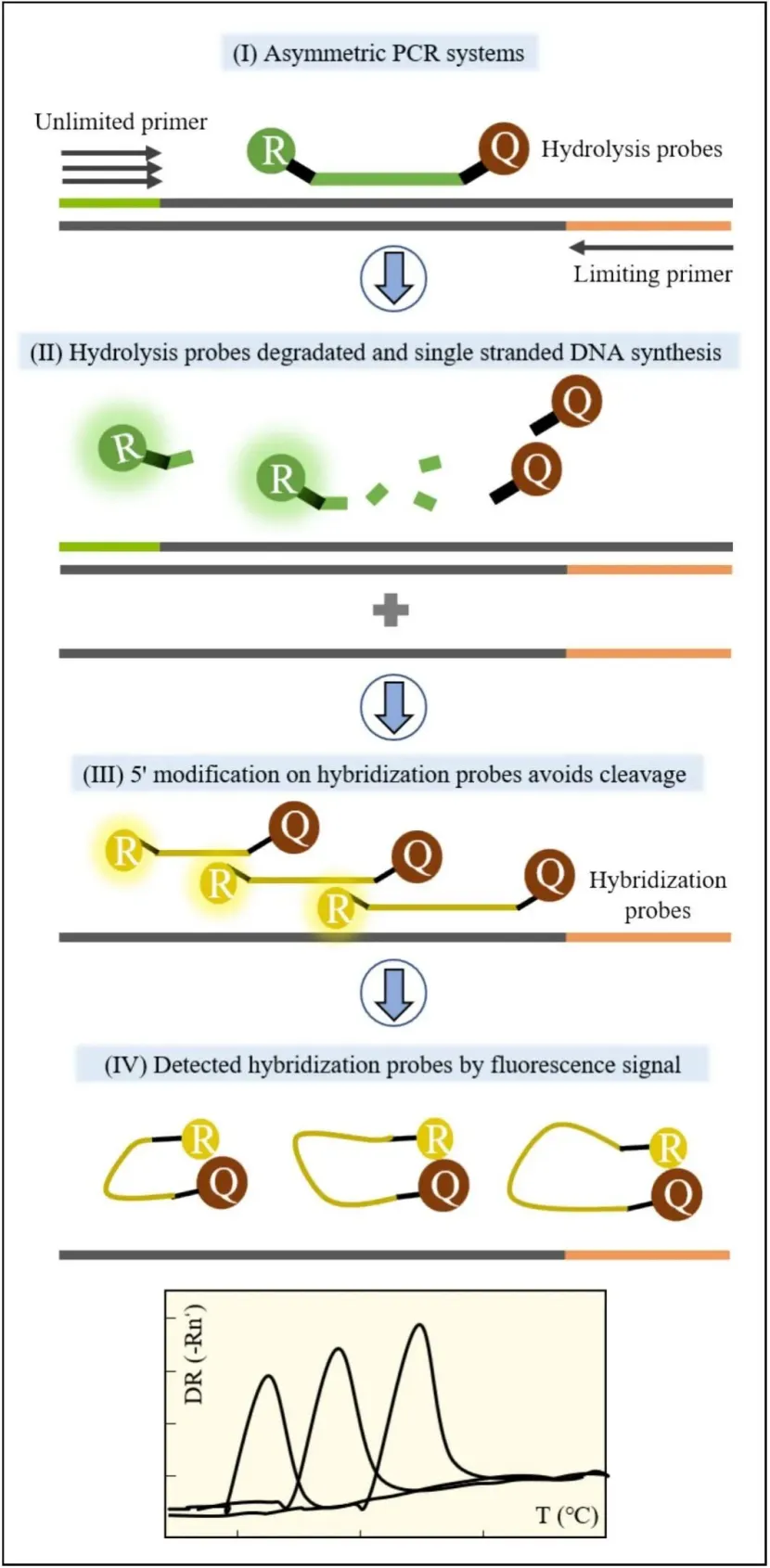
水解探针(TaqMan探针)的兼容方案:传统水解探针在扩增过程中会被Taq酶的5'-3'核酸外切酶活性切割,荧光基团与淬灭基团永久分离,无法用于扩增后的熔解曲线分析。通过优化体系,可将水解探针与通道兼容的饱和染料(如SYTO 82、BOXTO)结合,水解探针负责实时定量检测,兼容染料负责熔解曲线的扩增特异性验证,实现单管内的定量+定性双重检测。 杂交探针体系与LATE-PCR技术:杂交探针仅在与靶标序列结合时产生荧光信号,扩增过程中不会被切割,可完整用于熔解曲线分析。为提升杂交探针的检测灵敏度,研究人员开发了LATE-PCR(指数后线性PCR)技术:通过调整引物的长度与GC含量,抵消非对称PCR的引物浓度差异带来的扩增效率下降,可高效生成大量单链DNA产物,同时探针Tm值的设计限制更少,可实现低丰度靶标、SNP位点的高灵敏度检测。