
关注康薪KANGLIFE,获取更多IVD及临床法规最新资讯

康薪咨询
KANGLIFE CONSULTING



欧盟2021/2282号卫生技术评估 (HTA,health technology assessment) 法规于2021年通过,历经三年过渡期后,于2025年1月12日正式施行。根据法规要求,HTA协调小组需于次年2月底前提交上一年度工作报告,年初,涵盖2025年全年工作的首份年度报告正式发布,为了解法规落地初期运行情况提供了官方依据。
本期基于该报告,梳理欧盟HTA协调小组及各专项小组2025年核心工作进展。
联合临床评估(JCA)
13项药品评估启动,器械评估准备就绪
联合临床评估(JCA)作为HTA法规核心机制,聚焦卫生技术相对有效性与安全性统一分析,结果为成员国定价和报销决策提供参考,所有符合条件的EMA*(European Medicines Agency,欧洲药品管理局)上市许可申请产品均纳入评估范围。
| 说明:
*欧洲药品管理局(EMA,European Medicines Agency):欧盟的一个科学机构,负责评估和监管在欧盟市场上销售的药品。在确保欧盟市场上药品的安全性、有效性和质量方面发挥着关键作用,是欧盟药品监管体系的核心机构。
01 | 药品联合临床评估(Joint Clinical Assessment, JCA)范围与流程
联合临床评估JCA启动于EMA通知HTA小组相关上市许可申请提交,由JCA小组指定主、副评估员负责,分启动与范围界定、档案准备、评估起草、报告认可与发布四阶段,最终报告经协调小组认可、欧盟委员会程序性审查后发布于Europa网站。
根据实施路径,2025—2027年药品JCA聚焦于用于癌症治疗的新活性物质以及先进治疗药品(Advanced Therapy Medicinal Products, ATMPs)。评估不设筛选环节,所有通过欧洲药品管理局(EMA)申请上市且属于上述类别的产品均纳入范围,并与EMA上市许可申请同步开展。
医疗器械(标准)联合临床评估程序的时间线与阶段
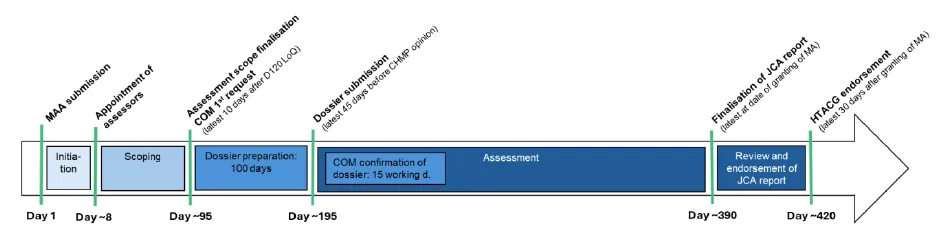
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
02 | 2025年药品JCA进展情况
截至2025年底,JCA小组已启动 13项联合临床评估,其中包括一种具有两个治疗适应(therapy medicinal products)的产品。
具体构成如下:
按产品类型:10项为肿瘤产品,3项为先进治疗药品(Advanced Therapy Medicinal Products, ATMPs)。
按资格认定:孤儿药/罕见病资格认定占比近半。
按开发主体:3项涉及中小企业(SMEs),1项涉及研究机构。
在进度方面,截至报告统计时,13项评估中:1项档案已获确认,3项正在接受档案确认,5项处于档案准备阶段,4项仍在制定评估范围,尚无进入最终认可阶段的案例。
正在进行的联合临床评估程序的项目
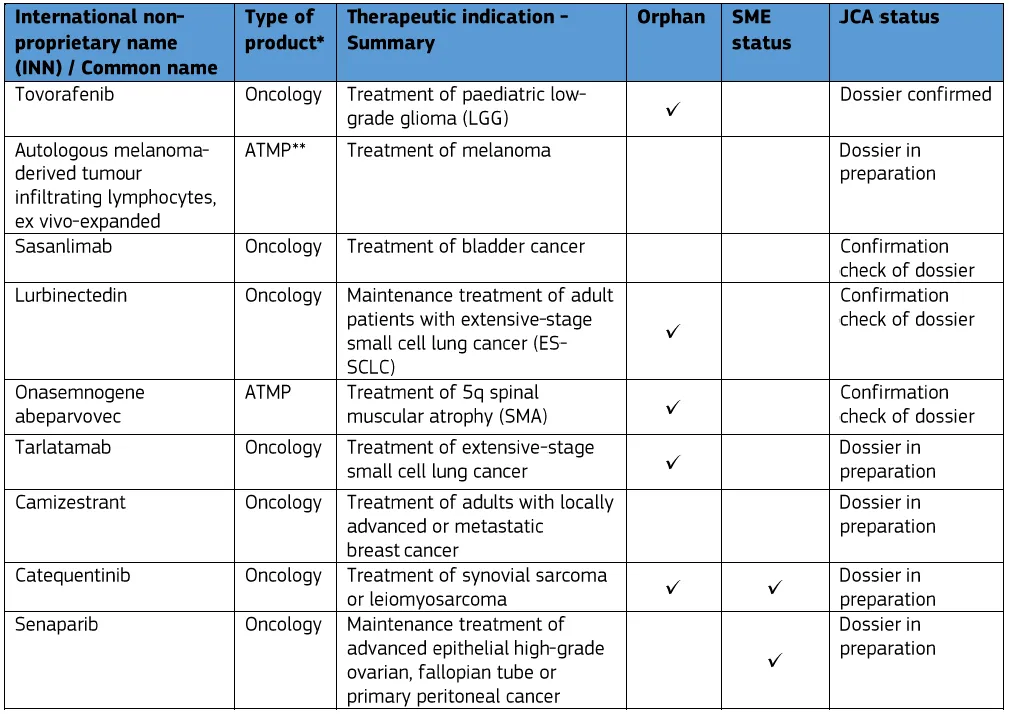
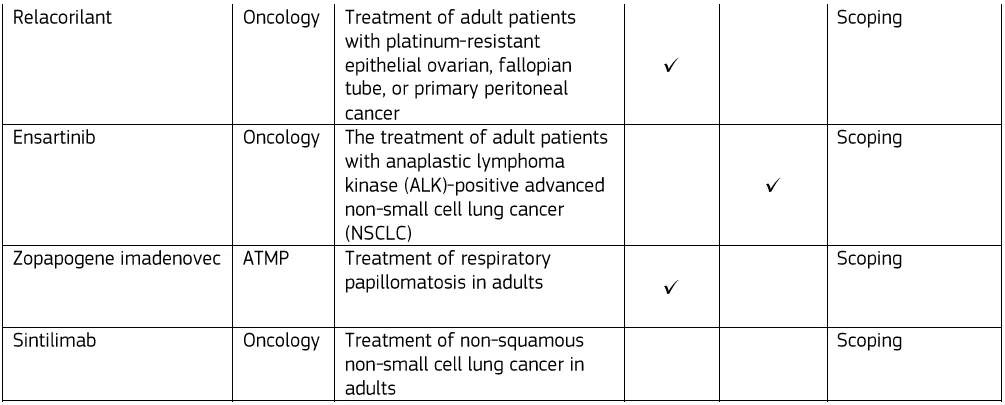
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
截至 2025 年底,各阶段联合临床评估(JCA)案例数量
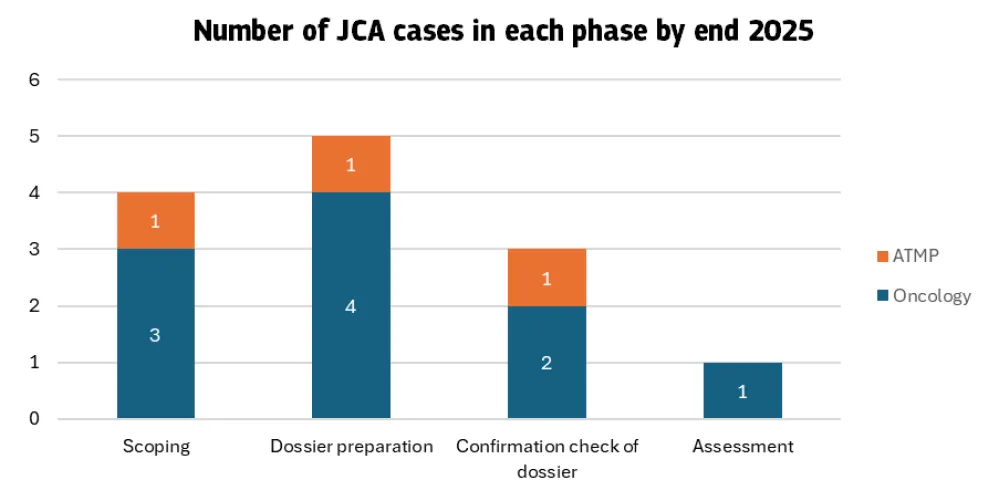
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
03 | 医疗器械JCA:2026年正式启动
医疗器械和体外诊断医疗器械的JCA将于2026年开始。2025年,JCA小组与医疗器械专项小组(MPG)合作,重点完成了多项指导文件的制定,为2026年首个器械推荐建议流程积累试点经验。
联合科学咨询(JSC)
7项入选,4项已完成
联合科学咨询为医疗技术开发商提供关于证据和数据需求的早期科学指导,以支持后续的联合临床评估(Joint Clinical Assessment, JCA),帮助规划卫生技术(health technology)的临床研究和临床调查(Clinical investigations),简化联合临床评估的证据准备工作,并提高证据生成的质量。
联合科学咨询特别提供关于相关临床研究设计方面或临床调查设计方面的指导,包括对照组(Comparators)、干预措施(Interventions)、健康结局(Health outcomes)和患者人群(Patient populations)。医疗技术开发商可选择性地提出与卫生经济学评估(Health economic assessment)相关的问题,可与EMA科学建议进行"并行联合科学咨询" (Parallel joint scientific consultations)。为自愿性、免费咨询,按HTA法规第17(3)条筛选案例。
01 | 申请与入选情况
2025年设 两个申请期(2月3日-3月3日针对药品;6月2日-6月30日针对药品及器械),累计收到17项药品申请,筛选出7项入选(4项含并行咨询请求),未收到器械申请。
2025 年评审期间收到及选定的 SC 请求概况
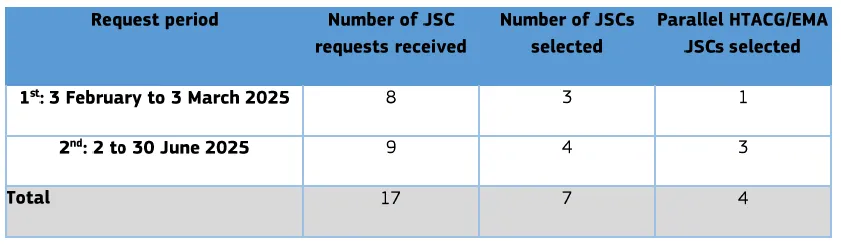
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
截至年底,4项已完成、1项被撤回、2项进行中;2项涉SMEs、4项涉孤儿药/罕见病、1项涉ATMPs。
治疗领域中,癌症药品占42%(3/7),神经退行性疾病(Neurodegenerative disorder)药品占28%(2/7),其余为14%神经肌肉(Neuromuscular disorder)、14%神经发育障碍(Neurodevelopmental disorder)药品。
2025 年联合科学咨询的治疗领域分布
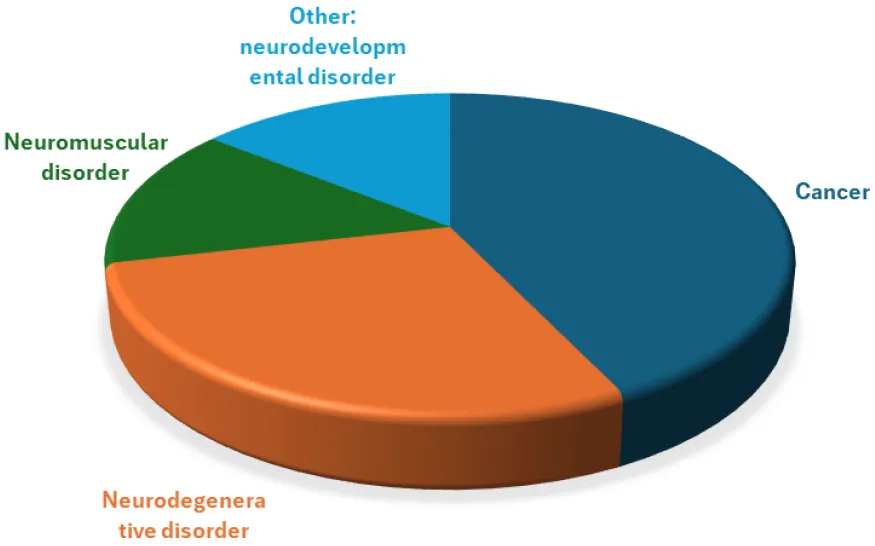
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
所有申请均咨询患者人群等相关问题,4项咨询干预措施,5项涉及卫生经济学,2项关注安全性及上市后证据生成。
2025 年联合科学咨询的咨询领域分布
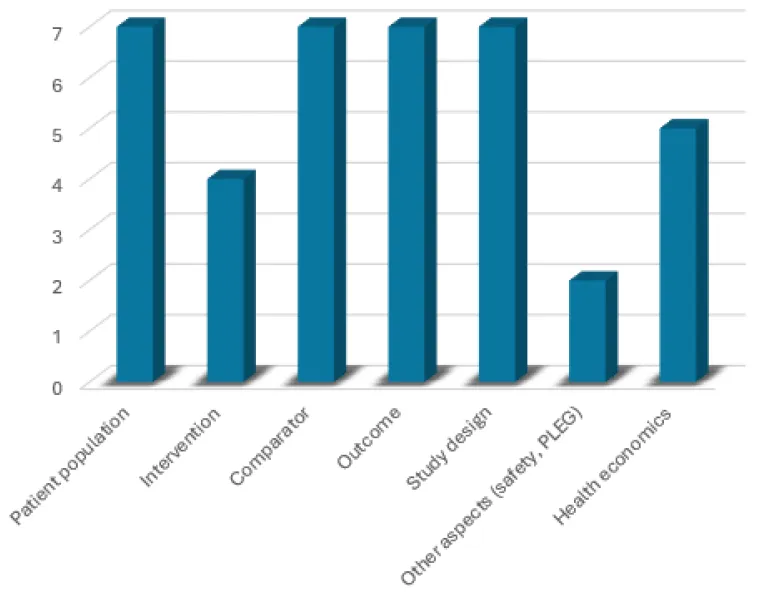
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
02 | 成果交付
JSC小组在2025年完成了四份成果文件(Outcome documents)。所有文件均通过书面程序获得协调小组(Coordination Group)批准,无进一步意见,随后发送给申请的医疗技术开发商。
截至本报告通过时,已完成联合科学咨询的平均完成时间为140天(约4.5个月),从提交初始简报文件包(Briefing package)到向医疗技术开发商发送JSC成果文件计算。

患者与临床专家参与
已识别300余名专家,48人次参与联合工作
根据HTA相关实施条例,每项联合临床评估或联合科学咨询都必须系统性纳入个别专家(Individual experts,即患者、护理人员或临床医生)。
2025年2月,欧盟委员会在HTA利益相关方网络(HTA Stakeholder Network)内成立了一个工作组,共同创建识别参与联合HTA活动的患者、护理人员和/或临床医生的流程。截至年底,已识别300余名符合条件专家(均提交利益声明),其中38人次参与JCA、10人次参与JSC,相关参与模板及指导文件已同步制定。
患者识别与筛选、数据图表及分层分析流程
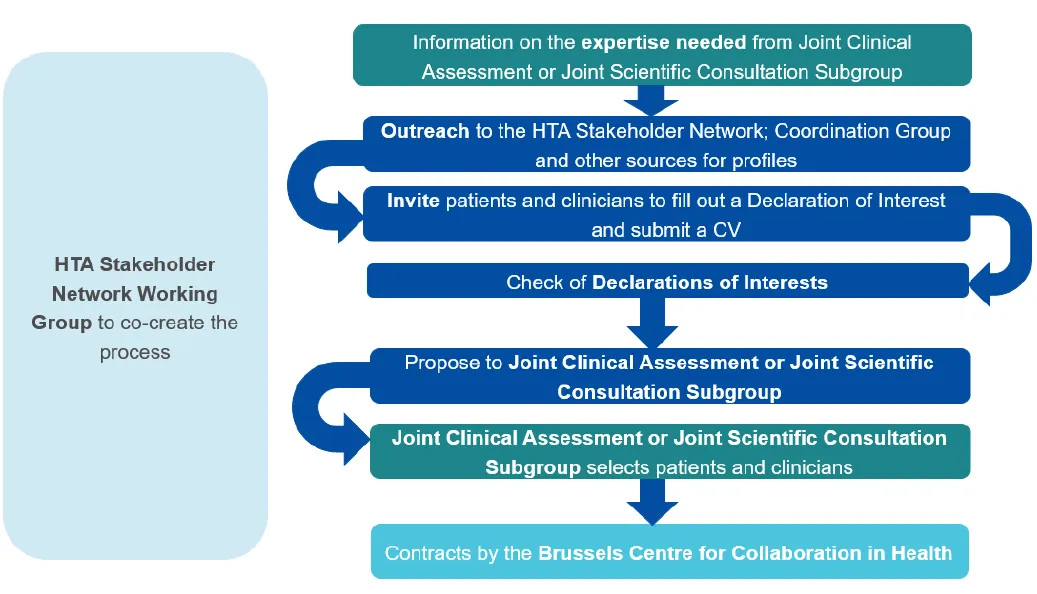
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
新兴卫生技术(EHT)
完成2025年报告,助力JCA规划
根据HTA法规第22条,协调小组需编制新兴卫生技术EHT(Emerging Health Technologies)报告,支持JCA工作规划。2025年EHT小组梳理地平线扫描系统,完成试点数据收集并举办网络研讨会;编制的2025年EHT报告(公开版2026年1月9日发布于Europa网站),聚焦2026年拟纳入法规范围的药品及器械,药品数据来自EMA和国际地平线扫描倡议(IHSI),器械数据来自EMA。
方法与程序指导
聚焦医疗器械相关文件
2025年重点推进医疗器械相关指导文件制定,MPG小组与JCA、JSC小组合作,完成器械JCA档案模板、评估程序、选择标准等5项指南;其下设PICO、统计学等支持小组已投入运行,全年召开9次会议,发布问答形式经验总结与澄清。
2025年,医疗器械小组与联合临床评估小组共同制定了以下关于医疗器械的方法学指导:
联合临床评估档案模板填写指南——医疗器械和体外诊断医疗器械(Medical Devices and In Vitro Diagnostic Medical Devices, MDs/IVDs)
医疗器械和体外诊断医疗器械联合临床评估程序指南
关于协调小组推荐选择医疗器械和体外诊断医疗器械进行联合临床评估的指南
MPG小组还与联合科学咨询小组合作制定了:
选择医疗器械和体外诊断医疗器械进行联合科学咨询的指南
医疗器械和体外诊断医疗器械联合科学咨询程序指南
IT平台
协作空间与用户数量显著增长
欧盟委员会搭建的专用安全内联网IT平台,为各相关方提供涉密信息交换渠道。2025年新增开发商工作空间86个,完成利益声明485份,举办培训11场,平台活跃度较法规实施前大幅提升。
HTA IT 平台架构
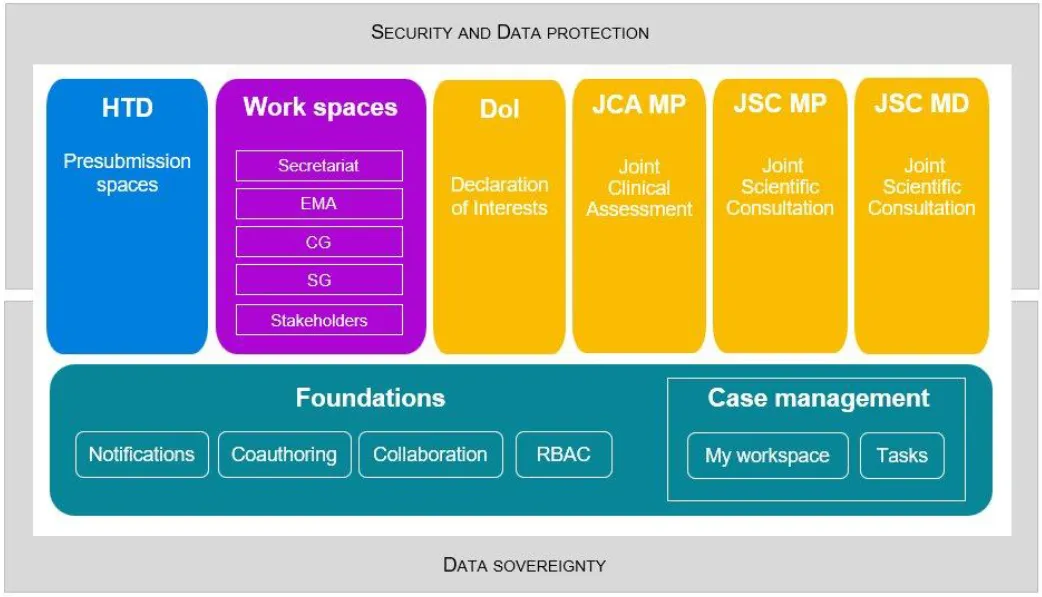
(*图表来源:HTA协调小组《2025年度报告(2025 Annual Report) 》
总 结
总体而言,2025年作为欧盟HTA法规实施元年,相关机制已正式启动并平稳运行。药品联合临床评估和联合科学咨询按计划推进,患者及临床专家的参与机制初步建立,医疗器械评估的准备工作基本完成。随着各项流程逐步成熟,未来欧盟层面的HTA合作将对区域内卫生技术准入产生持续影响。
给制造商的建议
研读MPG小组发布的JCA、JSC相关指导文件,熟练掌握2026年器械JCA评估流程、档案要求及选择标准,避免流程延误;
利用JSC自愿免费咨询机制,在研发阶段获取临床研究、证据生成等科学指导,提升证据质量,降低评估风险;
关注EHT报告及地平线扫描动态,结合2026年重点评估方向,优化产品研发与布局,贴合HTA导向;
依托欧盟HTA专用IT平台,完成工作对接等操作,参与平台培训,为产品市场准入奠定基础。
康薪咨询海外HTA专项服务
作为专注于医疗器械与IVD领域的专业CRO(临床研究组织)与咨询机构,康薪咨询已成功助力数百家国内外IVD企业获取欧盟、东南亚、拉美等市场的上市准入。我们的HTA服务涵盖以下四大核心服务模块,为企业提供端到端的全链条支持:
|HTA全流程战略辅导
提供从起点到终点的全程陪伴式服务,涵盖目标市场HTA路径诊断与规划;缺口数据补充与多维度证据整合;符合目标机构(如欧盟JCA、英国NICE)方法学的高质量报告撰写;提交后的进度跟踪、官方问询模拟与专业应答;直至评估通过后的医保对接、采购谈判与上市后证据长期维护。
|全球法规合规协同
确保您的HTA策略与复杂的全球监管体系精准协同。我们提供欧盟HTAR法规深度解读与JCA实操指南;确保HTA核心证据与欧盟IVDR(CE认证)、REACH等法规要求保持一致;并提供专业的商业机密保护策略,保障企业核心信息资产安全。
|学术影响力构建
增值基础评估,助力企业构建长期学术影响力,包括设计并实施支撑HTA的高水平临床研究(RCT/真实世界研究),助力成果发表于《Value in Health》等国际顶刊;对接海外顶尖HTA机构、高校及医院,促成联合研究;并通过发布行业白皮书、支持国际学术会议亮相等方式,提升企业在全球学术圈的影响力与话语权。
|本地化落地保障
依托我们在泰国、西班牙等地的海外办事处网络,解决本地化落地难题。我们提供目标市场的本地化临床与卫生经济学数据收集;报告的专业语言翻译与文化适配;以及直接对接当地HTA机构、医保支付方和采购决策者的高效沟通渠道,显著降低跨境管理与沟通成本,加速市场准入。
康薪咨询团队可承接欧洲多国、泰国、中国等多国医疗器械及IVD器械注册要求的临床实验研究项目(可出具伦理批件),可为IVD企业提供全生命周期的解决方案服务。
康薪KANGLIFE
业务范围
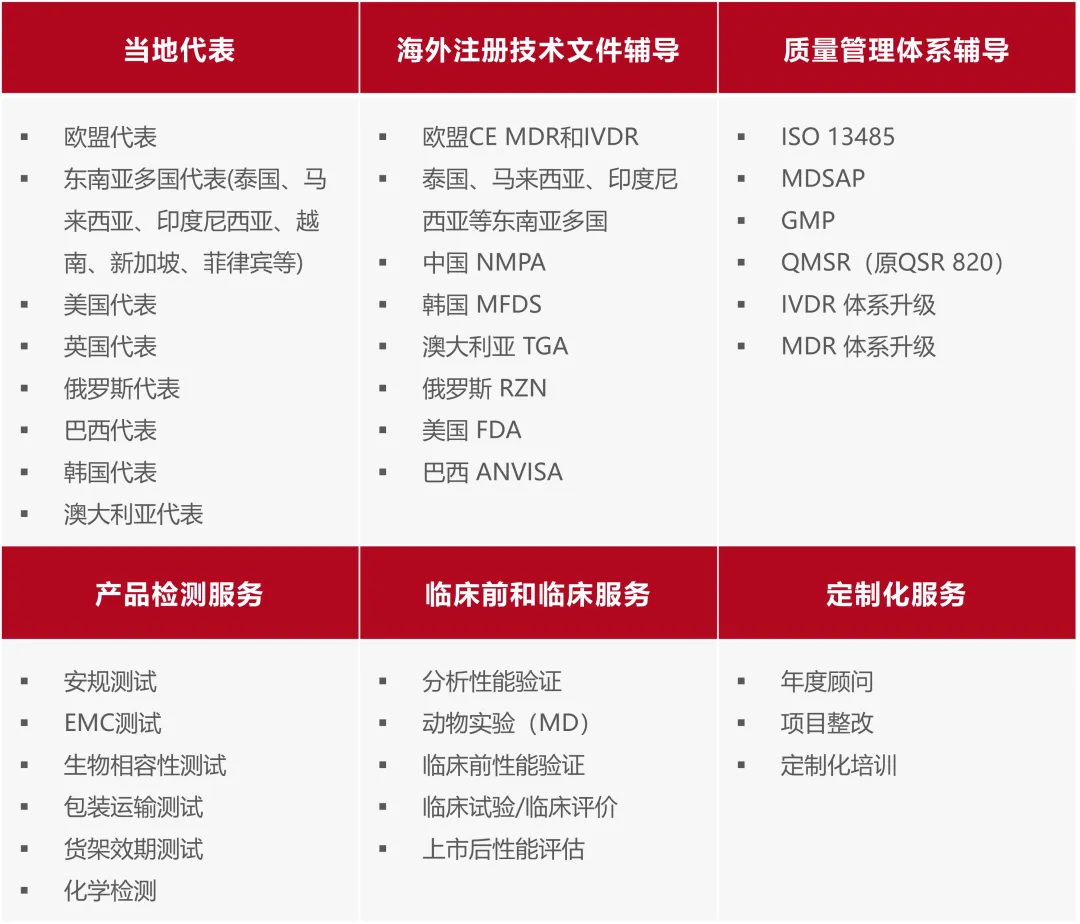
注册服务支持区域
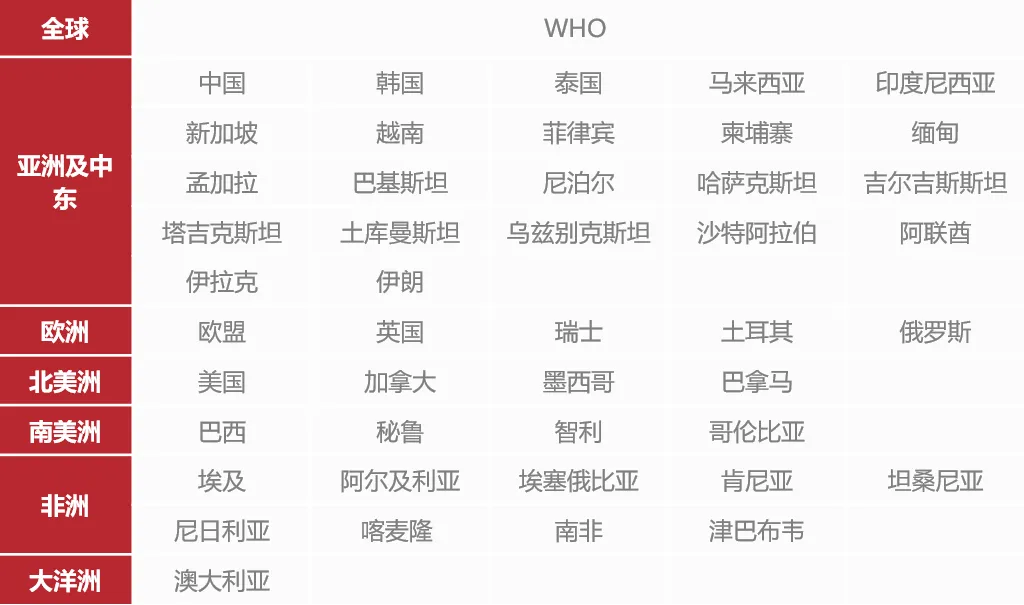
临床实验室资源

关于康薪咨询
ABOUT KANGLIFE
| 专业特色:
协同企业,共同定制出海战略服务。
| 核心文化:
协助国内外优秀体外诊断及医疗器械企业实现战略发展、培养合规人才,携手共筑中国企业出海愿景。
康薪咨询成立以来已与数百家企业强强联合,协同高效合作,提供定制化服务,成功获得多个欧美和东南亚市场准入资质。
业务咨询
CONTACT US

华北区咨询顾问
Harold Hua

华东区咨询顾问
Joyce Hua

华南区咨询顾问
Fitter Cao


关注康薪咨询
Follow KANGLIFE
点击下方”阅读原文“,即刻与我们取得进一步联系!


