特瑞普利单抗为是君实生物自主研发的中国首个成功上市的国产PD-1单抗,也是FDA批准上市的首个中国自主研发和生产的创新生物药。2025年特瑞普利单抗国内市场销售收入约20.68亿元,占公司整体收入的80%以上,同比增长约 38%。
特瑞普利单抗已在国内获批上市12项适应症,全部纳入国家医保目录,是目录中唯一用于肾癌、三阴性乳腺癌和黑色素瘤治疗的抗PD-1单抗药物。
用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗(2018年12月);
用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗(2021年2月);
用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗(2021年4月);
联合顺铂和吉西他滨用于局部复发/转移性鼻咽癌患者的一线治疗(2021年11月);
联合紫杉醇和顺铂用于不可切除局部晚期/复发或远处转移性食管鳞癌患者的一线治疗(2022年5月);
联合培美曲塞和铂类适用于EGFR基因突变阴性和ALK阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌的一线治疗(2022年9月);
联合化疗围手术期治疗,继之本品单药作为辅助治疗,用于可切除IIIA-IIIB期非小细胞肺癌的成人患者(2023年12月);
联合阿昔替尼用于中高危的不可切除或转移性肾细胞癌患者的一线治疗(2024年4月);
联合依讬泊苷和铂类用于广泛期小细胞肺癌(ES-SCLC)的一线治疗(2024年6月);
联合注射用紫杉醇(白蛋白结合型)用于经充分验证的检测评估PD-L1阳性(CPS≥1)的复发或转移性三阴性乳腺癌(TNBC)的一线治疗(2024年6月);
联合贝伐珠单抗用于不可切除或转移性肝细胞癌患者的一线治疗(2025年3月);
用于不可切除或转移性黑色素瘤的一线治疗(2025年4月)。
2025年1月,用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗的适应症获得NMPA同意,由附条件批准转为常规批准。
2025年3月,联合贝伐珠单抗用于不可切除或转移性肝细胞癌患者的一线治疗的sNDA获得NMPA批准。
2025年4月,用于不可切除或转移性黑色素瘤的一线治疗的sNDA获得 NMPA批准。
2025年8月,联合维迪西妥单抗用于HER2表达的(HER2表达定义为HER2免疫组织化学检查结果为1+、2+或3+)局部晚期或转移性尿路上皮癌患者的sNDA获得NMPA受理。
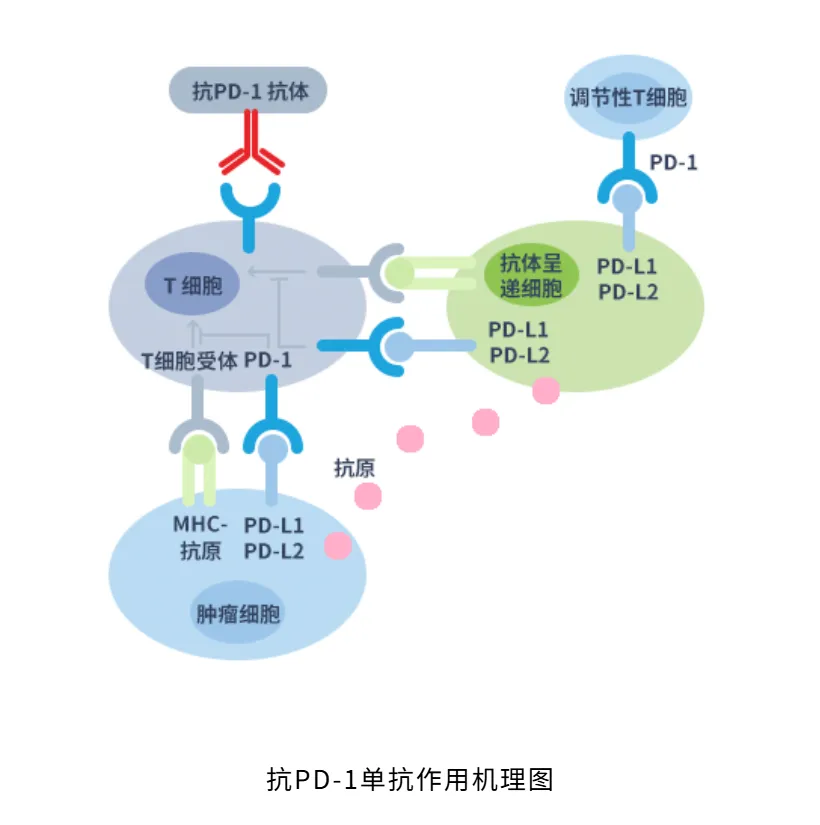
2025年1月,特瑞普利单抗联合顺铂/吉西他滨作为转移性或复发性局部晚期鼻咽癌成人患者的一线治疗,以及作为单药治疗既往含铂治疗过程中或治疗后疾病进展的复发性、不可切除或转移性鼻咽癌的成人患者的上市许可申请获得澳大利亚TGA批准上市,特瑞普利单抗成为澳大利亚首个用于鼻咽癌的肿瘤免疫治疗药物。
2025年3月,特瑞普利单抗联合顺铂和吉西他滨用于复发、不能手术或放疗的,或转移性鼻咽癌成人患者的一线治疗的上市许可申请获得新加坡HSA批准上市。特瑞普利单抗成为新加坡首个获批用于鼻咽癌的肿瘤免疫治疗药物。
2025年6月,特瑞普利单抗一线治疗鼻咽癌和一线治疗食管鳞癌的适应症在阿联酋和科威特正式获批上市。
2025年9月及2025年10月,特瑞普利单抗联合顺铂/吉西他滨作为转移性或复发性局部晚期鼻咽癌成人患者的一线治疗,以及作为单药治疗既往含铂治疗过程中或治疗后疾病进展的复发性、不可切除或转移性鼻咽癌的成人患者的2项适应症分别在巴基斯坦和加拿大获批上市。
2025年11月,特瑞普利单抗在中国香港获批新适应症,用于联合化疗一线治疗食管鳞癌。
2025年12月,特瑞普利单抗一线治疗鼻咽癌和一线治疗食管鳞癌的适应症在巴林获批上市。
2026年2月,特瑞普利单抗一线治疗鼻咽癌和一线治疗食管鳞癌的适应症在阿曼、卡塔尔获批上市。
2025年,特瑞普利单抗期刊发表超过210篇,合计影响因数超过1,100分,研究成果多次登上《美国医学会杂志》(JAMA)、《新英格兰医学杂志》(NEJM)等国际权威期刊,以及美国临床肿瘤学会(ASCO)年会、欧洲肿瘤内科学会(ESMO)年会等国际学术大会,并多次在各大学术会议上作口头报告。


