дҪ“еҶ…еөҢеҗҲжҠ—еҺҹеҸ—дҪ“Tз»ҶиғһпјҲin vivo CAR-TпјүжҠҖжңҜжҳҜеҖҹеҠ©йқ¶еҗ‘жҖ§еҹәеӣ йҖ’йҖҒиҪҪдҪ“зі»з»ҹпјҢе°Ҷзј–з ҒеөҢеҗҲжҠ—еҺҹеҸ—дҪ“пјҲCARпјүзҡ„зӣ®зҡ„еҹәеӣ пјҢзӣҙжҺҘйҖ’йҖҒиҮіжӮЈиҖ…дҪ“еҶ…еҫӘзҺҜжҲ–з»„з»ҮеҺҹдҪҚTж·Ӣе·ҙз»ҶиғһпјҢе®һзҺ°Tз»ҶиғһдҪ“еҶ…еҺҹдҪҚеҹәеӣ дҝ®йҘ°гҖҒCARз»“жһ„еҠҹиғҪжҖ§иЎЁиҫҫгҖҒжҠ—еҺҹзү№ејӮжҖ§жҙ»еҢ–еҸҠиӮҝзҳӨз»Ҷиғһйқ¶еҗ‘жқҖдјӨзҡ„жІ»з–—ж–№ејҸгҖӮиҜҘжҠҖжңҜзӘҒз ҙдј з»ҹCAR-Tзҡ„з»ҶиғһдҪ“еӨ–ж“ҚдҪңжЁЎејҸпјҢе°ҶдёӘдҪ“еҢ–з»Ҷиғһдә§е“ҒиҪ¬еҢ–дёәиҝ‘дјјж ҮеҮҶеҢ–иҚҜзү©зҡ„жІ»з–—еҪўејҸпјҢдҫқжүҳдҪ“еҶ…з”ҹзҗҶеҫ®зҺҜеўғе®ҢжҲҗCAR-Tз»Ҷиғһзҡ„еҺҹдҪҚз”ҹжҲҗдёҺеҠҹиғҪжҙ»еҢ–пјҢеұһдәҺз»Ҷиғһе…Қз–«жІ»з–—дёҺеҹәеӣ йҖ’йҖҒжҠҖжңҜдәӨеҸүиһҚеҗҲзҡ„еүҚжІҝйўҶеҹҹгҖӮ
иҮӘдҪ“ CAR-TпјҲex vivoпјүз”ҹдә§жөҒзЁӢпјҲж•°е‘ЁпјүпјҡйҮҮиЎҖгҖҒеҲҶзҰ» T з»ҶиғһгҖҒдҪ“еӨ–еҹәеӣ зј–иҫ‘гҖҒжү©еўһгҖҒж·Ӣе·ҙжё…йҷӨйў„еӨ„зҗҶгҖҒеӣһиҫ“гҖҒжқҖдјӨиӮҝзҳӨз»ҶиғһгҖӮж•ҙдёӘиҝҮзЁӢиҖ—ж—¶ж•°е‘ЁпјҢжӮЈиҖ…жңүзӯүеҫ…иҝҮзЁӢдёӯз–ҫз—…еҸ‘з”ҹиҝӣеұ•зҡ„йЈҺйҷ©гҖӮ
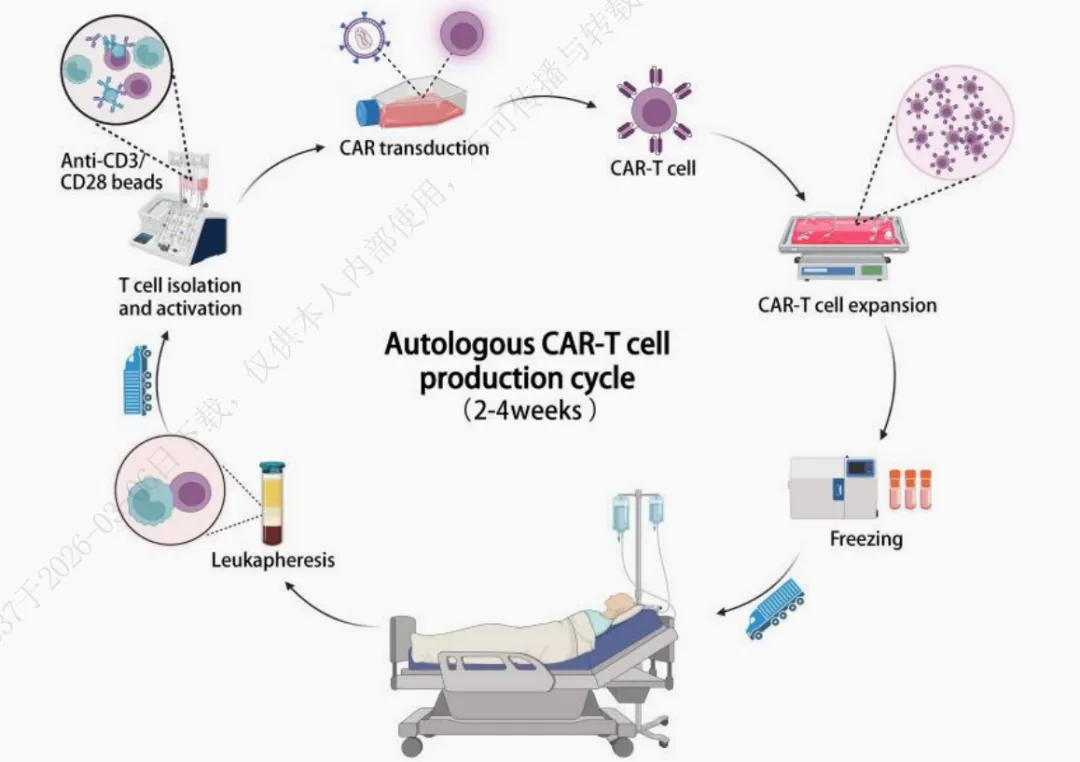
In vivo CAR-T з”ҹдә§жөҒзЁӢпјҲж•°еӨ©пјүпјҡйқҷи„үжіЁе°„йқ¶еҗ‘иҪҪдҪ“пјҲз—…жҜ’ / LNPпјүгҖҒдҪ“еҶ… T з»Ҷиғһиў«зІҫеҮҶиҪ¬еҜјгҖҒеҺҹдҪҚиЎЁиҫҫ CARгҖҒжҲҗдёәеҠҹиғҪжҖ§ CAR-TгҖҒзӣҙжҺҘжқҖдјӨиӮҝзҳӨз»ҶиғһгҖӮ
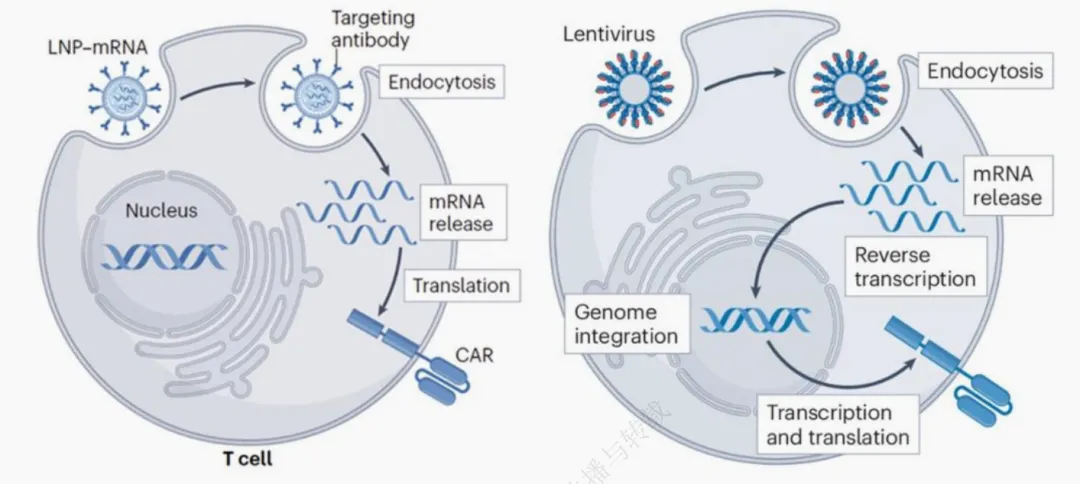
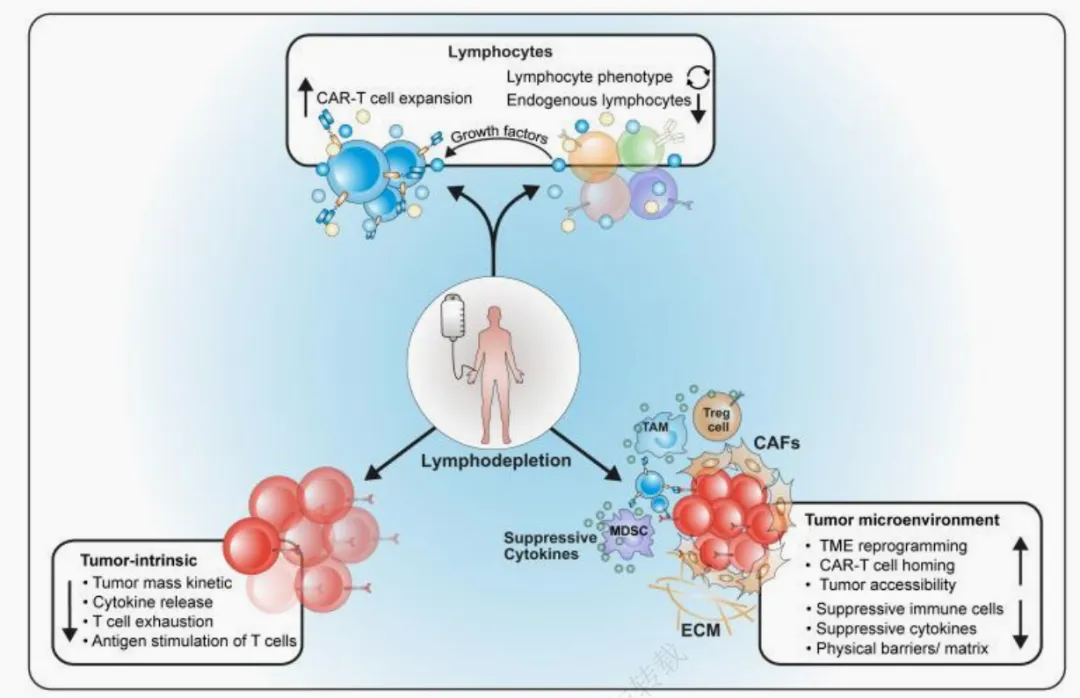
еҸҰеӨ–иҮӘдҪ“CAR-Tз»ҷиҚҜеүҚйңҖжё…ж·ӢпјҢеҸҜиғҪеҜјиҮҙдёҘйҮҚдёҚиүҜеҸҚеә”пјҢз”ҹдә§жҲҗжң¬дәҰеҫҲй«ҳгҖӮ
in vivo CAR-Tзҡ„ж ёеҝғзӘҒз ҙйӣҶдёӯдәҺйқ¶еҗ‘жҖ§еҹәеӣ йҖ’йҖҒзі»з»ҹдјҳеҢ–дёҺCARз»“жһ„е·ҘзЁӢеҢ–ж”№йҖ дёӨеӨ§ж–№еҗ‘пјҢзӣ®еүҚдё»жөҒйҖ’йҖҒиҪҪдҪ“еҲҶдёәз—…жҜ’иҪҪдҪ“дёҺйқһз—…жҜ’иҪҪдҪ“дёӨеӨ§зұ»пјҢеқҮе®һзҺ°йқ¶еҗ‘Tз»ҶиғһзІҫеҮҶиҪ¬еҜјпјҢйҒҝе…Қйқһзү№ејӮжҖ§з»„з»Үдҝ®йҘ°гҖӮж…ўз—…жҜ’е’Ң LNP(йқ¶еҗ‘и„ӮиҙЁзәізұійў—зІ’)В жҳҜжңҖеёёз”Ёзҡ„жҠҖжңҜи·ҜзәҝгҖӮ
еҪ“еүҚin vivo CAR-TдёҙеәҠз®ЎзәҝйӣҶдёӯдәҺв… жңҹгҖҒв…ЎжңҹдёҙеәҠжҺўзҙўйҳ¶ж®өпјҢж ёеҝғеёғеұҖдјҒдёҡиҒҡз„Ұ欧зҫҺеҸҠеӣҪеҶ…еӨҙйғЁз”ҹзү©еҢ»иҚҜе…¬еҸёпјҢйқ¶зӮ№д»ҘиЎҖж¶ІиӮҝзҳӨжҲҗзҶҹйқ¶зӮ№дёәдё»пјҢйҖҗжӯҘжӢ“еұ•иҮіиҮӘиә«е…Қз–«з—…дёҺе®һдҪ“зҳӨпјҢйҡҸзқҖдёҙеәҠж•°жҚ®зҡ„йҖҗжӯҘз§ҜзҙҜдёҺжҠҖжңҜиҝӯд»ЈпјҢйў„и®ЎжңӘжқҘеҮ е№ҙе°ҶжңүйҰ–жү№дә§е“ҒиҺ·жү№дёҠеёӮпјҢйҮҚеЎ‘е…Қз–«жІ»з–—дёҙеәҠж јеұҖпјҢжҲҗдёәжҒ¶жҖ§иӮҝзҳӨеҸҠйҡҫжІ»жҖ§иҮӘиә«е…Қз–«з—…зҡ„ж–°жІ»з–—жүӢж®өгҖӮ
гҖҗе…ҚиҙЈеЈ°жҳҺгҖ‘жң¬ж–ҮдҝЎжҒҜжқҘжәҗдәҺдёҠеёӮе…¬еҸёе…¬е‘Ҡзӯүе…¬ејҖиө„ж–ҷпјҢдёҚдҝқиҜҒзңҹе®һгҖҒеҮҶзЎ®гҖҒе®Ңж•ҙпјҢдёҚд»ЈиЎЁжң¬дәәз«ӢеңәеҸҠд»»дҪ•жҠ•иө„е»әи®®гҖӮ
гҖҗдҪңиҖ…з®Җд»ӢгҖ‘еҺҰй—ЁеӨ§еӯҰзЎ•еЈ«пјҢеҢ»еӯҰгҖҒжі•еӯҰеӨҚеҗҲиғҢжҷҜпјҢдҝқиҚҗд»ЈиЎЁдәәпјҢжіЁеҶҢдјҡи®ЎеёҲпјҢеҫӢеёҲпјҢ10+е№ҙжҠ•иЎҢз»ҸйӘҢпјҢжҹҗеҲёе•ҶеңЁиҒҢе‘ҳе·ҘгҖӮ


