
l 简单务实 l 专注精进 l 行稳致远 l 值得托付 l
免责声明
本内容仅供交流分享,不构成任何投资推荐或建议,订阅者应当充分了解各类投资风险,根据自身情况自主做出投资决策并自行承担投资风险,本微信公众号及相关主体不对任何因使用本公众号所载内容所引致或可能引致的损失承担任何责任。
本资料为常旸基金所有,未经常旸基金许可,任何机构和个人不得以任何形式转发、复制、翻版、发布或引用本资料的全部或部分内容。


太长不看版
(要点总结)
本篇主要简单介绍了一些热门的偶联药物衍生平台(XDC):
·放射性核素偶连药物(RDC):以核素为有效载荷,有望实现“诊疗一体化”。
·多肽-药物偶联物(PDCs):以多肽为配体,具有比ADC更强的渗透性和低免疫原性。
·小分子偶联药物(SMDC):以小分子为配体,组织渗透性进一步提升,但需寻找具有靶向性的小分子并阐明其靶向机理。
·免疫刺激抗体偶联物( ISACs):采用免疫激动剂/调节剂为载荷,通过让免疫激动剂在肿瘤微环境中定向释放,可激活免疫系统对肿瘤组织的免疫应答,杀伤肿瘤。
·抗体-核酸偶联物(AOC):以核酸药物(包括ASO、siRNA、免疫激活型CpG片段、PMO等)为有效载荷,借助配体的靶向性,有望解决核酸药物的肝外递送难题。
·定向降解抗体偶联物/降解剂抗体偶联药物(DAC):以靶向蛋白降解剂为载荷(PROTAC 或分子胶),通过直接降解细胞质来治疗疾病,有望覆盖一些难成药靶点和一些传统药物难以治疗的疾病。
随着对配体、有效载荷的不断拓展,当前的偶联药物早已不局限于ADC一种模式,更多样的新型偶联药物(XDC)正在如雨后春笋般出现,重塑当前疾病诊疗的新范式。
1
放射性核素偶连药物(RDC)
放射性核素偶连药物(Radionuclide Drug Conjugates,RDC)/靶向放射配体疗法(RLT):是目前最成功的XDC疗法且已经实现了商业化落地。该药物通常有四个主要组件构成:靶向配体(抗体、多肽或小分子)、连接子(Linker)、螯合剂(Chelator)与放射性核素。其中螯合剂负责在系统循环过程中稳固结合并稳定放射性核素;放射性核素需根据具体医疗用途进行挑选(治疗/诊断),需谨慎考虑其物理半衰期、释放辐射类型及化学性质等特征。
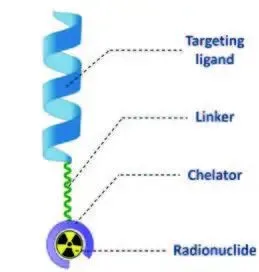
RDC的基础结构
*资料来源:先通医药招股说明书
RDC的最大特点是将放射性核素作为有效载荷,通过选用不同的放射性核素即可实现特定的诊断或治疗功能。
·从诊断方面来看:核药是目前唯一能实现活体代谢过程功能显像技术的方式,能够在核素半衰期内发出信号并通过分子影像学得出全面而精准的医学影像;
·从治疗方面来看:RDC的辐射杀伤机制有助于克服其他治疗方式常见的耐药性;
·从诊疗效率来看:RDC只需更换核素部位就可实现诊疗一体化,患者在诊断出疾病后即可使用相应药物配合治疗,从而大幅提高患者的治疗效率。
2
多肽-药物偶联物(PDCs)
多肽-药物偶联物(PDCs,Peptide-Drug Conjugate):是将ADC的抗体部分替换为多肽的一类新兴偶联物。由于多肽相较抗体,分子量更小、更容易合成生产,因此相较于ADC,PDC具有更强的肿瘤渗透性、更低的毒性(多肽通常由氨基酸组成,代谢产物毒性小)、生产过程更容易规模放大等优点。
由于PDC在靶向性和代谢稳定性等方面略逊色于ADC,因此未来PDC 技术改进的方向主要包括:(1)增强靶点识别特异性,目前主要是通过开发双靶PDC 或双环肽PDC;(2)改善药物药代动力学特征。
3
小分子偶联药物(SMDC)
小分子偶联药物(SMDC):是由小分子的靶向配体与细胞毒药物偶联所得,由三部分构成:小分子靶向配体、细胞毒分子和连接子,其作用机制与ADC 类似。但与ADC相比,SMDC能更快速均匀地分散到肿瘤组织中,且成本低、无免疫原性。
4
免疫刺激抗体偶联物(ISACs)
免疫刺激抗体偶联物(Immune-stimulating antibody conjugates, ISACs):和以上采用毒素为主要载荷的XDC不同,ISACs的最大特点是采用免疫激动剂/调节剂为载荷,通过让免疫激动剂在肿瘤微环境中定向释放,可激活免疫系统对肿瘤组织的免疫应答,杀伤肿瘤。
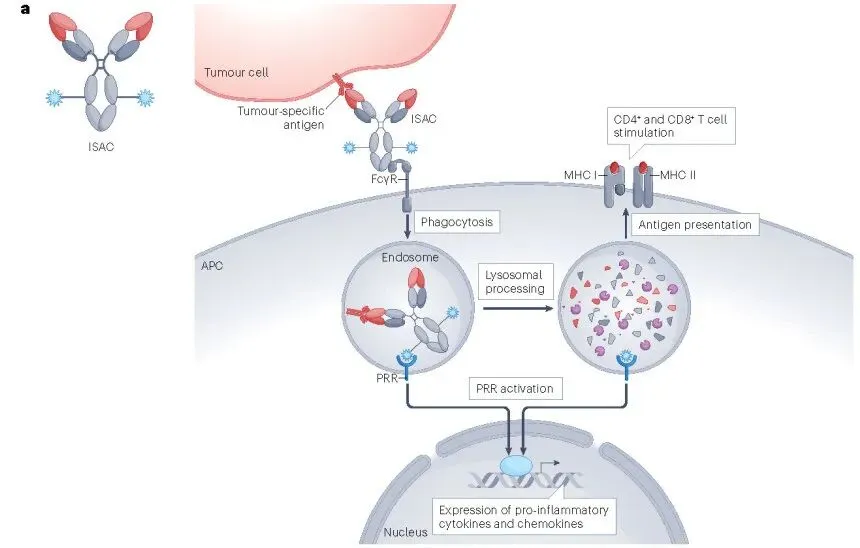
ISAC药物的作用机理
*资料来源:Tsuchikama K, Anami Y, Ha SYY, Yamazaki CM. Exploring the next generation of antibody-drug conjugates. Nat Rev Clin Oncol. 2024;21(3):203-223. doi:10.1038/s41571-023-00850-2
ISAC最主要的优点在于:可以通过诱导免疫记忆效应来实现持久的抗肿瘤效果并降低复发风险。但同时值得注意的是,这些药物在全身给药时,可能会因过度激活免疫系统而导致严重的不良反应,因此如何“在增强肿瘤特异性免疫应答的同时减少全身不良反应”是ISAC设计的核心挑战。
5
抗体-核酸偶联物(AOC)
抗体-核酸偶联物(Antibody-Oligonucleotide Conjugates,AOC):是一种新兴的生物药形式,其主要特点是以核酸药物(包括反义寡核苷酸(ASO)、siRNA、免疫激活型CpG片段、PMO(磷酰二胺吗啉代寡核苷酸)等)为有效载荷,通过定点偶联或非定点偶联在特定靶向性的抗体上。AOC的出现有助于解决核酸药物的一个长期存在的难题——“肝外递送局限性”。
由于核酸药物易被核酸酶降解、难以穿过细胞膜(因其负电荷特性),因此需要依赖特殊递送系统进行药物递送,而主流的递送系统GalNac仅可特异性递送至肝脏细胞,极大限制了核酸药物的治疗范围。AOC药物可利用抗体的特异性将核酸药物的治疗范围拓展至骨骼肌、中枢神经系统、肿瘤组织等肝脏以外部位,目前AOC已经开始了在罕见病、中枢神经系统疾病、肿瘤领域的探索。
6
定向降解抗体偶联药物(DAC)
定向降解抗体偶联物/降解剂抗体偶联药物(Degrader–antibody conjugates,DAC):是将抗体通过连接子与靶向蛋白降解剂(PROTAC 或分子胶)偶联起来的新分子模式。与ADC通过毒素小分子直接损伤肿瘤细胞不同,DAC在进入细胞后,释放出携带的PROTAC或分子胶来直接降解细胞质中的目标蛋白,从而为疾病患者提供了新型治疗策略,有望覆盖一些难以成药靶点和传统药物难以治疗的疾病。
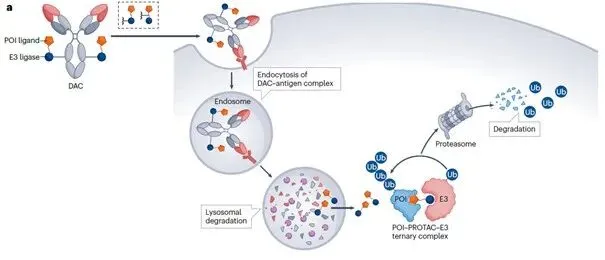
DAC药物的作用机理
*资料来源:Tsuchikama K, Anami Y, Ha SYY, Yamazaki CM. Exploring the next generation of antibody-drug conjugates. Nat Rev Clin Oncol. 2024;21(3):203-223. doi:10.1038/s41571-023-00850-2
目前,DAC的开发仍存在以下挑战:(1)DAC载荷疏水性较强,容易引发药物聚集;(2)DAC分子复杂度大幅提升,增加DAC的生产工艺复杂度和生产成本;(3)连接子释放技术的把控等。
7
总结
衍生XDC平台总结
XDC | 配体 | 连接子 | 载荷 | 特点 |
放射性核素偶连药物(RDC) | 抗体、多肽或小分子 | 不可裂解连接子+螯合剂 | 核素 | 诊疗一体化 |
多肽-药物偶联物(PDCs) | 多肽 | 可/不可裂解 | 多种载荷 | 强渗透性、低毒 |
小分子偶联药物(SMDC) | 小分子 | 可/不可裂解 | 多种载荷 | 更强渗透性 |
免疫刺激抗体偶联物(ISACs) | 肿瘤靶向抗体 | 不可裂解连接子 | 免疫激动剂/调节剂 | 诱导免疫反应抗肿瘤 |
抗体-核酸偶联物(AOC) | 抗体 | 可/不可裂解,无连接子 | 核酸 | 解决核酸药物肝外递送难题 |
定向降解抗体偶联药物(DAC) | 抗体 | 可/不可裂解 | PROTAC /分子胶 | 靶向降解目标蛋白 |
由于配体和载荷的多样性,XDC具有较大的拓展性和差异化空间。目前包括ADC在内的XDC技术已超过10 种,除了上文介绍过的几个热门方向外,其他还包括:抗体光敏剂偶联药物(APC)、抗体细胞偶联药物(ACC)、抗体生物聚合物偶联物(ABC)、核酸适体药物偶联物(ApDC)、病毒样颗粒药物偶联物(VDC)、“毒素+免疫激动剂”的免疫刺激双载荷ADC(iADC)等众多形式。
衍生技术XDC的出现,为多种药物类型构建了桥梁,形成了一种“药物互联”新范式,从而为全球带来了新型、多样化的产品组合和治疗方案,有望解决传统药物的部分难点、攻克难治性疾病、为临床需求尚未满足的患者提供新的治疗希望。
The End
注:本资料所载来源被认为是可靠的,但常旸基金不保障其准确性和完整性,相关分析推测可能会根据后续研究做出更改。
更多详细资料和最新投研观点,欢迎合格投资者与我司进行深入沟通!



