工信部人才中心统考发证——
3月14日药品质量体系工程师、药品数据管理工程师、药品验证工程师、药品研发工程师、实验室管理工程师、EHS管理工程师
3月28日药品合规审计官、CSV工程师、设备工程师、药物分析工程师、项目管理工程师
3月17日《PIC/S法规与中国GMP对质量系统要求的差异分析、检查重点与缺陷解析》
3月31日《新版GMP无菌药品附录的要求变化与应对策略要点解析专题培训》
3月20-21日广州《符合FDA、欧盟法规要求的质量体系实施关键点解析及进阶研修班》
3月20-21日成都+线上《药品企业审计关键模块要点解析及核心技能提升案例实操专题研修班》
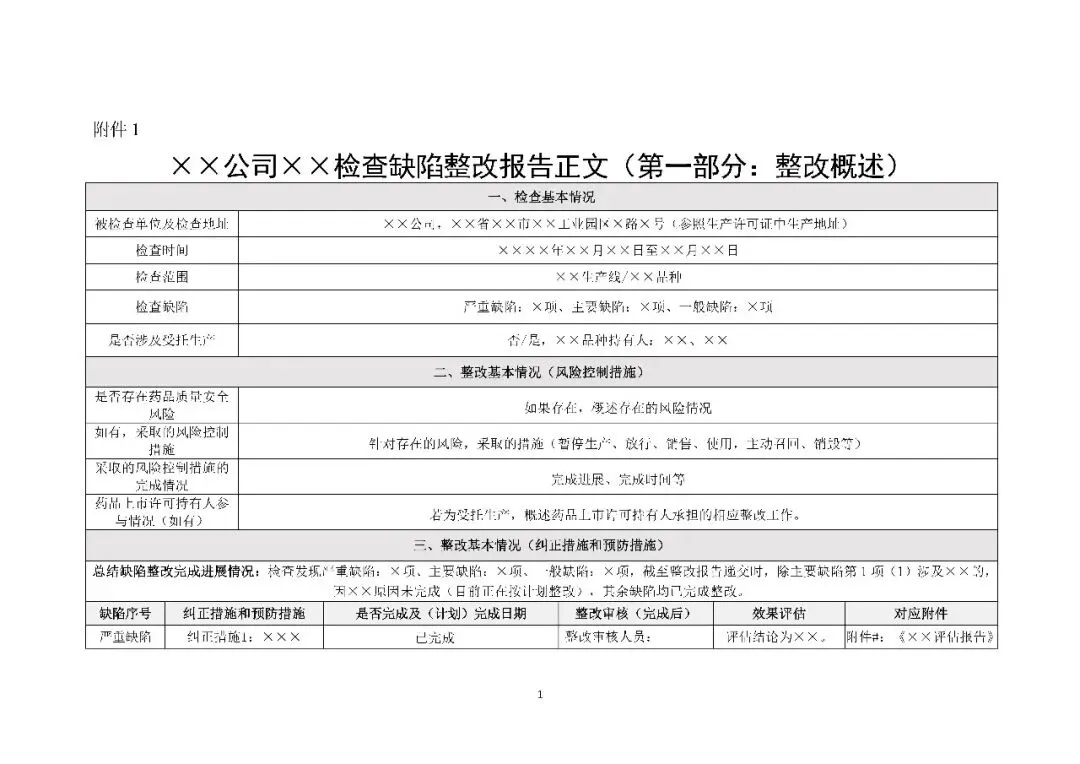
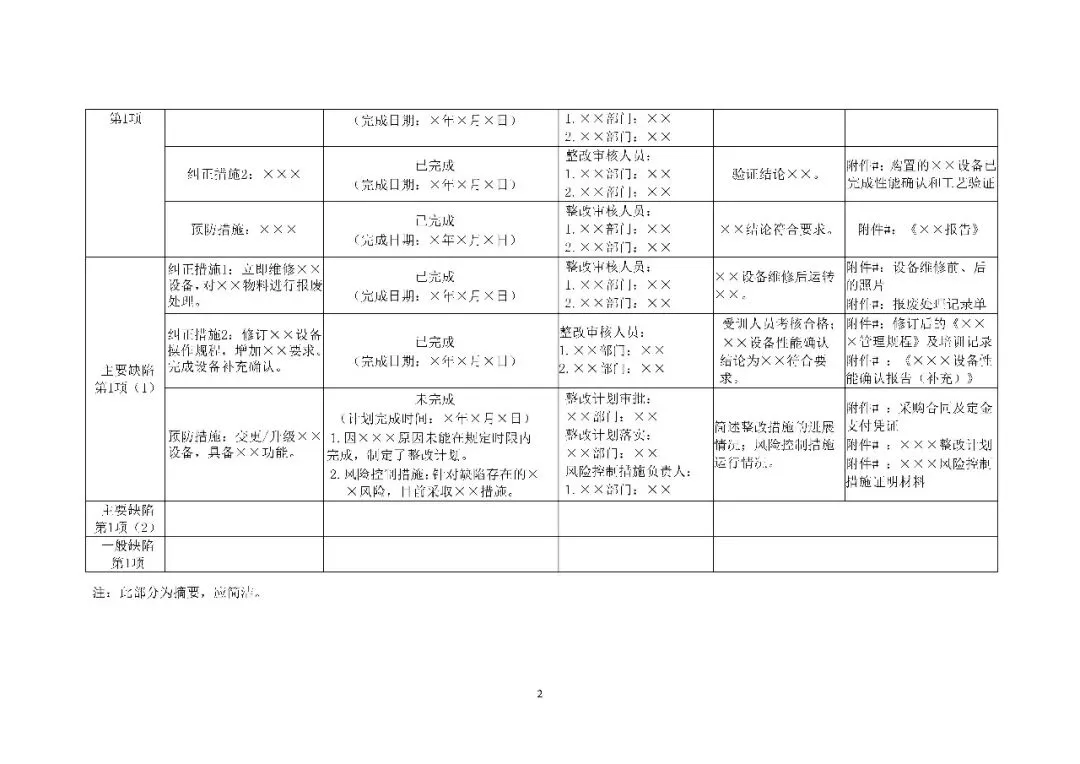
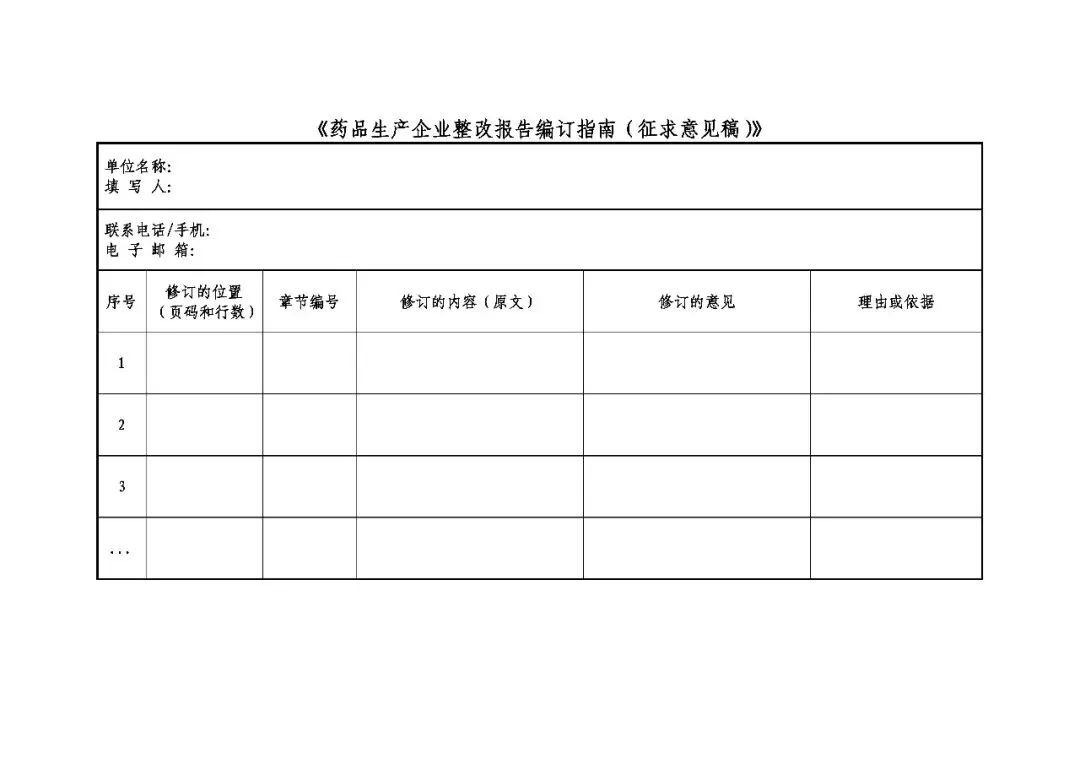
为规范和统一药品生产企业现场核查/检查缺陷整改报告的编订要求,提高企业编订和监管部门审核效率,督促企业强化质量风险闭环管理,持续完善质量管理体系,国家药监局核查中心组织起草了《药品生产企业整改报告编订指南(征求意见稿)》,现面向社会公开征求意见。
请于2026年3月27日前填写意见反馈表并发送电子邮件至liujx@cfdi.org.cn,邮件标题请注明“反馈意见-《药品生产企业整改报告编订指南(征求意见稿)》”。
感谢参与和支持。
国家药监局核查中心
2026年2月27日