科济药业是一家生物制药公司,专注于开发创新CAR-T细胞疗法,现拥有10款CAR-T管线产品,包含4款自体CAR-T和6款通用型CAR-T,均为自主研发且拥有全球权益。自体产品中,全人源BCMA自体CAR-T细胞产品赛恺泽®(泽沃基奥仑赛注射液)已在中国获批上市。公司的Claudin18.2自体人源化CAR-T产品舒瑞基奥仑赛注射液(CT041)是全球第一款递交新药上市申请的实体瘤CAR-T产品。除自体产品外,科济药业还在推进多款差异化的通用型CAR-T细胞产品开发。
CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy 嵌合抗原受体 T 细胞免疫疗法),一种通过基因工程技术改造患者自身 T 细胞,使其表达能精准识别并杀伤肿瘤细胞的嵌合抗原受体(CAR),再回输体内的个体化精准细胞免疫治疗,是血液瘤疗效天花板和单次给药即可“治愈”的代名词。
CycloCAR技术 :增强实体瘤疗效
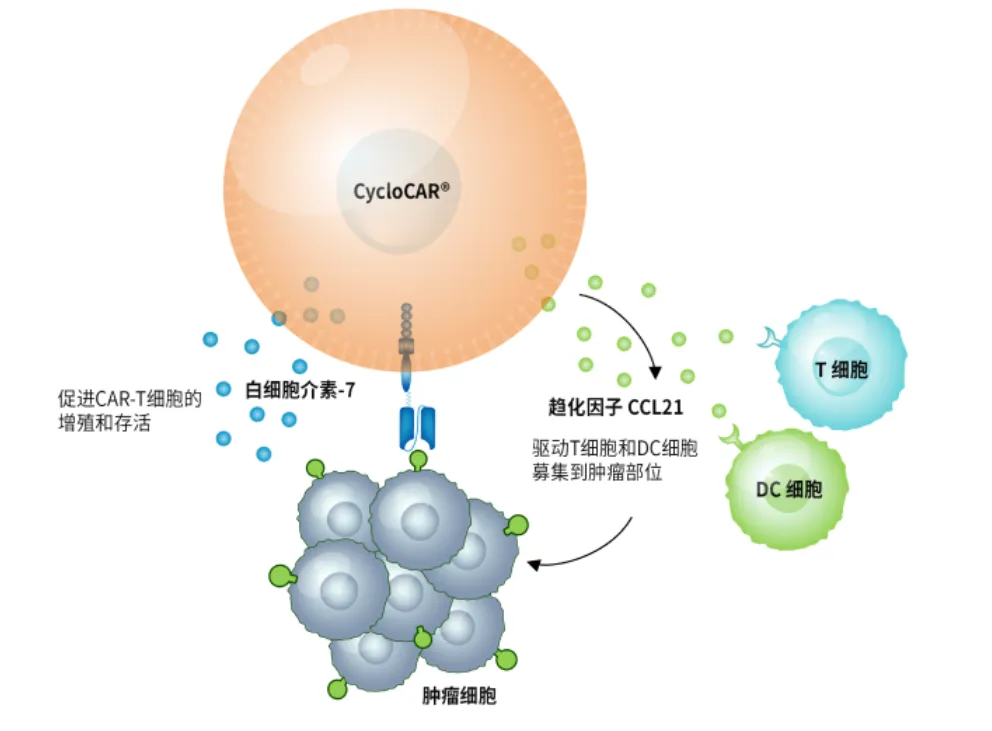
CycloCAR® T细胞,通过设计表达细胞因子IL-7(白介素-7)和趋化因子CCL21,有望显著增强针对实体瘤CAR-T细胞的疗效。T细胞的募集、存活和增殖是CAR-T细胞疗法在实体瘤治疗中的重要限制。IL-7 作为一种细胞因子,可以增强CAR-T细胞的增殖和存活,而 CCL21作为一种趋化因子,可以驱动淋巴细胞和树突状细胞募集到肿瘤部位。
在体内研究中,在三种实体瘤模型并且是无需环磷酰胺预处理的条件下,CycloCAR® T细胞显示出优于传统CAR-T细胞或7x19 CAR-T细胞(共表达IL-7和CCL19)的优越治疗效果。
CycloCAR® T细胞还可以抑制具有异质抗原表达的肿瘤组织的生长,甚至可以诱导肿瘤的完全缓解。从机制上讲,IL-7 和 CCL21 显著改善了肿瘤中CAR-T细胞和树突状细胞的存活和浸润。此外,免疫组化证实CCL21还可以抑制肿瘤的血管生成。
THANK-uCAR技术 :差异化的通用型CAR-T,增强CAR-T细胞的增殖和持久性
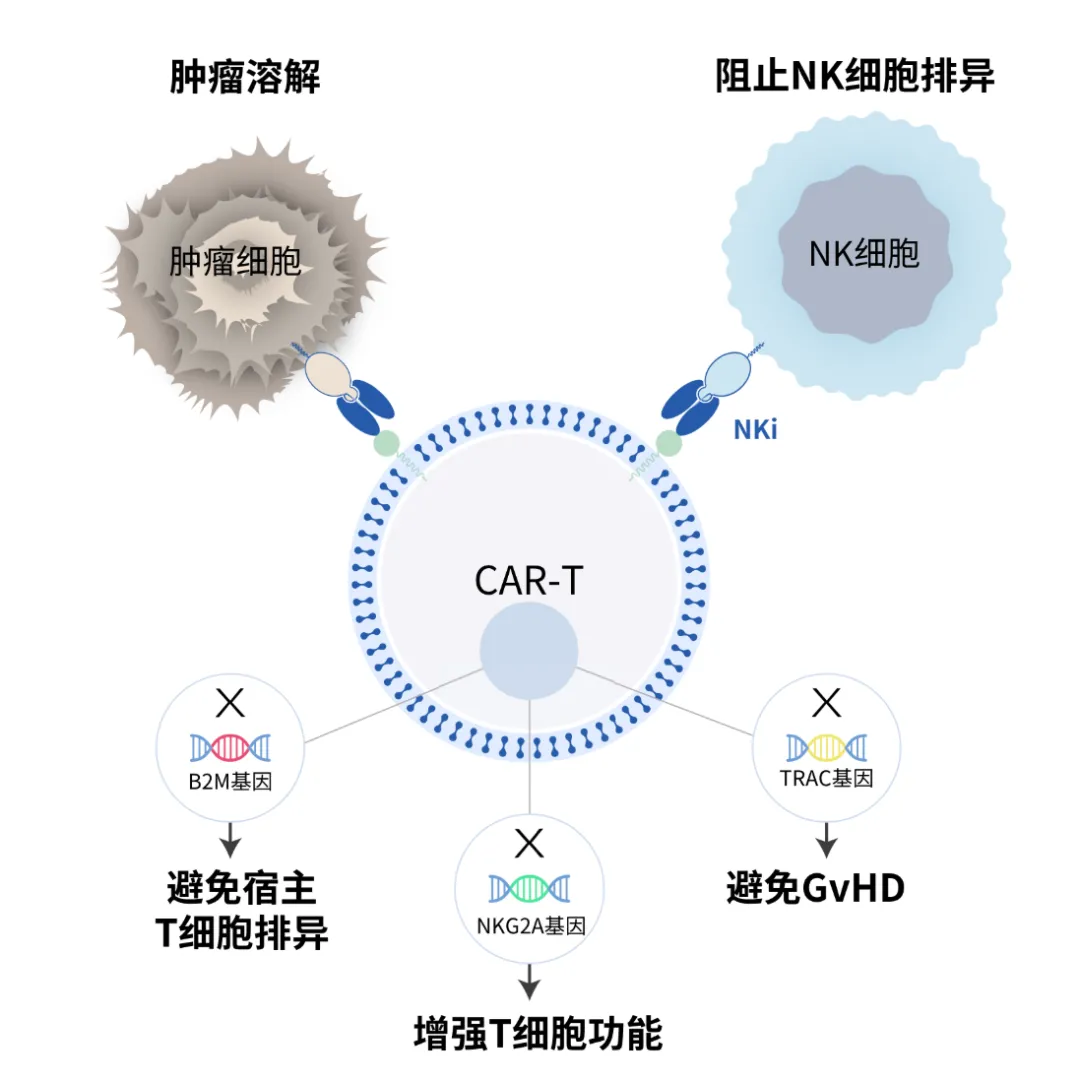
通用型的 CAR-T 技术普遍存在的问题是宿主抗移植物反应。为了避免宿主 T 细胞对于同种异体 CAR-T 细胞的排异,通常会敲除 B2M 基因。但是,缺乏 B2M 基因的同种异体 CAR-T细胞会被宿主的 NK 细胞排异,导致同种异体 CAR-T 细胞的增殖和持久性降低。为了解决这个问题,公司研发了THANK(Target to Hinder the Attack of NK细胞)-uCAR®技术,将一种识别 NK 细胞表面蛋白-NKG2A 的 CAR 被装载到同种异体 CAR-T 细胞中,用来阻止宿主 NK 细胞的攻击,增强CAR-T细胞的增殖和持久性。临床前数据表明,在 NK 细胞存在的情况下,THANK-uCAR T细胞比 TCR/B2M 双除同种异体 T 细胞能更好地存活和增殖。
LADAR技术 :精确靶向的多功能平台
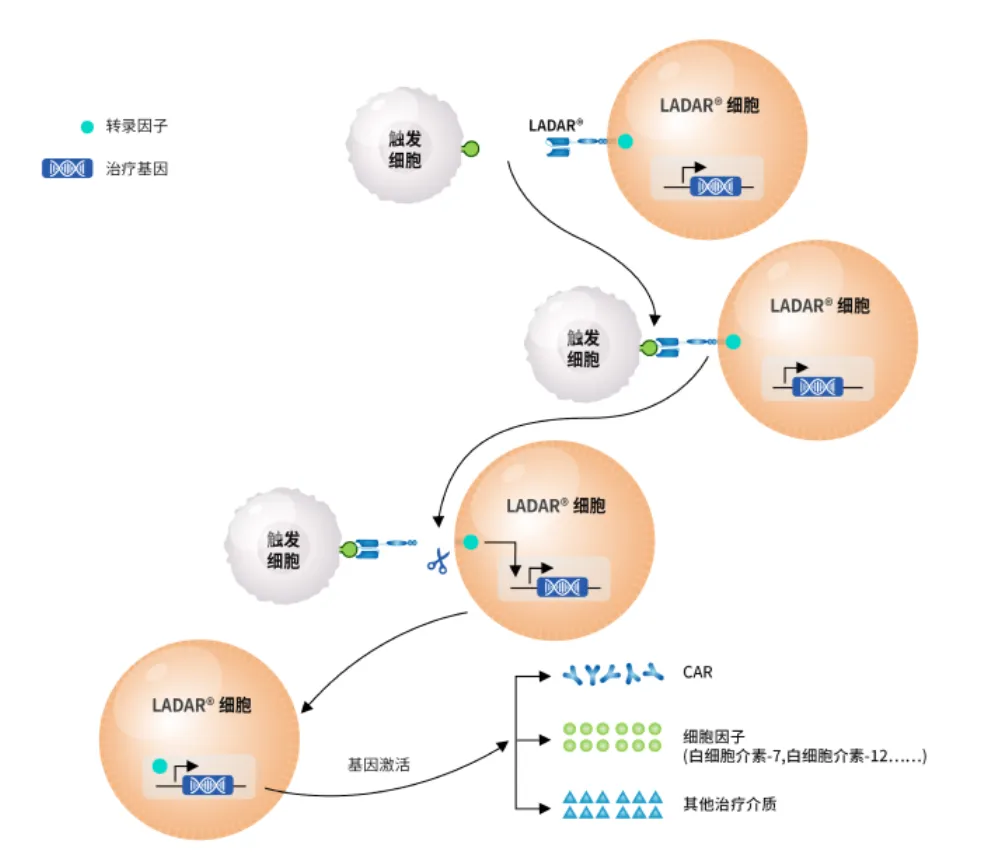
为了探索提高 CAR-T 细胞疗法药物靶点可及性,公司开发了 LADAR 技术,其目的基因的细胞内转录由嵌合调节抗原受体控制,通过 LADAR 人工受体,只有当细胞外结构域与特定抗原结合而激活时,才会触发细胞内活动,从而有可能精确控制免疫细胞对癌细胞发挥作用的时间和位置。
大多数肿瘤相关抗原也在正常组织中表达,这对包括免疫细胞疗法在内的靶向治疗的发展提出了巨大挑战。为了解决靶向可用性方面的挑战,我们继续探索创新技术,以提高药物靶点可用性,从而使不可成药的靶点成为可成药靶点。我们开发了LADAR®技术,其中目标基因的细胞内转录由一个人工受体控制,该受体在细胞内结构域中含有转录因子。一旦LADAR®受体的胞外结构域与触发抗原(发送者抗原)结合,转录因子就会被切割并转移到细胞核,从而触发目标基因的表达。目的基因可能是嵌合抗原受体(CAR)、细胞因子或任何需要的治疗介质。
LADAR-CAR通路需要用于LADAR®的发送者抗原和用于CAR识别的目标抗原的同时存在,以杀死目标细胞,从而减少在同一正常组织中不同时表达这两种抗原的在靶脱瘤毒性。在我们的体外研究中,LADAR®系统触发抗原结合时诱导了强烈的基因表达,在没有触发抗原的情况下几乎没有泄漏表达。