EICR研究报告:运动诱导单核细胞来源巨噬细胞组蛋白乳酰化改善脓毒症相关心肌病
Nature communications:运动诱导单核细胞来源巨噬细胞组蛋白乳酰化改善脓毒症相关心肌病出处:Sun S, Lai C, Huang C, et al. Exercise-induced histone lactylation in monocyte-derived macrophages restores cardiac immune homeostasis and function in sepsis-induced cardiomyopathy. Nat Commun. 2025;17(1):756.
作者介绍:
尚敏研究员,浙江大学医学院,博士生导师。长期从事免疫细胞代谢与组织重塑及临床转化研究。积极的生活方式可预防心血管疾病,但其在调节心脏免疫环境并维持心功能方面的机制仍不清楚。
本研究在运动干预的雄性小鼠中鉴定出一类单核细胞来源的心脏巨噬细胞亚群,命名为 iNOS⁺Arg1⁺ 巨噬细胞,其同时表达促炎与促修复相关基因。在该亚群中抑制促炎因子 iNOS 或促修复因子 Arg1,均可抵消运动诱导的心功能维持效应。
机制上,运动增强单核细胞的糖酵解,提高乳酸生成,并诱导 H3K18 位点的组蛋白乳酰化;该过程由 p300 作为相关乳酰转移酶介导,并受 HDAC2 作为去乙酰化酶的拮抗调控。H3K18la 加速心脏巨噬细胞向促修复状态转变,从而恢复免疫稳态并维持心功能。
值得注意的是,与缺乏运动人群相比,体力活动个体的人外周血单核细胞中 Pan-Kla 与 H3K18la 水平均升高。重要的是,采用高组蛋白乳酰化单核细胞进行回输可恢复脓毒症诱导心肌病的心功能,这可能转化为一种具有前景的心肌病治疗策略。
脓毒症是重症监护病房(ICU)死亡的主要原因之一,其特征为宿主感染触发的多器官功能障碍¹˒²。脂多糖(lipopolysaccharide, LPS)是一种来源于革兰阴性菌的强效内毒素,在脓毒症及其相关器官衰竭的发病机制中起关键作用³–⁵。在脓毒症患者中,多达 60% 会出现心功能障碍⁶,被称为脓毒症诱导心肌病(sepsis-induced cardiomyopathy, SICM)。SICM 的临床表现为射血分数降低、左心室扩张以及早期可逆的心肌功能障碍⁷–⁹。值得注意的是,SICM 是多器官功能障碍的重要促成因素,并显著影响脓毒症患者的预后与死亡率;与无心功能障碍的脓毒症患者相比,其死亡率约高出 3 倍¹⁰˒¹¹。
心脏免疫稳态在逆转脓毒症应激后的心肌功能障碍并促进心脏康复中起关键作用⁵˒¹²,而巨噬细胞是脓毒症心脏中募集的主要免疫细胞⁵。巨噬细胞具有高度可塑性与异质性,不同亚群在不同免疫环境调控下呈现差异化功能¹³–¹⁶。我们及其他研究者此前表明,代谢重编程可协同调控募集性巨噬细胞在肿瘤、肌肉退行性变及脓毒症等状态下执行细胞碎片清除与组织重塑等关键功能¹⁵–¹⁸。因此,阐明巨噬细胞亚群及其诱导信号,可能为恢复脓毒症心脏的心脏稳态提供策略。规律体力运动可减轻与多种炎症相关疾病相关的代谢与免疫学适应性改变¹⁹˒²⁰,从而对心血管疾病(cardiovascular diseases, CVD)和肿瘤产生保护作用²¹–²³。规律运动可动员并重新分布自然杀伤(natural killer, NK)细胞以抑制肿瘤生长²⁴。此外,运动可降低造血祖细胞增殖与白细胞生成,从而减少动脉粥样硬化中的炎症并改善结局²⁵。规律体力运动对免疫系统²⁶–²⁸及 CVD 进展²²˒²⁹˒³⁰的有益影响已得到充分研究。然而,体力运动对心脏免疫图谱的影响仍有待进一步阐明。因此,我们研究自愿跑轮是否以及如何通过“预训练”心脏巨噬细胞,使其预先适应并在脓毒症中保护心功能。本研究发现,自愿跑轮可在脓毒症中维持心功能并保持免疫稳态。为探究运动如何调控 SICM 中的心脏免疫细胞,我们构建了心脏免疫单细胞图谱,为识别可模拟运动获益的 SICM 治疗策略提供了有价值的资源。其免疫调节获益归因于组蛋白赖氨酸乳酰化(histone lysine lactylation, Kla),尤其是 H3K18la;该修饰分别由 p300 与 HDAC2 作为乳酰转移酶与去乳酰化酶介导。运动诱导的乳酸触发H3K18la,有效地在 SICM 中使单核细胞来源的巨噬细胞在进入心脏募集之前即完成对脓毒症的预适应。最后,通过回输经乳酸“预处理”的单核细胞,我们证明该策略可在 SICM 中维持心功能,为利用运动的心脏保护效应提供一种潜在的细胞治疗途径。规律体力运动通过调控心脏免疫微环境保护 SICM 中的心功能
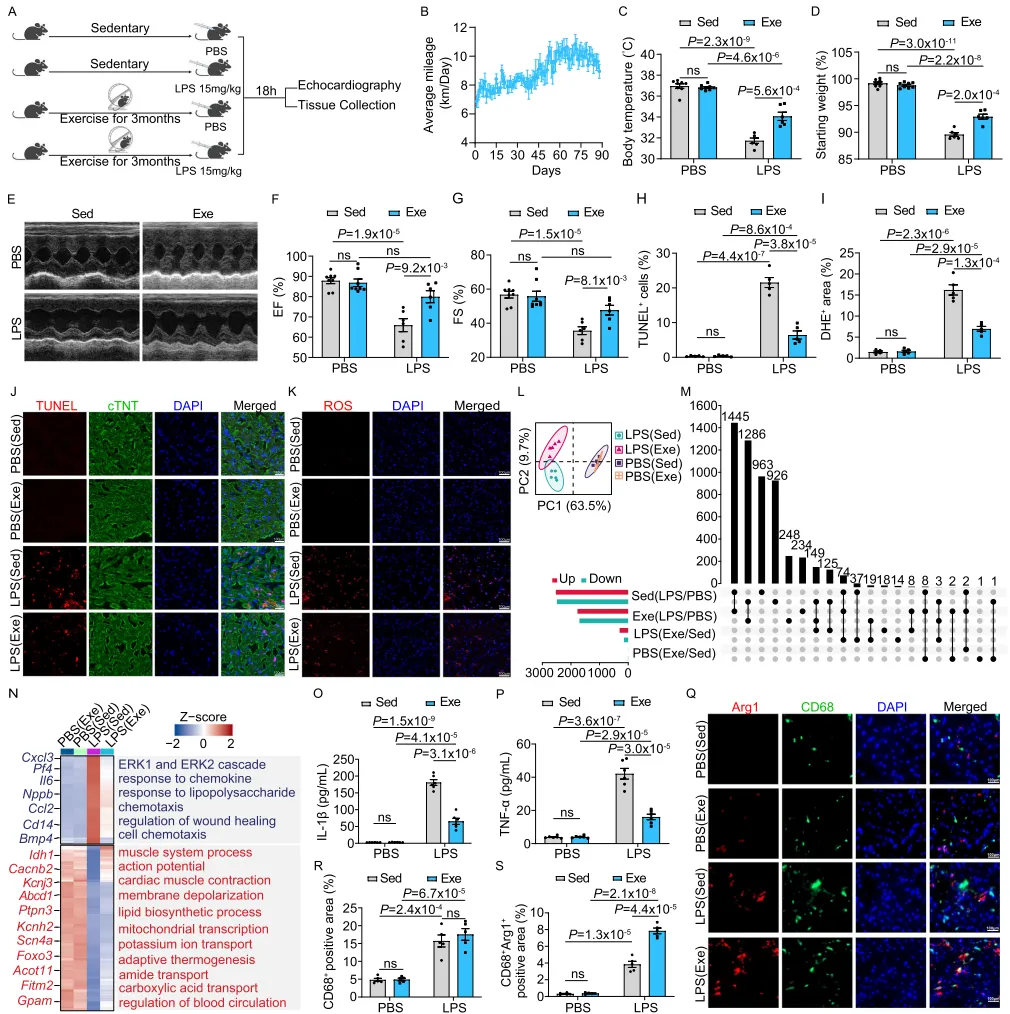
为评估规律体力运动对脓毒症心功能的影响,我们为小鼠提供跑轮进行自愿运动 3 个月。随后,向缺乏运动(Sed)与运动(Exe)组小鼠腹腔注射脂多糖(LPS)或等体积磷酸盐缓冲液(PBS),以模拟内毒素性脓毒性休克并诱导脓毒症诱导心肌病(SICM)(图 1A、B)。我们的观察显示,规律运动可抵御 LPS 诱导的脓毒症,其表现为注射后 18 h 体温与体重下降幅度减小(图 1C、D)。尽管 LPS 注射损害了缺乏运动小鼠的心功能,运动小鼠仍保持心功能相对完整,射血分数(EF)与缩短分数(FS)分别提高约 21% 与 34%(图 1E–G)。一致地,TUNEL 与二氢乙啶(DHE)染色显示,SICM 小鼠在运动条件下心脏细胞凋亡与氧化损伤减少(图 1H–K)。相反,在 PBS 对照组中,Sed 与 Exe 小鼠的体温、体重与心功能相当(图 1C–K)。综上,自愿跑轮可在脓毒症过程中维持心功能。
为阐明规律运动在脓毒症期间保护心功能的机制,我们对 PBS(Sed)、PBS(Exe)、LPS(Sed)与 LPS(Exe)小鼠的左心室进行 bulk RNA 测序分析。主成分分析(PCA)显示,与 PBS 对照组相比,SICM 组中的运动诱导转录变化更为显著(图 1L)。差异表达基因(DEG)分析发现,LPS(Exe)与 LPS(Sed)之间共有 447 个 DEGs,而 PBS(Exe)与 PBS(Sed)之间仅有 14 个 DEGs(图 1M)。在这 14 个 DEGs 中,2 个基因(Marco、Gbp11)被运动上调,12 个基因(Cd300lf、Fgr、Mmp8、Ccl22、Vwa3b、Cd177、Hspa1a、Hsd11b2、Slc7a11、Fndc7、Nr4a3、Mcemp1)被运动下调(图 1M)。相较之下,在 SICM 中受运动影响的 447 个 DEGs 里,运动抑制了 111 个由 SICM 上调的基因(包括 Cxcl3、Il6、Ccl2 与 Cd14),这些基因主要参与趋化因子反应、趋化作用与细胞趋化等通路;另一方面,运动激活了 274 个由 SICM 下调的基因,其中包括与动作电位、心肌收缩、脂质生物合成过程等相关的基因(图 1N)。这些发现提示,规律运动可减轻 SICM 引发的过度免疫激活,同时恢复被 SICM 扰乱的、与心功能相关的转录通路。为进一步验证这一点,我们测定血清 IL-1β 与 TNF-α 浓度,发现体力运动可有效减弱 LPS 诱导的促炎反应(图 1O、P)。尽管 CD68⁺ 巨噬细胞总浸润量未发生改变,但运动脓毒症心脏中的 Arg1⁺ 促修复巨噬细胞较缺乏运动脓毒症心脏增加 104%(图 1Q–S)。这些结果提示,规律运动在脓毒症期间的心脏保护效应很可能归因于其对心脏免疫微环境的调控。图 1|规律体力运动通过调控心脏免疫微环境保护 SICM 中的心功能小鼠处理流程示意图(A)及平均自愿跑轮距离(km/日)(B)。本分析共纳入 14 只小鼠。图由 BioRender 制作,Shang, M.(2025)tc3zfga。缺乏运动(Sed;PBS 组 n = 8,LPS 组 n = 6)与运动(Exe;PBS 组 n = 8,LPS 组 n = 6)小鼠在腹腔注射 PBS 或 LPS 后 18 h 的体温(C)及体重变化百分比(D)。代表性超声心动图图像(E)及 PBS 或 LPS 腹腔注射后 18 h 的射血分数(EF%)(F)与缩短分数(FS%)(G)定量分析;Sed(PBS 组 n = 8,LPS 组 n = 6)与 Exe(PBS 组 n = 8,LPS 组 n = 6)。心脏切片中 TUNEL(H、J)与二氢乙啶(DHE)(I、K)的代表性图像及定量结果:Sed(PBS 组 n = 5,LPS 组 n = 5)与 Exe(PBS 组 n = 5,LPS 组 n = 5),均为腹腔注射 PBS 或 LPS 后 18 h;实验展示 3 次独立重复实验中的代表性结果。PBS(Sed)、PBS(Exe)、LPS(Sed)与 LPS(Exe)组转录组的主成分分析(PCA)(L)。Upset 图显示 LPS(Sed)与 PBS(Sed)、LPS(Exe)与 PBS(Exe)、LPS(Exe)与 LPS(Sed)、PBS(Exe)与 PBS(Sed)各比较中差异表达基因(DEGs)的数量及重叠情况(M)。差异表达模式热图(N):上方标示不同组别样本,并展示代表性基因及其相关 GO 术语。ELISA 检测 Sed 与 Exe 小鼠血清 IL-1β(O)与 TNF-α(P);每组分析 6 份样本。浸润巨噬细胞(CD68⁺)(R)与 CD68⁺Arg1⁺ 细胞(S)的定量,以及相应处理条件下小鼠心脏中 CD68(绿色)与 Arg1(红色)免疫荧光染色的代表性图像(Q)。比例尺 = 100 µm(J、K、Q)。为进一步表征运动脓毒症心脏的免疫微环境,且鉴于 PBS(Sed)与 PBS(Exe)组间差异有限,我们从 PBS(Sed)、LPS(Sed)与 LPS(Exe)小鼠中分离 CD45⁺ 细胞群,并使用 10X Genomics 平台进行单细胞 RNA 测序(scRNA-seq)分析(图 2A)。共有 50,471 个通过质控的细胞用于后续分析,产生 40,892 个 CD45⁺ 细胞与 19,184 个表达基因(表 S1)。无偏聚类分析揭示了 13 个不同的心脏免疫细胞簇,包括巨噬细胞(Adgre1、C1qa)、单核细胞(Plac8、Ly6c2)、常规树突状细胞(cDC;Cd209a、Fscn1)、浆细胞样树突状细胞(pDC;Siglech)、中性粒细胞(Mmp9、Csf3r)、自然杀伤(NK)细胞(Nkg7、Klrb1c)、CD4⁺ 与 CD8⁺ T 细胞(Cd3g、Cd4、Cd8a)、γδT(gdT)细胞(Trdc、Trdv4)、B 细胞(Cd79a、Cd19)、2 型固有淋巴样细胞(ILC2;Gata3、Rora)、肥大细胞(Gata2、Mcpt8)以及增殖细胞(Mki67、Stmn1)(图 2B、C)。与既往研究一致¹²,脓毒症诱导单核细胞与中性粒细胞浸润心脏(图 2D、E)。重要的是,规律体力运动显著增强了脓毒症心脏中的单核细胞浸润(图 2F)。基于 bulk RNA 测序数据的免疫浸润分析与上述观察一致,并进一步显示 PBS(Sed)与 PBS(Exe)组之间无显著差异(图 S1)。综上,这些数据提示,规律体力运动可能通过调控脓毒症心脏中的单核细胞来源巨噬细胞,从而重塑心脏免疫微环境。
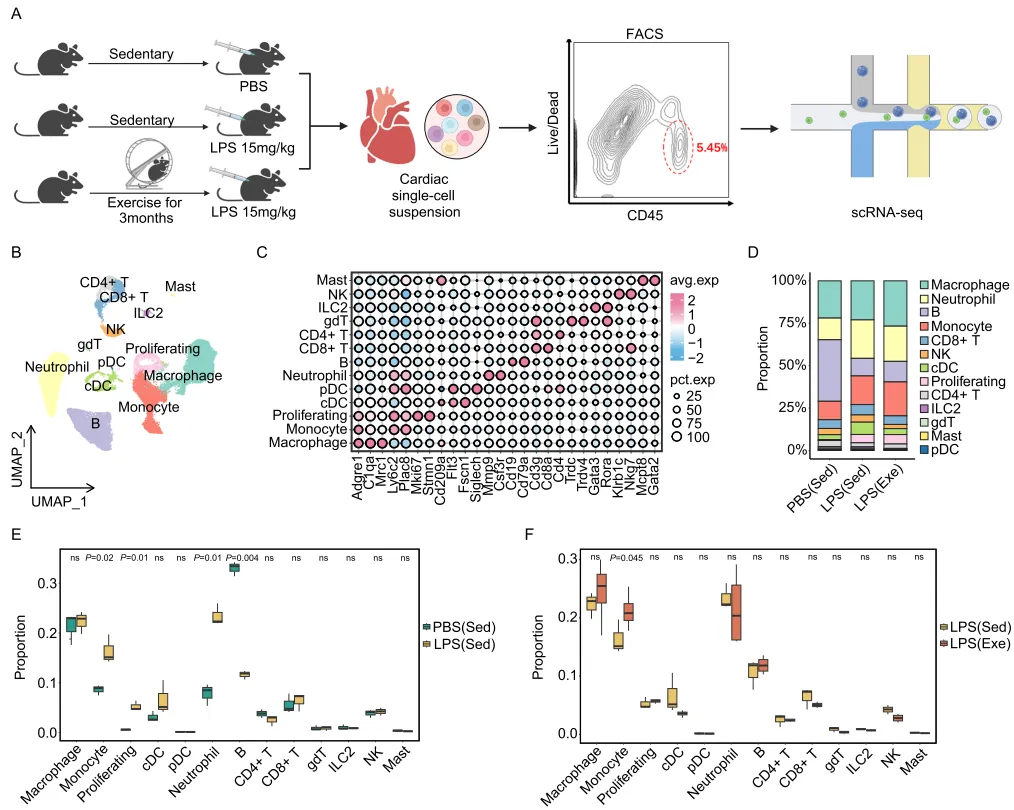
图 2|自愿跑轮重塑脓毒症心脏免疫微环境
用于分析从 C57BL/6 小鼠心脏左心室分离的 CD45⁺ 免疫细胞的 10X Chromium 单细胞 RNA 测序(scRNA-seq)工作流程示意图(A)。小鼠分为缺乏运动(Sed)或运动(Exe)并接受 PBS 或 LPS 的腹腔注射。图由 BioRender 制作,Shang, M.(2025)ly8ygbn。展示 40,892 个心脏免疫细胞的统一流形近似与投影(UMAP)图,并按细胞类型着色(B)。点图显示各细胞群中相对于其他已鉴定细胞群的高表达代表基因(C)。各组中鉴定到的不同细胞群比例(D)。箱线图比较 PBS(Sed)与 LPS(Sed)之间(E),以及 LPS(Sed)与 LPS(Exe)之间(F)免疫细胞群比例差异。纳入分析的样本量:PBS(Sed)n = 3;LPS(Sed)n = 3;LPS(Exe)n = 4。
自愿跑轮调控 SICM 中的心脏单核细胞与巨噬细胞亚群
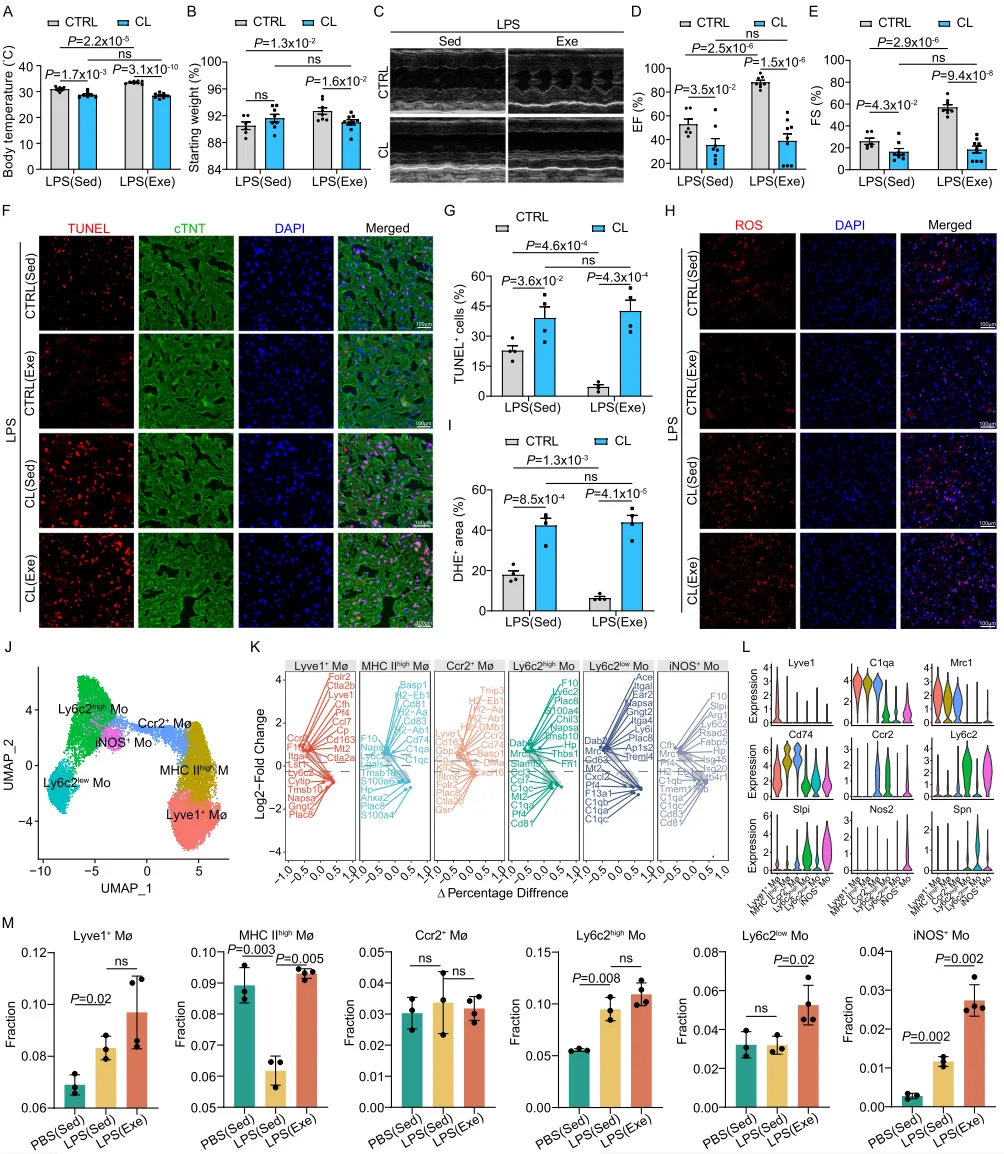
鉴于单核细胞与巨噬细胞群体几乎占脓毒症心脏全部免疫细胞的一半,我们将研究重点放在这两类细胞上,以理解自愿跑轮在 SICM 期间如何影响其募集与功能。我们首先使用氯膦酸二钠脂质体(clodronate liposomes)¹³¹–³³清除单核细胞与巨噬细胞区室,从而评估其在规律运动所赋予的心脏保护中的作用。与我们先前的观察一致,运动可减轻脓毒症期间的体重下降、维持体温并保护心功能。值得注意的是,当单核细胞与巨噬细胞被清除后,这些有益效应被完全消除,清除后 LPS(Sed)与 LPS(Exe)小鼠之间不再存在显著差异(图 3A–E)。此外,单核细胞与巨噬细胞清除也消除了先前在自愿跑轮小鼠中观察到的脓毒症心脏细胞凋亡与氧化损伤降低(图 3F–I)。总体而言,我们的数据表明,单核细胞与巨噬细胞对于规律运动在 SICM 中提供的心脏保护是必需的。
为进一步阐明单核细胞与巨噬细胞对 SICM 中心脏免疫稳态的贡献,我们进行二次聚类分析,并基于亚群特征基因与经典标志物³⁴–³⁷鉴定出 6 个亚群。其中包括 2 个单核细胞簇与 3 个巨噬细胞簇:Ly6c2^low Mo、Ly6c2^high Mo、Lyve1⁺ Mø(Lyve1⁺MHC II^lowCcr2⁻)、MHC II^high Mø(Lyve1⁻MHC II^highCcr2⁻)以及 Ccr2⁺ Mø(Lyve1⁻MHC II^highCcr2⁺)(图 3J)。基于 Ly6c2 表达水平,单核细胞被分为促炎单核细胞(Ly6c2^high Mo)与抗炎单核细胞(Ly6c2^low Mo)。Lyve1⁺ Mø 主要依赖自我更新,MHC II^high Mø 部分由单核细胞补充,而 Ccr2⁺ Mø 则完全由单核细胞补充(图 3J–L)。重要的是,我们鉴定出一个与 Ly6c2^high Mo 相邻的亚群,其特征为表达 iNOS(iNOS⁺ Mo)。有趣的是,该亚群在脓毒症心脏中同时表达促炎与促修复基因,如 Slpi、Arg1 与 Fabp5(图 3K)。关键在于,这一单核细胞来源的 iNOS⁺ 亚群在脓毒症心脏中显著升高,并可被体力运动进一步诱导(图 3M;图 S2)。比较不同组间各亚群相对比例时,我们观察到脓毒症心脏中 Lyve1⁺ Mø 显著升高而 MHC II^high Mø 显著降低;然而规律体力运动可抵消这一下降,将 MHC II^high Mø 水平恢复至正常(图 3M)。此外,我们还在心脏组织中鉴定出不同的树突状细胞(DC)与 T 细胞亚群(图 S3、S4),并进行细胞间通讯分析,以理解运动如何调控脓毒症心脏免疫细胞间的相互作用与共调控(图 S5)。综上,这些发现提示,规律运动可调控单核细胞与巨噬细胞亚群的分化与组成,从而在 SICM 中保护心功能。图 3|自愿跑轮调控 SICM 中的心脏单核细胞与巨噬细胞亚群缺乏运动(Sed)与运动(Exe)小鼠在使用氯膦酸二钠脂质体(clodronate liposomes)或对照脂质体(CTRL)进行巨噬细胞清除后,于 LPS 腹腔注射 18 h 记录体温(A)与体重变化百分比(B)。纳入分析的样本量:Sed(CTRL,n = 6;CL,n = 8),Exe(CTRL,n = 8;CL,n = 9)。代表性超声心动图图像(C)及 LPS 腹腔注射后 18 h 的射血分数(EF%)(D)与缩短分数(FS%)(E)定量结果:Sed 与 Exe 小鼠均为氯膦酸二钠脂质体或 CTRL 处理。纳入分析的样本量:Sed(CTRL,n = 6;CL,n = 8),Exe(CTRL,n = 8;CL,n = 9)。LPS 腹腔注射后 18 h,心脏切片中 TUNEL(F、G)与二氢乙啶(DHE)(H、I)的代表性图像及定量分析:每组分析 4 份样本,来自 3 次独立重复实验。展示 14,767 个单核细胞-巨噬细胞并划分为 6 个亚群的 UMAP 图(J)。火山图突出显示各单核细胞-巨噬细胞亚群相对于其他亚群表达最高与最低的前 10 个基因(K)。经典单核细胞-巨噬细胞标志基因在各亚群中的表达水平(L),纵轴为归一化表达值。箱线图显示不同处理条件下单核细胞-巨噬细胞亚群比例差异(M)。纳入分析的样本量:PBS(Sed)n = 3;LPS(Sed)n = 3;LPS(Exe)n = 4。比例尺:100 µm(F、H)。规律运动诱导单核细胞来源的 iNOS⁺ 亚群以保护脓毒症心功能
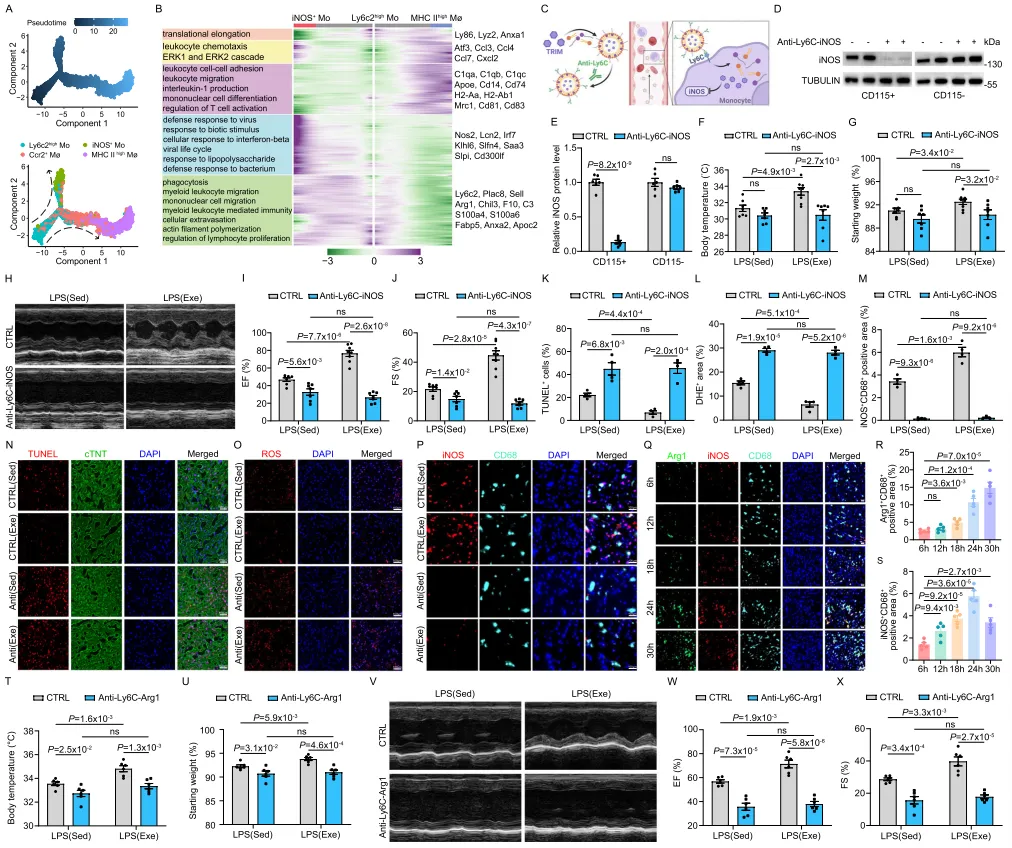
考虑到 Ccr2⁺ Mø 与 MHC II^high Mø 的补充分别完全或部分依赖 Ly6c2^high Mo 的分化,我们使用 Monocle2 算法进行拟时序分析以推断分化轨迹。结果显示,Ly6c2^high Mo 位于拟时序轨迹起始端,而 MHC II^high Mø 与 iNOS⁺ Mo 位于终末端(图 4A)。随后,我们沿 MHC II^high Mø 与 iNOS⁺ Mo 两条谱系对基因表达进行建模,鉴定出 5 组具有特定表达模式的基因集。对各模式代表基因及其功能富集分析显示:在 Ly6c2^high Mo 向 MHC II^high Mø 分化过程中,与白细胞介素-1 生成、T 细胞激活调控及白细胞迁移相关的基因逐渐上调;在 Ly6c2^high Mo 分化早期及向 iNOS⁺ Mo 转变过程中,与吞噬作用、肌动蛋白丝聚合及淋巴细胞增殖调控等功能相关基因处于活跃状态。同时,调控抗炎与促修复功能的基因(如 Arg1、Fabp5)持续表达。值得注
意的是,分化为 iNOS⁺ Mo 时与抗菌相关的功能显著激活(图 4B),提示该细胞类型在心脏脓毒症中可能具有“前线”作用。
为阐明 iNOS⁺ 单核细胞在 SICM 中的作用,我们设计了一种靶向纳米抑制剂:利用小分子抑制剂 TRIM,特异性抑制 Ly6C⁺ 单核细胞中的 iNOS(图 4C)。TRIM 被包封于由 PEG-DSPE 与 DSPE-PEG-NHS 构建的脂质体核心,并在脂质体表面接枝靶向 Ly6C 的抗体以实现精准单核细胞靶向。该靶向纳米抑制剂呈单分散粒径分布,粒径为 93.12 nm,且具有规则球形形态(图 S6A–C)。其载药量与抗体接枝量分别为 38.53% 与 2.13%。此外,通过监测颗粒长期粒径变化评估其稳定性,结果显示随时间推移未见明显解体(图 S6D)。Western blot 分析证实该纳米颗粒可有效抑制单核细胞 iNOS 表达(图 4D、E)。与既往研究提示“心脏损伤早期缺乏炎症性巨噬细胞会导致凋亡心肌细胞累积并损害修复”³⁸–⁴¹一致,我们观察到抑制单核细胞 iNOS 可消除运动在脓毒症期间降低体温下降与体重丢失的有益效应(图 4F、G)。与此前一致,体力活动可维持心功能(图 4H–J);然而,抑制单核细胞 iNOS 会消除运动对脓毒症诱导心肌损伤的保护作用。有趣的是,与对照小鼠相比,在缺乏运动小鼠中抑制单核细胞 iNOS 甚至加重了 LPS 诱导的心功能障碍。该效应亦与运动小鼠中先前观察到的心肌细胞凋亡与氧化损伤下降被抵消相一致(图 4K–P)。进一步对 SICM 期间心脏巨噬细胞进行时间序列分析显示,巨噬细胞存在由 iNOS⁺ 向 Arg1⁺ 的转变(图 4Q–S),且运动似乎加速该转变(图 1Q–S 及图 4M、P–S)。为进一步研究 SICM 中单核细胞 Arg1 的作用,我们使用上述纳米颗粒特异性抑制 Ly6C⁺ 单核细胞中的 Arg1(图 4C 与图 S6E–G)。单核细胞 Arg1 抑制消除了运动在降低体温下降、体重丢失、IL-1β 与 TNF-α 水平以及脓毒症诱导心肌损伤方面的保护效应(图 4T–X 与图 S6H–K)。此外,先前观察到的心脏巨噬细胞由 iNOS⁺ 向 Arg1⁺ 加速转变也被单核细胞 Arg1 抑制所扰乱(图 S6L)。综上,这些结果表明,单核细胞来源巨噬细胞中 iNOS 与 Arg1 的表达共同参与 SICM 期间心功能保护,而运动可加速巨噬细胞由 iNOS⁺ 向 Arg1⁺ 的转变。图 4|规律运动诱导单核细胞来源的 iNOS⁺ 亚群以保护脓毒症心功能Monocle 预测的单核细胞-巨噬细胞发育轨迹,涵盖 Ly6c2^high Mo、Ccr2⁺ Mø、MHC II^high Mø 与 iNOS⁺ Mo(A)。基于 Monocle2 在拟时序中共享动力学特征的差异表达基因热图(B);每种模型对应的不同 GO 术语与代表性基因分别标示于左侧与右侧。用于特异性抑制单核细胞 iNOS 的纳米抑制剂示意图(C)。图由 BioRender 制作,Shang, M.(2025)lbdglen。通过 WB 检测纳米抑制剂对单核细胞 iNOS 的抑制效率(D、E)。β-Tubulin 作为上样内参。数字表示相对于 β-Tubulin 的灰度定量倍数变化。每组分析 6 份样本。缺乏运动(Sed;CTRL,n = 7;Anti-Ly6C-iNOS,n = 7)与运动(Exe;CTRL,n = 8;Anti-Ly6C-iNOS,n = 7)小鼠在腹腔注射 LPS 并给予 Anti-Ly6C-iNOS 或对照处理后 18 h 的体温(F)与体重变化百分比(G)。代表性超声心动图图像(H)及 LPS 腹腔注射后 18 h 的射血分数(EF%)(I)与缩短分数(FS%)(J)定量:Sed(CTRL,n = 7;Anti-Ly6C-iNOS,n = 7)与 Exe(CTRL,n = 8;Anti-Ly6C-iNOS,n = 7)小鼠均给予 Anti-Ly6C-iNOS 或对照处理。Sed 与 Exe 小鼠在 LPS 注射后 18 h,接受 Anti-Ly6C-iNOS 或对照(CTRL)处理的心脏中 TUNEL⁺ 细胞(N、K)、DHE⁺ 区域(O、L)以及 iNOS⁺CD68⁺ 细胞(P、M)的代表性图像与定量分析。每组分析 4 份样本,来自 2 次独立重复实验。LPS 注射后时间序列中,小鼠心脏内 Arg1、CD68 与 iNOS 的代表性图像与定量分析(Q–S);每组分析 5 份样本,来自 3 次独立重复实验。Sed 与 Exe 小鼠在腹腔注射 LPS 并给予 Anti-Ly6C-Arg1 或对照处理后 18 h 的体温(T)与体重变化百分比(U);每组分析 6 份样本。代表性超声心动图图像(V)及 LPS 腹腔注射后 18 h 的射血分数(EF%)(W)与缩短分数(FS%)(X)定量:Sed 与 Exe 小鼠均给予 Anti-Ly6C-Arg1 或对照处理;每组分析 6 份样本。比例尺:100 µm(N–P),50 µm(Q)。运动增强单核细胞来源巨噬细胞在 SICM 中的糖酵解及后续组蛋白乳酰化
随后我们旨在阐明 iNOS⁺ 单核细胞表现出抗炎功能的机制,尤其是运动是否以及如何影响其代谢特征。我们及其他研究团队的既往研究表明,巨噬细胞的代谢改变可影响其功能¹⁵˒¹⁶˒⁴²。首先,我们采用 Compass 算法进行通量平衡分析,以评估基因组尺度代谢网络中特定反应的活性。Compass-score 差异活性检验显示,缺乏运动的 SICM 心脏中代谢通量显著升高;相反,运动通过促进或抑制多条代谢通路重塑了脓毒症心脏中的巨噬细胞代谢(图 S7)。为进一步深入,我们使用 scMetabolism 分析评估运动如何调控心脏单核细胞与巨噬细胞总体及特定亚群的代谢谱(图 S8)。结果显示,与缺乏运动的 SICM 心脏相比,运动在单核细胞与巨噬细胞总体、单核细胞、巨噬细胞以及 iNOS⁺ Mo 中显著增强糖酵解并抑制三羧酸循环(TCA cycle)(图 5A 与图 S8)。这些观察与 Compass-score 分析结果一致(图 5B 与图 S7)。
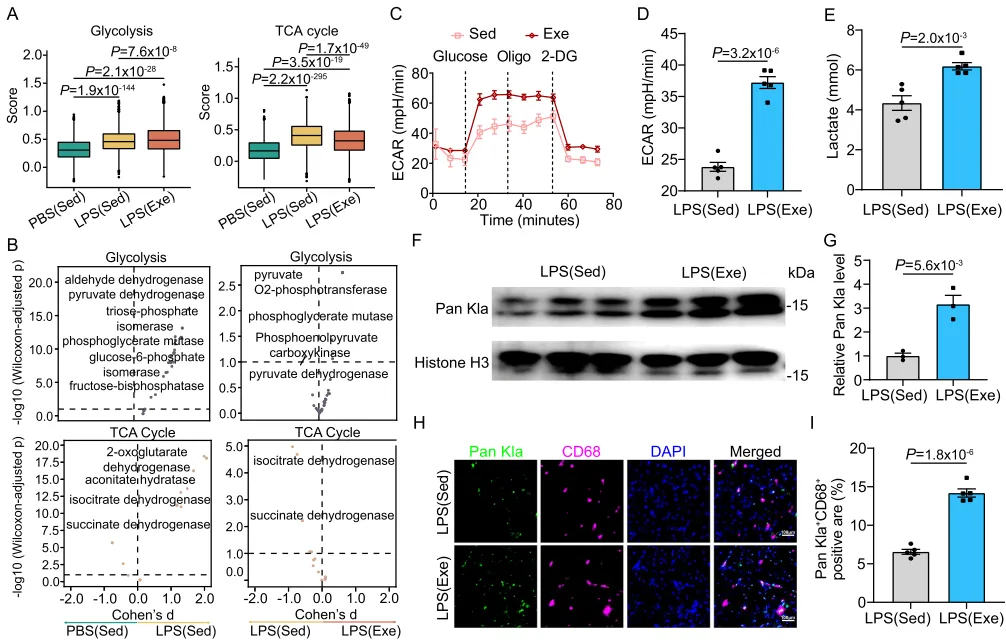
为验证上述发现,我们从外周血分离单核细胞并检测细胞外酸化率(ECAR)。与缺乏运动组相比,运动脓毒症小鼠单核细胞的糖酵解水平约升高 55%(图 5C、D)。这一无氧糖酵解增强亦由细胞内乳酸水平升高所证实:LPS 注射后,运动组单核细胞乳酸水平较缺乏运动对照约升高 50%(图 5E)。近期研究表明,糖酵解来源的乳酸可调控组蛋白乳酰化,从而触发与创伤修复相关的基因表达⁴³˒⁴⁴。值得注意的是,我们在 SICM 中观察到运动诱导的全局组蛋白赖氨酸乳酰化(Kla)在循环单核细胞与心脏巨噬细胞中均升高(图 5F–I)。综上,这些结果提示,运动增强单核细胞糖酵解并增加组蛋白乳酰化,进而在单核细胞来源巨噬细胞中引发代谢重编程,该过程可能有助于在 SICM 中保护心功能。图 5|运动在 SICM 期间增强单核细胞来源巨噬细胞的糖酵解及后续组蛋白乳酰化采用单细胞代谢分析(scMetabolism)评估的糖酵解与三羧酸循环(TCA cycle)活性评分(A)。纳入分析的细胞数:缺乏运动(Sed)或运动(Exe)组分别为 PBS(Sed)n = 2722;LPS(Sed)n = 2517;LPS(Exe)n = 7940。下须、下铰链、箱体中线、上铰链与上须分别代表最小值、下四分位数、中位数、上四分位数与最大值。Compass-score 差异活性检验显示糖酵解与 TCA 循环的代谢通量水平(B)。LPS 注射后 18 h,从运动(Exe)或缺乏运动(Sed)小鼠分离单核细胞的细胞外酸化率(ECAR)(C、D);图中显示每种条件下 5 次生物学重复的数值。LPS 注射后 18 h,小鼠单核细胞内 L-乳酸水平(E);每组分析 5 份样本。PBS 或 LPS 注射后 18 h,小鼠单核细胞中 Pan Kla 的 Western blot(F、G)。组蛋白 H3 作为内参,并标注相对于组蛋白 H3 的灰度定量倍数变化;每组分析 3 份样本。SICM 小鼠心脏中 CD68 与 Pan Kla 的代表性图像及定量分析(H、I),比较是否运动。比例尺:100 µm(H)。自愿跑轮诱导单核细胞来源巨噬细胞的组蛋白乳酰化在 SICM 中保护心功能
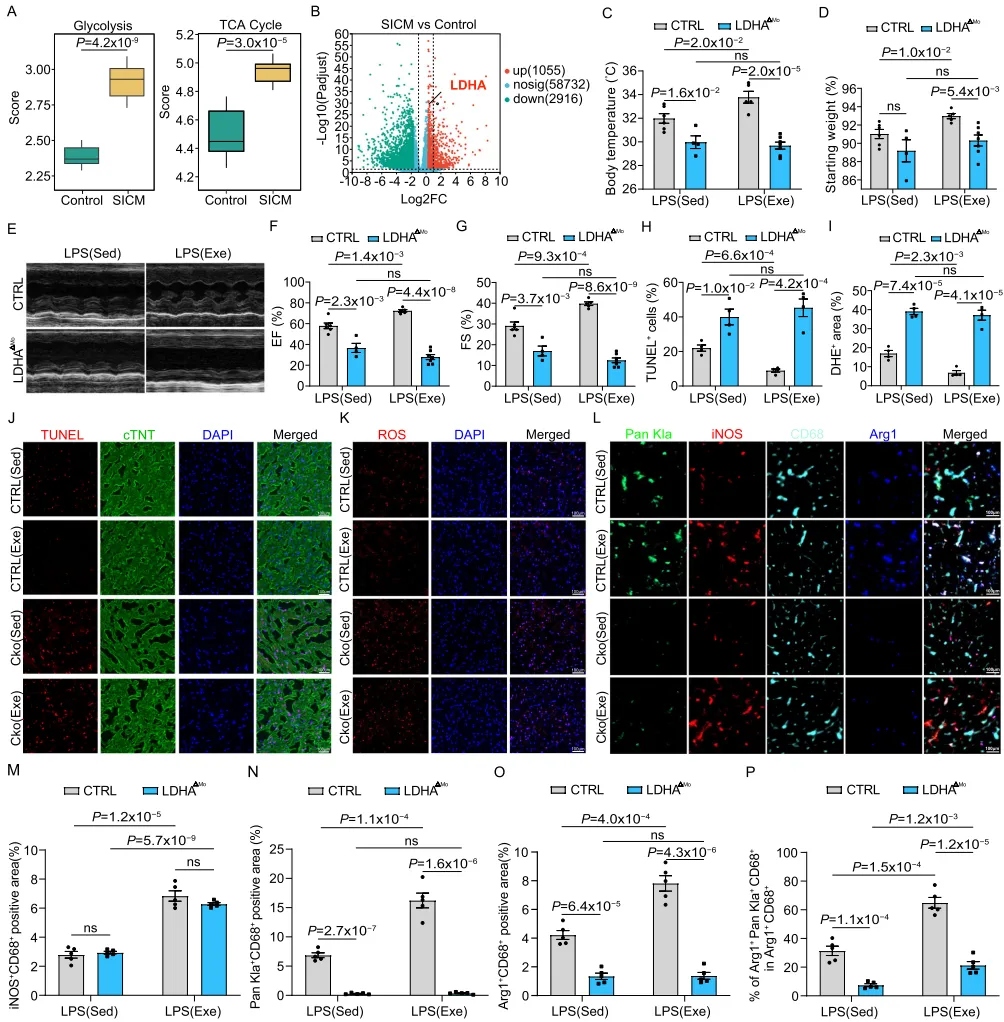
为评估该保护机制的临床相关性,我们使用 CD14⁺ 磁珠分别从 SICM 患者与健康供者外周血中分离单核细胞,并进行 RNA 测序分析。与小鼠观察一致,与健康供者相比,SICM 患者单核细胞表现出糖酵解与三羧酸循环(TCA cycle)增强(图 6A;表 S2)。有趣的是,无氧糖酵解中将丙酮酸转化为乳酸的关键酶——乳酸脱氢酶 A(LDHA)的表达在 SICM 患者单核细胞中显著升高(图 6B)。
为进一步探究运动诱导的组蛋白乳酰化在单核细胞来源巨噬细胞缓解 SICM 中的作用,我们构建了髓系细胞特异性缺失 Ldha 的小鼠模型。具体而言,将 Ldha floxed 小鼠(Ldha L/L)与髓系细胞特异性的 LysM: Cre 转基因系进行杂交(图 S9A、B),以下简称 LdhaΔMo 小鼠。LdhaΔMo 小鼠可在单核细胞中选择性抑制组蛋白乳酰化,并消除运动诱导的组蛋白 Kla 升高(图 S9C)。与在单核细胞中抑制 iNOS 或 Arg1 的效应相似,LdhaΔMo 小鼠在脓毒症期间表现为规律运动对体温下降与体重丢失的保护效应被逆转(图 6C、D)。与此一致,LdhaΔMo 小鼠也丧失了规律运动通常可带来的脓毒症心功能改善,以及脓毒症心脏细胞凋亡与氧化损伤降低(图 6E–G)。此外,免疫荧光分析与我们先前观察一致:运动可减少脓毒症心脏中心肌细胞凋亡与氧化损伤,但在 LdhaΔMo 小鼠中这一效应消失(图 6H–K)。值得注意的是,与缺乏运动对照相比,运动使心脏巨噬细胞的组蛋白乳酰化水平提高近 3 倍。该升高与创伤修复标志物 Arg1 的表达相关:在运动的 SICM 小鼠心脏中,组蛋白乳酰化对于 Arg1 表达至关重要,约 70% 的 Arg1⁺ 巨噬细胞呈现组蛋白乳酰化。然而,在 LdhaΔMo 小鼠中,组蛋白乳酰化增强与 Arg1 表达均被消除(图 6L–P;图 S9D)。总体而言,这些数据提示,运动诱导的单核细胞及单核细胞来源巨噬细胞组蛋白乳酰化在脓毒症期间维持心功能中起关键作用。图 6|自愿跑轮诱导单核细胞来源巨噬细胞的组蛋白乳酰化,从而在 SICM 中保护心功能基于 GSVA 分析的健康供者与 SICM 患者外周血单核细胞糖酵解与三羧酸循环(TCA cycle)活性评分(A)。纳入分析的样本量:对照组 n = 9;SICM 组 n = 10。下须、下铰链、箱体中线、上铰链与上须分别代表最小值、下四分位数、中位数、上四分位数与最大值。显示健康供者与 SICM 患者差异基因表达的火山图,图中标注 LdhA(B)。髓系细胞特异性 Ldha 缺失(LdhaΔMo)与对照小鼠在 LPS 注射后 18 h 的体温(C)与体重变化百分比(D),比较是否运动。分组包括缺乏运动(Sed;CTRL,n = 6;LdhaΔMo,n = 4)与运动(Exe;CTRL,n = 5;LdhaΔMo,n = 7)。LdhaΔMo 或对照小鼠在 LPS 注射后 18 h 的代表性超声心动图图像(E)及射血分数(EF%)(F)与缩短分数(FS%)(G)定量结果,比较是否运动。分组包括缺乏运动(CTRL,n = 6;LdhaΔMo,n = 4)与运动(CTRL,n = 5;LdhaΔMo,n = 7)。LdhaΔMo 或对照小鼠在 LPS 注射后 18 h 的心脏中 TUNEL(J、H)与 DHE(K、I)阳性面积的代表性图像与定量分析,比较是否运动;每组分析 4 份样本。L–P,LdhaΔMo 或对照小鼠在 LPS 注射后 18 h 的心脏中 Pan Kla、iNOS、CD68 与 Arg1 的代表性图像与定量分析,比较是否运动;每组分析 5 份样本。比例尺:100 µm(J–L)。运动在人体与小鼠单核细胞中增强 H3K18 组蛋白乳酰化
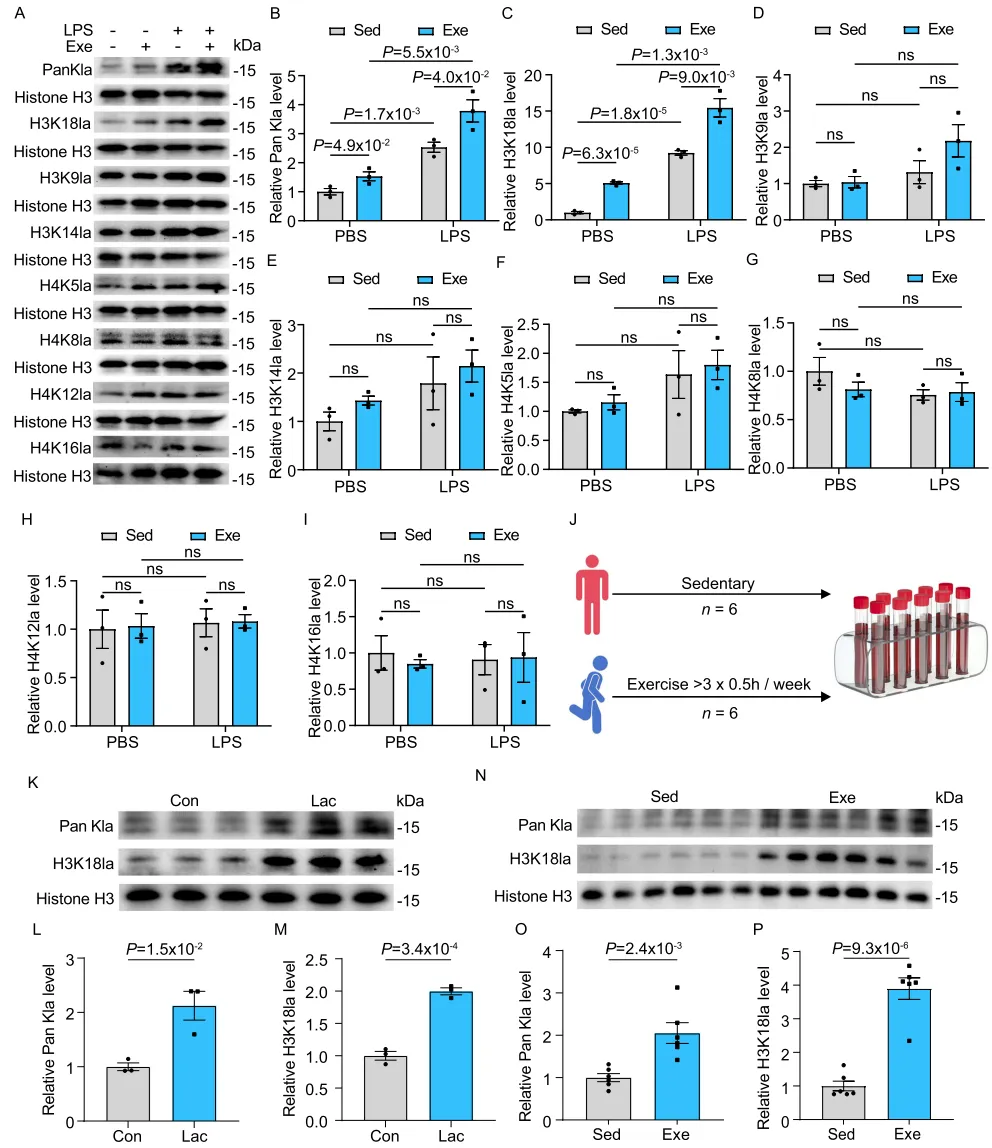
接下来,我们试图鉴定运动在单核细胞中诱导的特异组蛋白乳酰化位点。除先前观察到运动在 SICM 期间提高 Pan Kla 水平(图 5F、G)外,我们发现与缺乏运动对照相比,运动也可在 PBS 注射小鼠中提高 Pan Kla 水平(图 7A、B)。为鉴定具体乳酰化位点,我们检测了缺乏运动与运动小鼠单核细胞中组蛋白 H3 第 18 位赖氨酸乳酰化(H3K18la),并同时检测 H3K9la、H3K14la、H4K5la、H4K8la、H4K12la 与 H4K16la;小鼠接受 LPS 处理或 PBS 作为对照。结果显示,在 PBS 注射条件下,运动后 H3K18la 水平较缺乏运动显著升高,并在 LPS 攻击后进一步增加(图 7A–C)。相反,在 LPS 攻击或 PBS 对照条件下,H3K9la、H3K14la、H4K5la、H4K8la、H4K12la 与
H4K16la 均未随运动出现显著变化(图 7A、D–I)。在这些标记中,仅 H3K18la 的变化与 Pan Kla 的模式高度一致,提示运动特异性诱导 H3K18la。
这些观察引出了一个问题:规律运动是否同样促进人体单核细胞 H3K18la。为此,我们招募了缺乏运动与活跃生活方式志愿者(图 7J;表 S3)。鉴于既往研究报道乳酸水平影响组蛋白乳酰化⁴⁰˒⁴⁵,我们将小鼠循环单核细胞暴露于不同浓度乳酸以诱导组蛋白乳酰化,并确定 20 mM 乳酸为最佳浓度(图 S9E、F)。随后,我们以 20 mM 外源乳酸处理缺乏运动志愿者的单核细胞,观察到 Pan Kla 与 H3K18la 水平均升高(图 7K–M)。一致地,活跃志愿者单核细胞中 Pan Kla 与 H3K18la 水平显著高于缺乏运动个体(图 7N–P)。接着,我们考察诱导单核细胞组蛋白乳酰化及其在 SICM 中对心功能产生保护效应所需的运动持续时间。时间序列分析显示:运动 1 天或 7 天的小鼠单核细胞中 Pan Kla 与 H3K18la 水平相当;但在运动 14 天后显著升高,并在运动 28 天后进一步增加(图 S10A–C)。与此一致,运动 14 天可在 LPS 攻击后减轻体重丢失并维持心功能,而延长至 28 天可进一步增强这些保护效应(图 S10D–G)。综上,这些结果表明,运动可在人体与小鼠单核细胞中诱导 H3K18la,并强调其在 SICM 中维持心功能的关键作用。图 7|运动增强人体与小鼠单核细胞中的 H3K18 组蛋白乳酰化对运动(Exe)与缺乏运动(Sed)小鼠在 PBS 或 LPS 注射后 18 h 分离的单核细胞进行 Western blot,以检测多种乳酰化位点,包括 Pan Kla、H3K18la、H3K9la、H3K14la、H4K5la、H4K8la、H4K12la 与 H4K16la(A–I)。组蛋白 H3 作为内参,并标注相对于组蛋白 H3 的灰度定量倍数变化。每组分析 3 份样本,结果来自 3 次独立重复实验。招募缺乏运动与活跃生活方式志愿者的示意图(J)。将人单核细胞与 20 mM 乳酸钠孵育 24 h 后检测 Pan Kla 与 H3K18la 的 Western blot(K–M)。组蛋白 H3 作为内参,并标注相对于组蛋白 H3 的灰度定量倍数变化。每组分析 3 份样本,结果来自 2 次独立重复实验。对人单核细胞进行 Pan Kla 与 H3K18la 的 Western blot 分析(N–P),比较规律运动习惯个体与缺乏运动对照。组蛋白 H3 作为内参,并标注相对于组蛋白 H3 的灰度定量倍数变化。运动通过 p300 与 HDAC2 增强单核细胞 H3K18 组蛋白乳酰化
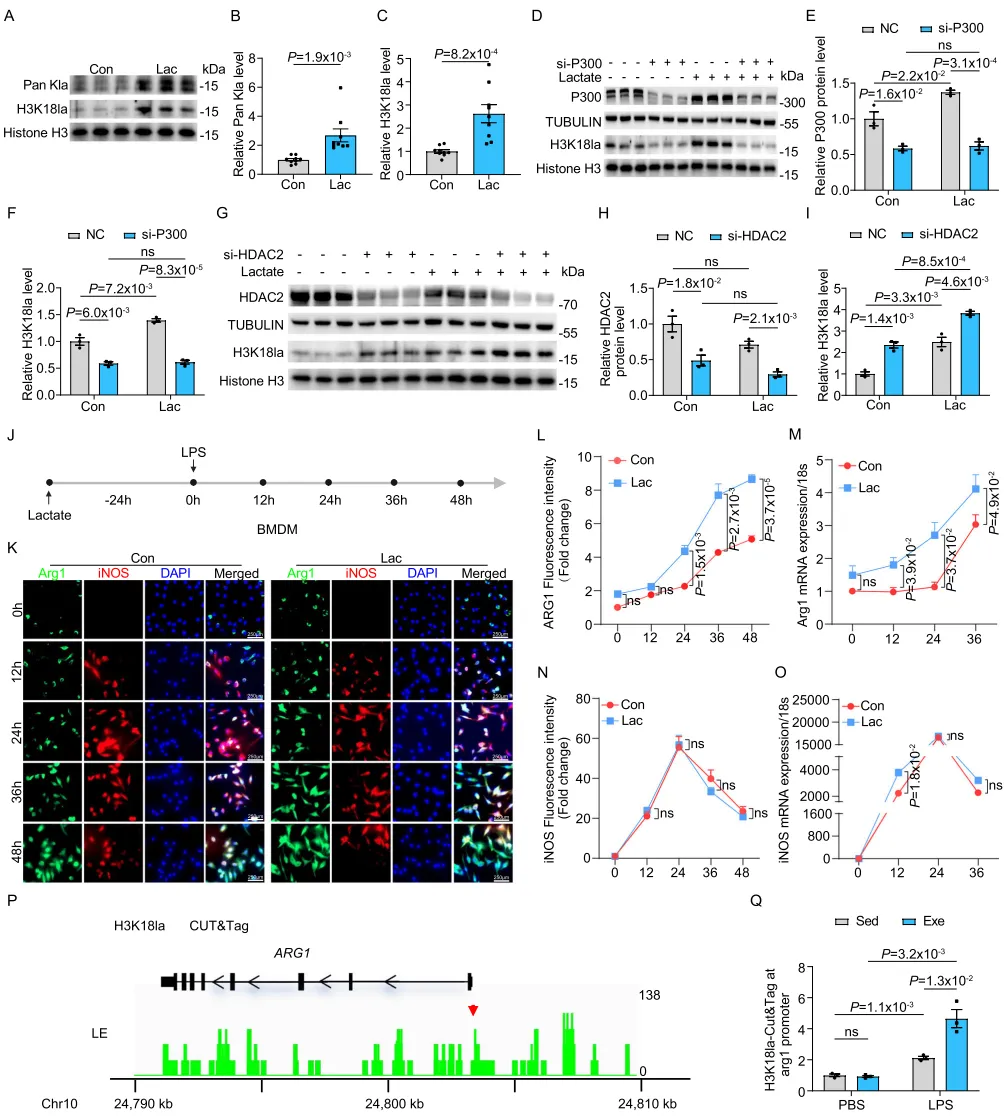
随后,我们旨在鉴定在单核细胞中负责添加或去除运动诱导 H3K18la 的乳酰转移酶与去乳酰化酶。既往研究报道 p300 可能是组蛋白乳酰化的“写入酶”⁴³˒⁴⁶。为验证其在运动诱导乳酰化中的作用,我们使用 siRNA 沉默单核细胞 p300,随后按此前方法将细胞与乳酸孵育以诱导乳酰化⁴⁴。结果显示,乳酸诱导的组蛋白乳酰化在全局 Pan Kla 与 H3K18la 水平均可观察到(图 8A–C);然而,当 p300 被沉默后,这种诱导效应被消除(图 8D–F)。这些发现提示,p300 在单核细胞中作为 H3K18la 的组蛋白乳酰化写入酶发挥作用。
为鉴定负责去除组蛋白乳酰化的去乳酰化酶,我们聚焦于已被报道可能作为组蛋白乳酰化“擦除酶”的 HDAC1–3⁴⁷。我们分别使用 siRNA 沉默 HDAC1、HDAC2 与 HDAC3,并评估乳酸诱导的单核细胞 H3K18la 水平。结果显示,敲低 HDAC2 可显著提高 H3K18la 水平(图 8G–I),而沉默 HDAC1 或 HDAC3 并不会升高 H3K18la(图 S11A–F)。这些结果确定 HDAC2 为单核细胞中 H3K18la 的主要去乳酰化酶。综上,p300 与 HDAC2 分别作为运动诱导单核细胞 H3K18la 的乳酰转移酶与去乳酰化酶,从而参与其在 SICM 中的保护效应。为阐明 H3K18la 是否调控先前观察到的巨噬细胞由 iNOS⁺ 向 Arg1⁺ 加速转变,我们分离骨髓来源巨噬细胞(BMDM)并与乳酸孵育 24 h。经该预处理后,对 BMDM 进行 LPS 刺激的时间序列实验。乳酸预处理显著增强 Arg1 表达而不影响 iNOS 表达,从而促进更快速地向创伤修复型巨噬细胞转变(图 8J–O)。这提示乳酸预处理巨噬细胞有助于在炎症挑战下加速免疫稳态的恢复。为探究 H3K18la 如何调控 Arg1 表达,我们使用抗 H3K18la 抗体进行全基因组 Cleavage Under Targets and Tagmentation(CUT&Tag)分析,并进行高通量 DNA 测序。数据揭示 H3K18la 在 Arg1 启动子区域显著富集(图 8P)。此外,CUT&Tag-qPCR 分析显示,与 PBS 注射相比,LPS 刺激后 Arg1 启动子区域的 H3K18la 富集增加,且在规律运动背景下增幅更大(图 8Q)。综上,这些结果表明,单核细胞中由 p300 与 HDAC2 调控的运动诱导 H3K18la,通过促进更快速向创伤修复型巨噬细胞转变并恢复免疫稳态,从而在 SICM 中介导运动的保护效应。图 8|运动通过 p300 与 HDAC2 增强单核细胞 H3K18 组蛋白乳酰化将小鼠单核细胞与 20 mM 乳酸钠孵育 24 h 后检测 Pan Kla 与 H3K18la 的 Western blot(A–C)。组蛋白 H3 作为内参,并标注相对于组蛋白 H3 的灰度定量倍数变化。每组分析 9 份样本。对小鼠单核细胞分别采用 si-P300(D–F)或 si-HDAC2(G–I)进行 p300 或 HDAC2 敲低,并与 20 mM 乳酸钠处理 24 h,同时设置相应对照组;随后进行 H3K18la 的 Western blot 检测。Tubulin 与组蛋白 H3 作为内参,并标注相对于 Tubulin 与组蛋白 H3 的灰度定量倍数变化。每组分析 3 份样本。骨髓来源巨噬细胞(BMDM)先与 20 mM 乳酸钠孵育 24 h,随后进行 LPS 刺激时间序列实验的流程示意图(J)。乳酸预孵育 BMDM 在 LPS 刺激后的 Arg1 与 iNOS 的代表性图像与定量分析(K、L、N);每组分析 4 份样本。乳酸预孵育 BMDM 在 LPS 刺激后的 Arg1(M)与 iNOS(O)的 RT-qPCR 分析;每组分析 3 份样本。CUT&Tag 分析的代表性轨迹显示 H3K18la 在 Arg1 启动子区域富集(P)。针对 Arg1 的 CUT&Tag 结果通过 qPCR 验证(Q);每组分析 3 份样本。比例尺:250 µm(K)。乳酰化乳酸诱导乳酰化的单核细胞回输可改善 SICM 中的心功能
最后,我们评估了上述发现的治疗学意义。为此,我们开展了多项实验。首先,我们采用更具临床相关性的盲肠结扎穿孔(cecal ligation and puncture, CLP)模型,在多菌种脓毒症背景下诱导 SICM。与 LPS 诱导模型中的观察一致,运动可显著预防 CLP 诱导 SICM 中的体温下降、体重丢失以及 IL-1β 与 TNF-α 生成升高(图 S12A–D)。此外,运动小鼠表现为心功能显著改善,SICM 小鼠心脏中的凋亡减少,氧化应激减轻(图 S12E–K)。
随后,我们进行了回输实验:将来自运动供体小鼠的单核细胞在 LPS 注射后输注至缺乏运动受体小鼠以诱导脓毒症。与缺乏运动小鼠相比,运动小鼠来源单核细胞的糖酵解增强(图 S12L–N)。单核细胞输注可显著缓解脓毒症导致的体温下降与体重丢失,并降低 IL-1β 与 TNF-α 的生成(图 9A–D)。此外,输注运动小鼠来源单核细胞可显著改善 SICM 小鼠心功能,并减少心脏凋亡(图 9E–I)。综上,这些结果表明,运动对循环单核细胞的“训练”在抵御 SICM 中起核心作用。
接着,为模拟自愿运动的获益,我们用乳酸“预处理”循环单核细胞以诱导组蛋白乳酰化(图 S9E、F)。这些乳酸预处理的单核细胞用 PKH26 标记后经尾静脉注射回输至 SICM 小鼠。结果证实标记单核细胞可在 SICM 小鼠心脏中定位(图 9J、K)。值得注意的是,与自愿运动所观察到的保护效应相似,回输组蛋白乳酰化水平升高的单核细胞可显著改善心功能,并降低脓毒症心脏中的凋亡与氧化损伤(图 9L–T)。
为进一步确认组蛋白乳酰化对 SICM 的保护作用,我们评估了 p300 被抑制的单核细胞在体内的影响。回输前,单核细胞以 p300 选择性抑制剂 C646⁴⁸进行预处理。接受 p300 抑制单核细胞回输的小鼠,运动所带来的保护效应被消除,包括体温、体重丢失、心功能及心肌凋亡改善的丧失(图 S13A–J)。这些发现表明,以 p300 为写入酶的 H3K18la 对维持 SICM 中的心功能至关重要。综上,我们的结果提示,与自愿运动的获益类似,乳酸诱导的单核细胞组蛋白乳酰化可通过恢复 SICM 中的免疫稳态来保护心功能。
图 9|乳酸预处理单核细胞回输可改善 SICM 中的心功能
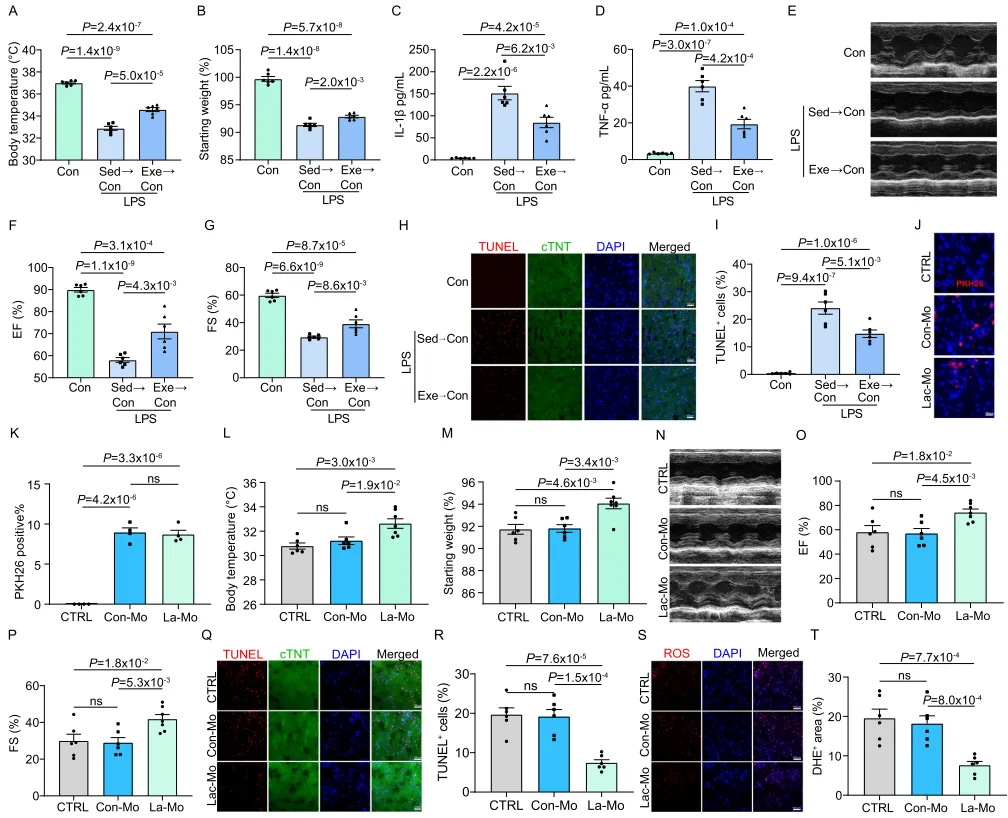
SICM 小鼠回输来自缺乏运动(Sed)或运动(Exe)小鼠的单核细胞后测定体温(A)与体重变化百分比(B);每组分析 6 份样本。SICM 小鼠回输来自缺乏运动或运动小鼠的单核细胞后,采用 ELISA 检测 IL-1β(C)与 TNF-α(D);每组分析 6 份样本。SICM 小鼠回输来自缺乏运动或运动小鼠的单核细胞后的代表性超声心动图图像(E)及射血分数(EF%)(F)与缩短分数(FS%)(G)定量;每组分析 6 份样本。SICM 小鼠回输来自缺乏运动或运动小鼠的单核细胞后,心脏切片中 TUNEL 的代表性图像(H)与定量分析(I);每组分析 6 份样本。PKH26 标记的单核细胞回输后 18 h 浸润至 SICM 小鼠心脏的代表性图像与定量分析(J、K);每组分析 4 份样本,来自 2 次独立重复实验。SICM 小鼠回输乳酸预处理单核细胞后体温(L)与体重变化百分比(M);纳入分析的样本量:CTRL 组 n = 6,Con-Mo 组 n = 6,La-Mo 组 n = 7。乳酸预处理单核细胞回输后,SICM 小鼠的代表性超声心动图图像(N)及射血分数(EF%)(O)与缩短分数(FS%)(P)定量;纳入分析的样本量:CTRL 组 n = 6,Con-Mo 组 n = 6,La-Mo 组 n = 7。乳酸预处理单核细胞回输后,SICM 小鼠心脏中 TUNEL(Q、R)与 DHE(S、T)阳性面积的代表性图像与定量分析;每组分析 6 份样本。比例尺:100 µm(H、Q、S),200 µm(J)。
心脏免疫环境在维持心肌稳态并促进损伤后修复中发挥关键作用⁴⁹–⁵²。巨噬细胞作为心脏中数量最多且功能最为多样的免疫细胞,显著参与心脏损伤后受损心肌的修复⁵³。发生损伤后,循环单核细胞被募集至心肌并分化为巨噬细胞。在心脏损伤早期阶段,单核细胞来源巨噬细胞对于清除组织碎片并释放细胞因子、生长因子以及成纤维细胞生长因子至关重要⁵⁴˒⁵⁵。急性期炎症细胞重要性还得到进一步证据支持:巨噬细胞清除会损害组织碎片与死亡细胞(包括坏死心肌细胞)的清除⁴⁰˒⁴¹。随着修复过程推进,巨噬细胞上调修复相关基因表达,重塑成纤维细胞,促进血管生成,并通过促进细胞外基质(ECM)降解来恢复组织完整性⁵⁶˒⁵⁷。然而,积极生活方式如何调控心脏免疫环境仍未被充分阐明。
在本研究中,我们结合 bulk RNA-seq 与 scRNA-seq 探索运动诱导的 SICM 心肌保护的分子机制。bulk RNA-seq 分析显示,运动主要通过抑制 SICM 相关的过度炎症而发挥心肌保护作用。在此基础上,我们利用 scRNA-seq 分析运动条件下 SICM 心脏的免疫细胞,从而构建了更为精细的心脏免疫细胞图谱。在这些细胞中,我们鉴定出一种运动诱导的 iNOS⁺Arg1⁺ 单核细胞来源巨噬细胞亚群。该亚群同时表达炎症与创伤修复相关基因,提示其在 SICM 期间心脏免疫应答中具有双重作用。iNOS⁺Arg1⁺ 亚群的存在提示其在 SICM 心脏免疫应答中具有双重功能:早期似乎增强促炎免疫反应,这对抵御早期感染至关重要;随后促进心脏巨噬细胞由炎症型向创伤修复型转变,从而推动心脏稳态的恢复。这种双重功能强调了运动可调控免疫反应,使其既支持即时防御机制,也有利于长期组织修复与恢复。众所周知,巨噬细胞在促进炎症与创伤修复过程中均发挥关键作用⁵⁸–⁶⁰。然而,这两种范式之间的精细平衡以及如何加以利用以改善损伤后心脏修复与功能恢复,仍相对缺乏深入研究。本研究表明,运动诱导的乳酸可使炎症性巨噬细胞发生预适应,从而在完成清除细胞碎片等促炎功能后,对其炎症消退阶段进行精细调控。运动通过增强糖酵解对单核细胞代谢进行重编程,继而产生的乳酸通过提升组蛋白乳酰化激活内源性“乳酸时钟”,从而诱导修复相关基因表达⁴³。首先,通过在单核细胞中选择性抑制 iNOS,我们发现 iNOS⁺ 促炎巨噬细胞对于 LPS 攻击后的细胞碎片清除是必需的。进一步地,我们试图理解何种因素驱动该单核细胞来源巨噬细胞亚群表达稳态相关基因并加速炎症消退过程,从而避免过度炎症(其可导致器官损伤甚至器官衰竭)。长期以来已知运动可诱导乳酸生成⁶¹。在本研究中,我们证实运动可增强单核细胞糖酵解,从而提高乳酸生成。乳酸水平升高随后驱动组蛋白乳酰化这一表观遗传修饰,增强包括 Arg1 在内的修复相关基因表达。结合近期研究,我们提出:运动可在单核细胞中引发由代谢重编程驱动的表观遗传修饰,而这些细胞随后浸润至受损心脏,加速心脏过度激活炎症的消退过程。本研究鉴定并验证了一种基于代谢物的“巨噬细胞预适应模式”,即巨噬细胞可对免疫挑战预先调整其应答,从而加速炎症消退,维持心功能并促进心肌恢复(图 S14)。除机制层面的意义外,本研究亦具有重要社会与临床启示。阐明积极与缺乏运动生活方式如何影响心脏健康与疾病进程,为应对包括心血管疾病(CVD)与 SICM 在内的全球重大健康挑战提供了一种成本效益高且高效的策略²³˒²⁹。除运动诱导组蛋白乳酰化外,回输乳酰化增强的单核细胞也可被视为一种潜在的 CVD 治疗策略,尤其在 SICM 中可通过恢复心脏免疫稳态并改善心功能而获益。尽管取得上述进展,本研究仍存在需要进一步探索的局限。第一,我们仅在 LPS 注射后 18 h 评估运动与单核细胞来源巨噬细胞对心功能的作用;未来纳入更多 LPS 刺激后的时间点,可为其在长期心脏重构中的作用提供重要信息。第二,尽管我们证明活跃志愿者单核细胞中 Pan Kla 与 H3K18la 水平均显著高于缺乏运动个体,且与小鼠研究结论一致,但技术限制使我们无法充分评估 SICM 患者单核细胞中 Pan Kla 与 H3K18la 的表达水平。这限制了我们在 SICM 患者中建立组蛋白乳酰化水平与心功能结局之间直接相关性的能力,而这本可进一步强化我们发现的转化意义。未来研究有必要检测 SICM 患者单核细胞中的组蛋白乳酰化,并将其表达水平与临床结局(如心功能进展与死亡率)相关联。 在我们此前关于肌肉再生的研究中,我们证明重编程巨噬细胞代谢可支持肌肉干细胞库并促进其分化¹⁶。本研究显示,运动可协调单核细胞代谢,增强组蛋白乳酰化,使单核细胞来源巨噬细胞发生预适应并加速其由炎症型向修复型巨噬细胞转变,从而在 SICM 期间维持心功能。本研究首先描绘了规律运动所塑造的心脏免疫图谱;其次证明运动小鼠单核细胞中由增强糖酵解诱导的组蛋白乳酰化可在 SICM 中保护心功能;最后,我们的数据提示,模拟规律体力活动获益的单核细胞回输治疗,是一种在 SICM 中保护心功能的潜在治疗策略。这些发现为通过代谢与表观遗传重编程探索心血管疾病的新研究方向与新治疗策略提供了可能性。