
01 爱尔康
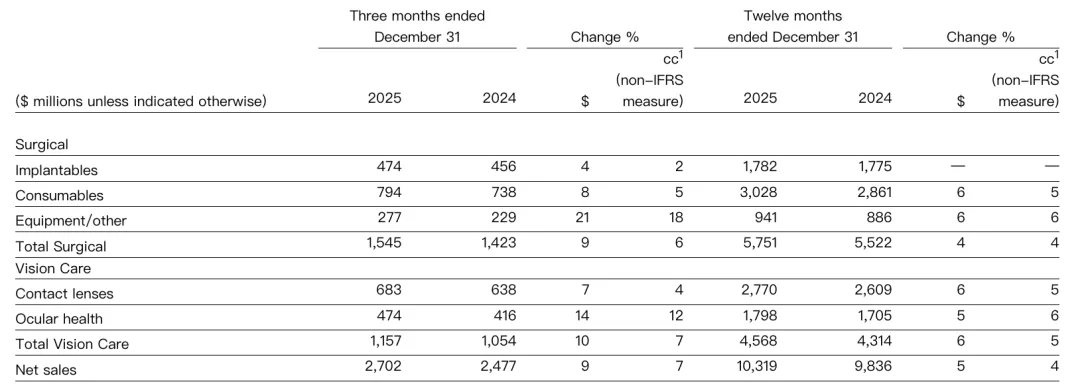
爱尔康 2 月 24 日报告称,其 2025年全年净销售额达 103 亿美元,较 2024全年增长 5%。2025Q4 销售额为 27 亿美元,比 2024Q4 增长 9%。
1.1 外科手术业务
2025年外科手术净销售额(植入产品、耗材和设备/其他)为 58 亿美元,同比 2024 年增长4%。
植入物:净销售额为 18 亿美元,与上年同期持平。这一业绩反映了PanOptix Pro在美国的上市,以及疲软的市场环境和激烈的市场竞争。
耗材:净销售额为 30 亿美元(增长 6%),主要得益于玻璃体视网膜手术量的增长和价格上涨,但部分被白内障市场疲软所抵消。
设备/其他:净销售额为 9.41 亿美元(增长 6%),主要原因是近期推出的设备(包括Unity VCS)的销售额部分被传统设备的销售额下降所抵消。
植入物:净销售额为 4.74 亿美元(增长 4%),这一增长主要得益于PanOptix Pro 在美国市场的强劲表现,但部分被持续的竞争压力所抵消,尤其是在国际市场。
耗材:净销售额为 7.94 亿美元(增长 8%),增长主要得益于白内障和玻璃体视网膜手术业务的增长以及价格上涨。
设备/其他:净销售额为 2.77 亿美元(增长 21%),这一增长主要得益于近期新设备的推出,包括Unity平台。
1.2 视力保健业务
2025年视力保健业务净销售额(包括隐形眼镜和眼部健康)为 46 亿美元,与 2024 年全年相比增长 6%。
隐形眼镜:净销售额为 28 亿美元,增长 6%,主要得益于价格上涨和产品创新,但部分被传统产品销售额下降所抵消。
眼部健康:净销售额为 18 亿美元,增长 5%,增长主要得益于干眼症产品组合,包括Tryptyr和Systane。上年同期数据包含部分在中国销售的眼药水,这些眼药水已于2024年底剥离并授权给其他公司。
2025Q4视力保健净销售额为 12 亿美元,与 2024Q4相比增长 10%。
隐形眼镜:净销售额为 6.83 亿美元,增长 7%,这一增长主要得益于价格上涨和产品创新,但部分被传统产品销售额的下滑所抵消。
眼部健康:净销售额为 4.74 亿美元,增长 14%,增长主要得益于干眼症产品组合,包括Tryptyr和Systane。
爱尔康预计 2026 年全年营收较 2025 年增长 5% 至 7%。
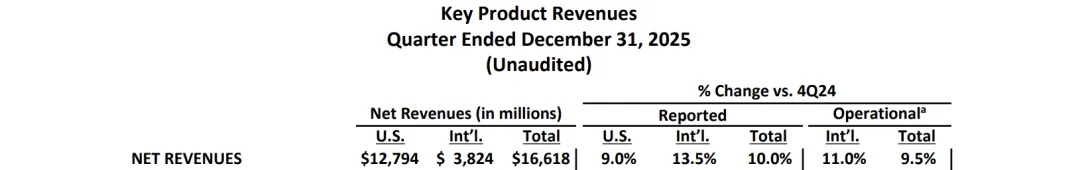
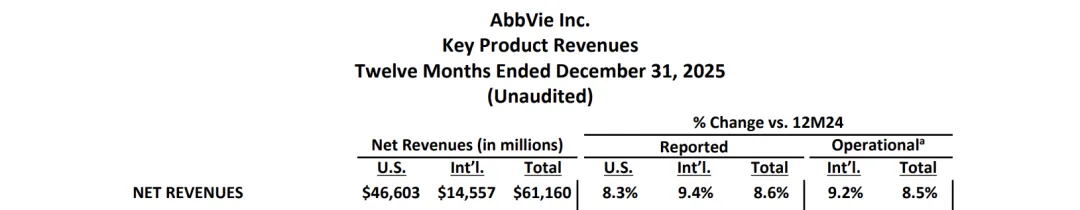
02 艾伯维
眼部护理业务收入21.09亿美元

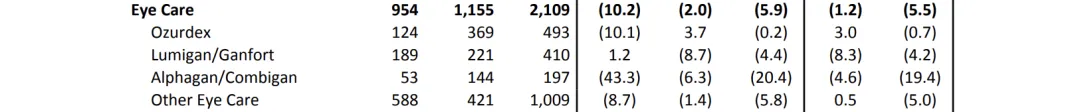
Ozurdex(眼底类固醇药物)2025 年全球收入较往年几乎持平,为 4.93 亿美元。主要受到美国市场业绩下滑影响。 Lumigan/Ganfort(青光眼降压药物)2025 年全球收入为 4.10 亿美元,同比下降4.4%。 Alphagan/Combigan(青光眼降压药物)2025 年全球收入为 1.97 亿美元,同比下降 20.4%。 其他眼部护理产品2025 年全球收入为 10.09 亿美元,同比下降 5.8%。
03 Apellis
Syfovre收入6.118亿美元Apellis 于 2 月 24 日公布,Syfovre 正持续改变地图状萎缩(GA)的治疗格局:
2025Q4 及 2025 全年,Syfovre 在美国净产品收入分别1.55 亿美元与 5.87 亿美元。
总注射量同比增长 17%,体现出持续旺盛的潜在需求;
公司在 GA 领域继续保持市场领先地位,市场份额约 60%;
2025Q4,向全美医生诊室交付约 102,000 剂 Syfovre,其中商业供货约 89,000 剂,免费赠药约 13,000 剂。
Syfovre 于 2023 年 3 月 1 日正式上市,用于治疗年龄相关性黄斑变性继发的地图状萎缩,并于 2023 年 10 月 1 日启用永久 J 编码。
此外,其新一代预充式注射器计划于 2026 年上半年提交监管申请。Syfovre 联合 APL‑3007 作为潜在的下一代疗法,可全面阻断视网膜与脉络膜的补体激活,目前处于 2 期临床阶段,预计 2027 年公布初步数据。
Apellis 2025 年全年总收入为 6.89 亿美元。
04 安斯泰来
Izervay前9个月收入3.58亿美元
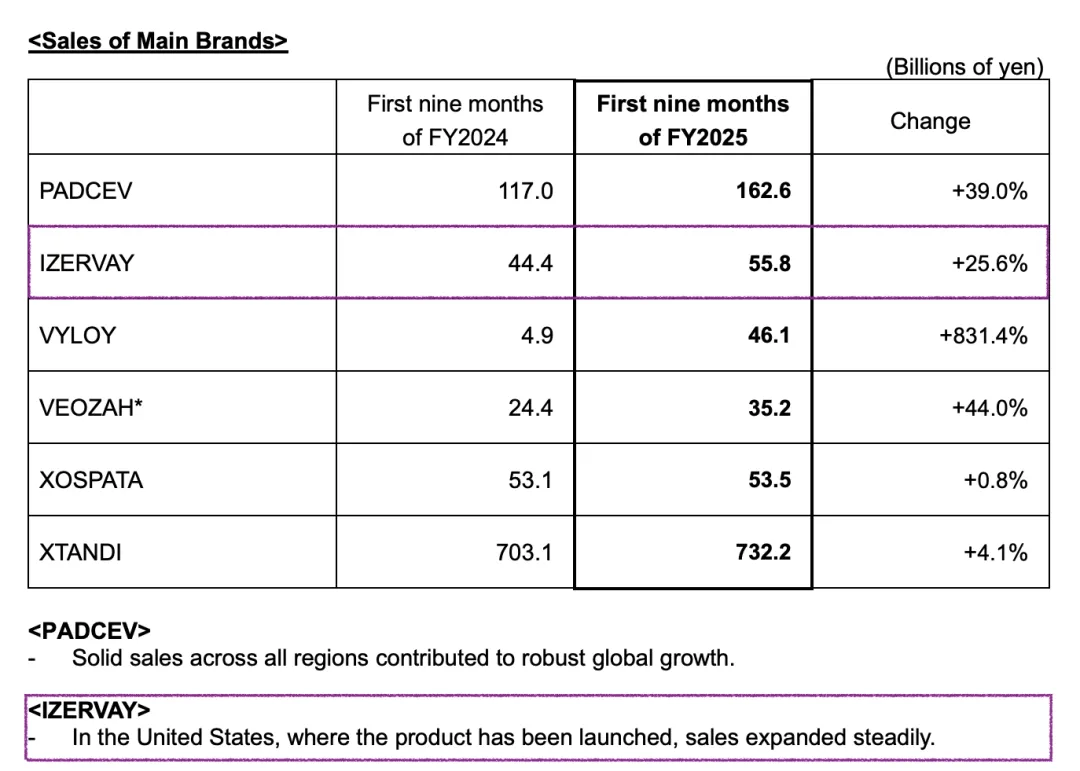
安斯泰来 2025 财年前九个月收入增长10.2%,达到 16,013.2 亿日元。Izervay 的销售稳定增长对此做出了贡献。
05 Immunocore
Kimmtrak年收入为4亿美元
Immunocore 2月25日报告称,其2025年来自公司主打产品 KIMMTRAK®(tebentafusp)的产品净收入为 4 亿美元,同比增长了29%。其中美国销售额为2.57亿美元,欧洲为1.314亿美元,其他国际地区为1160万美元。
2025Q4 销售产生的总净产品收入为 1.045亿美元。与 2024 年同期相比增长了24%。公司预计2026年收入增长将放缓。
KIMMTRAK® 适用于治疗不可切除或转移性葡萄膜黑色素瘤。它于2022年1月获FDA批准,并于2022年4月获欧洲批准。目前已在 39 个国家获得批准,在 30 个国家上市,用于治疗 HLA-A*02:01 阳性的未经治疗的转移性葡萄膜黑色素瘤 (mUM) 患者。KIMMTRAK 在其上市的大多数市场中继续成为治疗标准。
公司凭借其实现了连续15个季度的收入增长,展现了强劲的商业发展势头,这主要得益于美国市场和全球市场的渗透。此外,公司正积极筹备潜在的黑色素瘤新适应证,目前正在开展三项III期临床试验:TEBE-AM和ATOM,旨在完善 KIMMTRAK® 的生命周期管理。
公司认为,在扩大 KIMMTRAK® 的患者覆盖范围方面,有三个关键的增长领域,包括继续在美国社区和全球市场渗透 mUM,潜在地扩展到 2L+ 晚期皮肤黑色素瘤 (CM),以及潜在地扩展到辅助性葡萄膜黑色素瘤。
转移性葡萄膜黑色素瘤
美国销售额同比增长 13%,平均治疗持续时间延长至 14 个月。
受欧洲市场需求增长和新品上市的推动,欧洲市场销售额同比增长 79%。
Adjuvant葡萄膜(或眼部)黑色素瘤
欧洲癌症研究与治疗组织 (EORTC) 继续扩大眼部黑色素瘤 3 期辅助治疗试验 (ATOM) 的试验点范围。
公司估计,美国和欧洲 HLA-A*02:01 阳性、高危辅助性葡萄膜黑色素瘤患者群体可能多达 1200 人。



