
传递中国声音,共享东方智慧
2026年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会(ASCO GU 2026)于当地时间2月26日-28日在美国旧金山举行。本次会议聚焦泌尿生殖系统肿瘤领域的新突破与临床进展。其中复旦大学附属肿瘤医院多项研究成果备受瞩目,医学界特整理其8项口头报告摘要内容,传递中国之声最新成果。
摘要号:56
Assistance of a large language model–based AI agent in preoperative communication for reduction of prostate cancer patients' anxiety and clinicians' burden: A prospective, randomized, single-blinded, phase II trial.
基于大语言模型AI智能体辅助术前沟通,降低前列腺癌患者焦虑与临床医师负担:一项前瞻性、随机、单盲、Ⅱ期临床试验
讲者:Zheng Liu教授
术前沟通对缓解患者焦虑至关重要,但需耗费临床医师大量精力。大语言模型虽具备解答医学咨询的潜力,其在术前沟通中的应用仍缺乏充分的临床验证。
▎研究方法
研究基于临床指南及本中心诊疗经验,依托DeepSeek-R1大模型研发用于术前沟通的AI智能体。纳入本中心新确诊、拟行根治性手术的前列腺癌患者,排除合并严重精神疾病或认知功能障碍者。患者入院后按病房区随机分为对照组与AI智能体辅助组。
两组患者均即刻完成基线情绪与认知评估,包括广泛性焦虑障碍量表7项版(GAD-7)、简化版疾病认知问卷(B-IPQ)等;通过本研究AI智能体收集两组患者的个性化问题。AI智能体辅助组由该AI系统提供个性化解答,所有解答内容均经科学准确性验证后推送。
随后两组均由对分组情况设盲的临床医师开展术前沟通,并再次完成情绪与认知评估;采用美国航空航天局任务负荷指数(NASA-TLX)评估临床医师工作负荷。
主要研究终点为GAD-7评分及NASA-TLX评分结果;次要研究终点包括其他情绪相关量表[视觉模拟焦虑评分(VAS-A)、简明正性负性情绪量表(I-PANAS-SF)]、疾病认知量表[阿姆斯特丹术前焦虑与信息量表(APAIS)、简化版疾病认知问卷(B-IPQ)]、患者满意度及临床医师沟通时长。
▎研究结果
2025年2-8月,共245例患者随机分为对照组(124例)与AI智能体辅助组(121例)。两组患者累计提出3294个问题,人均13.94个,问题涵盖麻醉、围手术期护理、术后管理等手术相关全维度内容。
与对照组相比,AI智能体辅助组患者焦虑水平显著降低,GAD-7评分下降[中位数(四分位距):3.5(2.0~5.0)比7.5(6.5~9.0),P<0.001];临床医师工作负荷显著减轻,NASA-TLX评分更低[中位数(四分位距):38.0(24.5~52.5)比57.0(37.0~77.5),P<0.001],沟通时长较对照组缩短近一半(9.78分钟比17.91分钟,P<0.001)。
▎结论
AI辅助术前沟通可显著降低患者焦虑水平、提升疾病认知、减轻临床医师工作负荷,同时挖掘出既往未被关注的患者诉求。
摘要号:150
ARTEMIS-003: A phase 2 study of HS-20093 (GSK5764227) in patients with metastatic castration-resistant prostate cancer (mCRPC).
ARTEMIS-003研究:HS-20093(GSK5764227)治疗转移性去势抵抗性前列腺癌(mCRPC)患者的Ⅱ期临床研究
讲者:卞晓洁教授
▎研究背景
B7-H3是包括前列腺癌在内的实体瘤中极具潜力的治疗靶点。本项多中心、开放标签Ⅱ期研究旨在评估HS-20093(GSK5764227),一款搭载拓扑异构酶1抑制剂有效载荷的新型抗B7-H3抗体药物偶联物(ADC),在mCRPC患者中的疗效与安全性(临床试验注册号:NCT06001255)。
▎研究方法
纳入经至少一线标准治疗后疾病进展的患者,予HS-200938.0mg/kg静脉输注,每3周1次。主要研究终点为依据RECIST1.1及PCWG3标准评估的、基线存在靶病灶患者的经确认客观缓解率(cORR);在接受≥1剂HS-20093的患者中分析安全性及其他疗效终点。
▎研究结果
截至2025年7月20日,共纳入50例中国成年患者,且均接受≥1剂HS-20093治疗。中位随访时间为8.7(0.1~16.7)个月,中位年龄68(49~79)岁,72.0%患者ECOG体能状态评分为1分。所有患者均接受过新型内分泌治疗,72.0%曾接受紫杉烷类化疗,既往中位治疗线数为2(1~8)。
33例基线存在靶病灶的患者中,cORR为33.3%(95%CI:18.0~51.8),疾病控制率(DCR)为87.9%(95%CI:71.8~96.6),中位缓解持续时间(DoR)尚未达到。共16例患者实现前列腺特异性抗原下降≥50%(PSA50),经确认PSA50缓解率为32.0%。中位影像学无进展生存期(rPFS)尚未达到,9个月rPFS率为55.7%(95%CI:34.3~72.5)。HS-20093在未接受及接受过紫杉烷类化疗的患者中均展现出抗肿瘤活性。
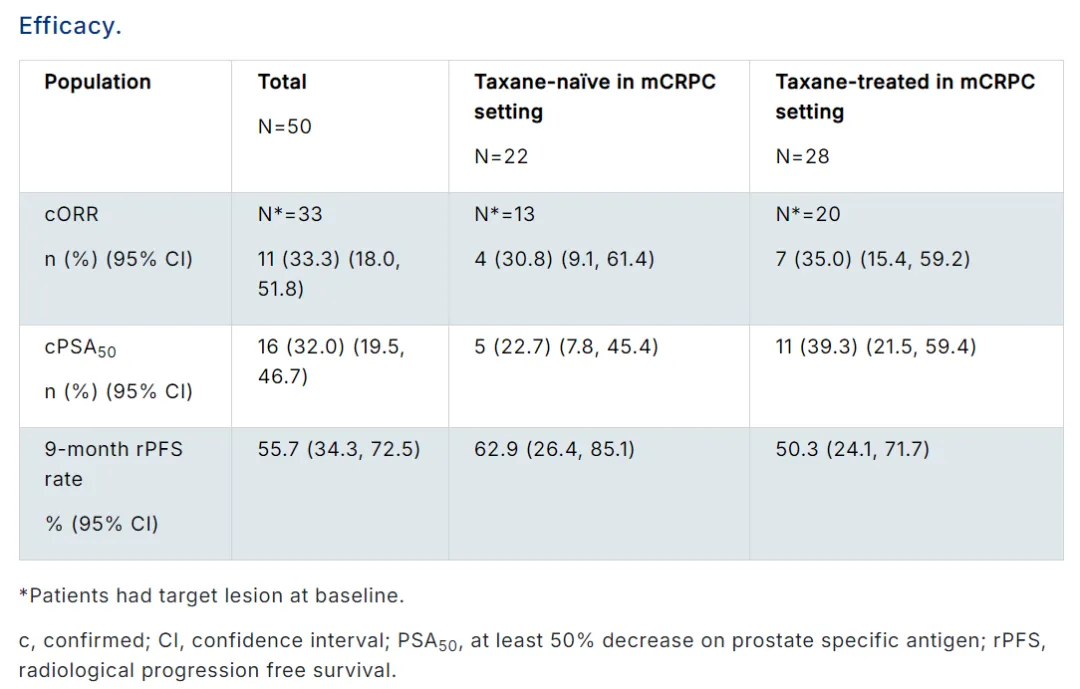
49例(98.0%)患者出现治疗相关不良事件(TRAEs),其中54.0%为≥3级,20.0%为严重不良事件(SAE);最常见的TRAEs为血液学毒性与胃肠道毒性,与既往报道的安全性特征一致。研究期间发生1例2级间质性肺疾病。
▎结论
HS-20093单药治疗mCRPC患者展现出较好的抗肿瘤活性,患者整体耐受性良好,安全性特征可控。
摘要号:169
A phase 1b/2 study to evaluate the safety and efficacy of igermetostat (XNW5004)in combination with enzalutamide in patients with metastatic castration-resistant prostate cancer.
Igermetostat(XNW5004)联合恩扎卢胺治疗mCRPC患者的安全性和有效性Ⅰb/Ⅱ期临床研究
讲者:YuanChang教授
▎研究背景
EZH2过表达与mCRPC患者预后不良相关。研究证实,抑制EZH2可逆转去势抵抗性前列腺癌(CRPC)对恩扎卢胺(E)的耐药。Igermetostat是一款高选择性小分子EZH2抑制剂。本文报告Ⅰb/Ⅱ期研究(NCT06702995)中,Igermetostat联合恩扎卢胺治疗mCRPC患者的安全性与有效性结果。
▎研究方法
本项中国多中心Ⅰb/Ⅱ期研究,纳入接受过1种非E的新型内分泌治疗(NHT)、且经PCWG3标准评估该治疗后疾病进展的mCRPC患者。
Ⅰb期采用3+3设计进行剂量爬坡:Igermetostat设3个剂量组(800、1200、1600mg,口服,每日2次)联合恩扎卢胺(160mg,每日1次),从中筛选2个剂量组确定Ⅱ期推荐剂量(RP2D)。
Ⅱ期采用Igermetostat1200mg每日2次联合恩扎卢胺进行剂量扩展。
主要研究终点:RP2D、安全性、rPFS;同时评估最佳总体缓解(BOR)、前列腺特异性抗原较基线下降≥50%(PSA50)及药代动力学(PK)特征。
▎研究结果
截至2025年9月5日,共84例mCRPC患者接受Igermetostat联合恩扎卢胺治疗,剂量分别为800mg每日2次(n=3)、1200mg每日2次(n=65)、1600mg每日2次(n=16)。中位年龄69岁,既往中位系统治疗线数为2;
83.3%患者既往接受过阿比特龙治疗,15.5%存在内脏转移,10.7%既往接受过紫杉烷类化疗;
发生率≥30%的最常见TEAEs:腹泻(65.5%)、贫血(58.3%)、恶心(48.8%)、呕吐(40.5%)、乏力(36.9%)、食欲减退(34.5%),多数为1~2级。
疗效分析纳入53例既往接受阿比特龙治疗的患者,中位随访13.2个月:中位rPFS未达到(10.97,未达到),12个月rPFS率59.8%;中位总生存期(mOS)未达到;15例基线可测量病灶患者:BOR率26.7%,含4例部分缓解(PR);35例PSA可评估患者:11例(31.4%)达到PSA50缓解;1200mg每日2次剂量组:中位随访11.9个月,mrPFS未达到(11.01,未达到),12个月rPFS率70.8%,mOS未达到。
▎研究结论
Igermetostat联合恩扎卢胺治疗经阿比特龙治疗后的mCRPC患者,展现出可观的抗肿瘤疗效,安全性特征可控。
摘要号:181
The efficacy and safety of 177Lu-PSMA-617 in Chinese patients with post-taxane metastatic castration-resistant prostate cancer: From a multicenter phase Il study.
¹⁷⁷Lu-PSMA-617治疗紫杉类药物经治的中国mCRPC患者的疗效与安全性:一项多中心Ⅱ期研究
讲者:叶定伟教授
▎研究背景
全球Ⅲ期VISION研究已证实,¹⁷⁷Lu-PSMA-617可用于治疗既往接受过至少1种雄激素受体通路抑制剂(ARPI)及1~2线紫杉烷类方案治疗的mCRPC患者。¹⁷⁷Lu-PSMA-617联合最佳标准治疗(BSoC)可使患者中位rPFS达到8.7个月。
▎研究方法
本项开放标签、多中心、单臂Ⅱ期研究(NCT05670106)旨在评估¹⁷⁷Lu-PSMA-617治疗前列腺特异性膜抗原(PSMA)阳性的中国mCRPC患者的疗效,入组患者均接受过至少1种ARPI及1~2线紫杉烷类方案治疗后疾病进展。研究采用两阶段设计:主体阶段仅纳入基线存在至少1个可测量软组织病灶的患者;扩展阶段额外纳入伴或不伴可测量病灶的患者。所有患者在接受最佳标准治疗的基础上,予¹⁷⁷Lu-PSMA-617(7.4GBq±10%)静脉输注,每6周1次,最多治疗6个周期。
主要研究终点为主体阶段患者经盲法独立中心审查(BICR)依据PCWG3修正版RECIST1.1标准评估的软组织客观缓解率(ORR)。
▎研究结果
2023年6月1日至2024年1月17日,研究共纳入62例患者(中位年龄68.5岁;72.6%的患者既往接受过≥3种ARPI治疗),其中59例接受治疗(主体阶段29例,扩展阶段30例)。
中位随访时间14.29个月,主体阶段患者ORR为41.4%(95%CI:23.5%~61.1%),与VISION研究结果相当(VISION研究中¹⁷⁷Lu-PSMA-617联合BSoC组为51.1%,单纯BSoC组为3.1%);基于所有可测量病灶患者的ORR为39.2%(95%CI:25.8%~53.9%,n=51)。
安全性分析集(n=59)中,44.1%的患者发生≥3级TRAEs,23.7%出现治疗相关SAE,18.6%因TRAEs终止治疗。发生率≥2%的最常见≥3级重点关注不良事件包括骨髓抑制(42.4%)、肝毒性(8.5%)及肾毒性(3.4%),未观察到3级口干事件。上述安全性特征与¹⁷⁷Lu-PSMA-617已知的安全性谱一致。
▎结论
本研究是首个证实¹⁷⁷Lu-PSMA-617在中国mCRPC患者中疗效与安全性的临床试验,支持该药物联合最佳标准治疗具有良好的获益-风险比。
摘要号:234
TRIM28-mediated SUMOylation of ERG at K389 and its association with cell proliferation, PARP inhibitor response, and 53BP1 expression in castration-resistant prostate cancer.
TRIM28介导ERG在K389位点的SUMO化修饰及其与CRPC细胞增殖、PARP抑制剂应答及53BP1表达的关联
讲者:Shiwei Liu教授
▎研究背景
携带同源重组修复(HRR)基因突变的前列腺癌(PCa)患者通常对PARP抑制剂(PARPi)敏感,但这种应答在HRR缺陷患者中并不一致。原发性及获得性PARP抑制剂耐药仍是CRPC治疗中的主要障碍,阐明其潜在分子机制具有重要意义。
▎研究方法
本研究首先分析PARP抑制剂耐药前列腺癌组织中ERG的表达水平,及其与CRPC细胞耐药的相关性;通过分子实验鉴定TRIM28介导的ERGSUMO化修饰及其修饰位点(K389),评估ERGSUMO化对SPOP介导的蛋白降解、TP53BP1转录及同源重组修复能力的影响;最后采用小分子抑制剂(2D08)与多肽抑制剂(ERGK389peptide)验证阻断ERGSUMO化可逆转PARP抑制剂耐药。
▎研究结果
ERG在PARP抑制剂耐药前列腺癌组织中高表达,且与CRPC细胞耐药呈正相关。TRIM28介导ERG在K389位点发生SUMO化修饰,该修饰可抑制SPOP依赖的ERG降解,增强蛋白稳定性;同时抑制TP53BP1转录,提升细胞同源重组修复能力,降低对PARP抑制剂的敏感性。值得注意的是,2D08或ERGK389多肽抑制剂可阻断ERGSUMO化、损伤DNA修复功能,进而逆转PARP抑制剂耐药。
▎结论
TRIM28介导的ERGK389位点SUMO化通过稳定ERG蛋白、增强同源重组修复,成为驱动CRPC发生PARP抑制剂耐药的关键轴。该信号轴可作为耐药预测的潜在生物标志物及可干预药物靶点,TRIM28/ERG靶向治疗联合PARP抑制剂有望改善ERG阳性CRPC患者的治疗结局。
摘要号:744
Sacituzumab tirumotecan (Sac-TMT) plus pembrolizumab (Pembro) in participants (Pts) with advanced urothelial carcinoma (UC): Results from phase 2 2870-002/SKB264-II-06 study.
芦康沙妥珠单抗(Sac-TMT)联合帕博利珠单抗(Pembro)治疗晚期尿路上皮癌(UC)患者:Ⅱ期2870-002/SKB264-II-06研究结果
讲者:卞晓洁教授
▎研究背景
对于不耐受顺铂的局部晚期或转移性尿路上皮癌(la/mUC)患者,一线治疗选择有限,存在尚未满足的新型治疗方案需求。芦康沙妥珠单抗(Sac-TMT,MK-2870/SKB264)是一款靶向TROP2的ADC,采用独特的双功能连接子,可最大化将新型贝洛替康衍生拓扑异构酶I抑制剂有效载荷递送至肿瘤细胞。该药在多种肿瘤中均展现出抗肿瘤活性,包括单药治疗尿路上皮癌。本研究旨在评估芦康沙妥珠单抗联合帕博利珠单抗治疗特定实体瘤患者的效果。
▎研究方法
入组标准:年龄≥18岁、既往未接受过治疗、不耐受顺铂的la/mUC患者。若患者既往接受过含铂新辅助/辅助化疗或纳武利尤单抗治疗,且治疗结束后疾病复发时间>12个月,仍符合入组条件。
患者接受芦康沙妥珠单抗4或5mg/kg静脉输注(非随机分组),每42天为一个治疗周期,分别于第1、15、29天给药;联合帕博利珠单抗400mg静脉输注,每42天周期第1天给药,最长治疗2年,直至疾病进展或出现不可耐受的毒性。
主要研究终点:安全性,以及研究者依据RECISTv1.1标准评估的ORR。次要研究终点:研究者评估的DCR、DoR及PFS。
▎研究结果
截至2025年5月21日,共40例患者接受芦康沙妥珠单抗联合帕博利珠单抗治疗(26例为4mg/kg剂量组,14例为5mg/kg剂量组)。中位随访时间14.5(范围:11.6~21.8)个月,中位年龄66.5岁,37例(93%)为亚洲患者,24例(60%)为上尿路尿路上皮癌。
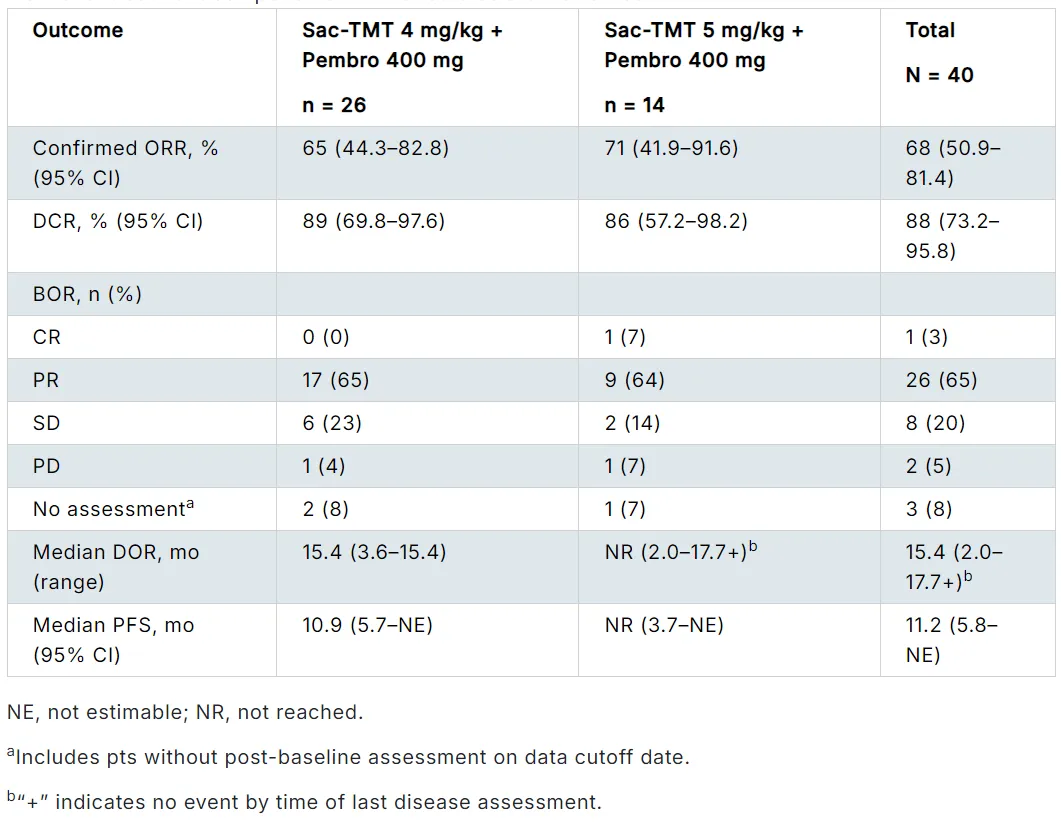
cORR为68%,中位DoR为15.4个月,中位PFS为11.2个月。
39例(98%)患者出现TRAEs,其中23例(58%)发生3~4级TRAEs;发生率≥10%的3~4级TRAEs为贫血(15%)、中性粒细胞计数降低(15%)及口腔炎(10%)。未发生治疗相关死亡事件。
▎结论
在既往未接受治疗、不耐受顺铂的la/mUC患者中,芦康沙妥珠单抗4mg/kg及5mg/kg剂量联合帕博利珠单抗均展现出令人鼓舞的抗肿瘤活性,安全性特征可控,且与单药治疗的安全性谱一致。该联合方案值得进一步开展临床研究。
摘要号:762
Intravesical T3011, an IL-12/anti-PD-1 armed oncolytic HSV-1,in BCG-naive high-risk NMIBC:A phase lla trial.
膀胱内灌注携带IL-12/抗PD-1的溶瘤Ⅰ型单纯疱疹病毒T3011治疗未接受卡介苗的高危非肌层浸润性膀胱癌:一项Ⅱa期临床试验
讲者:叶定伟教授
▎研究背景
膀胱内灌注卡介苗(BCG)是未接受过BCG治疗的高危非肌层浸润性膀胱癌(NMIBC)患者的标准治疗方案。然而,BCG制剂短缺是全球性问题,加之BCG治疗本身的不良反应,约30%~40%的患者无法获得有效的BCG治疗。因此,寻找优于BCG的替代治疗方案以满足临床需求至关重要。
疱疹病毒T3011注射液(MVR-T3011)是一款处于临床阶段、用于肿瘤免疫治疗的溶瘤Ⅰ型单纯疱疹病毒(HSV-1)。该病毒经基因工程改造,在肿瘤局部表达两种强效免疫调节因子:白细胞介素-12(IL-12)与抗PD-1抗体。本研究旨在评估膀胱内灌注T3011治疗未接受BCG的高危NMIBC患者的疗效与安全性。
▎研究方法
本研究纳入未接受过BCG治疗的NMIBC患者,采用两个剂量水平的MVR-T3011行膀胱内灌注:2.0×10⁹空斑形成单位(PFU)、1.0×10¹⁰PFU(均为50mL溶液)。为简化给药流程,治疗前不进行膀胱冲洗。
MVR-T3011诱导治疗为每周1次,共6周(必要时可进行第二次诱导治疗);维持治疗为每3周1次,直至满2年。
主要疗效终点为无原位癌(CIS)的乳头状Ta/T1期患者12个月无复发生存率(RFS)。
▎研究结果
截至2025年10月10日,共16例乳头状Ta/T1期患者接受MVR-T3011单药治疗(3例予2×10⁹PFU剂量,13例予1×10¹⁰PFU剂量),其中8例完成疗效评估。在可评估疗效的患者中,3个月(n=8)、6个月(n=5)、9个月(n=3)、12个月(n=1)及15个月(n=1)RFS均为100%。
研究未报告3级及以上TEAEs或SAE。
▎结论
MVR-T3011在乳头状Ta/T1期病变中展现出令人鼓舞的初步疗效,且安全性特征良好,有望成为未接受BCG治疗的NMIBC患者的有效替代治疗方案。
摘要号:764
Phase 1/2 study of an anti-PD-L1/L-15 variant fusion protein (SIM0237)in BCG-unresponsive high-risk non-muscle-invasive bladder cancer(NMIBC).
抗PD-L1/IL-15变体融合蛋白(SIM0237)治疗卡介苗无应答高危非肌层浸润性膀胱癌(NMIBC)的Ⅰ/Ⅱ期临床研究
讲者:叶定伟教授
▎研究背景
卡介苗(BCG)无应答的非肌层浸润性膀胱癌(NMIBC)治疗选择有限。抗PD-1单药治疗、IL-15激动剂联合BCG,在BCG无应答的原位癌(CIS)型NMIBC中已展现出临床疗效。同时靶向PD-L1与IL-15能否在NMIBC中产生协同作用尚不明确。
SIM0237是一种抗PD-L1/IL-15变体融合蛋白。在剂量爬坡阶段,该药单药用于BCG无应答NMIBC患者已显示出良好的安全性与积极的疗效信号。本文报告正在开展的Ⅰ/Ⅱ期研究(NCT06186414)中,SIM0237单药治疗剂量爬坡与剂量扩展阶段的数据。
▎研究方法
入组BCG无应答的高危NMIBC患者,接受膀胱内灌注SIM0237治疗,遵循标准诱导/维持方案。若患者在第3个月仍存在持续性原位癌或高级别Ta期病变,可进行再诱导治疗。
主要研究终点包括:剂量限制性毒性(DLT)、安全性、耐受性、PK及疗效指标(原位癌型NMIBC的完全缓解率(CR)及DoR;单纯乳头状NMIBC的无病生存期(DFS)及特定时间点无病生存率)。
▎研究结果
2024年1月10日至2025年8月8日数据截止日,共43例患者接受SIM0237单药治疗(10例为伴或不伴Ta/T1病变的原位癌,33例为单纯乳头状癌);给药剂量分别为75mg(3例)、150mg(10例)、300mg(30例)。
患者中位年龄62岁,男性占81%,既往接受BCG灌注中位次数为13次。在7例完成至少1次基线后肿瘤评估的原位癌患者中,6例最佳疗效达到CR,其中5例持续维持CR状态。在33例单纯乳头状癌患者中,中位随访时间4.57个月,中位DFS尚未成熟,12个月无病生存率为75.4%(95%CI:48.9%~89.4%)。
安全性方面:38例(88.4%)患者出现TEAEs,23例(53.5%)出现TEAEs,绝大多数为1/2级,且局限于泌尿系统。
▎结论
膀胱内灌注SIM0237用于BCG无应答高危NMIBC患者,安全性与耐受性良好,且展现出积极的临床疗效。SIM0237单药用于该人群的Ⅲ期临床研究正在规划中。


 更多医疗资讯,点击“阅读原文”查看
更多医疗资讯,点击“阅读原文”查看

