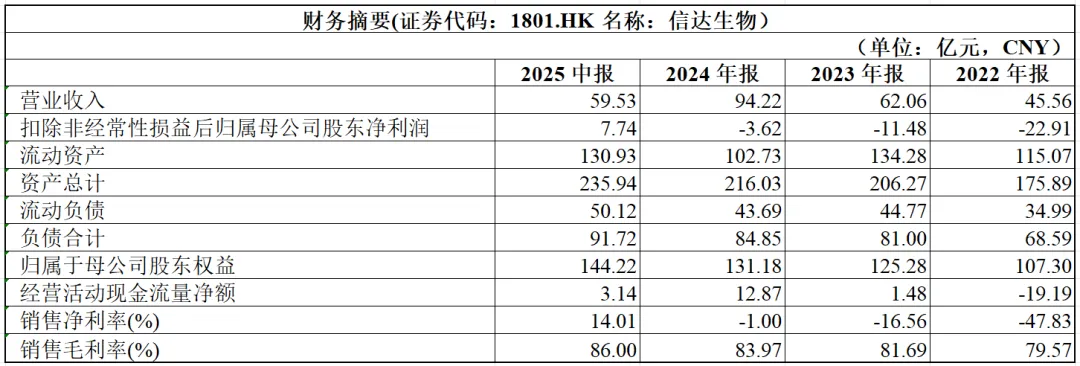
截至2025年9月,公司申请专利1408项,其中PCT国际申请212件,国内外授权专利251件,已在中国、美国、欧洲、日本、韩国、澳大利亚等多个国家或地区进行专利布局。公司已经建立一条包括37个新药品种的产品链,覆盖肿瘤、代谢疾病等多个疾病领域。已有18个产品获得批准上市。同时,4个新药分子进入III期或关键性临床研究,另外还有15个新药品种已进入临床研究。
二、产品
公司产品丰富,已有18个产品获得批准上市,它们分别是信迪利单抗注射液(达伯舒®),贝伐珠单抗注射液(达攸同®),阿达木单抗注射液(苏立信®),利妥昔单抗注射液(达伯华®),佩米替尼片(达伯坦®),奥雷巴替尼片(耐立克®), 雷莫西尤单抗注射液(希冉择®),塞普替尼胶囊(睿妥®),伊基奥仑赛注射液(福可苏®),托莱西单抗注射液(信必乐®),氟泽雷塞片(达伯特®),匹妥布替尼片(捷帕力®),己二酸他雷替尼胶囊(达伯乐®),利厄替尼片(奥壹新®),替妥尤单抗N01注射液(信必敏®),玛仕度肽注射液(信尔美®),匹康奇拜单抗注射液(信美悦®)和伊匹木单抗N01注射液(达伯欣®)。目前,4个新药分子进入III期或关键性临床研究,另外还有15个新药品种已进入临床研究。
达伯舒®(信迪利单抗注射液):是信达生物制药和礼来制药共同合作研发的具有国际品质的创新 PD-1 抑制剂药物。信迪利单抗是一种人类免疫球蛋白 G4(IgG4)单克隆抗体,能特异性结合 T 细胞表面的 PD-1 分子,从而阻断导致肿瘤免疫耐受的 PD-1/ 程序性死亡受体配体 1(Programmed Death-Ligand 1, PD-L1)通路,重新激活淋巴细胞的抗肿瘤活性,从而达到治疗肿瘤的目的。
适应症(九项,前八项进医保):至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗;表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、 不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌的一线治疗;表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI) 治疗失败的 EGFR 基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌患者的治疗;不可手术切除的局部晚期或转移性鳞状非小细胞肺癌的一线治疗;既往未接受过系统治疗的不可切除或转移性肝细胞癌的一线治疗;不可切除的局部晚期、复发或转移性食管鳞癌的一线治疗;不可切除的局部晚期、复发或转移性胃及胃食管交界处腺癌的一线治疗;联合呋喹替尼胶囊用于既往系统性抗肿瘤治疗后失败且不适合进行根治性手术治疗或根治性放疗的晚期错配修复完整(pMMR)的子宫内膜癌患者;联合伊匹木单抗N01用于可手术切除IIB-III期的MSI-H/dMMR结肠癌新辅助治疗(附条件批准)。
达攸同 ®(贝伐珠单抗注射液):是由信达生物自主开发的重组抗 VEGF人源化单克隆抗体药物。适应症包括非小细胞肺癌、结直肠癌、胶质母细胞瘤、肝细胞癌(联合阿替利珠单抗)、上皮性卵巢癌、输卵管癌或原发性腹膜癌、宫颈癌、肝细胞癌(联合信迪利单抗)和EGFR-TKI治疗失败非小细胞肺癌(联合信迪利单抗)八项。
达伯华 ®(利妥昔单抗注射液):由信达生物和礼来制药共同开发的重组人-鼠嵌合抗 CD20 单克隆抗体注射液。适应症包括弥漫性大B细胞淋巴瘤,滤泡性淋巴瘤及慢性淋巴细胞性白血病。
苏立信®(阿达木单抗注射液,国际商标:SULINNO®):由信达生物自主开发的重组人抗肿瘤坏死因子-α(TNF-α)单克隆抗体药物。适应症包括类风湿关节炎、强直性脊柱炎、银屑病、多关节型幼年特发性关节炎、儿童斑块状银屑病、成年非感染性葡萄膜炎、成人和儿童克罗恩病。
达伯坦 ®(佩米替尼片,英文商标:Pemazyre®):由 Incyte 和信达生物共同开发,是全球首个获批靶向FGFR2融合/重排胆管癌的口服小分子抑制剂。主要治疗胆管癌。
玛仕度肽:是全球首个GCG/GLP-1双受体激动减重、降糖药物,作为一种哺乳动物胃泌酸调节素(OXM)类似物,玛仕度肽除了通过激动GLP-1R促进胰岛素分泌、降低血糖和减轻体重外,还可通过激动GCGR增加能量消耗增强减重疗效,同时改善肝脏脂肪代谢。适应症为成人肥胖和2型糖尿病患者的血糖控制。
三、管线
肿瘤管线:
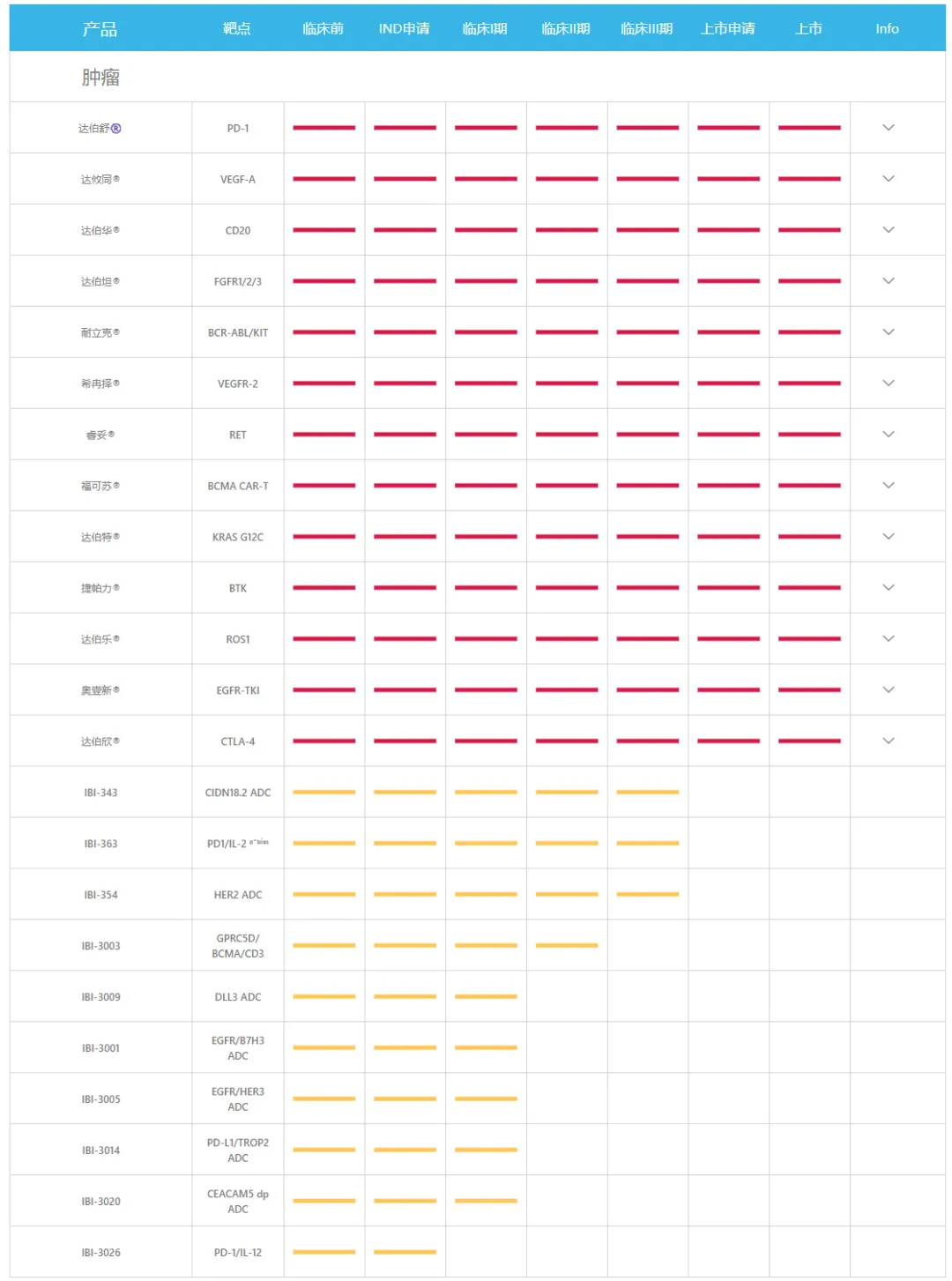
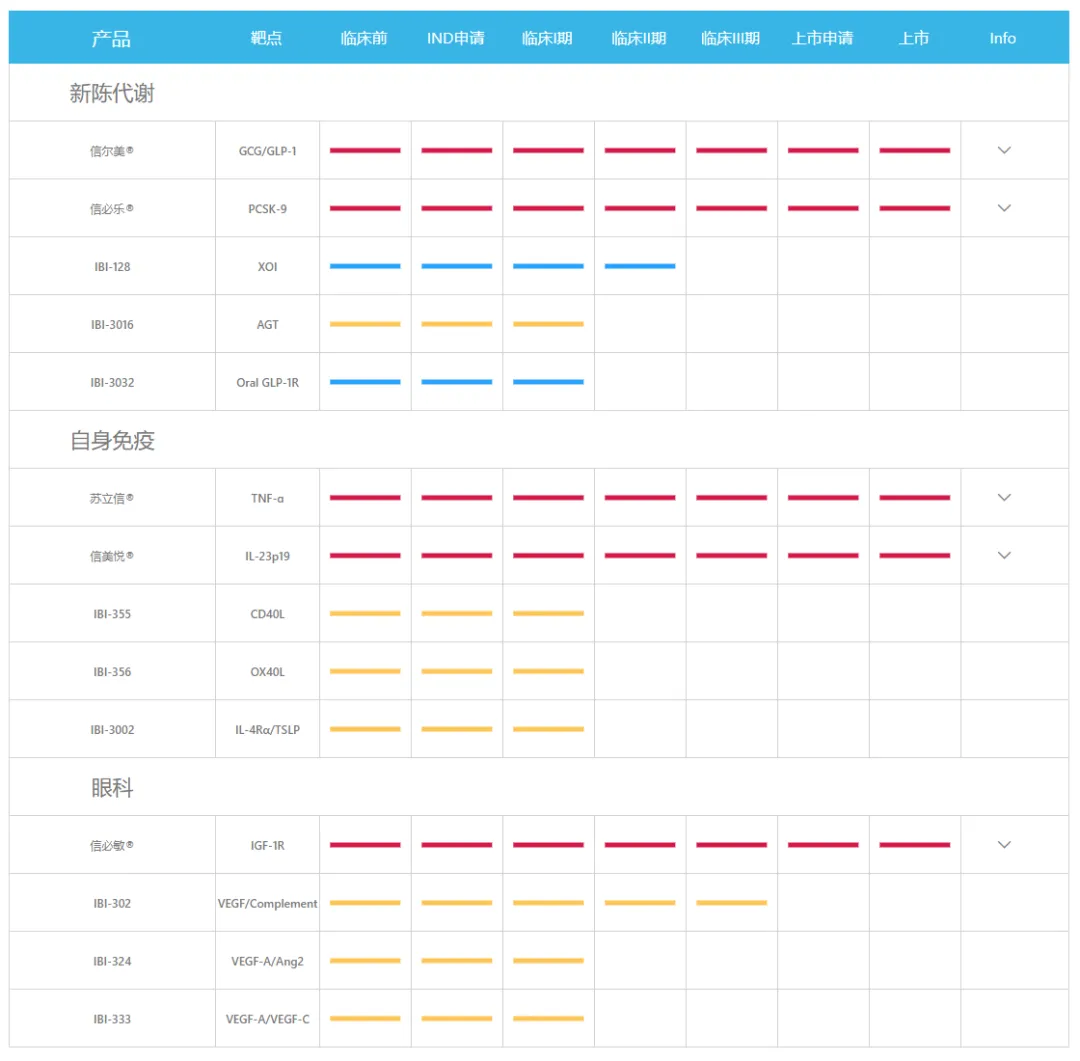
公司已与礼来、罗氏、武田、赛诺菲、Incyte和MD Anderson 癌症中心等国际合作方达成30多项战略合作,与美国礼来制药集团达成了多次总金额超过113.5亿美元的全面合作。