需要下载完整版报告的朋友,可以扫下方优惠券付费成为会员,40000+份报告,随意下载,不受限制,报告涵盖全行业,星球保持每日更新。客服微信:sgcwjc

专业/及时/全面的行研智库
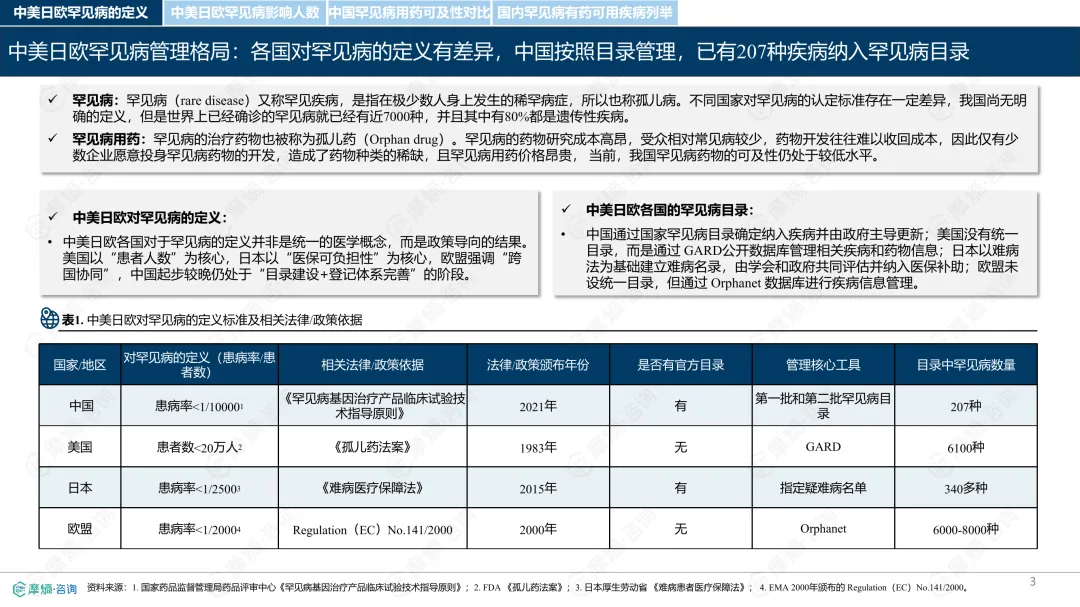
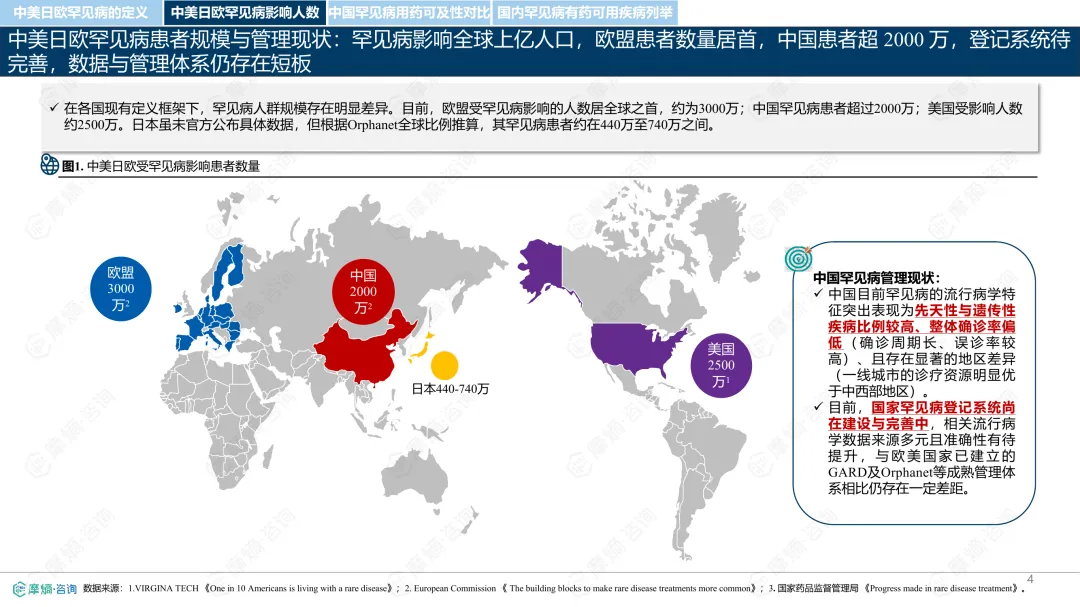
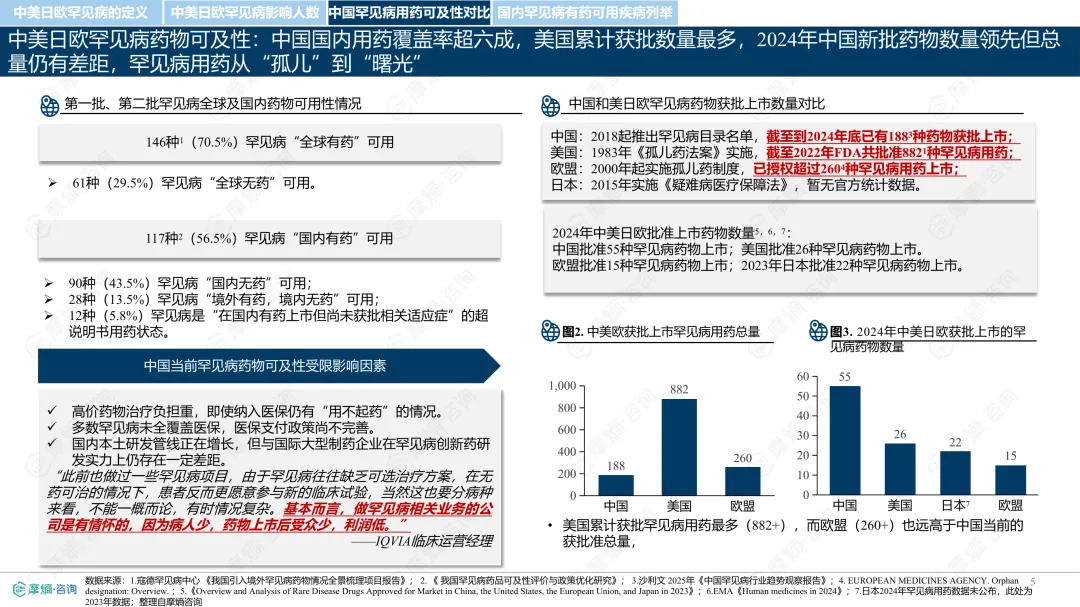
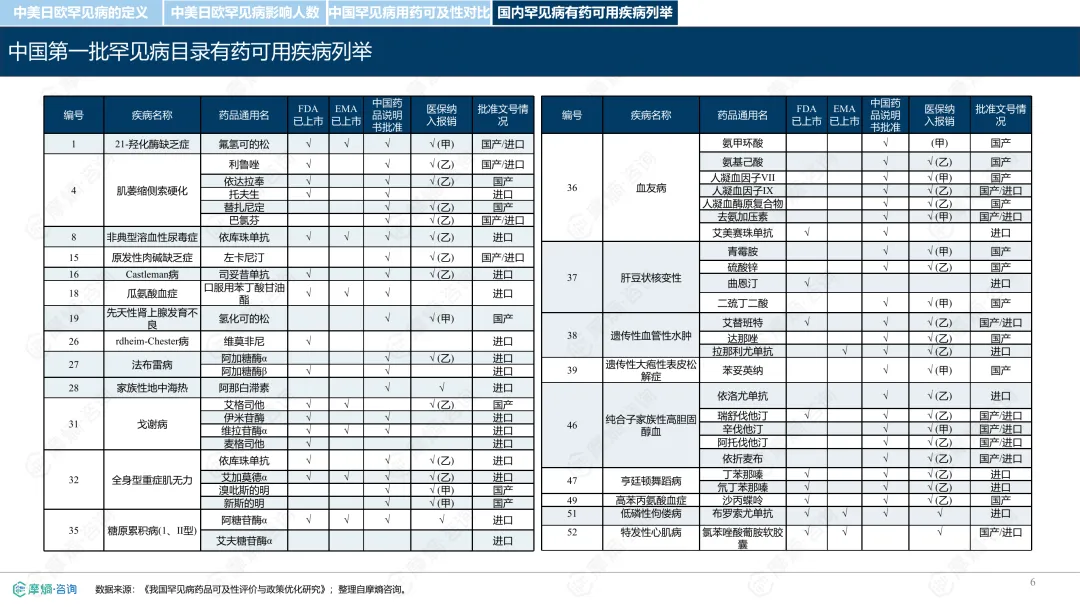
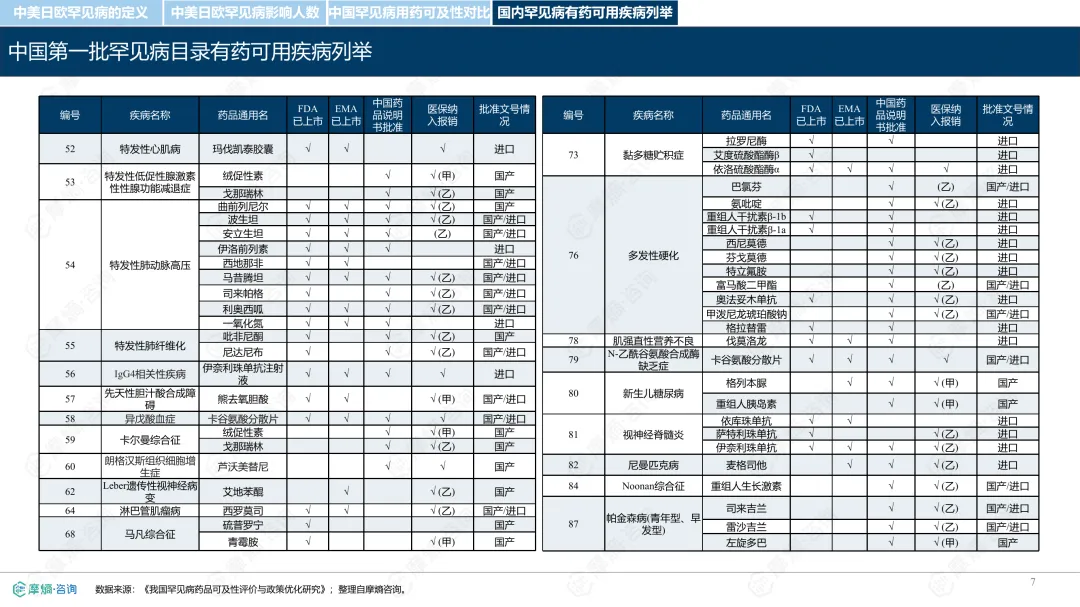
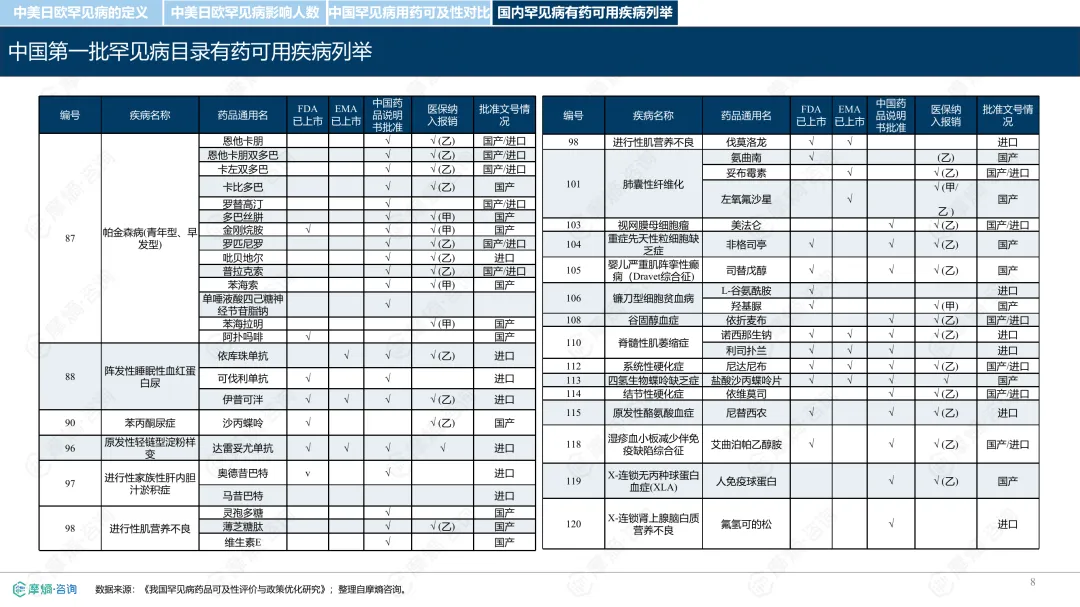
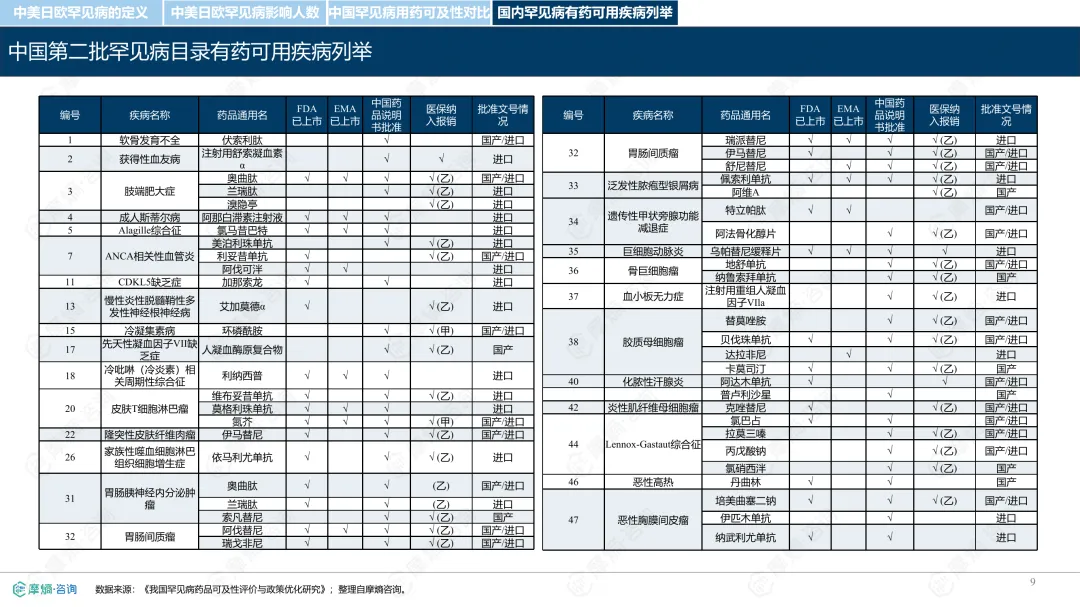
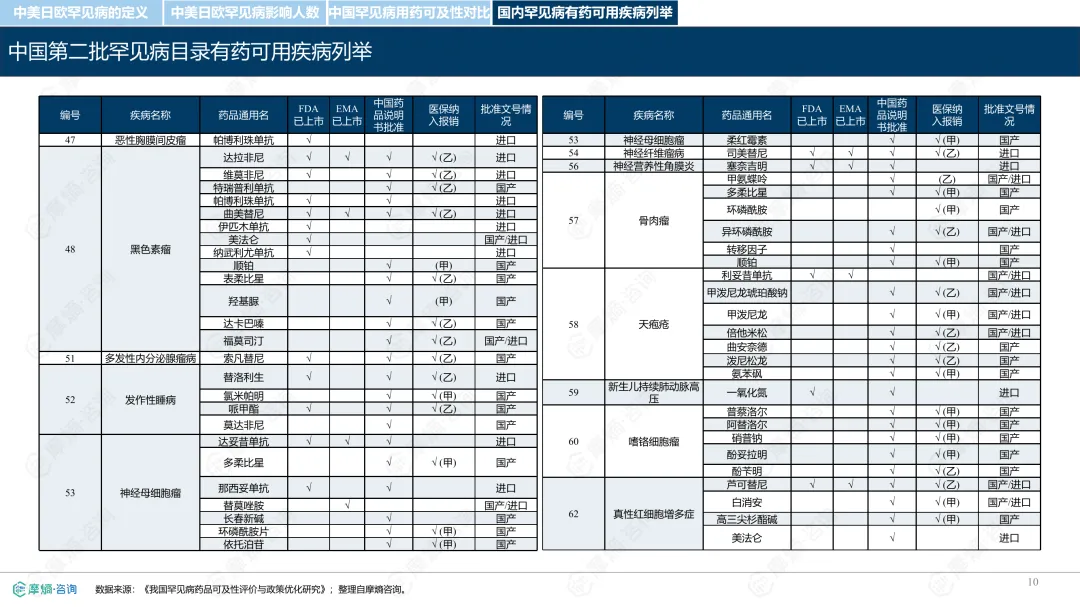
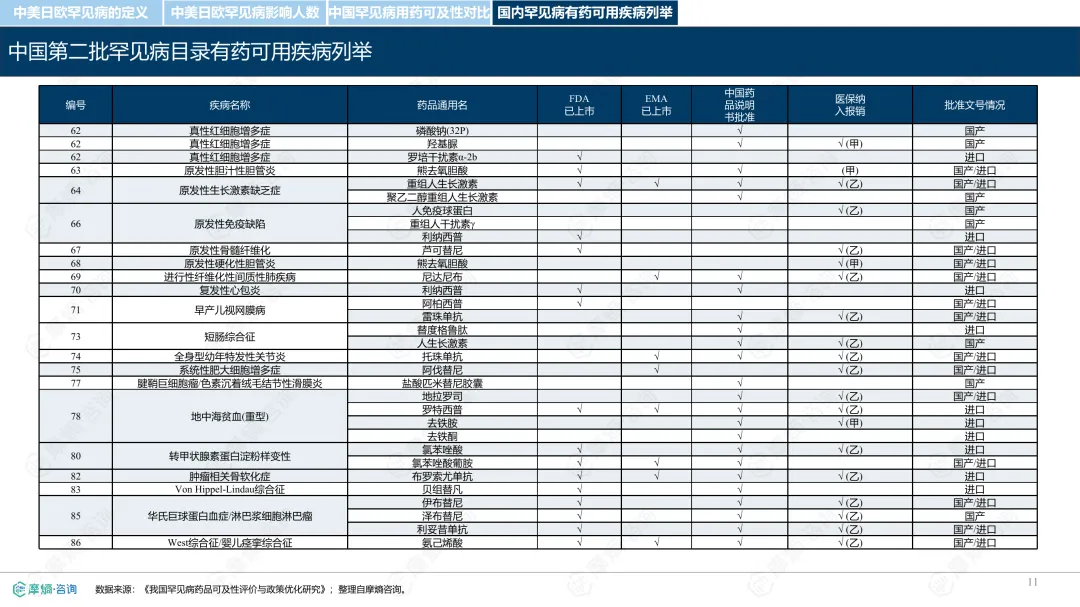
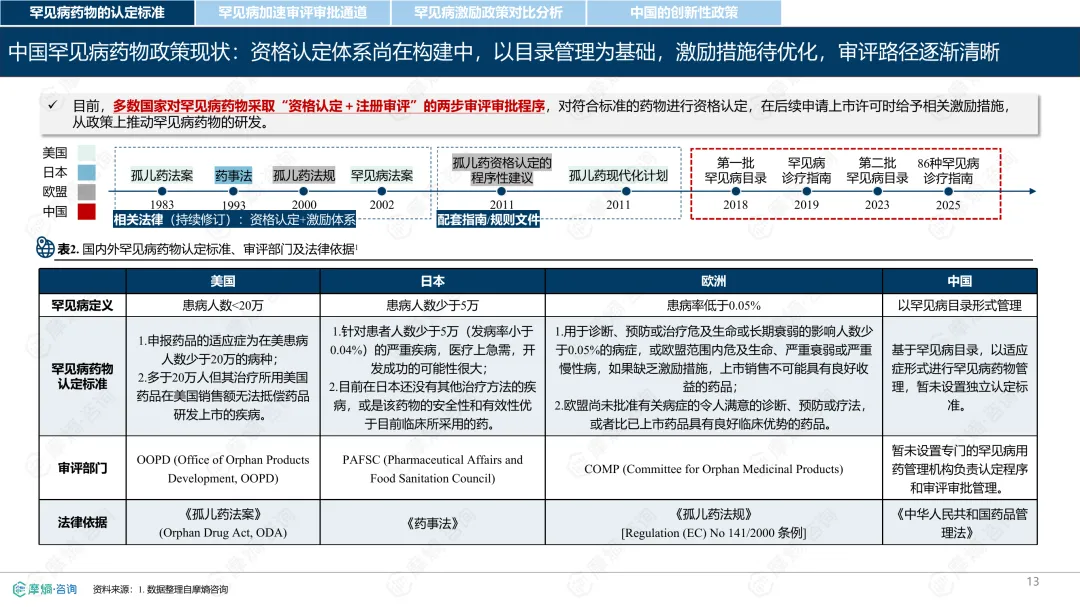
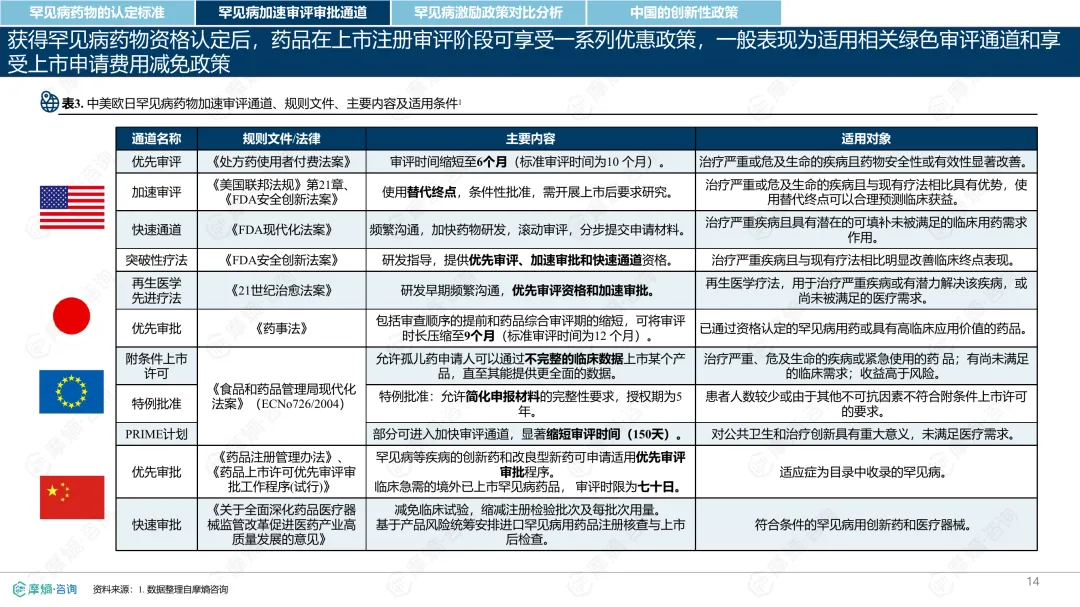
罕见病指在极少数人群中发生的疾病,全球已确认的种类接近7000种,其中80%为遗传性疾病。各国对罕见病的定义和管理方式存在差异。中国通过国家罕见病目录进行管理,目前已有207种疾病纳入;美国主要依赖GARD数据库进行信息管理,未设统一目录;日本以“难病”为基础建立名录,强调医保可负担性;欧盟则通过Orphanet数据库进行疾病信息管理,但未设立统一目录。从患者数量看,欧盟受影响人数最多,约3000万;中国超过2000万;美国约2500万;日本根据推算约为440万至740万。中国罕见病患者中,先天性和遗传性疾病占比高,确诊率低且地区间差异明显,登记系统尚在建设中。在药物可及性方面,截至2024年底,中国已有1883种罕见病药物获批上市,覆盖约70.5%的罕见病,但仍有近三成疾病无药可用。美国累计批准8821种罕见病用药,数量远超其他国家;欧盟批准超过2604种;日本暂无官方数据。2024年,中国批准55种罕见病药物,美国26种,欧盟15种,日本22种。中国罕见病用药可及性受限的原因包括:高价药物仍难以负担,多数疾病未纳入医保,本土研发能力虽在提升,但与国际领先企业相比仍有差距。部分药物虽在国内上市,但尚未获批适应症,或境外有药但境内未获批准。罕见病药物开发成本高、受众少,导致市场回报有限,企业投入意愿较低。尽管如此,部分企业仍因患者需求而参与相关研究,表现出一定的人文关怀。
来源:摩熵·咨询



完整版报告已上传至星球,扫下方优惠券加入即可下载所有报告


戳“阅读原文”下载报告


