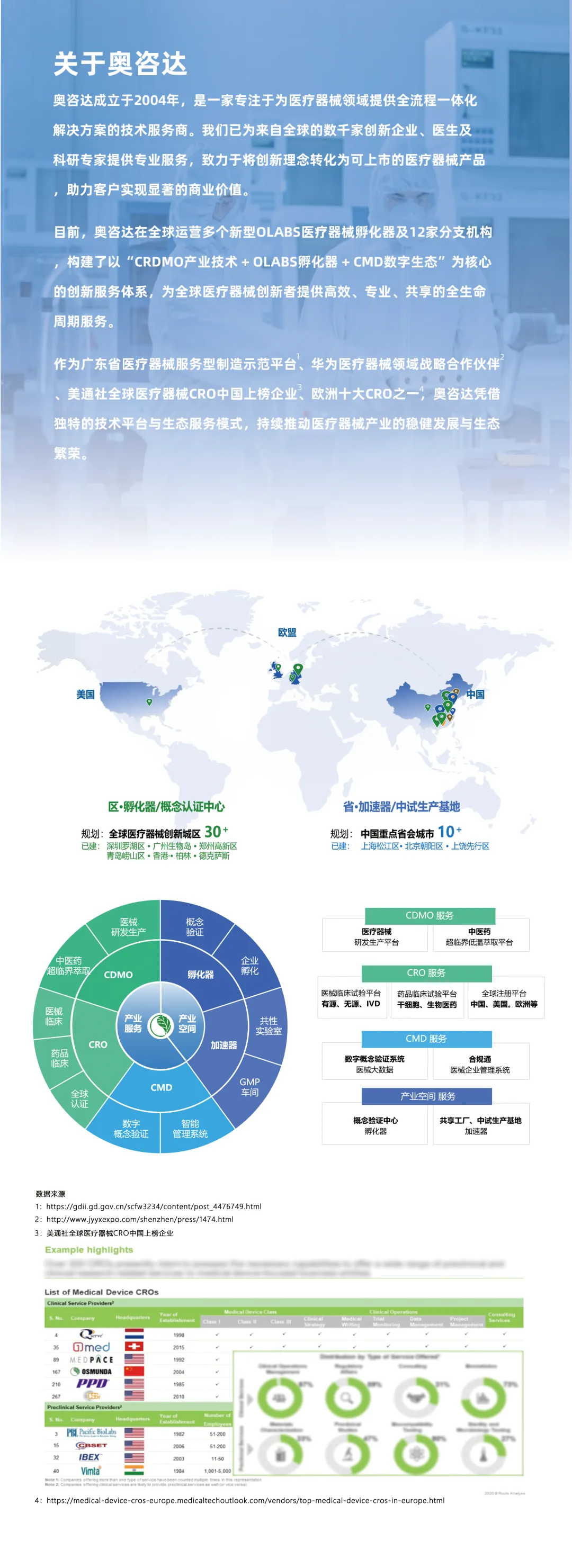
2025年已收官,医疗器械行业在结构性调整中孕育新机。基于奥咨达平台数据洞察,2025年上半年行业呈现重要转折信号:医疗器械出口总额达241亿美元,同比增长5.0%;创新医疗器械批准数量45个,同比大幅增长87%。2026,奥咨达基于全球视野与行业洞察,为企业提供破局前行的战略路径。
具体数据回顾《从 “国产替代” 到 “全球竞合”,2025医疗器械这些新机会别错过!》
一、
2026趋势:四大方向引领行业变革
1. AI医疗器械从"辅助"走向"核心"
AI诊断软件从影像领域向病理、生理信号分析全面扩展
预期AI赋能的治疗设备将进入快速爆发期
奥咨达布局:已服务30+ AI医疗项目,覆盖算法验证、数据合规、临床评价全流程
2. 全球注册从"单点"走向"协同"
中美欧三地同步注册成为头部企业标配
MDR过渡期结束将加速行业深度洗牌
奥咨达优势:依托全球网络,提供"一次测试、多国申报"解决方案,助力企业平均缩短40% 上市时间
3. 出海模式从"产品"走向"生态"
单纯产品出口升级为技术标准输出
本地化生产和运营成为深度国际化关键
奥咨达助力:通过CDMO+全球注册组合,已帮助200+ 企业实现从制造到品牌的全链条出海
4. 创新器械从"单一"走向"融合"
药物器械组合产品、数字疗法等跨界产品集中涌现
材料科学、生物技术与微电子的融合创新成为新增长极
奥咨达准备:组建跨领域专家团队,为融合创新产品提供一体化解决方案
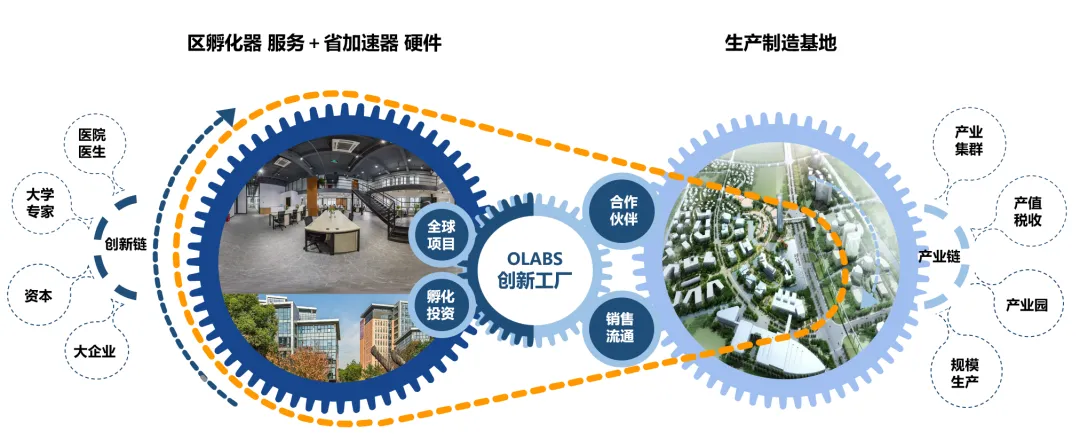
二、
奥咨达三维赋能:让全球竞合更简单
1.技术转化加速器
CDMO专业支撑:覆盖有源、无源、IVD全品类医疗器械制造
研发制造协同:设计阶段即考虑可制造性和法规符合性
成本优化:通过共享产能降低企业前期投入30%以上
2.法规合规导航仪
全球注册一站式:同步规划中美欧市场准入策略
临床试验全流程:从方案设计到中心管理,确保数据合规有效
法规动态预警:实时追踪政策变化,提前布局应对
3.出海落地护航舰
本地化服务网络:在重点出口市场建立深度合作
质量体系接轨:构建符合FDA QSR、ISO 13485的国际标准
市场精准匹配:针对各国医保支付特点,制定差异化策略

三、
实战案例:数据见证成效
案例一:电生理企业欧盟突破
某企业通过奥咨达MDR服务,9个月完成技术文档更新,较行业平均缩短40%,2025年上半年对欧出口增长65%。
案例二:AI医疗器械优先审评
借助奥咨达"研审联动",某AI诊断产品12个月获NMPA批准,创同类最快审批纪录。
案例三:骨科企业出海转型
通过奥咨达全球注册能力,某骨科企业海外业务占比从15%提升至35%,成功化解集采压力。
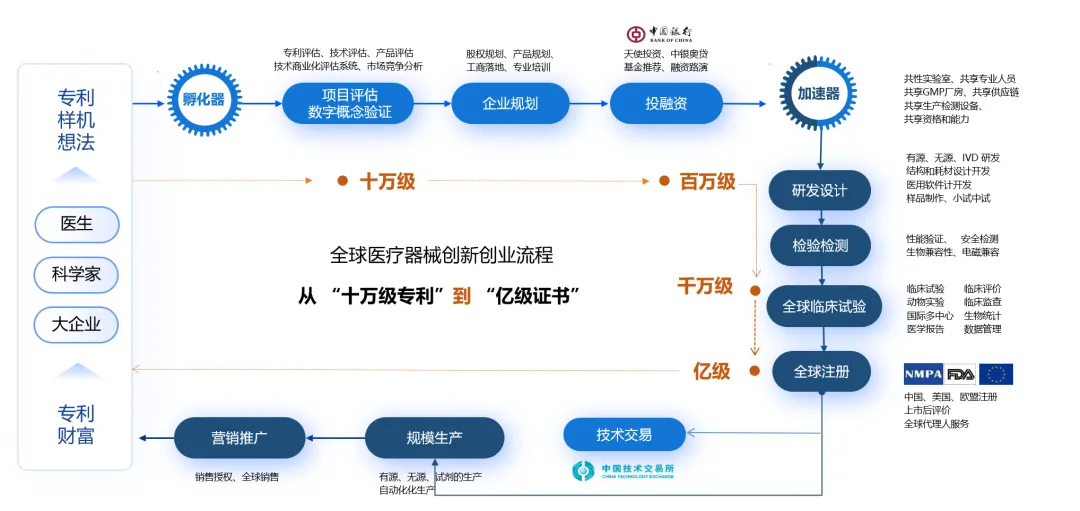
四、
2026战略建议:与奥咨达共赴新蓝海
基于对行业趋势的深度洞察,奥咨达为企业提供2026年精准布局建议:
技术领先型企业:聚焦AI医疗器械、脑机接口等前沿领域,借助我们的概念验证中心快速完成技术商业化论证,抢占创新制高点。
市场导向型企业:深耕家用医疗、可穿戴设备等消费医疗赛道,通过我们的CDMO柔性制造实现小批量、多品类的快速市场测试。
出海先锋企业:重点布局欧盟、东南亚等增长市场,依托我们的全球注册网络实现多国同步上市,最大化市场机会。
成本敏感型企业:利用我们的共享制造平台降低固定资产投入,通过MAH制度实现轻资产运营,专注核心能力构建。

客服二维码(热线400-6768632)

医械查小程序