2023年,枫林集团携手中科院上海药物所,针对国内外药物研发进展、政策热点及市场动态发布一系列行业调研及分析,希望该系列文章对生命健康产业领域创新生态系统参与者们有所启示。
CRISPR相关基因编辑技术是当前热门的生物工具之一。自2013年以来,CRISPR技术相关研究呈爆发式增长,2020年,艾曼纽·夏彭蒂耶与珍妮弗·道德纳因发现基因技术最锐利的工具之一——CRISPR/Cas9“基因剪刀”荣获诺贝尔化学奖。由于基因编辑可以解决临床前评价体系、新靶标发现、耐药性等问题,而受到广泛关注。本文将阐述CRISPR/Cas9技术的原理、技术优势与局限性、临床应用及产业情况。
技术发展历程及原理
基因编辑是一种对基因组序列进行精确修饰的技术,通过基因插入、基因敲除和碱基替换等对基因组靶位点进行一系列的人工修饰,以获得新的功能或表型。传统的基因编辑工具主要包括锌指核酸酶(zinc finger nucleases,ZFNs)、转录激活-效应器核酸酶(transcription activator-like effector nucleases,TALENs)和聚集的规则间隔短回文重复序列(clustered regularly interspaced short palindromic repeat,CRISPR)。ZFNs、TALENs第一代和第二代基因编辑技术,存在目标识别率低、成本高、脱靶率高、结构复杂及需要设计特定的蛋白识别靶DNA等缺点。2013年,Cell、Science、Nature Biotechnology等杂志接连报道了CRISPR/Cas9(clustered regularly interspaced short palindromic repeats-associated protein 9)基因编辑技术,将靶向基因编辑技术推向高潮。与传统的基因编辑技术相比,该技术具有良好的靶向性、构建简单、可同时操作多条基因等优点,迅速成为生物医学领域的前沿热点,引发了新一轮的基因治疗研究热潮。
发展历程及原理
CRISPR/Cas是原核生物抵御病毒感染或噬菌体入侵产生的一种适应性免疫系统,其主要通过适应、表达、干扰三个基本阶段来保护细菌免受病毒反复攻击。1987年,CRISPR序列首次被报道;2005年,研究者发现CRISPR中的居间序列并非细菌自身染色体所有,而是与病毒的部分基因组序列高度一致,因此,推测细菌可通过特定方式获取病毒DNA片段并整合到自身CRISPR序列中,当再次遇到相同的入侵者时,细菌可利用这些序列信息进行识别并将其破坏;2012年,Jennifer Doudna和Emmanuelle Charpentier等人证明CRISPR/Cas9系统可在体外切割双链DNA。2013年,Jennifer Doudna、George Church和张锋分别带领3个研究团队相继证明了CRISPR序列与Cas9蛋白结合后,可在人类细胞中高效地定位、剪切和修改基因组(图1)。此后,CRISPR技术迅速发展,多个具有特定功能的Cas9变异体被鉴定出来。自2016年以来,基于CRISPR的基因编辑技术陆续应用于临床并取得了巨大成功。

图1:CRISPR/Cas技术发展中的主要事件时间表
CRISPR/Cas系统包括三种主要类型(Ⅰ型、Ⅱ型和Ⅲ型),但在实现核酸识别的分子机制上各不相同。与Ⅰ型和Ⅲ型相比,Ⅱ型系统仅依赖于RNA引导的单一蛋白进行特异性的DNA识别和切割,因此,成为最常用的基因组编辑工具。CRISPR/Cas9系统属于Ⅱ型CRISPR/Cas系统,来源于SF370酿脓链球菌株(streptococcus pyogenes SF370),主要由引导RNA(guide RNA,gRNA)和Cas9蛋白组成。Cas9蛋白本质上是一种多域DNA核酸内切酶,负责切割目的基因形成双链断裂,也被称为遗传剪刀。在使用CRISPR/Cas9系统进行基因编辑时,研究人员把crRNA和反式激活crRNA(transactivating crRNA,tracrRNA)组合起来设计成单个引导RNA(single guide RNA,sgRNA),用来引导Cas9蛋白对对特异靶向DNA进行识别和切割,使DNA双链断裂,产生特异性DNA双链断裂(double strand break,DSB)。DSB形成之后,会经细胞自身的非同源末端连接(NHEJ)或同源重组修复(HDR)对双链断裂进行修复,最终实现目标基因敲除、敲入和碱基编辑等基因组遗传修饰。然而,NHEJ很容易出错,因此,可在DSB形成后,向细胞内导入靶位点的同源序列作为修复模板,然后,进行HDR,实现基因的精准编辑(图2)。
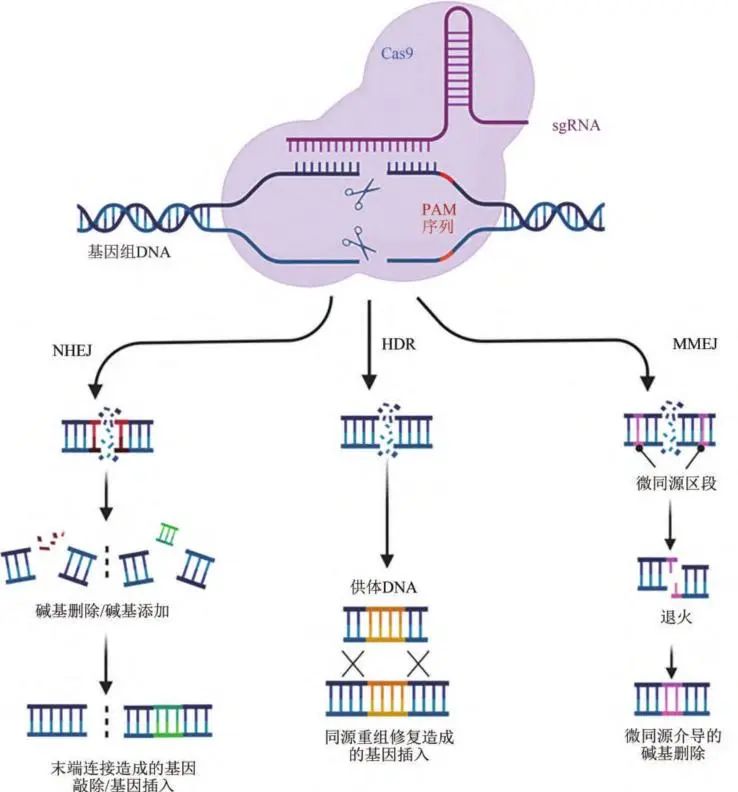
注:左侧为非同源末端连接修复(NHEJ)介导的片段删除/片段插入原理图;中间为同源重组修复(HDR)介导的基因编辑原理图;右侧为微同源末端连接(MMEJ)介导的基因编辑原理图
图2:CRISPR/Cas9基因编辑原理示意图
【参考资料】
1.Li T, Yang Y, Qi H, et al. CRISPR/Cas9 therapeutics: progress and prospects. Signal Transduct Target Ther, 2023, 8(1): 36.
2. 彭海航, 靳春鹏. CRISPR/Cas9技术在乙肝治疗中的研究与进展. 中国医药生物技术, 2022, 17(5): 433-439.
3. 程得洛. CRISPR/Cas9基因编辑技术及其在肿瘤治疗方面的研究进展. 系统医学, 2020, 5(20): 195-198.
4.庞紫燕, 官阳阳, 孙嘉磊, 等.CRISPR/Cas9基因编辑工具开发与应用研究进展. 生物化工, 2022, 8(5): 140-148.
5. 滕小龙, 史硕博. CRISPR/Cas9系统在基因组编辑中的优化与发展. 合成生物学, 2023, 4(1): 67-85.
6.博雅辑因、邦耀生物等公司官网.
7.药明康德、生物谷等媒体报道.
往期回顾:
撰稿:枫林集团、中科院药物所
枫林国际
www.fenglin-group.com





▇ 扫码关注我们



