以下文章来源于生物药大时代
2019年针对冠状病毒(COVID-19)的mRNA疫苗取得了巨大成功后,引起了人们对mRNA表达治疗性蛋白质的兴趣,过去十年广泛的研究使mRNA更有希望在临床实现其治疗潜力。与基于DNA载体的经典基因治疗相比,mRNA具有多种优势,例如瞬时表达、不需要进入细胞核并且没有染色体整合的风险等,在传染病预防、癌症甚至罕见病领域等均具有广阔的应用前景。
mRNA疫苗或药物的生产工艺,主要分为质粒DNA原液制备、mRNA原液制备、mRNA制剂制备三个阶段。质粒是生产用于治疗和预防传染病及癌症所需的mRNA疫苗和药物的重要原料,在近几年来市场需求强劲,质粒介导的水平基因转移被认为是细菌适应和多样化的主要驱动力。质粒DNA在基因治疗和基因疫苗接种的临床研究应用中变得越来越重要,这一快速发展领域的经济前景强调了GMP级别的大规模、稳定、高效质粒生产迫在眉睫。
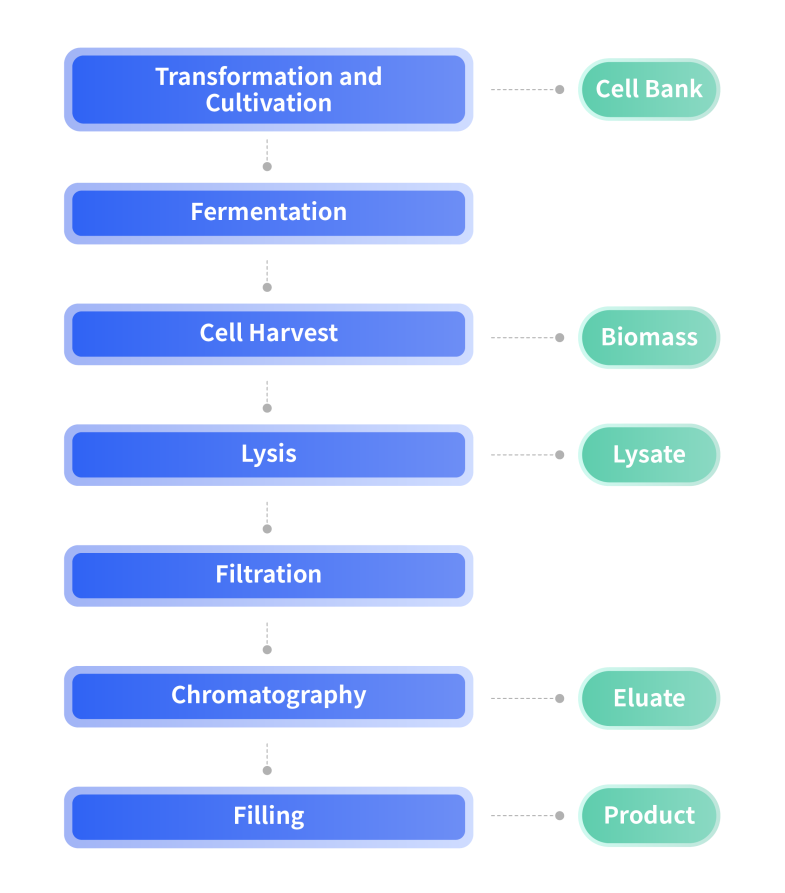
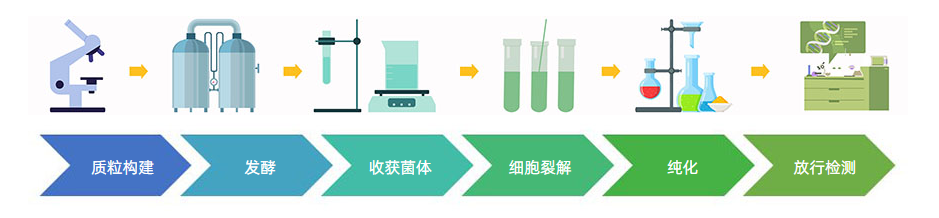
质粒DNA是双链共价闭环DNA分子,其大小范围为0.8 ~120kb;质粒DNA的形式有:超螺旋、开环及线性形式。质粒DNA的生产流程包括发酵、初步分离和纯化等步骤,总结如图1所示。因质粒DNA在临床试验中的应用以及未来作为批准药物使用的广阔前景,使得根据GMP制定的稳健和可扩展的质粒DNA生产过程应运而生,且必须满足相应的准则和法律的要求。大肠杆菌K12宿主细胞经转染质粒DNA后进行扩增。除了使用合格且来源清楚的生产菌株进行所需质粒DNA的微生物扩增外,用于生产质粒的病毒和细菌细胞库的制备应在GMP条件下进行,并且至少有一个主细胞库(MCB/WCB),细胞库必须明确证实拥有足够的数量且保存适宜以便用于后续的生产,确保生产的连续性,并且可以建立MCB和WCB生长和生产率的可比性。这种高细胞密度的培养物已经被描述为来自大肠杆菌的各种产品,包括重组蛋白、抗体或聚羟基丁酸酯。生产的DNA质量主要取决于生产条件。设计质粒载体和选择宿主的早期过程应考虑到大规模生产中对高产量的需求,并预测发酵和下游加工过程中反复出现的一些问题,通过选择高拷贝数的质粒载体或对生长温度进行调节可以有效降低下游纯化中RNA和gDNA受污染的程度,且用于临床级质粒DNA生产的载体应该来源清楚,溯源明确。此外,为了获得可重复的结果,在可控条件下的发酵罐中进行细胞培养是至关重要的。在摇床中,气体交换是不可控的,也不可能调节pH和在某些情况下的进料流,在此过程中振动筛的填充量即使有微小的变化也会导致不可再现的结果。对高密度、大规模培养,需要考虑连续流离心或微过滤方式浓缩收集菌体。菌体收获后,可采用机械破碎(如珠磨法、渗透压冲击方法等)、酶解法、热裂解和碱裂解法进行裂解。其中碱裂解法是较常用的质粒DNA提取方法,其优点是收获率高,适于多数的菌体,所得产物经纯化后可满足多数的DNA重组操作。这一过程步骤至关重要,因为质粒DNA产物的主要污染源是细菌染色体DNA(chrDNA),此步骤释放的也是chrDNA,但是裂解时间、pH值、菌体和碱混合均匀程度等因素严重影响着质粒DNA的产量和质量。
基于质粒DNA药物的高质量要求,以及监管部门(EMEA 1998,FDA 1998)制定的指南,导致了不同纯化策略的开发。在大多数情况下,质粒DNA通过碱裂从细胞中释放出来,然后通过离心或过滤进行澄清。在碱性裂解过程中,染色体DNA和质粒DNA均被碱性的pH调节法变性。由于染色体DNA具有极强的剪切敏感性,容易导致DNA片段化,因此细胞破碎的放大是整个纯化过程的关键步骤之一。简单地将实验室规模的碱裂解放大到工业搅拌釜式反应器,在间歇模式下,会对质粒和宿主细胞染色体DNA产生剪切力,从而降低产品浓度,污染产品流。
温和裂解可以通过将生物质悬浮液和裂解缓冲液连续混合,然后在静态混合器中和裂解液来实现,但这种方法并未解决碎片去除的问题。为此,必须采用耗时的程序,如离心或过滤,并且在这些澄清步骤中的剪切力也可能导致含有小片段染色体DNA的产品流的污染。大规模生产质粒中需注意的问题
---充分考虑生产工艺稳健放大
虽然质粒是通过发酵在大肠杆菌中产生的,许多重组蛋白也是如此,但是关于其大规模生产的加工方法的报道,无论是来自工业界还是学术界都很少。因此,开发和运行能够可重复地满足产品规格和监管机构制定的标准的大规模生产和纯化过程是一个挑战。
大规模工艺应在预期治疗用途所固有的纯度、效力、特性、有效性和安全性规格下生产一定量的质粒(以质量或生物活性来衡量),其中一些要求是在产品和工艺开发过程中逐一确定的。事实上,治疗药物和开发中疾病的特定因素(如剂量、给药途径、给药频率和疾病状态)对于制定产品规格非常重要。
质粒安全性和效价与纯度直接相关,如果质粒不纯,其含有的杂质和污染物会严重影响转染复合体的形成,可以诱导一系列免疫学和生物学反应。而且质粒的纯度会严重影响到转染的效率,转染效率将直接决定病毒载体的产量,此外,如果质粒中残余内毒素成分,不仅会严重影响转染效率,还存在着安全隐患。质粒载体应主要以超螺旋形式存在,这种认识虽然没有明确的理论支撑,但普遍认为超螺旋形式可以比开放环状、线性、多聚体或部分变性的DNA更有效地转移基因表达。因此,对于最终产品中允许的超螺旋形式的最小质粒量,应该存在一个规格。质粒DNA的规模化生产通常是在高密度发酵情况下进行的,而在大规模生产过程中,发酵罐中细胞生长到高密度往往伴随着热量、动量和质量传递问题。在某些质粒-宿主系统中,由于氧气供应不足导致的氧限制会导致强烈的分离不稳定性。质粒的生产会受到不稳定性问题的阻碍,包括下游加工过程中的稳定性、应用后的稳定性以及储存和运输过程中的稳定性。在分裂过程中,质粒在子细胞之间的分配缺陷而导致的分离不稳定性,可以通过调节分离步骤(par A位点与CER功能)的基因或通过在培养基中添加抗生素来抑制分离后无质粒细胞的增殖来解决。但在生产培养过程中,应尽量避免选择抗生素,防止产品中可能存在对某些抗生素(如β-内酰胺类)残留的过敏反应,导致多聚体形成等问题的结构稳定性更难消除。金斯瑞蓬勃生物拥有完善且工艺稳定的GMP生产平台,能确保批次间和批次内质粒质量的稳定性,保证质粒高质量交付,能够为客户提供从临床前到商业化阶段的环状质粒和线性化质粒一站式服务。金斯瑞蓬勃生物的线性化质粒GMP平台拥有两套成熟的生产工艺,能够根据项目质粒特点,提供最优解决方案。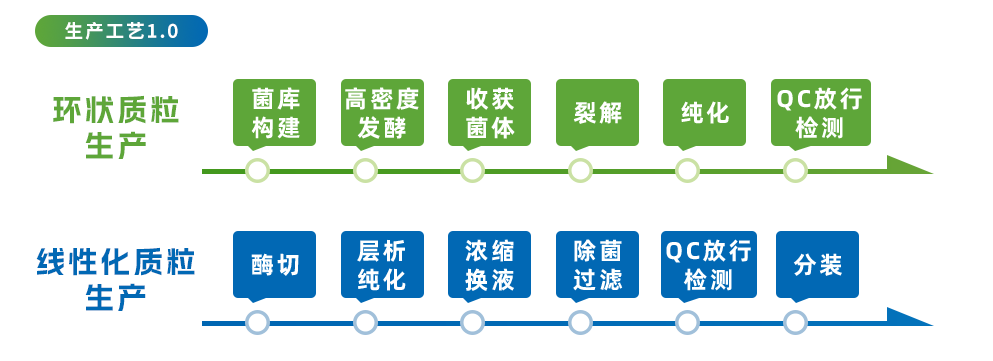
高密度培养工艺
经典三步纯化
环状质粒生产&放行
线性化质拉生产&放行
高密度培养工艺
环状中间体管控
减纯化步骤,提高回收率
总产量提高2-3倍
线性化质粒质量标准不变
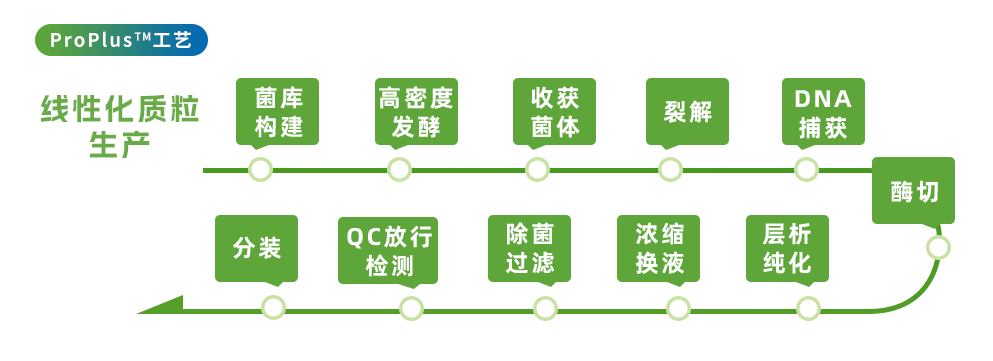
金斯瑞蓬勃生物的线性化质粒服务整体解决方案涵盖了非注册临床、工艺开发、注册临床和商业化全阶段质粒生产。ProPlus™工艺由金斯瑞蓬勃生物自主开发,并已申请专利。该工艺有着回收率高、产量高、生产周期短的特点。在保持线性化质粒高质量标准的同时,使总产量提高2~3倍,周期缩短50%。金斯瑞蓬勃生物已支持中国第一个mRNA项目获得EUA,并支持全球客户获得近40个IND临床批件。为了满足临床和商业化需求,探寻mRNA质粒生产利器,9月6日15:00,药融圈邀请金斯瑞蓬勃生物 Dr. Ming Ni 就“mRNA质粒生产策略:线性化质粒生产工艺ProPlus™,助力产量提升并缩短周期”为主题进行分享,在此次会议中,让我们一起寻找mRNA模板质粒不同的生产策略,探讨金斯瑞蓬勃生物的ProPlus™工艺。点击下方关注公众号
后台回复“0906”即可获得报名二维码
识别二维码点击【立即预约】即可报名
点击开播提醒不错过
金斯瑞子公司金斯瑞蓬勃生物(GenScriptProBio)拥有一站式生物药研发生产平台,主要致力于为细胞和基因治疗(CGT)药物、疫苗、抗体及重组蛋白药物等提供从靶点开发到商业化生产的端到端CDMO服务。金斯瑞蓬勃生物在美国、荷兰、韩国、上海、香港、南京等地设有公司以服务全球客户。自2017年10月,共助力美国、欧洲、亚太等区域客户获得60余个IND批件。
金斯瑞蓬勃生物的细胞和基因治疗整体解决方案涵盖了非注册临床、工艺开发,注册临床和商业化全阶段质粒、病毒、mRNA疫苗及核酸药物生产。金斯瑞蓬勃生物的生物药开发解决方案涵盖生物药尤其是抗体药发现、抗体工程和抗体评价。在生物药CDMO服务方面,金斯瑞蓬勃生物为客户提供包括细胞系开发、宿主细胞商业化授权、上下游工艺开发、分析方法开发和临床样品及商业化生产等在内的一体化CDMO服务,并提供分批补料和灌流工艺以满足增长的抗体蛋白药的需求。GMP生产车间满足FDA、EMA和NMPA监管要求。
金斯瑞蓬勃生物始终以“合作加速创新”为理念,致力于帮助客户缩短生物药进入临床的时间,显著降低客户的研发成本,加速医药转化,共创健康未来。