
01 爱尔康
爱尔康公司于 5 月 6 日公布,其 2026 年第一季度净销售额为 26.9 亿美元,比 2025 年第一季度的 24.5 亿美元增长 10%。
1.1 外科手术业务
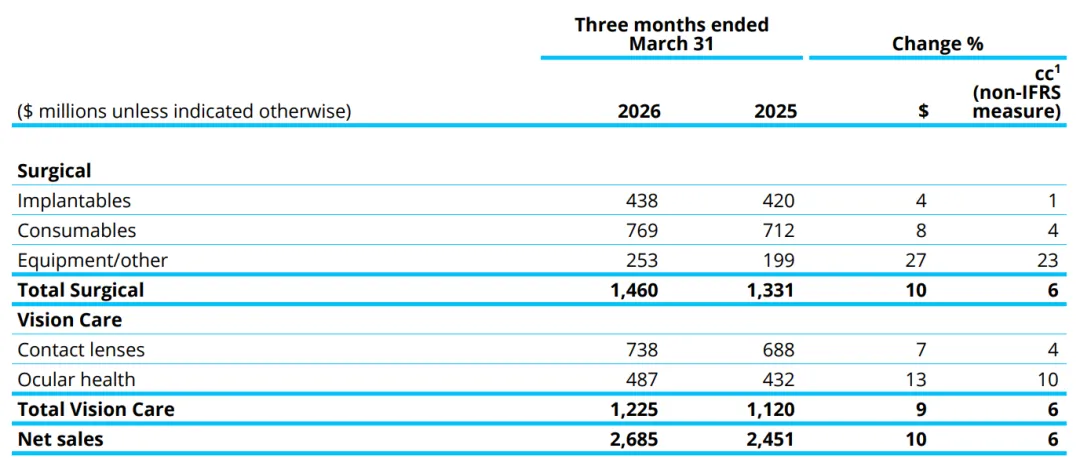
2026 年第一季度,外科手术业务净销售额(含植入物、耗材及设备 / 其他业务)为15 亿美元,较 2025 年同期增长 10%。
植入物:净销售额为 4.38 亿美元,增长 4%。该业绩增长主要得益于PanOptix Pro产品的强劲市场表现;同时受国际市场持续竞争压力、青光眼手术产品销量下滑拖累。
耗材:净销售额为7.69 亿美元,增长 8%。主要受白内障市场需求疲软及产品提价共同作用。
设备/其他:净销售额为 2.53 亿美元,同比增长 27%。增长主要由Unity 一体化平台等新款设备上市驱动。
2026 年第一季度,视力保健业务净销售额(含隐形眼镜和眼健康产品)为 12 亿美元,较 2025 年第一季度按报告汇率计算增长 9%。
隐形眼镜:净销售额为 7.38 亿美元,增长 7%。增长源于产品创新与价格上调,部分被传统老旧产品销量下滑所抵消。
眼部健康:净销售额为 4.87 亿美元,增长了 13%。业绩增长由Tryptyr、Systane(思然)等干眼症产品组合强势拉动。
02 豪雅
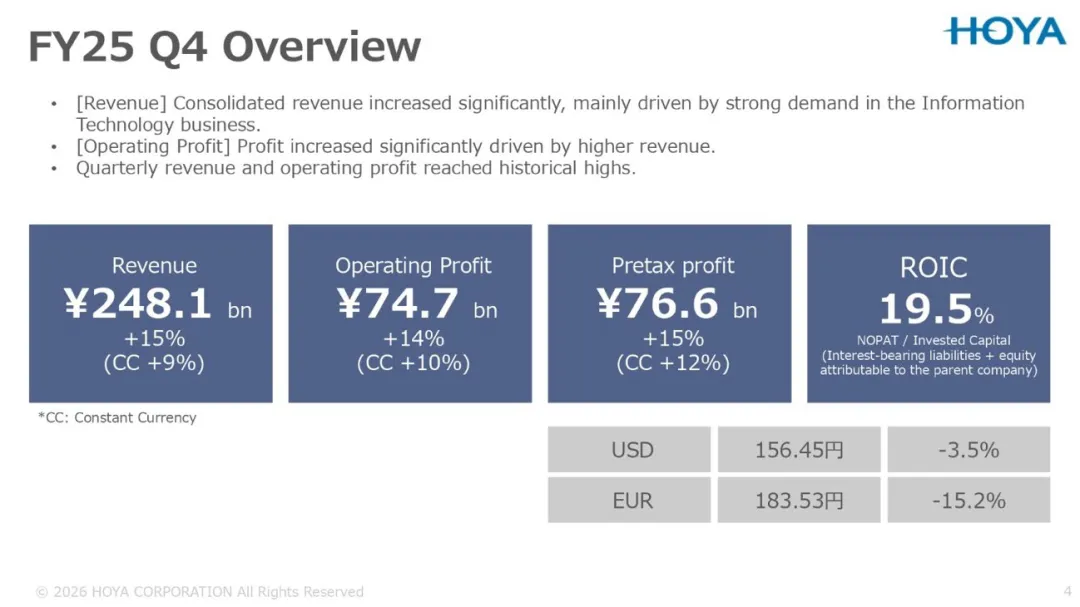
豪雅 4 月 30 日公布,公司截至 2026 年 3 月 31 日总收入(即 2025 财年第四季度)为 2481 亿日元(约16亿美元),比 2025 年同期增长 15%。
2.1 生活护理业务
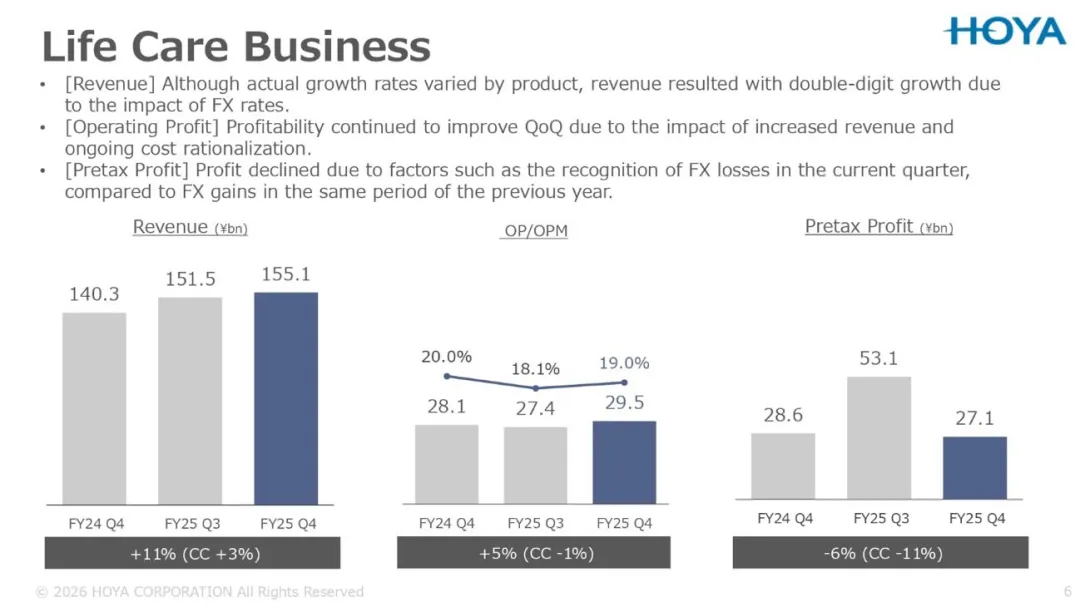
生活护理业务收入为1551 亿日元,同比增长11%。各产品、区域增长分化,整体增长温和,但全年盈利能力稳步提升,季度营业利润率持续改善,2026 财年将延续这一趋势。
其中眼镜镜片同比增长为11%。欧美市场疲软,亚非拉市场支撑业绩;中国市场凭借第二代 MiYOSMART iQ 上市、渐进镜片销量提升重回增长轨道。2026 财年目标:全面推广 MiYOSMART iQ、推出新款渐进镜片,实现稳健增长。

其中隐形眼镜同比增长 4%。自有品牌产品、订阅服务提升客户留存;高附加值产品(日抛、多焦点镜片)占比提升。2026 财年目标:精准获客、打通线下门店与订阅服务体验,开拓新销量。

人工晶状体增长了8%。日本核心市场单焦点IOL医院销售稳定;中东地缘冲突导致销量下滑;中国市场在实行集采政策后出现萎缩,导致已获监管部门批准的产品的潜在市场规模缩小,短期内,公司计划将成本控制在当前营收水平,而中长期来看,将通过高附加值产品寻求增长。2026 财年目标:扩大三焦点 / 增强型单焦点IOL销量、稳定供应链,实现超越市场的增长。

2.2 信息技术业务
非医疗领域略。
03 安进
安进 4 月 30 日报告称,其 Tepezza 产品 2026 年第一季度的收入为4.9 亿美元,比 2025 年第一季度的 3.81 亿美元增长 29%。
Pavblu(阿柏西普生物类似药,对应原研药 Eylea)2026 年第一季度实现营收2.8 亿美元,较上年同期的 9900 万美元大幅增长183%;其中美国市场收入 2.76 亿美元,美国以外市场收入 400 万美元。安进公司于 2024 年第四季度推出了 Pavblu,这是美国首个用于治疗视网膜疾病的 Eylea 生物类似药,包括湿性年龄相关性黄斑变性、视网膜静脉阻塞后黄斑水肿、糖尿病性黄斑水肿和糖尿病性视网膜病变。
04 Ocular

该公司表示,截至 2026 年 3 月 31 日,其现金余额为 6.667 亿美元,预计可维持到 2028 年,并将继续推进 Axpaxli 用于治疗视网膜疾病的研发。
05 Xbrane
Xbrane于 5 月 5 日报告称,其 Ximluci(Lucentis 的生物类似药)2026 年第一季度的收入为 1720 万瑞典克朗(约为 180 万美元),而该公司的总收入为 1730 万瑞典克朗。
相比之下,Ximluci 在 2025 年第一季度的销售额为 4660 万瑞典克朗(460 万美元),总收入为 9320 万瑞典克朗(930 万美元)。
Xbrane 表示,尽管销量有所下降,但在毛利率相对较高的市场,2026 年第一季度终端客户销售收入实现增长,使得实际利润分成与 2025 年第四季度基本持平。本季度,Xbrane 向 STADA 交付的最终产品数量减少,实现收入1700 万瑞典克朗。不过,受此前库存累积影响,各季度交付量差异较大,全年收入流将呈现不均衡状态。
Xbrane 正积极推进产品生产成本优化措施,预计2027 年开始见效。此外,公司已于2026 年 4 月下旬向 FDA 提交上市许可申请,预计审批决定日期为2026 年 11 月。此前导致公司在 2025 年 10 月收到 FDA 完整回复函(CRL)的合同生产企业,现已完成 FDA 检查所有整改事项,并已向监管机构提交相关证明文件。
Ximluci是雷珠单抗的生物类似药候选药物,对应原研药 Lucentis,属于 VEGFa 抑制剂,用于治疗多种严重眼部疾病。Ximluci 所针对的全球市场规模约为每年 130 亿欧元。
2022 年,欧洲药品管理局(EMA) 批准 Ximluci 在欧洲 27 个成员国用于治疗以下适应证:湿性年龄相关性黄斑变性(AMD)、糖尿病性黄斑水肿(DME)、糖尿病性视网膜病变(PDR)、视网膜静脉阻塞(RVO)、脉络膜新生血管(CNV)导致的视力损伤。Ximluci 在欧洲获批的剂型为小瓶注射液,由眼科医生抽取至注射器后进行眼内注射。
Ximluci 由 Xbrane 合作方STADA于2023 年第一季度在欧洲上市。截至当季末,Ximluci 已在欧洲20 个市场及欧洲以外4 个市场获批上市。
Xbrane 计划于2026 年 4–5 月向美国 FDA提交上市许可申请,预计6 个月后获得审批结果。2024 年 5 月,STADA 与 Xbrane 同 Valorum 签署合作协议,由 Valorum 负责 Ximluci 在美国的商业化。
STADA 正积极推动 Ximluci 在中东、拉美、东南亚等其他地区的上市,已向上述地区多家监管机构提交上市申请。



