引言
利用游离DNA(cfDNA)进行常见胎儿非整倍体的产前筛查,即游离无创产前检测(cfNIPT),目前已被广泛采用,并被推荐作为提供给所有妊娠个体的一线筛查方法¹。游离DNA筛查对21三体、18三体和13三体具有高灵敏度和特异性,还能够评估胎儿性染色体非整倍体和微缺失的风险。
高风险cfDNA结果后的当前标准诊疗流程是转诊进行绒毛膜绒毛取样(CVS)或羊膜穿刺术的诊断性检测。CVS通常在妊娠10至14周进行,具有早期诊断的优势,但受限于较窄的操作时间窗和可及性限制。在许多地区,特别是农村和服务不足地区,接受过CVS操作培训的医师相对较少,这给及时诊疗造成了地理和后勤障碍²。羊膜穿刺术虽然更易获得,但在妊娠较晚阶段进行,通常在妊娠16周后,可能会延迟诊断。这两种操作均为有创性,存在虽小但具有临床意义的妊娠丢失风险,这可能影响患者的决策。因此,患者和临床医师在决定进行有创检测时,需要更多信息来更好地解读高风险cfDNA结果。显然存在对一种非侵入性方法的未满足需求,尤其是在妊娠早期,以支持更知情、个体化的临床决策。
循环胎儿细胞提供了一个独特的机会,可以在无需有创操作的情况下直接分析代表胎儿遗传物质的完整细胞。这些细胞在母体循环中的存在和丰度与胎盘发育密切相关,通常在妊娠10至15周之间达到峰值可用性³⁻⁹。这种基于胎儿细胞的检测可以提供一个可及的确认性数据点,其准确性潜力与CVS未培养细胞的结果相当⁴'⁷。
基于这一生物学基础,我们开发了一种循环胎儿细胞捕获(CFC)检测方法,从母体血液中分离这些胎儿细胞,并应用单细胞基因组分析来评估染色体拷贝数。通过整合细胞型生物标志物和信息丰富的SNP基因分型来区分胎儿胎盘细胞与母体细胞,这种方法比单独的cfDNA能够更直接地评估胎儿染色体状态。
这种方法的临床影响是显著的。通过在高风险cfDNA结果后提供额外的非侵入性基因组信息,CFC检测使患者和临床医师能够就诊断性检测做出更知情的决策。这在CVS可及性有限的情况下尤为重要,因为地理差异、培训差距和操作时间限制可能会限制患者的选择¹⁰。对于考虑羊膜穿刺术的患者,CFC提供了一个在妊娠后期进行有创操作之前获得更多清晰度的机会。虽然羊膜穿刺术是金标准,但大多数具有高风险cfDNA筛查结果的患者并未寻求或无法获得诊断确认的选择¹¹'¹²。对于这些患者,CFC分析能够在比妊娠中期胎儿解剖学检查更早的孕周提供胎儿基因组组成的额外见解,且不产生风险。
在本白皮书中,我们描述了这种CFC检测的开发和初步临床性能,并讨论其通过更精确、可及和以患者为中心的诊疗来改善产前保健的潜力。
方法
研究设计与研究对象
本研究纳入单胎妊娠的妊娠个体。评估了两个人群:(1)符合临床标准的常见非整倍体(21三体、18三体、13三体和性染色体非整倍体,以及22q11.2微缺失)高风险cfDNA筛查结果的个体,和(2)低风险cfDNA结果的个体队列。本研究经WCG IRB批准。CFC检测工作流程与CVS工作流程的比较见图1。
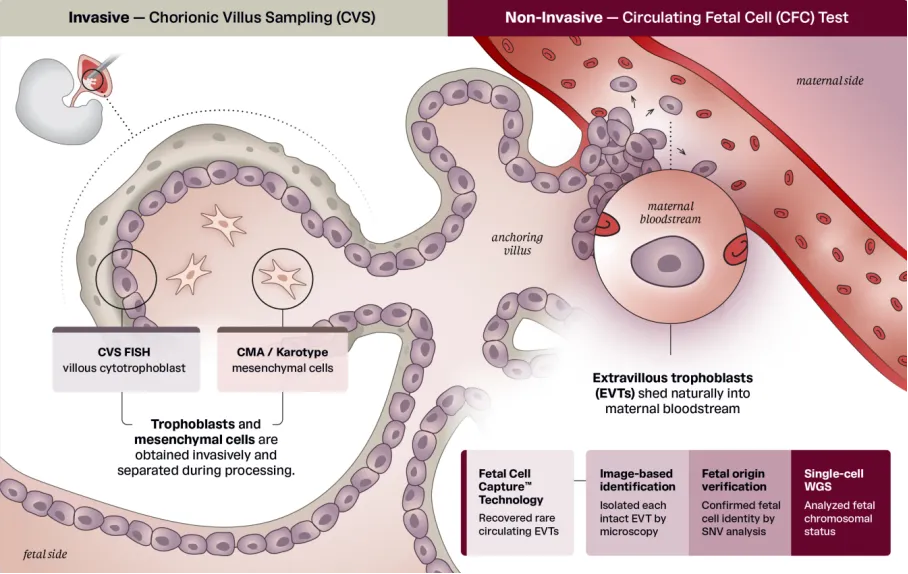
图1. 有创绒毛膜绒毛取样(CVS)与无创循环胎儿细胞捕获(CFC)检测的比较。(左)在CVS中,通过有创胎盘活检获得滋养层细胞和间充质细胞。滋养层细胞通过荧光原位杂交(FISH)分析,使用结合特定染色体位点的靶向探针,间充质细胞通过染色体微阵列或核型分析进行检测。(右)循环胎儿细胞(CFC)检测(Unity Confirm™,BillionToOne)利用绒毛外滋养层细胞(EVT),这些细胞由胎盘自然脱落进入母体血流。捕获循环的完整滋养层细胞,在单细胞水平分离,并对每个单独细胞进行全基因组测序(WGS),从而能够在全基因组范围内进行染色体拷贝数计数,而无需承担与有创取样相关的操作风险。
样本与细胞分析
采集母体外周血样本并处理以富集有核细胞,包括候选胎盘滋养层细胞。富集方法旨在减少有核母体白细胞(WBC)背景并增加稀有胎儿滋养层细胞的回收率。使用基于成像的方法,结合与滋养层细胞身份一致的形态学特征和免疫表型标志物,识别候选细胞。
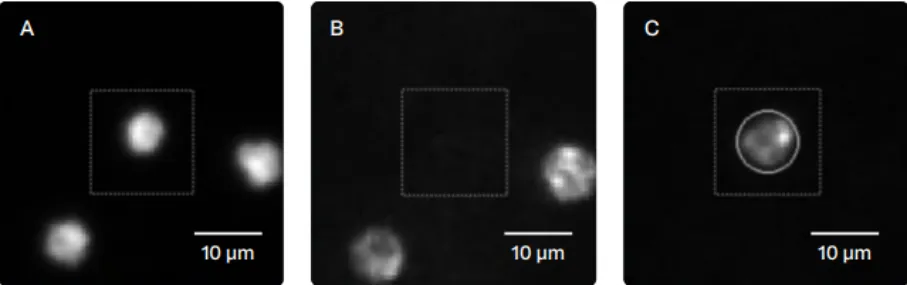
图2. 使用靶向细胞特异性蛋白的抗体染色进行免疫荧光显微镜检查。(A)为细胞核染色,对细胞类型非特异性。(B)为白细胞特异性染色,以确认该细胞是母体细胞。(C)为滋养层细胞特异性染色,以确认胎儿来源。
在进行免疫荧光成像后,分离单个候选滋养层细胞进行单细胞全基因组扩增(WGA),随后进行全基因组测序(WGS)。为了对所选细胞的胎儿来源进行二次确认,将每个分离细胞的测序数据与通过基因组DNA分析确定的母体基因型进行比较。使用信息丰富的单核苷酸变异(SNV)评估每个单细胞检测中非母源等位基因的存在。表现出父源等位基因统计学显著富集的细胞被分类为胎儿来源。
结果解读与一致性分析
胎儿确认的细胞进行单细胞全基因组拷贝数分析。基于全基因组标准化的读深分布推断染色体拷贝数(图3)。对于每个病例,基于对一个或多个胎儿确认细胞的分析确定结果。没有胎儿确认细胞达到质量阈值的病例报告为无存活细胞。CFC检测的端到端工作流程见图4。
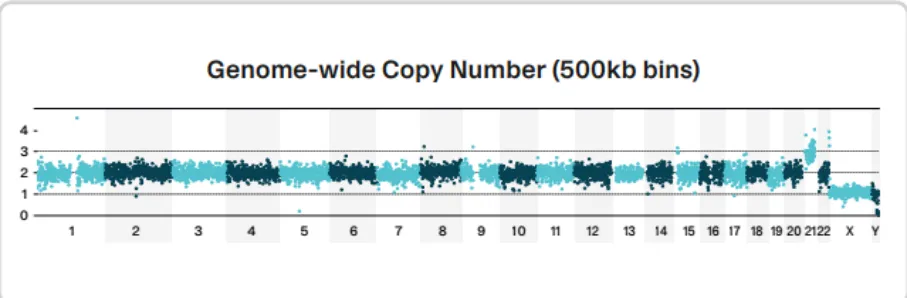
图3. 单个滋养层细胞拷贝数分析结果。该细胞的染色体组成为47, XY+21,与CVS结果一致。
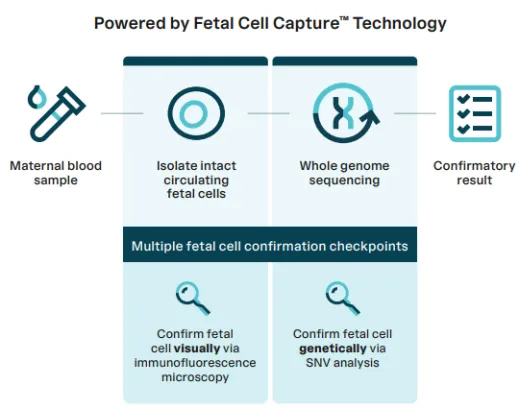
图4. Unity Confirm工作流程概述。在妊娠10至15 6/7周之间,从基于初始UNITY筛查结果具有临床指征的妊娠个体采集母体血液。使用免疫荧光显微镜识别循环胎儿细胞,并进行单细胞基因组分析,基于父源SNP的统计学显著富集确认胎儿来源。然后对胎儿确认的细胞进行全基因组拷贝数分析以评估染色体拷贝数。
将CFC结果与产前诊断检测结果(CVS或羊膜穿刺术,如可用)以及产后诊断检测进行比较。当未进行诊断检测时,临床结局如超声发现或新生儿检查作为参考标准¹³。当CFC发现与已知或预测的胎儿或新生儿染色体状态一致时,结果被认为是一致的。
结果
共有16例符合纳入标准。采血时的平均孕周为15周,捕获并测序的平均胎儿细胞数为2.9个(表1)。
均值 | 中位数 | 范围 | |
采血时孕周 | 15 0/7 | 15 3/7 | 10 0/7 - 19 6/7 |
样本体积 (mL) | 22.5 | 22.5 | 15 - 37.5 |
确认的滋养层细胞数 | 2.9 | 2 | 1 - 12 |
表1. 16例病例的特征
所有16例CFC结果均与胎儿染色体或微阵列分析或临床诊断一致(表2)。在9例中,CFC结果与CVS、羊膜穿刺术或妊娠产物分析一致,包括1例经Panorama™ NIPT鉴定为18三体高风险,但CFC和CVS分析均为整倍体的病例。在7例中,CFC结果与临床诊断一致。有1例CFC鉴定为47, XY, +13,超声发现与13三体一致,包括全前脑无裂畸形、喙状鼻、生殖器模糊和手足多指畸形。该病例经NIPT鉴定为13三体高风险。最后,有6例CFC鉴定为整倍体,孩子的父母报告婴儿健康。所有这些病例的NIPT结果也均为低风险。9例确认的非整倍体或22q11.2病例也经NIPT鉴定为特定染色体缺陷高风险。对于所有16例,CFC鉴定的性染色体与诊断检测性染色体或指定性别一致,并且除了X三体外,所有病例的NIPT性染色体异常结果均为低风险。
初始NIPT结果 | 总病例数 (n) | CFC确认病例数 (n) | 最终确认病例数 (n) | 确认方法 | cfDNA NIPT一致性 | CFC一致性 |
21三体 | 5 | 5 | 5 | 诊断性检测 | 100% | 100% |
18三体* | 2 | 1 | 1 | 诊断性检测 | 50% | 100% |
22q11.2 | 1 | 1 | 1 | 诊断性检测 | 100% | 100% |
X三体 | 1 | 1 | 1 | 诊断性检测 | 100% | 100% |
13三体 | 1 | 1 | 1 | 胎儿解剖扫描 | 100% | 100% |
低风险 | 6** | 6 | 6 | 临床检查 | 100% | 100% |
总计 | 16 | 100% |
表2. 循环胎儿细胞(CFC)和cfDNA NIPT结果与最终诊断或临床结局的一致性
* 1例经NIPT(Panorama™ NIPT)鉴定为T18高风险,CFC和诊断检测均为整倍体。** 所有6例经临床检查确认的整倍体病例,NIPT也均为低风险。
讨论
本研究结果表明,无创循环胎儿细胞捕获(CFC)通过直接分析从母体血液中分离的、代表胎儿基因型的完整胎盘滋养层细胞,能够在妊娠中提供准确的胎儿染色体评估。在这个队列中,CFC显示出与已知或预测的胎儿或新生儿结局完全一致。
虽然cfDNA筛查仍然是人群水平非整倍体风险评估的标准一线方法,但高风险结果后的临床管理仍然具有挑战性。通过绒毛膜绒毛取样(CVS)获得早期诊断检测的可及性受限于孕周时间、地理可用性和医师专业知识²。此外,相当比例的具有高风险cfDNA结果的患者未继续进行有创诊断检测¹¹'¹²。在这种情况下,额外的非侵入性信息可以帮助患者和提供者更好地解读胎儿风险,并指导关于妊娠管理和诊断操作的决策。CFC检测在妊娠早期尤为重要,它可以在羊膜穿刺术的孕周时间窗之前以及超声可检测结构异常之前提供见解。
CFC直接评估胎儿来源细胞中的染色体拷贝数。这种方法与基于cfDNA的筛查有着根本的不同,后者依赖于从混合的母体-胎儿cfDNA池中检测染色体代表的相对差异。因此,CFC有可能提供更特异性的胎儿染色体状态评估。
从妊娠个体外周血中检测和分析循环胎儿细胞并不是一个新概念,多项先前的研究已经证明了这种方法的可行性和实用性⁴'⁷。本研究的发现与这一更广泛的文献体系一致并得到其支持。本工作的贡献在于证明了该技术作为高风险cfDNA筛查后确认工具的临床应用,使胎儿细胞分析能够更实际和临床整合地使用。
本研究的优势在于证明了CFC确认检测的可行性和临床有效性,其真实诊断结局代表了最常见的胎儿非整倍体。本研究的局限性在于样本量适中。目前正在进行的一项研究旨在将数据集扩展到最大的CFC前瞻性研究,并将在更广泛的染色体异常和临床场景中进一步验证这种方法。还存在重要的检测特异性限制。CFC分析依赖于成功识别和分离稀有的循环滋养层细胞;通常仅分离1-6个细胞。循环滋养层细胞的频率随着孕周增加而降低,并且在约10%的妊娠个体中,在任何孕周都不存在¹⁴。虽然如本数据集所示,在早孕时间窗之后仍可识别胎儿细胞,但随着妊娠进展,成功细胞回收的可能性下降,因此在临床实践中需要设定孕周上限。最后,由于这种方法依赖于胎盘来源的滋养层细胞,在限制性胎盘嵌合的情况下,结果可能反映胎盘而非真实的胎儿染色体状态。由于X单体嵌合率高,这种CFC检测未设计用于该适应症¹⁵。
结论
结合先前的研究,这些发现支持CFC在评估胎儿染色体状态方面的范式。通过能够直接分析胎儿来源细胞而不承担与有创操作相关的风险,这种方法具有改善胎儿风险评估和在妊娠早期扩展获得有意义基因组信息的潜力。这些结果代表了重要的一步,持续的研究将进一步明确CFC分析在不断发展的产前保健领域中的作用。
致谢
我们感谢参与本研究的患者。我们还要感谢亚利桑那州凤凰城Valley Perinatal Services的Nayo Williams博士。
参考文献
1. American College of Obstetricians and Gynecologists' Committee on Practice Bulletins—Obstetrics; Committee on Genetics; Society for Maternal-Fetal Medicine. Screening for fetal chromosomal abnormalities: ACOG Practice Bulletin, Number 226. Obstet Gynecol. 2020;136(4):e48–e69. doi:10.1097/AOG.0000000000004084.
2. Suskin BG, Sciscione AM, Teigen N, Jenkins TC, Wapner RJ, Gregg AR, et al. Revisiting the challenges of training maternal fetal medicine fellows in chorionic villus sampling. Am J Obstet Gynecol. 2016;215(6):777.e1–777.e4. doi:10.1016/j.ajog.2016.08.011.
3. Hatt L, Brinch M, Singh R, Møller K, Lauridsen RH, Schlütter JM, et al. A new marker set that identifies fetal cells in maternal circulation with high specificity. Prenat Diagn. 2014;34(11):1066–72. doi:10.1002/pd.4429.
4. Stampalija T, Forcato C, Grati FR, Volpe P, De Robertis V, Izzi C, et al. Single-cell-based non-invasive screening for fetal pathogenic microimbalances using maternal blood: comparison with invasive prenatal diagnosis. Ultrasound Obstet Gynecol. 2026;67(4):500–509. doi:10.1002/uog.70201.
5. Weymaere J, Vander Plaetsen AS, van den Branden Y, Pospisilova E, Tytgat O, Deforce D, et al. Enrichment of circulating trophoblasts from maternal blood using filtration-based Metacell® technology. PLoS One. 2022;17:e0271226. doi:10.1371/journal.pone.0271226.
6. Jeppesen LD, Hatt L, Singh R, et al. Screening for fetal aneuploidy and sex chromosomal anomalies in a pregnant woman with mosaicism for Turner syndrome—applications and advantages of cell-based NIPT. Front Genet. 2021;12:741752. doi:10.3389/fgene.2021.741752.
7. Bellair M, Amaral E, Ouren M, et al. Noninvasive single-cell-based prenatal genetic testing: a proof of concept clinical study. Prenat Diagn. 2024;44:304–316. doi:10.1002/pd.6529.
8. Chakchouk I, van den Veyver IB. Whole-genome amplification on single circulating trophoblast cell. Methods Mol Biol. 2026;3003:11–23. doi:10.1007/978-1-0716-5060-8_2.
9. Zhuo X, Wang Q, Vossaert L, et al. Use of amplicon-based sequencing for testing fetal identity and monogenic traits with single circulating trophoblast (SCT) as one form of cell-based NIPT. PLoS One. 2021;16:e0249695. doi:10.1371/journal.pone.0249695.
10. Sullivan HK, Armstrong JC, Fox K, Cohen JL, Sinaiko AD. Use of maternal-fetal medicine subspecialist services by commercially insured pregnant people. JAMA Netw Open. 2025;8(1):e2454565. doi:10.1001/jamanetworkopen.2024.54565.
11. Platt LD, Janicki MB, Prosen T, Goldberg JD, Adashek J, Figueroa R, et al. Impact of noninvasive prenatal testing in regionally dispersed medical centers in the United States. Am J Obstet Gynecol. 2014;211(4):368.e1–368.e7. doi:10.1016/j.ajog.2014.03.065.
12. Dar P, Curnow KJ, Gross SJ, et al. Clinical experience and follow-up with large scale single-nucleotide polymorphism-based noninvasive prenatal aneuploidy testing. Am J Obstet Gynecol. 2014;211(5):527.e1–527.e17. doi:10.1016/j.ajog.2014.08.006.
13. DiNonno W, Demko Z, Martin K, Billings P, Egbert M, Zneimer S, et al. Quality assurance of non-invasive prenatal screening (NIPS) for fetal aneuploidy using positive predictive values as outcome measures. J Clin Med. 2019;8(9):1311. doi:10.3390/jcm8091311.
14. Vossaert L, Wang Q, Salman R, McCombs AK, Patel V, Qu C, Mancini MA, Edwards DP, Malovannaya A, Liu P, Shaw CA, Levy B, Wapner RJ, Bi W, Breman AM, Van den Veyver IB, Beaudet AL. Validation Studies for Single Circulating Trophoblast Genetic Testing as a Form of Noninvasive Prenatal Diagnosis. Am J Hum Genet. 2019 Dec 5;105(6):1262-1273. doi: 10.1016/j.ajhg.2019.11.004.
15. Malvestiti F, Agrati C, Grimi B, Pompilii E, Izzi C, Martinoni L, et al. Interpreting mosaicism in chorionic villi: results of a monocentric series of 1001 mosaics in chorionic villi with follow-up amniocentesis. Prenat Diagn. 2015;35(11):1117–27. doi:10.1002/pd.4656.


