ж‘ҳиҰҒ
REPORT жҢҮеҚ—жҳҜдёҖд»Ҫеё®еҠ©дҪ й«ҳж•ҲгҖҒйҖҸжҳҺең°жҠҘе‘ҠдёҙеәҠз ”з©¶зҡ„ вҖңе®һж“ҚжҢҮеҚ—вҖқгҖӮжң¬жҢҮеҚ—ж—ЁеңЁиЎҘе……е…¬и®Өзҡ„йҰ–йҖүжҠҘе‘Ҡе·Ҙе…·пјҲеҰӮдёҙеәҠиҜ•йӘҢжҠҘе‘Ҡз»ҹдёҖж ҮеҮҶ CONSORTпјүпјҢиЎҘе……жҲ‘们дҪңдёәдҪңиҖ…жӣҫйҒҮеҲ°гҖҒжҲ–дҪңдёәжңҹеҲҠе®ЎзЁҝдәәеҸҠзј–иҫ‘зңӢеҲ°д»–дәәйҒҮеҲ°зҡ„жҠҘе‘Ҡзӣёе…ійҡҗжҖ§зҹҘиҜҶпјҲеҚід№ еҫ—зҡ„гҖҒйқһжӯЈејҸзҡ„жҲ–йҡҗеҗ«зҡ„зҹҘиҜҶпјүгҖӮжң¬жҢҮеҚ—иҒҡз„ҰйҡҸжңәеҜ№з…§иҜ•йӘҢпјҢеҗҢж—¶д№ҹйҖӮз”ЁдәҺе…¶д»–з ”з©¶и®ҫи®ЎгҖӮREPORT жҢҮеҚ—ж¶өзӣ–зҡ„еҶ…е®№еҢ…жӢ¬жҠҘе‘Ҡжё…еҚ•гҖҒиҜ•йӘҢжҠҘе‘Ҡз»“жһ„гҖҒж ҮйўҳйҖүжӢ©гҖҒеҶҷдҪңйЈҺж јгҖҒиҜ•йӘҢжіЁеҶҢдёҺжҠҘе‘ҠдёҖиҮҙжҖ§гҖҒеҒҸеҖҡжҠҘе‘ҠжҲ–жёІжҹ“гҖҒйҖҸжҳҺеҢ–ж•°жҚ®еұ•зӨәпјҲеӣҫиЎЁпјүгҖҒејҖж”ҫиҺ·еҸ–иҖғйҮҸгҖҒж•°жҚ®е…ұдә«зӯүгҖӮйў„еҚ°жң¬пјҲејҖж”ҫиҺ·еҸ–пјүпјҡhttps://doi.org/10.31219/osf.io/qsxdzгҖӮ
еј•иЁҖ
дҪңдёәдёҙеәҠз ”з©¶йЎ№зӣ®зҡ„дё»иҰҒз ”з©¶иҖ…пјҢдҪ д»ҳеҮәдәҶеӨ§йҮҸеҠӘеҠӣгҖӮдҪ иҠұиҙ№ж•°жңҲзӯ№еӨҮйЎ№зӣ®пјҢз”ҡиҮіж•°е№ҙ收йӣҶе’ҢеҲҶжһҗж•°жҚ®гҖӮеҰӮд»ҠдҪ еҮҶеӨҮе°Ҷз ”з©¶жҲҗжһңж’°еҶҷдёә科еӯҰи®әж–ҮпјҲд»ҘдёӢз®Җз§° вҖңиҜ•йӘҢжҠҘе‘ҠвҖқпјүпјҢ并жҠ•зЁҝиҮіеҗҢиЎҢиҜ„е®Ўзҡ„еӯҰжңҜжңҹеҲҠгҖӮдҪ иҝҪжұӮжҠҘе‘Ҡзҡ„иҙЁйҮҸдёҺйҖҸжҳҺеәҰпјҢеёҢжңӣз»Ҳз«ҜиҜ»иҖ…иғҪе°Ҷе…¶еә”з”ЁдәҺдёҙеәҠе·ҘдҪңпјҢжҲ–дёәз§‘з ”е·ҘдҪңиҝӣиЎҢйҮҚеӨҚйӘҢиҜҒгҖӮдҪ зҡ„е…ұеҗҢдҪңиҖ…еҜ№зЁҝ件иҚүзЁҝжҸҗеҮәдәҶдёҚеҗҢз”ҡиҮізӣёжӮ–зҡ„ж„Ҹи§ҒпјҢдҪ иҜҘеҰӮдҪ•еә”еҜ№иҝҷз§Қжғ…еҶөпјҹ
еңЁжӯӨдёәдҪ д»Ӣз»Қ REPORT жҢҮеҚ—гҖӮжң¬жҢҮеҚ—ж—ЁеңЁж•ҙдҪ“жҸҗеҚҮдёҙеәҠз ”з©¶зҡ„жҠҘе‘ҠиҙЁйҮҸпјҢ并йқһжӣҝд»Је…¬и®Өзҡ„жҠҘе‘Ҡжё…еҚ•пјҲеҰӮдёҙеәҠиҜ•йӘҢжҠҘе‘Ҡз»ҹдёҖж ҮеҮҶ CONSORTпјүвҖ”вҖ” иҝҷзұ»е·Ҙе…·е§Ӣз»ҲжҳҜдҪ жҠҘе‘Ҡж’°еҶҷзҡ„ вҖңйҰ–йҖүвҖқ жҢҮеҜјиө„жәҗгҖӮзӣёеҸҚпјҢжҲ‘们е°Ҷ REPORT жҢҮеҚ—е®ҡдҪҚдёәдёҖд»Ҫ вҖңе®һж“ҚеһӢвҖқ е®һж–ҪжҢҮеҚ—дёҺзӣ®еҪ•пјҢж•ҙеҗҲдәҶйҡҗжҖ§зҹҘиҜҶеҸҠй«ҳж•ҲгҖҒйҖҸжҳҺж’°еҶҷиҜ•йӘҢжҠҘе‘Ҡзҡ„дҝЎжҒҜжқҘжәҗеҸӮиҖғгҖӮжҲ‘们зәіе…ҘдәҶиҮӘе·ұдҪңдёәдҪңиҖ…жӣҫйҒҮеҲ°гҖҒд»ҘеҸҠдҪңдёәе®ЎзЁҝдәәжҲ–зј–иҫ‘зңӢеҲ°е…¶д»–дҪңиҖ…йҒҮеҲ°зҡ„жҠҘе‘Ҡзӣёе…ій—®йўҳгҖӮжҲ‘们еңЁ 2017 е№ҙеҸ‘еёғдәҶ PREPARE иҜ•йӘҢжҢҮеҚ—пјҢж—ЁеңЁеҚҸеҠ©дёҙеәҠиҜ•йӘҢз ”з©¶зҡ„зӯ№еӨҮдёҺ规еҲ’гҖӮREPORT жҢҮеҚ—жҳҜ PREPARE жҢҮеҚ—зҡ„иҮӘ然延伸пјҢиҒҡз„ҰдёҙеәҠиҜ•йӘҢз ”з©¶зҡ„жҠҘе‘ҠзҺҜиҠӮгҖӮиӢҘдҪ жӣҫдҪҝз”Ё PREPARE иҜ•йӘҢжҢҮеҚ—规еҲ’з ”з©¶пјҢREPORT жҢҮеҚ—е°ҶеҠ©еҠӣдҪ е®ҢжҲҗжҠҘе‘Ҡж’°еҶҷпјӣеҚідҫҝжңӘдҪҝз”Ё PREPARE жҢҮеҚ—пјҢREPORT жҢҮеҚ—д№ҹеҸҜдҪңдёәзӢ¬з«Ӣе·Ҙе…·пјҢиҫ…еҠ©дҪ е®ҢжҲҗд»»дҪ•з ”究зҡ„жҠҘе‘Ҡж’°еҶҷгҖӮ
REPORT жҢҮеҚ—жҸҗдҫӣжҸҗеҚҮжҠҘе‘ҠиҙЁйҮҸдёҺйҖҸжҳҺеәҰзҡ„зӣёе…ідҝЎжҒҜпјҢж ёеҝғиҒҡз„ҰйҡҸжңәеҜ№з…§иҜ•йӘҢпјҲRCTпјҢд»ҘдёӢз®Җз§° вҖңиҜ•йӘҢвҖқпјүпјҢеҗҢж—¶д№ҹйҖӮз”ЁдәҺе…¶д»–з ”з©¶и®ҫи®ЎгҖӮ
дёҙеәҠиҜ•йӘҢжҠҘе‘Ҡз»ҹдёҖж ҮеҮҶпјҲCONSORTпјүжё…еҚ•еҸҠеҹәдәҺ CONSORT зҡ„зҪ‘з»ңиҫ…еҠ©еҶҷдҪңе·Ҙе…·пјҡйҮҚиҰҒзҡ„第дёҖжӯҘ
жҠҘе‘Ҡж’°еҶҷзҡ„йҰ–иҰҒе…ій”®жӯҘйӘӨпјҢжҳҜжүҫеҲ°дёҺз ”з©¶и®ҫи®ЎеҢ№й…Қзҡ„жҠҘе‘Ҡжё…еҚ•гҖӮ EQUATOR зҪ‘з»ңзҪ‘з«ҷеҸҜжҹҘиҜўе…Ёйқўзҡ„жҠҘе‘Ҡжё…еҚ•еҲ—иЎЁгҖӮй’ҲеҜ№дёҙеәҠиҜ•йӘҢпјҢйҖӮз”Ёзҡ„жҠҘе‘Ҡжё…еҚ•дёә CONSORT жё…еҚ•пјҢиҜҘжё…еҚ•иҝҳжңүеӨҡйЎ№еҸҜиғҪйҖӮз”Ёзҡ„жү©еұ•зүҲжң¬гҖӮжҲ‘们е»әи®®дҪ и®ҝй—® EQUATOR зҪ‘з»ңзҪ‘з«ҷзҡ„ вҖңе·Ҙе…·еҢ…вҖқ жқҝеқ—пјҢиҺ·еҸ–йҖүжӢ©еҗҲйҖӮжҠҘе‘Ҡжё…еҚ•зҡ„зӣёе…ідҝЎжҒҜгҖӮдҪ д№ҹеҸҜдҪҝз”ЁеҹәдәҺ CONSORT зҡ„зҪ‘з»ңе·Ҙе…·пјҲCOBWEBпјүиҫ…еҠ©еҶҷдҪңдёҺжё…еҚ•дҫқд»ҺжҖ§ж ёжҹҘгҖӮCOBWEB зҪ‘з«ҷжҳҺзЎ®иҜҙжҳҺпјҡвҖңCOBWEB жҳҜдёҖж¬ҫеңЁзәҝзЁҝ件еҶҷдҪңиҫ…еҠ©е·Ҙе…·пјҢж—ЁеңЁжҢҮеҜјдҪңиҖ…жҢүз…§дёҙеәҠиҜ•йӘҢжҠҘе‘Ҡз»ҹдёҖж ҮеҮҶпјҲCONSORTпјүеҸҠе…¶еҗҺз»ӯжү©еұ•зүҲжң¬е®ҢжҲҗйҡҸжңәеҜ№з…§иҜ•йӘҢзЁҝ件撰еҶҷвҖқгҖӮжҲ‘们ејәзғҲжҺЁиҚҗдҪҝз”ЁиҜҘе·Ҙе…·пјҢе®ғиғҪеҠ©еҠӣй«ҳж•Ҳе®ҢжҲҗиҜ•йӘҢжҠҘе‘Ҡж’°еҶҷпјҢйҒҝе…Қ CONSORT дҫқд»ҺжҖ§зӣёе…ізҡ„еёёи§Ғй—®йўҳпјҢеҰӮйҡҸжңәеҢ–ж–№жі•жҠҘе‘ҠдёҚ规иҢғгҖҒж ·жң¬йҮҸдј°з®—жҸҸиҝ°дёҚжё…зӯүгҖӮ
ж’°еҶҷжҠҘе‘Ҡж—¶пјҢеҗҢжӯҘжҹҘйҳ…иҜ•йӘҢж–№жЎҲдёҺжіЁеҶҢдҝЎжҒҜ
иҜ•йӘҢжҠҘе‘ҠжҠ•зЁҝиҮіеӯҰжңҜжңҹеҲҠеҗҺпјҢжңҹеҲҠе®ЎзЁҝдәәдёҺзј–иҫ‘жҳҜйҰ–жү№дё“дёҡиҜ»иҖ…гҖӮ他们дјҡж ёжҹҘдҪ жҳҜеҗҰжҢүи®ЎеҲ’е®ҢжҲҗз ”з©¶пјҢиӢҘжңӘе®ҢжҲҗпјҢйңҖжҳҺзЎ®еҸҳжӣҙеҺҹеӣ гҖӮ他们дјҡжҹҘйҳ…е…¬ејҖзҡ„иҜ•йӘҢжіЁеҶҢдҝЎжҒҜдёҺж–№жЎҲпјҢжҲ–йҡҸжҠҘе‘ҠжҸҗдәӨзҡ„жіЁеҶҢж–Ү件дёҺж–№жЎҲпјҢеҜ№жҜ”иҜ•йӘҢжіЁеҶҢеә“дёҺиҜ•йӘҢжҠҘе‘Ҡдёӯзҡ„е…ій”®иҜ•йӘҢзү№еҫҒпјҢж ёжҹҘдёҖиҮҙжҖ§гҖӮзі»з»ҹиҜ„д»·дҪңиҖ…еңЁзәіе…ҘдҪ зҡ„иҜ•йӘҢ并撰еҶҷиҜ„д»·ж—¶пјҢд№ҹдјҡжү§иЎҢзӣёеҗҢж“ҚдҪңпјҢиҜ„дј°жҠҘе‘Ҡз»“жһңйҖүжӢ©зӯүзҺҜиҠӮзҡ„еҒҸеҖҡгҖӮ
жҲ‘们е»әи®®дҪ ж’°еҶҷиҜ•йӘҢжҠҘе‘Ҡж—¶пјҢйҮҮз”ЁдёҺе®ЎзЁҝдәәгҖҒзј–иҫ‘зӣёеҗҢзҡ„ж ёжҹҘж–№ејҸгҖӮж’°еҶҷж—¶еҗҢжӯҘжү“ејҖиҜ•йӘҢж–№жЎҲдёҺжіЁеҶҢж–Ү件пјҢеҜ№е…ій”®иҜ•йӘҢзү№еҫҒйҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢжҸҗеҚҮеҗҢдёҖз ”з©¶йЎ№зӣ®дёӨйЎ№зӣёе…іе·ҘдҪңзҡ„йҖҸжҳҺеәҰдёҺдёҖиҮҙжҖ§пјҲеӣҫ 1пјүгҖӮз”ұдәҺж–№жі•еӯҰйғЁеҲҶй«ҳеәҰзӣёдјјпјҢжңҹеҲҠзҡ„жҹҘйҮҚзі»з»ҹжңүж—¶дјҡж Үи®°иҜ•йӘҢжҠҘе‘ҠгҖӮиҜ·зЎ®дҝқеј•з”ЁеүҚжңҹз ”з©¶жҲҗжһңпјҢ并еңЁжҠ•зЁҝдҝЎе’Ң / жҲ–иҜ•йӘҢжҠҘе‘ҠдёӯиҜҙжҳҺйҮҮз”ЁиҜҘж–№ејҸзҡ„еҗҲзҗҶжҖ§гҖӮMiguel Roig еҚҡеЈ«ж’°еҶҷзҡ„гҖҠйҒҝе…ҚжҠ„иўӯгҖҒиҮӘжҠ„иўӯеҸҠе…¶д»–дёҚеҪ“еҶҷдҪңиЎҢдёәпјҡеӯҰжңҜеҶҷдҪңдјҰзҗҶжҢҮеҚ—гҖӢжҳҜдёҖд»Ҫе®һз”Ёдё”иҜҰз»Ҷзҡ„еҸӮиҖғиө„ж–ҷгҖӮRoig еҚҡеЈ«жҸҗеҮәпјҢй’ҲеҜ№жҠҖжңҜжҸҸиҝ°зҡ„ж–Үжң¬еӨҚз”ЁпјҢзј–иҫ‘еә”з»ҷдәҲжӣҙеӨҡзҒөжҙ»жҖ§пјҢе°Өе…¶еҜ№дәҺйқһиӢұиҜӯжҜҚиҜӯдҪңиҖ…гҖӮжңҖеҗҺпјҢиӢҘдҪ е·ІеҸ‘иЎЁиҜ•йӘҢж–№жЎҲпјҢиҜ·ж ёжҹҘдҪңиҖ… / еҮәзүҲе•ҶзүҲжқғеҚҸи®®пјҢйҒҝе…ҚдҫөжқғгҖӮ
еӣҫ 1В жҲ‘们е»әи®®ж’°еҶҷж—¶еҗҢжӯҘжү“ејҖиҜ•йӘҢж–№жЎҲдёҺиҜ•йӘҢжіЁеҶҢж–Ү件пјҢйҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢжҸҗеҚҮиҜ•йӘҢж–№жЎҲгҖҒжіЁеҶҢдҝЎжҒҜдёҺжҠҘе‘ҠдёүиҖ…зҡ„дёҖиҮҙжҖ§гҖӮ
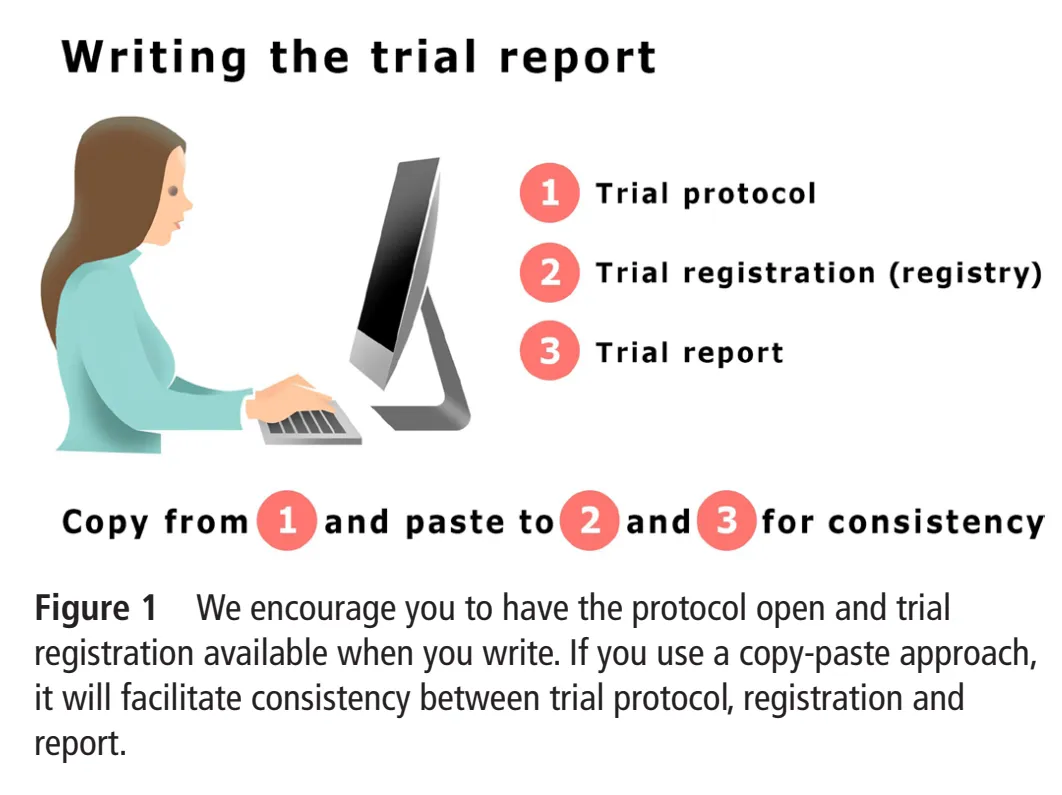
йҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢеҸҜзЎ®дҝқе…ій”®иҜ•йӘҢйЎ№зӣ®жҢүжіЁеҶҢдҝЎжҒҜзҡ„зӣёеҗҢйЎәеәҸгҖҒзӣёеҗҢжҺӘиҫһжҠҘе‘ҠгҖӮе…ій”®иҜ•йӘҢйЎ№зӣ®еҢ…жӢ¬з ”究зӣ®зҡ„гҖҒзәіе…ҘжҺ’йҷӨж ҮеҮҶгҖҒз»“еұҖжҢҮж ҮзӯүгҖӮиӢҘдҪ еҒҸзҰ»дәҶз ”з©¶и®ЎеҲ’пјҲиҜҘжғ…еҶөиҫғдёәеёёи§ҒпјҢжңүеҗҲзҗҶи§ЈйҮҠеҚіеҸҜпјүпјҢиҜ·йҖҸжҳҺжҠҘе‘ҠеҒҸзҰ»жғ…еҶөеҸҠеҺҹеӣ гҖӮеӨҡж•°жңҹеҲҠиҰҒжұӮе°ҶиҜ•йӘҢж–№жЎҲдҪңдёәиЎҘе……жқҗж–ҷдёҠдј иҮіиҜ•йӘҢжҠҘе‘ҠгҖӮеӨҚеҲ¶ - зІҳиҙҙж–№ејҸеҸҜејәеҢ–дёӨд»Ҫж–Ү件зҡ„е…іиҒ”пјҢжҸҗеҚҮеҸҜиҜ»жҖ§гҖӮиӢҘж— жі• 100% еӨҚеҲ¶зІҳиҙҙжҺӘиҫһд»ҘдҝқиҜҒдёҖиҮҙжҖ§пјҢиҜ·д»”з»Ҷж ёжҹҘиҜӯд№үжҳҜеҗҰдёҖиҮҙгҖӮдҫӢеҰӮпјҢеӨҡж¬Ўдҝ®ж”№иҜ•йӘҢжҠҘе‘ҠеҗҺдҪ жӢҹе®ҡдәҶжӣҙеҗҲйҖӮзҡ„ж ҮйўҳпјҢжҲ–дјҳеҢ–дәҶиҜ•йӘҢзӣ®зҡ„зҡ„иЎЁиҝ°гҖӮ
дёҙеәҠиҜ•йӘҢжҠҘе‘Ҡж’°еҶҷ
з»“жһ„пјҡеј•иЁҖгҖҒж–№жі•гҖҒз»“жһңгҖҒи®Ёи®әпјҲIMRaD з»“жһ„пјү
еӨҡ数科еӯҰжңҹеҲҠеҒҸеҘҪдёҙеәҠиҜ•йӘҢжҠҘе‘ҠйҮҮз”Ё IMRaD з»“жһ„пјҲеҚіеј•иЁҖгҖҒж–№жі•гҖҒз»“жһңгҖҒи®Ёи®әпјүгҖӮдҪ еҸҜеңЁ PLOS зі»еҲ—еҮәзүҲзү©дёӯиҺ·еҸ–з§‘з ”и®әж–Үз»“жһ„ж’°еҶҷзҡ„йҖҡз”ЁеҸӮиҖғдҝЎжҒҜгҖӮдёӢж–ҮжҲ‘们е°ҶиЎҘе……иҜ•йӘҢжҠҘе‘Ҡеҗ„йғЁеҲҶзҡ„дё“еұһж’°еҶҷиҰҒзӮ№гҖӮ
жӢҹе®ҡ вҖңеҗёзқӣж ҮйўҳвҖқ
йҷҲиҝ°жҖ§ж ҮйўҳдёҺжҸҸиҝ°жҖ§ж ҮйўҳжҳҜиҝҗеҠЁдёҺиҝҗеҠЁеҢ»еӯҰйўҶеҹҹжңҖеёёи§Ғзҡ„ж Үйўҳзұ»еһӢгҖӮйҷҲиҝ°жҖ§ж ҮйўҳзӣҙжҺҘзӮ№жҳҺж ёеҝғдҝЎжҒҜпјҲйҖҡеёёдёәе…ій”®з»“жһңпјҢеҰӮ вҖңеүҚдәӨеҸүйҹ§еёҰж–ӯиЈӮж—¶еҗҲ并еҚҠжңҲжқҝжҲ–иҪҜйӘЁжҚҹдјӨпјҢдёҺеүҚдәӨеҸүйҹ§еёҰжҚҹдјӨеҗҺ 2~10 е№ҙжӮЈиҖ…жҠҘе‘Ҡз»“еұҖйў„еҗҺиҫғе·®зӣёе…іпјҡдёҖйЎ№зі»з»ҹиҜ„д»·вҖқпјүгҖӮжҸҸиҝ°жҖ§ж ҮйўҳиҜҙжҳҺиҜ»иҖ…еҸҜд»ҺиҜ•йӘҢжҠҘе‘ҠдёӯиҺ·еҸ–зҡ„еҶ…е®№пјҲйҖҡеёёдёәз ”з©¶зұ»еһӢгҖҒз ”з©¶дәәзҫӨжҲ–з»“еұҖжҢҮж ҮпјҢеҰӮ вҖңе“Әз§ҚжІ»з–—еҜ№и·ҹи…ұзӮҺжӮЈиҖ…жңҖжңүж•ҲпјҹдёҖйЎ№зәіе…Ҙ 29 йЎ№йҡҸжңәеҜ№з…§иҜ•йӘҢзҡ„еҠЁжҖҒзі»з»ҹиҜ„д»·дёҺзҪ‘зҠ¶ Meta еҲҶжһҗвҖқпјүгҖӮжӢҹе®ҡиҜ•йӘҢжҠҘе‘Ҡж Үйўҳж—¶пјҢйңҖиҖғиҷ‘д»Ҙеҗёеј•иҜ»иҖ…гҖҒе‘ҠзҹҘиҜ»иҖ…дёәзӣ®ж ҮпјҢжҲ–дёӨиҖ…е…јйЎҫпјҢе°ҪеҸҜиғҪеңЁж Үйўҳжң«е°ҫж ҮжіЁз ”з©¶и®ҫи®Ўзұ»еһӢгҖӮ
з§‘з ”еҶҷдҪңиҖ…еҸҜеңЁдҝқжҢҒдёҘи°ЁжҖ§зҡ„еүҚжҸҗдёӢеҸ‘жҢҘеҲӣж„ҸпјҢйҒҝе…ҚиҪ»жө®гҖҒзҗҗзўҺжҲ–дёҚеӯҰжңҜзҡ„иЎЁиҝ°гҖӮеҗёзқӣж ҮйўҳдёҚзӯүдәҺеӯҳеңЁ вҖңжёІжҹ“еҒҸеҖҡвҖқгҖӮжҲ‘们е»әи®®е°ҪеҸҜиғҪйҮҮз”ЁйҷҲиҝ°жҖ§ж Үйўҳ вҖ”вҖ” ж ҮйўҳжҳҜз»ҷиҜ»иҖ…з•ҷдёӢ第дёҖеҚ°иұЎзҡ„е…ій”®пјҢе°Ҫз®ЎжҲ‘们зҗҶи§ЈдҪ 并йқһжҖ»иғҪиҮӘдё»йҖүжӢ©ж Үйўҳзұ»еһӢгҖӮйҮҮз”Ё вҖңеҗёеј• + е‘ҠзҹҘвҖқ зҡ„йЈҺж јпјҢеҸҜеңЁйҒөеҫӘеӯҰжңҜ规иҢғзҡ„еүҚжҸҗдёӢеҸ‘жҢҘеҲӣж„ҸпјҢйҒҝе…Қиў«дёҘиӢӣзј–иҫ‘дҝ®ж”№гҖӮзӨәдҫӢпјҡвҖңи·‘еҗ‘дјӨз—…пјҹеҚҠ马жҲ–全马еӨҮжҲҳи·‘иҖ…зҡ„жҚҹдјӨдёҺз–ҫз—…еҸ‘з”ҹзҺҮгҖҒжӮЈз—…зҺҮеҸҠеҪұе“ҚвҖқгҖӮ
еҗёзқӣж ҮйўҳеҸҜеҢ…еҗ« 2~3 йғЁеҲҶпјҡпјҲ1пјүеҗёеј•зӮ№пјҡеҸҜйҮҮз”ЁеҸҢе…іиҜӯжҲ–жҜ”е–»пјӣпјҲ2пјүж ёеҝғдҝЎжҒҜпјҡиҜҙжҳҺиҜ»иҖ…йҳ…иҜ»зҡ„д»·еҖјпјӣпјҲ3пјүиҜ•йӘҢжҠҘе‘Ҡж ёеҝғзү№еҫҒпјҡеҰӮз ”з©¶дәәзҫӨзү№еҫҒгҖҒиҜ•йӘҢзұ»еһӢпјҲеҰӮеҸҢзӣІдјҳж•ҲжҖ§иҜ•йӘҢпјүгҖҒж•°жҚ®ж”¶йӣҶж—¶й—ҙиҢғеӣҙзӯүгҖӮдёәдҝқйҡң PubMed жӯЈзЎ®зҙўеј•дёҺиҜҶеҲ«пјҢCONSORT е·ҘдҪңз»„е»әи®®дҪңиҖ…еңЁж Үйўҳдёӯзәіе…Ҙз ”з©¶и®ҫи®ЎпјҲеҰӮ вҖңдёҖйЎ№йҡҸжңәеҜ№з…§иҜ•йӘҢвҖқпјүгҖӮ
еӯҰжңҜеҶҷдҪңйЈҺж јпјҡ3 дёӘжҸҗеҚҮиҜ»иҖ…е…іжіЁеәҰзҡ„е»әи®®
з§‘з ”еҶҷдҪңдёҺеҲӣж„ҸеҶҷдҪң并йқһеҜ№з«ӢгҖӮе…ідәҺеҗёзқӣж Үйўҳзҡ„и§ӮзӮ№йңҖеҶҚж¬Ўејәи°ғпјҡз§‘з ”еҶҷдҪңиҖ…еҸҜеңЁдҝқжҢҒдёҘи°ЁжҖ§зҡ„еүҚжҸҗдёӢеҸ‘жҢҘеҲӣж„ҸгҖӮдёҺж ҮйўҳжӢҹе®ҡеҗҢзҗҶпјҢжҲ‘们зҗҶи§ЈйғЁеҲҶеҶҷдҪңйЈҺж јж— жі•иҮӘдё»йҖүжӢ©пјҲеҰӮйғЁеҲҶжңҹеҲҠиҰҒжұӮйҮҮ用第дёүдәәз§°пјҢзҰҒжӯўдҪҝз”Ё вҖңжҲ‘们йҮҮз”ЁзӯүйҖҹжөӢеҠӣд»ӘжөӢйҮҸиӮЎеӣӣеӨҙиӮҢеҠӣйҮҸвҖқ зӯү第дёҖдәәз§°иЎЁиҝ°пјүгҖӮ
е»әи®® 1пјҡдҪҝз”Ёе…·дҪ“иЎЁиҝ°пјҢж‘’ејғиў«еҠЁеҸҘ
е°Ҷ вҖңи®ӯз»ғиҙҹиҚ·зҡ„йҮҸеҢ–ж–№жі•жңүеӨҡз§ҚвҖқ жӣҝжҚўдёә вҖңжөӢйҮҸи®ӯз»ғиҙҹиҚ·зҡ„е·Ҙе…·иҮіе°‘жңү 3 з§ҚвҖқгҖӮжӣҙе…·дҪ“зҡ„иЎЁиҝ°дёәпјҡвҖңжҲ‘们д»Ӣз»Қ 3 з§ҚдёҙеәҠеҢ»з”ҹеҸҜз”ЁдәҺжөӢйҮҸдј‘й—Іи·‘иҖ…и®ӯз»ғиҙҹиҚ·зҡ„е·Ҙе…·вҖқпјҢеҺҹеӣ еҰӮдёӢпјҡпјҲ1пјүиҜ»иҖ…жҳҺзЎ®еҸҜиҺ·еҸ–зҡ„и®ӯз»ғиҙҹиҚ·жөӢйҮҸж–№жі•ж•°йҮҸпјӣпјҲ2пјүиҜ»иҖ…дәҶи§Јз ”з©¶дәәзҫӨзү№еҫҒпјҢеҗҢж—¶жҳҺзЎ®иЎҢдёәдё»дҪ“гҖҒиЎҢдёәдёҺеҜ№иұЎпјҡдёҙеәҠеҢ»з”ҹпјҲдё»дҪ“пјүжөӢйҮҸпјҲиЎҢдёәпјүдј‘й—Іи·‘иҖ…зҡ„и®ӯз»ғиҙҹиҚ·пјҲеҜ№иұЎпјүгҖӮзј–еҸ·жҲ–жңүеәҸеҲ—иЎЁеҸҜеё®еҠ©жўізҗҶжҖқи·ҜпјҢеҗ‘иҜ»иҖ…дј йҖ’жё…жҷ°дҝЎжҒҜгҖӮ
е»әи®® 2пјҡдҪҝз”Ёдё»еҠЁеҠЁиҜҚй©ұеҠЁзҡ„дё»еҠЁеҸҘеҶҷдҪң
еҚідҫҝжңҹеҲҠиҰҒжұӮйҷҗеҲ¶дәҶеҶҷдҪңзҒөжҙ»жҖ§пјҢжҲ‘们д»Қе»әи®®йҮҮз”Ёдё»еҠЁеҶҷдҪңж–№ејҸзӣҙжҺҘдёҺиҜ»иҖ…жІҹйҖҡгҖӮдҪ еҸҜйҖүжӢ©з®ҖжҙҒгҖҒжё…жҷ°гҖҒиҝһиҙҜзҡ„еҸҘеӯҗпјҢд№ҹеҸҜйҖүжӢ©жЁЎзіҠгҖҒиў«еҠЁгҖҒеҶ—й•ҝзҡ„еҸҘеӯҗгҖӮе“Әз§ҚеҸҘеӯҗжӣҙиғҪеҗёеј•иҜ»иҖ…пјҹе…·дҪ“иЎЁиҝ°дҪҝз”Ёдё»еҠЁеҠЁиҜҚпјҲеҰӮжҸҸиҝ°гҖҒжҺўзҙўгҖҒжҜ”иҫғгҖҒжөӢйҮҸпјүпјҢйҒҝе…ҚжҠҪиұЎеҗҚиҜҚпјҲеҰӮйҮҸеҢ–гҖҒдәӨжөҒгҖҒе®ҢжҲҗгҖҒжңүж•ҲжҖ§гҖҒзҰ»ж•ЈеҢ–пјүпјҢжҳҺзЎ®иЎҢдёәдё»дҪ“гҖҒиЎҢдёәдёҺеҜ№иұЎгҖӮ
е»әи®® 3пјҡжўізҗҶзЁҝ件дёӯзҡ„ be еҠЁиҜҚпјҢжӣҝжҚўдёәдё»еҠЁеҠЁиҜҚ
be еҠЁиҜҚеҗ„зұ»еҪўејҸпјҲеҰӮ wasгҖҒwereгҖҒbeenгҖҒbeingгҖҒareгҖҒisгҖҒshownпјүжҳҜдјҳеҢ–еҶҷдҪңзҡ„йҮҚзӮ№дҝ®ж”№еҜ№иұЎгҖӮвҖңеҸҜиў«жөӢйҮҸвҖқвҖңз»“жһңжҳҫзӨәвҖқ зӯүиў«еҠЁеҸҘејҸдјҡйҷҚдҪҺж–Үеӯ—иЎЁзҺ°еҠӣгҖӮе°қиҜ•е°ҶжҜҸж®өдёӯзҡ„йғЁеҲҶ be еҠЁиҜҚжӣҝжҚўдёәз”ҹеҠЁзҡ„дё»еҠЁеҠЁиҜҚпјҲеҰӮдјӘиЈ…гҖҒејҖе…·гҖҒж»ҡеҠЁгҖҒйҒҝе…ҚпјүгҖӮ
дјҳиҙЁеҶҷдҪңжҳҜеҲ»ж„ҸгҖҒз»ҶиҮҙгҖҒе®Ўж…Һзҡ„иҝҮзЁӢпјҢжҳҜйңҖиҰҒж—¶й—ҙдёҺз»ғд№ зҡ„жҠҖиғҪгҖӮдҪ еҸҜеңЁи‘—еҗҚиҜӯиЁҖеӯҰж•ҷжҺҲгҖҒз§‘з ”еҶҷдҪңжҢҮеҜј Helen Sword зҡ„зҪ‘з«ҷиҺ·еҸ–еҶҷдҪңиө„жәҗдёҺжҺЁиҚҗйҳ…иҜ»иө„ж–ҷгҖӮREPORT жҢҮеҚ—зҡ„ 5 дҪҚдҪңиҖ…дёӯпјҢжңү 4 дҪҚ并йқһиӢұиҜӯжҜҚиҜӯиҖ…гҖӮжҲ‘们еңЁз§‘з ”еҶҷдҪңдёӯйҮҮз”ЁдёҠиҝ° 3 йЎ№е»әи®®пјҢеҗҢж—¶з§үжҢҒ вҖңжһҒз®ҖиЎЁиҫҫвҖқ еҺҹеҲҷпјҢйҒҝе…ҚйҮҚеӨ§иҜӯиЁҖй”ҷиҜҜпјҢжҸҗеҚҮйқһиӢұиҜӯжҜҚиҜӯиҜ»иҖ…зҡ„еҸҜиҜ»жҖ§гҖӮLingard зӯүдәәзҡ„дјҳиҙЁгҖҠеҶҷдҪңжҠҖе·§гҖӢзі»еҲ—ж–Үз« пјҢжҖ»з»“дәҶиҘҝзҸӯзүҷиҜӯгҖҒжі•иҜӯгҖҒиҚ·е…°иҜӯгҖҒеҫ·иҜӯжҜҚиҜӯиҖ…иӢұж–ҮеҶҷдҪңзҡ„ж ёеҝғиҜӯжі•йҡҫйўҳпјҢ并жҸҗдҫӣе®һз”ЁжҠҖе·§пјҲиЎЁ 1пјүгҖӮ
иЎЁ 1В иҘҝзҸӯзүҷиҜӯгҖҒжі•иҜӯгҖҒиҚ·е…°иҜӯгҖҒеҫ·иҜӯз ”з©¶иҖ…иӢұж–ҮеҶҷдҪңзҡ„ж ёеҝғиҜӯжі•йҡҫйўҳ
иЎЁж ј
еҸҜе°қиҜ•д»ҘдёӢ 3 йЎ№ж“ҚдҪңпјҡи§ӮзңӢ Sword ж•ҷжҺҲи®Іи§ЈеҰӮдҪ•йҒҝе…ҚеҗҚиҜҚеҢ–гҖӮе°ҶеҶҷдҪңеҶ…е®№йҖҡиҝҮеңЁзәҝе·Ҙе…·дјҳеҢ–гҖӮеҸӮдёҺ Wordcraft еҶҷдҪңи®ӯз»ғгҖӮ
ж‘ҳиҰҒпјҡйҒөеҫӘ CONSORT 规иҢғж’°еҶҷ
иҜ•йӘҢжҠҘе‘Ҡж‘ҳиҰҒзҡ„йҳ…иҜ»йҮҸйҖҡеёёиҝңй«ҳдәҺе…Ёж–ҮпјҢеӣ жӯӨиҮіе…ійҮҚиҰҒгҖӮеӨҡж•°жңҹеҲҠеҜ№ж‘ҳиҰҒжңүеӯ—ж•°йҷҗеҲ¶пјҢйғЁеҲҶжңҹеҲҠиҰҒжұӮеӣәе®ҡз»“жһ„дёҺж ҮйўҳгҖӮиҝҷдәӣйҷҗеҲ¶дёәж’°еҶҷжё…жҷ°гҖҒйҖҸжҳҺгҖҒиҜҰз»Ҷзҡ„ж‘ҳиҰҒеёҰжқҘжҢ‘жҲҳпјҢйңҖеҒҡеҲ°еӯ—еӯ—зҸ зҺ‘гҖӮиӢҘжңҹеҲҠж јејҸе…Ғи®ёпјҢйҮҮз”Ё CONSORT жңҹеҲҠдёҺдјҡи®®ж‘ҳиҰҒйҡҸжңәиҜ•йӘҢжҠҘе‘Ҡ规иҢғж’°еҶҷгҖӮиҜҘ规иҢғй…ҚеҘ—и§ЈйҮҠдёҺиҜҰз»ҶиҜҙжҳҺж–Ү件пјҢд»ҘеҸҠж‘ҳиҰҒжқЎзӣ®жё…еҚ•пјҢеҸҜд»Һ CONSORT зҪ‘з«ҷдёӢиҪҪгҖӮCONSORT е·ҘдҪңз»„еҲқжӯҘз ”з©¶жҳҫзӨәпјҢжё…еҚ•жүҖжңүжқЎзӣ®еҸҜеңЁ 250~300 иҜҚеҶ…е®Ңж•ҙе‘ҲзҺ°гҖӮCONSORT зҪ‘з«ҷиҝҳжҸҗдҫӣиҗҪе®һ CONSORT жё…еҚ•зҡ„ж ·жң¬з ”究пјҢеҢ…еҗ«жҳ“еҮәзҺ°й—®йўҳзҡ„ж‘ҳиҰҒз»“жһңж’°еҶҷзӨәдҫӢгҖӮ
жҳҺзЎ®иҜ•йӘҢжЎҶжһ¶пјҲеҰӮ вҖңдјҳж•ҲжҖ§иҜ•йӘҢвҖқпјүеҸҜдёҺж‘ҳиҰҒеҗҺз»ӯеҶ…е®№еҪўжҲҗиүҜеҘҪиЎ”жҺҘпјҢе…іиҒ”д»ҘдёӢеҶ…е®№пјҡз ”з©¶иҖ…еҒҮи®ҫдјҳдәҺеҜ№з…§жҺӘж–Ҫзҡ„е№Ійў„жҺӘж–ҪпјҲз ”з©¶зӣ®зҡ„пјүгҖҒдё»иҰҒз»“еұҖжҢҮж ҮдёҺиҜ„дј°ж—¶й—ҙпјҲдё»иҰҒз»“еұҖдёҺз»ҲзӮ№пјүгҖҒеҒҸеҖҡйЈҺйҷ©жҸҗзӨәпјҲйҡҸжңәеҢ–дёҺеҲҶжһҗжғ…еҶөгҖҒзӣІжі•гҖҒиҜ•йӘҢжіЁеҶҢпјүгҖҒдјҳж•ҲжҖ§жҸҗзӨәпјҲж•Ҳеә”йҮҸгҖҒдё»иҰҒз»“еұҖз»„й—ҙеә”зӯ”е·®ејӮпјүгҖҒжҢүеҒҮи®ҫеҫ—еҮәзҡ„дјҳж•ҲжҖ§з»“и®әпјҲз»“и®әпјүгҖӮдёәйҒҝе…Қз»“и®әдёӯеҮәзҺ°ж— ж„Ҹзҡ„жҠҘе‘ҠеҒҸеҖҡжҲ–жёІжҹ“еҒҸеҖҡпјҢжҲ‘们е»әи®®йҰ–еҸҘеӣҙз»•з ”з©¶зӣ®зҡ„дёҺеҜ№еә”дё»иҰҒз»“еұҖж’°еҶҷз»“и®әпјҢйҮҮз”Ё PICOT жЎҶжһ¶пјҲз ”з©¶дәәзҫӨгҖҒе№Ійў„жҺӘж–ҪгҖҒеҜ№з…§жҺӘж–ҪгҖҒз»“еұҖжҢҮж ҮгҖҒж—¶й—ҙиҢғеӣҙпјүгҖӮзӨәдҫӢпјҡвҖңдёҺеҜ№з…§жҺӘж–Ҫ C зӣёжҜ”пјҢе№Ійў„жҺӘж–Ҫ I еңЁ T ж—¶й—ҙзӮ№жңӘжҳҫи‘—йҷҚдҪҺ P дәәзҫӨзҡ„дё»иҰҒз»“еұҖжҢҮж Ү OвҖқгҖӮйҡҸеҗҺ继з»ӯжҠҘе‘Ҡж¬ЎиҰҒз»“еұҖпјҡвҖңй’ҲеҜ№ж¬ЎиҰҒз»“еұҖжҢҮж Ү XгҖҒYгҖҒZпјҢз»“жһңжҳҫзӨәвҖҰвҖҰвҖқпјҲеӣҫ 2пјүгҖӮ
еӣҫ 2В ж’°еҶҷз»“и®әйҰ–еҸҘж—¶пјҢз»“еҗҲз ”з©¶зӣ®зҡ„гҖҒеҒҮи®ҫдёҺиҜ•йӘҢи®ҫи®ЎпјҢеҸҜејәеҢ–з»“и®әдёҺз ”з©¶зӣ®зҡ„гҖҒеҒҮи®ҫзҡ„е…іиҒ”жҖ§гҖӮ
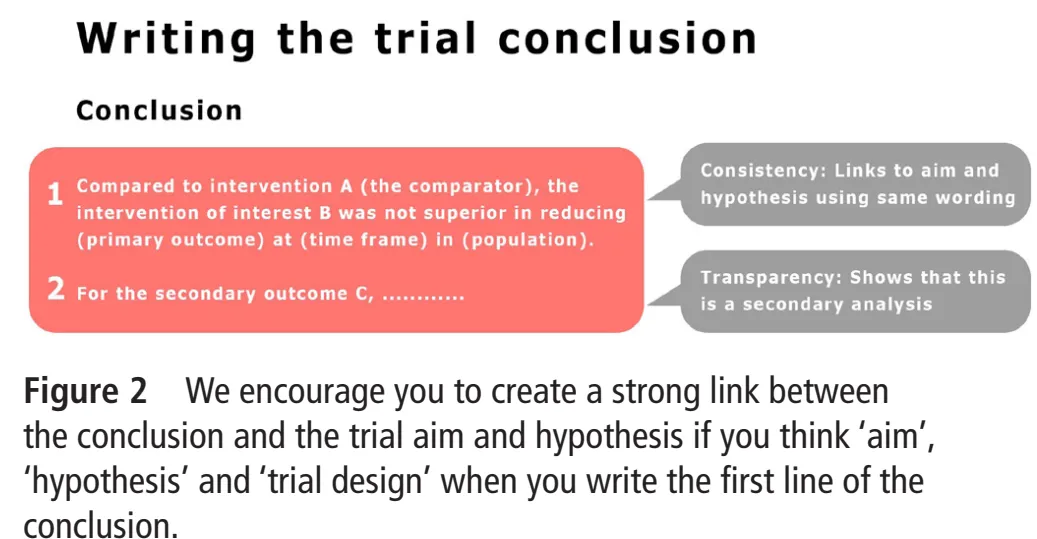
иӢҘиҜ•йӘҢдёәеүҚзһ»жҖ§жіЁеҶҢпјҢе»әи®®еңЁж‘ҳиҰҒжң«е°ҫж ҮжіЁпјҡвҖңиҜ•йӘҢжіЁеҶҢеҸ·пјҡпјҲзј–еҸ·пјүпјҲеүҚзһ»жҖ§жіЁеҶҢпјүвҖқгҖӮиӢҘеӣ зү№ж®ҠеҺҹеӣ жңӘеңЁйҰ–дҫӢеҸ—иҜ•иҖ…е…Ҙз»„еүҚе®ҢжҲҗжіЁеҶҢпјҲеүҚзһ»жҖ§ / йў„жіЁеҶҢпјүпјҢе»әи®®еңЁж‘ҳиҰҒеә•йғЁйҖҸжҳҺж ҮжіЁпјҡвҖңиҜ•йӘҢжіЁеҶҢеҸ·пјҡпјҲзј–еҸ·пјүпјҲеӣһйЎҫжҖ§жіЁеҶҢпјүвҖқгҖӮиҝҷжҳҜзӣ®еүҚ BMC зі»еҲ—жңҹеҲҠжҺҘ收еӣһйЎҫжҖ§жіЁеҶҢиҜ•йӘҢзҡ„зј–иҫ‘ж”ҝзӯ–гҖӮеңЁиҜ•йӘҢжҠҘе‘ҠжӯЈж–ҮдёӯпјҢжҲ‘们е»әи®®иҜҙжҳҺжіЁеҶҢж–№ејҸзҡ„еҺҹеӣ пјҢ并йҷҲиҝ°иҜ•йӘҢеҗҜеҠЁеҗҺжҳҜеҗҰеҸ‘з”ҹе…ій”®еҸҳжӣҙпјҢеӣ ж— е…¬ејҖи®°еҪ•еҸҜж ёжҹҘдҪ зҡ„з ”з©¶еҲқиЎ·гҖӮиӢҘдҪ е·Іе°ҶиҜ•йӘҢжҠҘе‘ҠеҸ‘еёғдёәејҖж”ҫиҺ·еҸ–йў„еҚ°жң¬пјҢе»әи®®еңЁж‘ҳиҰҒеә•йғЁж·»еҠ йў„еҚ°жң¬дҝЎжҒҜпјҲйў„еҚ°жң¬зӣёе…іеҶ…е®№иҜҰи§ҒдёӢж–ҮпјүпјҢеё®еҠ©иҜ»иҖ…иҺ·еҸ–иҜ•йӘҢжҠҘе‘Ҡзҡ„ејҖж”ҫиҺ·еҸ–зүҲжң¬пјҢ并йҖҡиҝҮж•°еӯ—еҜ№иұЎж ҮиҜҶз¬ҰпјҲDOIпјүе…іиҒ”дёӨд»Ҫж–Ү件пјҡвҖңйў„еҚ°жң¬пјҲејҖж”ҫиҺ·еҸ–пјүпјҡhttp://doi.org/пјҲDOI зј–еҸ·пјүвҖқгҖӮе»әи®®еҜ№ж‘ҳиҰҒе…ій”®дҝЎжҒҜйҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢзЎ®дҝқдёҺиҜ•йӘҢжіЁеҶҢгҖҒе·ІеҸ‘иЎЁж–№жЎҲеҸҠиҜ•йӘҢжҠҘе‘ҠжӯЈж–ҮпјҲеҰӮз ”з©¶зӣ®зҡ„гҖҒз»“и®әпјүдёҖиҮҙгҖӮ
еј•иЁҖпјҡжҳҺзЎ®иҜ•йӘҢзҡ„ вҖңз ”з©¶еҝ…иҰҒжҖ§вҖқ
жң¬йғЁеҲҶйңҖйҳҗиҝ°иҜ•йӘҢзҡ„з ”з©¶еҝ…иҰҒжҖ§пјҢеҚіејҖеұ•жң¬иҜ•йӘҢзҡ„ж ёеҝғдҫқжҚ®гҖӮиӢҘдҪ дёҺе…ұеҗҢдҪңиҖ…жңӘжҳҺзЎ®з ”з©¶еҝ…иҰҒжҖ§пјҢе°Ҷйҡҫд»ҘеңЁиҜ•йӘҢжҠҘе‘Ҡдёӯжё…жҷ°дј йҖ’гҖӮиҜ»иҖ…е·ІйҖҡиҝҮж ҮйўҳдёҺж‘ҳиҰҒзӯӣйҖүпјҢе…·еӨҮйҳ…иҜ»е…ҙи¶ЈпјҢдҪҶеј•иЁҖжҳҜжңҹеҲҠе®ЎзЁҝдәәдёҺзј–иҫ‘еҲӨж–ӯиҜ•йӘҢжҠҘе‘ҠйҮҚиҰҒжҖ§зҡ„е…ій”®гҖӮеӣ жӯӨпјҢеј•иЁҖйңҖе…је…·и¶Је‘іжҖ§дёҺз®ҖжҙҒжҖ§пјҢжҳҺзЎ®жң¬иҜ•йӘҢжӢҹеЎ«иЎҘзҡ„з ”з©¶з©әзҷҪгҖӮ
еј•иЁҖйңҖйҳҗиҝ°з§‘з ”иғҢжҷҜдёҺз ”з©¶дҫқжҚ®пјҢеә”дёҺиҜ•йӘҢж–№жЎҲзҡ„иғҢжҷҜйғЁеҲҶдҝқжҢҒдёҖиҮҙпјҢеӣ ејҖеұ•иҜ•йӘҢзҡ„ж ёеҝғеҺҹеӣ жңӘеҸ‘з”ҹж”№еҸҳгҖӮеӣ жӯӨпјҢеј•иЁҖеҸҜеҹәжң¬еӨҚеҲ¶зІҳиҙҙиҜ•йӘҢж–№жЎҲеҶ…е®№гҖӮдҪҶеңЁиҜ•йӘҢзӯ№еӨҮдёҺе®һж–Ҫжңҹй—ҙпјҢиӢҘе…¶д»–з ”з©¶иҖ…еҸ‘иЎЁдәҶзӣёе…із ”究жҲҗжһңпјҢж— и®әж”ҜжҢҒжҲ–еҸҚеҜ№дҪ зҡ„з»“жһңпјҢеқҮйңҖеңЁеј•иЁҖдёӯжҸҗеҸҠгҖӮеј•иЁҖеә”зәіе…Ҙзӣёе…із ”究зҡ„жҖ»з»“пјҢеҚіжңҖж–°зҡ„зі»з»ҹиҜ„д»·пјҢжҲ–иҮіе°‘зәіе…Ҙжң¬йўҶеҹҹжңҖж–°еҸ‘иЎЁзҡ„зі»з»ҹиҜ„д»·гҖӮж–ҮзҢ®з»јиҝ°йңҖйҒҝе…ҚйҖүжӢ©жҖ§еј•з”ЁпјҢеҗҰеҲҷеҸҜиғҪиҜҜеҜјиҜ»иҖ…гҖҒеўһеҠ иҜҒе®һеҒҸеҖҡйЈҺйҷ©пјҢжҲ–ж— ж„ҸеӨёеӨ§з ”究з©әзҷҪзҡ„规模дёҺйҮҚиҰҒжҖ§гҖӮеҸҜеҗ‘иҜ»иҖ…иҜҙжҳҺдҪ е·Іе…Ёйқўж ёжҹҘзҺ°жңүиҜҒжҚ®пјҢ并еҹәдәҺжңҖдҪіиҜҒжҚ®жҳҺзЎ®иҜ•йӘҢеҝ…иҰҒжҖ§пјҡвҖңжңҖж–°дёҖйЎ№е…ідәҺпјҲе№Ійў„жҺӘж–ҪпјүеҜ№пјҲзӣ®ж Үз»“еұҖжҢҮж Үпјүжңүж•ҲжҖ§зҡ„зі»з»ҹиҜ„д»·дёҺ Meta еҲҶжһҗз»“и®әдёәпјҲж ёеҝғз»“жһңпјүгҖӮиҜҘзі»з»ҹиҜ„д»·еҸ‘иЎЁеҗҺпјҢпјҲдҪңиҖ…пјүеҸ‘иЎЁзҡ„дёӨйЎ№иҝ‘жңҹиҜ•йӘҢжҠҘе‘Ҡж”ҜжҢҒиҜҘз»“и®әвҖқгҖӮ
иҜ•йӘҢж–№жЎҲзҡ„иғҢжҷҜеҶ…е®№йҖҡеёёиҫғдёәеҶ—й•ҝпјҢиҜ•йӘҢжҠҘе‘Ҡеј•иЁҖеҸҜйҖӮеҪ“зІҫз®ҖгҖӮз»“еҗҲзӣ®ж ҮиҜ»иҖ…зҫӨдҪ“и°ғж•ҙеј•иЁҖеҶ…е®№пјҢ专科жңҹеҲҠж— йңҖйҳҗиҝ°йўҶеҹҹеҶ…йҖҡиҜҶзҹҘиҜҶгҖӮиӢҘж’°еҶҷиҝҗеҠЁжҚҹдјӨжІ»з–—зӣёе…іеҶ…容并жӢҹжҠ•зЁҝиҮіиҝҗеҠЁеҢ»еӯҰжңҹеҲҠпјҢж— йңҖиҜҰз»Ҷйҳҗиҝ°жӮЈз—…зҺҮгҖҒеҢ»з–—жҲҗжң¬гҖҒжҚҹдјӨжңәеҲ¶жҲ–жІ»з–—жңүж•ҲжҖ§зҡ„йҮҚиҰҒжҖ§пјҢжңҹеҲҠиҜ»иҖ…е·ІжҺҢжҸЎжӯӨзұ»дҝЎжҒҜгҖӮйҮҚзӮ№иҒҡз„ҰиҜ•йӘҢз ”з©¶дҫқжҚ®гҖҒе…·дҪ“科еӯҰй—®йўҳдёҺз ”з©¶зӣ®зҡ„пјҢзІҫз®ҖеҶ—дҪҷиЎЁиҝ°пјҢе°Ҷеӯ—ж•°з”ЁдәҺжӣҙе…ій”®зҡ„еҶ…е®№гҖӮ
еј•иЁҖз»“е°ҫйңҖжҳҺзЎ®иҜ•йӘҢз ”з©¶зӣ®зҡ„дёҺеҒҮи®ҫгҖӮз ”з©¶зӣ®зҡ„дёҺеҒҮи®ҫзҡ„еҢәеҲҶ并йқһжҳ“дәӢпјҢдҪҶеҒҮи®ҫйҖҡеёёжӣҙе…·дҪ“пјҢдёҺйҖүе®ҡзҡ„иҜ•йӘҢи®ҫи®ЎгҖҒз»“еұҖжҢҮж ҮгҖҒз»ҹи®ЎеҲҶжһҗи®ЎеҲ’пјҲSAPпјүеҜҶеҲҮзӣёе…іпјҢиҝҷжҳҜеј•иЁҖзҡ„ж ёеҝғеҶ…е®№гҖӮе»әи®®еӨҚеҲ¶зІҳиҙҙиҜ•йӘҢжіЁеҶҢеә“е’Ң / жҲ–е·ІеҸ‘иЎЁж–№жЎҲзҡ„еҶ…е®№д»ҘдҝқиҜҒдёҖиҮҙжҖ§пјҲеӣҫ 1пјүпјҢеҗҢж—¶еҜ№ж‘ҳиҰҒдёҺиҜ•йӘҢжҠҘе‘ҠжӯЈж–ҮйҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢзЎ®дҝқж‘ҳиҰҒдёҺжӯЈж–Үзҡ„з ”з©¶зӣ®зҡ„дёҖиҮҙгҖӮ
ж–№жі•пјҡжҳҺзЎ®иҜ•йӘҢзҡ„ вҖңе®һж–Ҫж–№ејҸвҖқ
жң¬йғЁеҲҶйңҖйҳҗиҝ°иҜ•йӘҢзҡ„е®һж–Ҫж–№ејҸпјҢеҚіеҰӮдҪ•еӣһзӯ”з ”з©¶еҝ…иҰҒжҖ§зӣёе…ій—®йўҳгҖӮж–№жі•еӯҰйғЁеҲҶдёәз ”з©¶е®һж–ҪиҝҮзЁӢзҡ„иҜҰз»ҶжҸҸиҝ°пјҢж ёеҝғдҪңз”ЁжңүдәҢпјҡпјҲ1пјүжҸҗдҫӣе……и¶ідҝЎжҒҜпјҢдҫҝдәҺиҜ»иҖ…жү№еҲӨжҖ§иҜ„дј°дёҺи§ЈиҜ»з»“жһңпјӣпјҲ2пјүдј йҖ’е®Ңж•ҙз»ҶиҠӮпјҢдҪҝе…¶д»–з ”з©¶иҖ…еҸҜе®Ңж•ҙжҲ–йғЁеҲҶйҮҚеӨҚиҜ•йӘҢгҖӮдёәдҝқйҡңиҜ•йӘҢз»“жһңзҡ„дёҙеәҠеә”з”ЁпјҢйңҖиҜҰз»ҶжҸҸиҝ°дәәзҫӨйҖүжӢ©гҖҒиҜ„дј°ж–№жі•дёҺе№Ійў„жҺӘж–ҪгҖӮж–№жі•еӯҰйғЁеҲҶзҡ„е…¶д»–е…ій”®еҶ…е®№пјҢжҳҜиҜ„дј°иҜ•йӘҢз§‘з ”иҙЁйҮҸгҖҒж•ҲеәҰдёҺдҝЎеәҰзҡ„ж ёеҝғдҫқжҚ®гҖӮ
зҗҶжғіжғ…еҶөдёӢпјҢж–№жі•еӯҰйғЁеҲҶеә”дёҺиҜ•йӘҢж–№жЎҲе®Ңе…ЁдёҖиҮҙгҖӮдҪҶе®һйҷ…иҜ•йӘҢе®һж–ҪдёӯпјҢе®Ңе…ЁйҒөеҫӘж–№жЎҲиҰҒжұӮеҮ д№Һж— жі•е®һзҺ°пјҢеӣ жӯӨеҝ…йЎ»жҠҘе‘Ҡж–№жЎҲзҡ„жүҖжңүеҒҸзҰ»дёҺиҝқ规жғ…еҶөгҖӮеҒҸзҰ»ж–№жЎҲ并йқһ вҖңз§‘з ”й”ҷиҜҜвҖқпјҢдҪҶйңҖжҠҘе‘ҠжүҖжңүеҸҜиғҪеҪұе“Қдё»иҰҒз»“еұҖдёҺе…ій”®ж¬ЎиҰҒз»“еұҖзҡ„еҒҸзҰ»жғ…еҶөпјҲиҝӣиҖҢеҪұе“Қж•ҙдҪ“иҜ•йӘҢз»“жһңи§ЈиҜ»пјүгҖӮе°Өе…¶йңҖжҳҺзЎ® вҖңи®ЎеҲ’еҶ…вҖқ еҒҸзҰ»пјҢеҰӮзәіе…ҘжҺ’йҷӨж ҮеҮҶеҸҳжӣҙпјҲеӣ е®үе…ЁжҖ§жҲ–жӢӣеӢҹзј“ж…ўпјүгҖҒд»ӘеҷЁи®ҫеӨҮеҸҳжӣҙпјҲеҰӮ MRI жү«жҸҸд»Әж•…йҡңжӣҙжҚўпјүгҖӮе»әи®®жҠҘе‘ҠеҒҸзҰ»жғ…еҶөгҖҒеҺҹеӣ еҸҠе…·дҪ“еӨ„зҗҶж–№ејҸгҖӮ
ж’°еҶҷиҜ•йӘҢж–№жі•еӯҰж—¶пјҢи®ҫжғідҪ зҡ„иҜ•йӘҢжҠҘе‘ҠжңӘжқҘдјҡиў«зәіе…Ҙзі»з»ҹиҜ„д»·жҲ–дёҙеәҠжҢҮеҚ—иҝӣиЎҢдёҘж јж ёжҹҘгҖӮе®ЎзЁҝдәәдјҡиҜ„дј°иҜ•йӘҢжҠҘе‘Ҡзҡ„зјәйҷ·пјҲжҲ–еҒҸеҖҡйЈҺйҷ©пјүпјҢеҚідҫҝдҪ дёҘи°Ёе®һж–ҪиҜ•йӘҢпјҲеҒҸеҖҡйЈҺйҷ©дҪҺпјүпјҢжҠҘе‘ҠдёҚе®Ңж•ҙд№ҹдјҡеҜјиҮҙе®ЎзЁҝдәәж— жі•жҳҺзЎ®ж–№жі•еӯҰз»ҶиҠӮпјҢиҝӣиҖҢйҷҚдҪҺиҜ•йӘҢиҙЁйҮҸиҜ„зә§гҖӮе»әи®®жҹҘйҳ…гҖҠCochrane е№Ійў„жҺӘж–Ҫзі»з»ҹиҜ„д»·жүӢеҶҢгҖӢпјҢиҜҘжүӢеҶҢжҸҗдҫӣдёӘдҪ“иҜ•йӘҢиҜ„дј°зҡ„иҜҰз»ҶдҝЎжҒҜпјҢжҳҺзЎ®е®ЎзЁҝдәәзҡ„ж ёжҹҘиҰҒзӮ№гҖӮдҫӢеҰӮпјҢе®ЎзЁҝдәәиҜ„дј°еҲҶй…Қйҡҗи—ҸеҒҸеҖҡйЈҺйҷ©ж—¶пјҢдјҡж ёжҹҘ вҖңйЎәеәҸзј–еҸ·гҖҒдёҚйҖҸжҳҺгҖҒеҜҶе°ҒдҝЎе°ҒвҖқ зӯүиЎЁиҝ°пјҢдәҶи§ЈиҜҘиҰҒзӮ№еҸҜеё®еҠ©дҪ жё…жҷ°жҠҘе‘ҠиҜ•йӘҢзҡ„еҲҶй…Қйҡҗи—Ҹе®һж–Ҫж–№ејҸгҖӮ
ж–№жі•пјҡз»“еұҖжҢҮж Ү
CONSORT жё…еҚ•дёӯ вҖңз»“еұҖжҢҮж ҮвҖқ жқЎзӣ®иҰҒжұӮжҠҘе‘ҠпјҡвҖңе®Ңж•ҙе®ҡд№үзҡ„йў„и®ҫдё»иҰҒдёҺж¬ЎиҰҒз»“еұҖжҢҮж ҮпјҢеҢ…жӢ¬иҜ„дј°ж–№ејҸдёҺж—¶й—ҙвҖқвҖңиҜ•йӘҢеҗҜеҠЁеҗҺз»“еұҖжҢҮж Үзҡ„жүҖжңүеҸҳжӣҙеҸҠеҺҹеӣ вҖқгҖӮйҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢеҸҜзӣҙжҺҘд»Һж–№жЎҲдёҺйў„жіЁеҶҢиҜ•йӘҢж‘ҳиҰҒдёӯеӨҚеҲ¶еҶ…е®№иҮіиҜ•йӘҢжҠҘе‘ҠпјҢдҝқиҜҒз»“еұҖжҢҮж Үж•°йҮҸгҖҒеұӮзә§дёҺжҺӘиҫһзҡ„дёҖиҮҙжҖ§гҖӮиӢҘиҜ•йӘҢжңҹй—ҙйңҖж–°еўһжҲ–еҲ йҷӨз»“еұҖжҢҮж ҮпјҢе»әи®®йҖҸжҳҺжҠҘе‘ҠеҸҳжӣҙжғ…еҶөеҸҠеҺҹеӣ гҖӮ
COMPare иҜ•йӘҢйЎ№зӣ®еӣўйҳҹзі»з»ҹж ёжҹҘдәҶ 2015 е№ҙ 10 жңҲиҮі 2016 е№ҙ 1 жңҲдә”еӨ§еҢ»еӯҰжңҹеҲҠеҸ‘иЎЁзҡ„жүҖжңүиҜ•йӘҢпјҢжҹҘжүҫз»“жһңжҠҘе‘Ҡй”ҷиҜҜдёҺз»“еұҖжҢҮж ҮеҸҳжӣҙжғ…еҶөпјҢеҸ‘зҺ°з»“еұҖжҢҮж ҮжҠҘе‘ҠеӯҳеңЁеӨ§йҮҸдёҚдёҖиҮҙй—®йўҳгҖӮиӢҘиҜ•йӘҢеҗҜеҠЁеҗҺйңҖеҸҳжӣҙз»“еұҖжҢҮж ҮпјҢйҖҸжҳҺйҷҲиҝ°еҸҳжӣҙжғ…еҶөеҸҠеҺҹеӣ гҖӮиӢҘи®ЎеҲ’еңЁеҗҺз»ӯпјҲж¬ЎиҰҒпјүиҜ•йӘҢжҠҘе‘ҠдёӯжҠҘе‘Ҡ已收йӣҶзҡ„з»“еұҖжҢҮж ҮпјҢе»әи®®еңЁдё»иҰҒиҜ•йӘҢжҠҘе‘ҠдёӯжҳҺзЎ®пјҡз»“еұҖжҢҮж Үе·ІжҢүиҜ•йӘҢжіЁеҶҢиҰҒжұӮ收йӣҶпјҢе°ҶеңЁеҗҺз»ӯжҠҘе‘Ҡдёӯе‘ҲзҺ°гҖӮдҫӢеҰӮиҜ•йӘҢдёӯ收йӣҶдәҶжңәеҲ¶жҖ§дёҺжҺўзҙўжҖ§з»“еұҖжҢҮж ҮпјҲеҰӮеҫ…еҗҺз»ӯе…ҲиҝӣеҲҶеӯҗеҲҶжһҗзҡ„иЎҖж¶Іж ·жң¬пјүпјҢжҳҺ确已收йӣҶеҸҜйҒҝе…Қз»“еұҖжҢҮж ҮиҜҜжҠҘгҖӮCOMPare иҜ•йӘҢйЎ№зӣ®еёёи§Ғй—®йўҳи§Јзӯ”дёӯиҜҙжҳҺпјҡвҖңй—®пјҡиӢҘйғЁеҲҶз»“еұҖжҢҮж ҮеңЁе…¶д»–еҮәзүҲзү©дёӯжҠҘе‘ҠиҜҘеҰӮдҪ•еӨ„зҗҶпјҹзӯ”пјҡеҸӘиҰҒеңЁиҜ•йӘҢеҸ‘иЎЁдёӯжҳҺзЎ®иҜҘжғ…еҶөеҚіеҸҜгҖӮдҫӢеҰӮиҜ•йӘҢжҠҘе‘ҠдёӯиҜҙжҳҺвҖҳжң¬ж–ҮжҠҘе‘Ҡ AгҖҒBгҖҒC з»“еұҖжҢҮж ҮпјҢеҗҺз»ӯи®әж–Үе°ҶжҠҘе‘Ҡ XгҖҒYгҖҒZ з»“еұҖжҢҮж ҮвҖҷпјҢеҲҷ XгҖҒYгҖҒZ з»“еұҖжҢҮж ҮдёҚи§ҶдёәжңӘжҠҘе‘ҠпјҢдёҚи®Ўе…ҘжңӘжҠҘе‘ҠеҲҶжҜҚвҖқгҖӮ
ж–№жі•пјҡе№Ійў„жҺӘж–Ҫ
规иҢғжҠҘе‘Ҡе№Ійў„жҺӘж–ҪпјҢеҜ№иҜ•йӘҢе№Ійў„зҡ„дёҙеәҠеә”з”ЁгҖҒз»“жһңзҡ„жӯЈзЎ®и§ЈиҜ»гҖҒдёҺеҗҢзұ»иҜ•йӘҢзҡ„еҜ№жҜ”гҖҒж–°з ”з©¶й—®йўҳзҡ„жҸҗеҮәиҮіе…ійҮҚиҰҒгҖӮйҒ—жҶҫзҡ„жҳҜпјҢе№Ійў„жҺӘж–ҪжҠҘе‘Ҡжҷ®йҒҚдёҚ规иҢғгҖӮдёәиҫ…еҠ©е№Ійў„жҺӘж–ҪжҠҘе‘ҠпјҢз ”з©¶дәәе‘ҳеҲ¶е®ҡдәҶгҖҠе№Ійў„жҺӘж–Ҫе®Ңе–„жҠҘе‘Ҡпјҡе№Ійў„жҸҸиҝ°дёҺйҮҚеӨҚжЁЎжқҝгҖӢпјҲTIDieRпјүжё…еҚ•пјҢеё®еҠ©е®Ңж•ҙгҖҒе…Ёйқўең°жҸҸиҝ°е№Ійў„жҺӘж–ҪгҖӮдҪ д№ҹеҸҜжҹҘйҳ…е№Ійў„жҺӘж–Ҫдё“еұһжҢҮеҚ—жҲ–жҠҘе‘Ҡжё…еҚ•пјҢеҰӮиҝҗеҠЁиҜ•йӘҢзҡ„иҝҗеҠЁжҠҘе‘Ҡе…ұиҜҶжЁЎжқҝпјҲCERTпјүгҖӮе»әи®®йҮҮз”ЁзӣёеҗҢж ҮеҮҶдёҺжё…еҚ•жҸҸиҝ° вҖң常规жҠӨзҗҶвҖқ жҲ–е…¶д»–еҜ№з…§жҺӘж–ҪгҖӮйғЁеҲҶеҜ№з…§жҺӘж–Ҫе·ІеҲ¶е®ҡдё“еұһжҠҘе‘Ҡжё…еҚ•пјҢеҰӮе®үж…°еүӮдёҺеҒҮе№Ійў„еҜ№з…§зҡ„жҠҘе‘Ҡжё…еҚ•гҖӮиӢҘдҪ е·ІеңЁе·ІеҸ‘иЎЁж–№жЎҲдёӯиҜҰз»ҶжҸҸиҝ°е№Ійў„жҺӘж–ҪдёҺеҜ№з…§жҺӘж–ҪпјҢиҜ•йӘҢжңҹй—ҙе№Ійў„жҺӘж–ҪжҲ–е®һж–Ҫж–№ејҸеҸ‘з”ҹеҸҳжӣҙж—¶пјҢеҸҜжӣҙж–°жҸҸиҝ°е№¶дҪңдёәиЎҘе……жқҗж–ҷйҡҸиҜ•йӘҢжҠҘе‘ҠжҸҗдәӨпјҢеҠ©еҠӣиҜ•йӘҢз»“жһңзҡ„йҮҚеӨҚдёҺдёҙеәҠеә”з”ЁгҖӮиӢҘжңӘеҸ‘иЎЁиҜҰз»Ҷзҡ„е№Ійў„жҺӘж–ҪжҸҸиҝ°пјҢеҸҜе°Ҷе…¶дҪңдёәиҜ•йӘҢжҠҘе‘ҠиЎҘе……жқҗж–ҷеҸ‘иЎЁпјҢ规йҒҝжңҹеҲҠжӯЈж–Үеӯ—ж•°йҷҗеҲ¶гҖӮ
ж–№жі•пјҡж ·жң¬йҮҸ
ж ·жң¬йҮҸйғЁеҲҶйңҖйҳҗиҝ°иҜ•йӘҢзӯ№еӨҮйҳ¶ж®өпјҢеҰӮдҪ•дҝқиҜҒиҜ•йӘҢе…·еӨҮи¶іеӨҹз»ҹи®ЎеӯҰж•ҲиғҪпјҢиҜҶеҲ«дё»иҰҒз»“еұҖзҡ„зү№е®ҡе·®ејӮпјҲзӣ®ж Үе·®ејӮпјүпјҢеҗҢж—¶иҜҙжҳҺжңӘзәіе…ҘиҜ•йӘҢжүҖйңҖд»ҘеӨ–зҡ„йўқеӨ–еҸ—иҜ•иҖ…гҖӮеӣ зӣёе…іеҲҶжһҗе·ІеңЁзӯ№еӨҮйҳ¶ж®өе®ҢжҲҗпјҢеҸҜзӣҙжҺҘеӨҚеҲ¶зІҳиҙҙиҜ•йӘҢж–№жЎҲеҶ…е®№гҖӮPREPARE иҜ•йӘҢжҢҮеҚ—иҜҰз»Ҷйҳҗиҝ°дәҶж ·жң¬йҮҸи®Ўз®—зҡ„еҹәзЎҖеҶ…е®№гҖӮ
ж–№жі•пјҡз»ҹи®ЎеҲҶжһҗ
з»ҹи®ЎжҠҘе‘ҠдёҚ规иҢғжҳҜз”ҹзү©еҢ»еӯҰж–ҮзҢ®дёӯй•ҝжңҹеӯҳеңЁгҖҒжҷ®йҒҚгҖҒжҪңеңЁдёҘйҮҚеҚҙжңӘиў«еӨҡж•°иҜ»иҖ…еҜҹи§үзҡ„й—®йўҳгҖӮзӣ®еүҚе·Іжңүз»ҹи®ЎеҲҶжһҗи®ЎеҲ’пјҲSAPпјүж’°еҶҷзҡ„йҖҡз”ЁжҢҮеҚ—пјҢжҺЁиҚҗдёҙеәҠиҜ•йӘҢеҲҶжһҗж•°жҚ®еүҚйңҖжҳҺзЎ®зҡ„жңҖдҪҺжқЎзӣ®иҰҒжұӮгҖӮиӢҘжңӘеңЁиҜ•йӘҢж–№жЎҲдёӯеҲ¶е®ҡдё“еұһз»ҹи®ЎеҲҶжһҗи®ЎеҲ’пјҢе»әи®®е’ЁиҜўз”ҹзү©з»ҹи®ЎеӯҰ家пјҢеңЁжҹҘзңӢж•°жҚ®жҲ–еҗҜеҠЁеҲҶжһҗеүҚе®ҢжҲҗеҲ¶е®ҡгҖӮ
з»ҹи®ЎеҲҶжһҗи®ЎеҲ’еҸҜдҝқиҜҒз»ҹи®Ўж–№жі•жҠҘе‘Ҡи¶іеӨҹиҜҰз»ҶпјҢдҪҝе…·еӨҮдё“дёҡзҹҘиҜҶзҡ„иҜ»иҖ…пјҲеҸҜиҺ·еҸ–еҺҹе§Ӣж•°жҚ®пјүиҜ„дј°жүҖйҖүз»ҹи®Ўж–№жі•зҡ„йҖӮз”ЁжҖ§дёҺ underlying assumptionsпјҢйӘҢиҜҒжҠҘе‘Ҡз»“жһңгҖӮз»ҹи®ЎеҲҶжһҗи®ЎеҲ’дёӯз»ҹи®Ўж–№жі•жҸҸиҝ°йҖҡеёёжһҒдёәиҜҰз»ҶпјҢе®Ңе…ЁеӨҚеҲ¶зІҳиҙҙеҸҜиғҪи¶…еҮәжңҹеҲҠзЁҝ件зҜҮе№…йҷҗеҲ¶гҖӮеӣ жӯӨе»әи®®е§Ӣз»Ҳе°Ҷз»ҹи®ЎеҲҶжһҗи®ЎеҲ’пјҲе°Ғйқўж ҮжіЁжңҖз»Ҳж—ҘжңҹпјүдҪңдёәиЎҘе……жқҗж–ҷжҸҗдәӨпјҢдҫҝдәҺзј–иҫ‘гҖҒеҗҢиЎҢе®ЎзЁҝдәәеҸҠе…¶д»–иҜ»иҖ…ж·ұе…ҘдәҶи§Јз»ҹи®Ўж–№жі•гҖӮ
жӯЈж–ҮйғЁеҲҶе»әи®®ж‘ҳеҪ•з»ҹи®ЎеҲҶжһҗи®ЎеҲ’дёӯзҡ„дё»иҰҒз»ҹи®ЎеҲҶжһҗеҶ…е®№гҖӮжҳҺзЎ®з ”з©¶зӣ®зҡ„еҗҺпјҢиҜ»иҖ…еҸҜзҗҶи§ЈиҜ•йӘҢзҡ„дё»иҰҒзӣ®ж ҮдёҺйў„жңҹз»“жһңгҖӮе»әи®®е®Ңж•ҙжҸҸиҝ°иҜ•йӘҢдё»иҰҒдёҺе…ій”®ж¬ЎиҰҒзӣ®зҡ„зҡ„еҲҶжһҗж–№жі•гҖӮйҖҡеёёйңҖеңЁдёҚеҗҢеҒҮи®ҫдёӢеҲҶжһҗж•°жҚ®йӣҶпјҲж•Ҹж„ҹжҖ§еҲҶжһҗпјүпјҢиҜ„дј°дё»иҰҒеҲҶжһҗзҡ„зЁіеҒҘжҖ§пјҢеҲҶжһҗж–№жі•еӨҡеҹәдәҺзјәеӨұж•°жҚ®еӨ„зҗҶзӯ–з•ҘжҲ–дёҚеҗҢиҜ•йӘҢдәәзҫӨпјҲеҰӮз¬ҰеҗҲж–№жЎҲйӣҶпјҢиҷҪеҸҜиғҪеӯҳеңЁеҒҸеҖҡдҪҶд»ҚжңүеҸӮиҖғд»·еҖјпјүгҖӮе»әи®®иҜҰз»ҶжҸҸиҝ°иҝҷдәӣеҲҶжһҗзӯ–з•ҘгҖӮзҺ°жңүдјҳиҙЁж•ҷеӯҰиө„жәҗеҸҜжҸҗдҫӣиҫ…еҠ©пјҢеҢ…жӢ¬ CONSORT и§ЈйҮҠдёҺиҜҰз»ҶиҜҙжҳҺж–Ү件гҖҒз»ҹи®ЎжҠҘе‘Ҡ SAMPL жҢҮеҚ—гҖҒжңҖж–°еҲ¶е®ҡзҡ„еҢ»еӯҰи®әж–Үз»ҹи®ЎиҜ„дј°жё…еҚ•пјҲCHAMPпјүеЈ°жҳҺгҖӮ
з»“жһңпјҡеҸ—иҜ•иҖ…и„ұиҗҪ
иӢҘеӨұи®ҝеҸ—иҜ•иҖ…зҡ„зү№еҫҒеңЁйҡҸжңәз»„й—ҙеӯҳеңЁе·®ејӮпјҲе°Өе…¶е·®ејӮзү№еҫҒдёҺиҜ•йӘҢз»“еұҖжҢҮж Үзӣёе…іпјүпјҢи„ұиҗҪдјҡеҜјиҮҙиҜ•йӘҢз»“жһңдә§з”ҹеҒҸеҖҡгҖӮиӢҘйҮҮз”Ё CONSORT жөҒзЁӢеӣҫеұ•зӨәиҜ•йӘҢжҰӮеҶөпјҢе»әи®®жҠҘе‘Ҡж„Ҹеҗ‘жҖ§еҲҶжһҗдәәзҫӨдёӯеҸ—иҜ•иҖ…зҡ„дәәеҸЈеӯҰзү№еҫҒпјҢиҝӣиЎҢеҗ„з»„жҸҸиҝ°жҖ§з»ҹи®ЎгҖӮе»әи®®жҢүз…§ CONSORT и§ЈйҮҠдёҺиҜҰз»ҶиҜҙжҳҺж–Ү件зҡ„жЎҶжһ¶пјҢеҲ¶дҪңз»Ҹе…ёзҡ„иЎЁ 1пјҲеҹәзәҝзү№еҫҒиЎЁпјүиҝӣиЎҢжҖ»з»“пјҢд№ҹеҸҜеҸӮиҖғ Dumville зӯүдәәзҡ„е»әи®®иЎҘе……иЎЁж јжқЎзӣ®пјҢдҪңдёәеҹәзәҝйҷ„еҪ•гҖӮ
е®ЎзЁҝдәәжңүж—¶дјҡиҰҒжұӮжҸҗдҫӣеҹәзәҝе·®ејӮзҡ„з»ҹи®ЎеӯҰжЈҖйӘҢз»“жһңгҖӮCONSORT е·ҘдҪңз»„зҡ„е»әи®®жҳҺзЎ®пјҡвҖңжӯӨзұ»еҒҮи®ҫжЈҖйӘҢж— ж„Ҹд№үпјҢеҸҜиғҪиҜҜеҜјз ”究иҖ…дёҺиҜ»иҖ…гҖӮеҹәзәҝз»„й—ҙжҜ”иҫғеә”еҹәдәҺжөӢйҮҸеҸҳйҮҸзҡ„йў„еҗҺд»·еҖјпјҢд»ҘеҸҠйҡҸжңәеҢ–еҜјиҮҙйҡҸжңәеҢ–еҸҜиғҪдә§з”ҹзҡ„д»»дҪ•дёҚеқҮиЎЎзҡ„е№…еәҰеӨ§е°ҸпјҢдё»и§ӮеҲӨж–ӯе…¶жҳҜеҗҰе…·жңүдёҙеәҠж„Ҹд№үгҖӮ
з»“жһңпјҡиҒҡз„Ұдё»иҰҒеҲҶжһҗдёҺз»„й—ҙе·®ејӮ
жӯЈзЎ®жҠҘе‘Ҡз»ҹи®ЎеҲҶжһҗз»“жһңпјҢйңҖжҳҺзЎ®еҲ—еҮәж•Ҳеә”дј°и®ЎеҖјеҸҠеҗҲйҖӮзҡ„жөӢйҮҸиҜҜе·®жҲ–дёҚзЎ®е®ҡжҖ§жҢҮж ҮпјҢеҰӮ 95% зҪ®дҝЎеҢәй—ҙпјҲCIпјүгҖӮйҡҸжңәеҜ№з…§иҜ•йӘҢж—ЁеңЁеҲҶжһҗз»„й—ҙе·®ејӮпјҢз»“жһңеә”иҒҡз„Ұз»„й—ҙе·®ејӮиҖҢйқһз»„еҶ…еҸҳеҢ–гҖӮдёҚиҝҮпјҢе‘ҲзҺ°еҗ„з»„ж•Ҳеә”дј°и®ЎеҖјжңүеҠ©дәҺйҖҸжҳҺжҠҘе‘ҠдёҺз»“жһңи§ЈиҜ»гҖӮжҲ‘们ејәзғҲе»әи®®йҒҝе…Қд»…жҠҘе‘Ҡз»ҹи®ЎеӯҰеҒҮи®ҫжЈҖйӘҢз»“жһңпјҲеҰӮ P еҖјпјүпјҢеӣ е…¶дҝЎжҒҜйҮҸжңүйҷҗпјҢж— жі•дј йҖ’ж•Ҳеә”йҮҸжҲ–дј°и®ЎеҖјзІҫеәҰзҡ„е…ій”®дҝЎжҒҜгҖӮжҠҘе‘Ҡ P еҖјж—¶пјҢе»әи®®жҠҘе‘Ҡе®һйҷ… P еҖјпјҢиҖҢйқһ Pпјң0.05пјҢйҷӨйқһж•°еҖјжһҒе°ҸпјҲеҰӮ Pпјң0.0001пјүгҖӮ
е»әи®®дјҳе…ҲжҢүеұӮзә§жҠҘе‘Ҡдё»иҰҒеҲҶжһҗз»“жһңпјҲдё»иҰҒз»“еұҖдјҳе…ҲдәҺж¬ЎиҰҒеҸҠе…¶д»–з»“еұҖпјүпјҢиҝҷдёҺиҜ•йӘҢж–№жЎҲе’Ңз»ҹи®ЎеҲҶжһҗи®ЎеҲ’дёӯзҡ„еұӮзә§дёҖиҮҙгҖӮдҝқжҢҒдёҖиҮҙ并йҮҮз”ЁеӨҚеҲ¶ - зІҳиҙҙж–№ејҸпјҢеҸҜеё®еҠ©иҜ»иҖ…еҲӨж–ӯдҪ жҳҜеҗҰйҒөеҫӘз»ҹи®ЎеҲҶжһҗи®ЎеҲ’гҖӮе»әи®®з»“жһңйғЁеҲҶйҒҝе…Қи§ЈиҜ»жҖ§иҜӯиЁҖпјҢд»…йҖҡиҝҮз»“жһңж–№еҗ‘жҸҗзӨәе…¶еҜ№жҹҗдёҖз»„зҡ„жңүеҲ©жҖ§гҖӮиӢҘдё»иҰҒеҲҶжһҗдёҺж•Ҹж„ҹжҖ§еҲҶжһҗзҡ„еҲҶжһҗйӣҶеӯҳеңЁе·®ејӮпјҢе»әи®®еңЁжӯЈж–ҮдёӯзӘҒеҮәж ҮжіЁпјҢеҸҜиғҪйңҖиҰҒжҠ•е…ҘжӣҙеӨҡзҜҮе№…и§ЈиҜ»з»јеҗҲз»“жһңпјҢеӣ еҚ•дёӘеҲҶжһҗзҡ„еҸҜдҝЎеәҰйҷҚдҪҺгҖӮ
ж•°жҚ®еҲҶжһҗиҝҮзЁӢдёӯеҸҜиғҪдә§з”ҹж–°зҡ„з ”з©¶жҖқи·ҜдёҺж„ҸеӨ–еҸ‘зҺ°пјҢиҝҷзұ»з»“жһңеҸҜиғҪе…·жңүйҮҚиҰҒд»·еҖје№¶жҺЁеҠЁз§‘з ”иҝӣеұ•гҖӮдҪҶйңҖжіЁж„ҸпјҢиҜ•йӘҢи®ҫи®ЎеҸҜиғҪж— жі•ж”ҜжҢҒжӯӨзұ»еҸ‘зҺ°зҡ„йӘҢиҜҒжҖ§еҲҶжһҗжҲ–з»“и®әпјҢйңҖеңЁз»ҹи®Ўж–№жі•йғЁеҲҶдёҺз»“жһңйғЁеҲҶжҳҺзЎ®иҜҙжҳҺиҜҘз»“жһңжңӘйў„и®ҫгҖӮеҗҢиЎҢе®ЎзЁҝдәәиҰҒжұӮеҜ№ж•°жҚ®йӣҶиҝӣиЎҢйўқеӨ–еҲҶжһҗзҡ„жғ…еҶөпјҲеёёиў«з§°дёә вҖңеҗҢиЎҢиҜ„е®ЎеҺӢеҠӣжөӢиҜ•вҖқпјүд№ҹиҫғдёәеёёи§ҒпјҢиҝҷзұ»иҰҒжұӮйҖҡеёёеҗҲзҗҶдё”жңүд»·еҖјпјҢдҪҶжһҒе°‘жӣҝд»ЈеҺҹе§ӢеҲҶжһҗзӯ–з•ҘпјҢйҷӨйқһиҜ•йӘҢи®ҫи®ЎеӯҳеңЁж №жң¬жҖ§зјәйҷ·жҲ–жүҖйҖүеҲҶжһҗж— жі•еҸҚжҳ иҜ•йӘҢи®ҫи®ЎгҖӮе»әи®®е°ҶеҗҢиЎҢе®ЎзЁҝдәәиҰҒжұӮзҡ„дәӢеҗҺеҲҶжһҗжҠҘе‘ҠдәҺиЎҘе……ж–Ү件дёӯпјҢ并еңЁдҝ®еӣһзЁҝ件зҡ„еӣһеӨҚдҝЎдёӯиҜҙжҳҺгҖӮ
з»“жһңпјҡж•°жҚ®йҖҸжҳҺеҢ–еұ•зӨә
иЎЁж јдёҺеӣҫиЎЁеә”еҸҜзӢ¬з«Ӣе‘ҲзҺ°дҝЎжҒҜпјҲеҰӮз”ЁдәҺжҠҘе‘ҠдёҺи®Іеә§пјүпјҢе»әи®®еңЁиЎЁж јдёҺеӣҫиЎЁи„ҡжіЁдёӯз®ҖиҰҒж ҮжіЁжүҖз”Ёз»ҹи®Ўж–№жі•гҖӮCONSORT жё…еҚ•дёҺи§ЈйҮҠж–Ү件жҸҗдҫӣеҗ„зұ»еӣҫиЎЁзҡ„дјҳиҙЁзӨәдҫӢдёҺиҜҙжҳҺпјҢCONSORT зҪ‘з«ҷжҸҗдҫӣеҸҜе…Қиҙ№дёӢиҪҪзҡ„жөҒзЁӢеӣҫжЁЎжқҝгҖӮе»әи®®еңЁжөҒзЁӢеӣҫдёӯиЎҘе……йўқеӨ–дҝЎжҒҜпјҢеҢ…жӢ¬дёҚеҗҢеҲҶжһҗзәіе…Ҙзҡ„еҸ—иҜ•иҖ…ж•°йҮҸпјҲеҰӮж„Ҹеҗ‘жҖ§еҲҶжһҗгҖҒеҸҜз”Ёз—…дҫӢеҲҶжһҗпјүгҖҒзјәеӨұж•°жҚ®зҡ„еЎ«иЎҘж•°йҮҸпјҲеҰӮйҖӮз”ЁпјүгҖӮзӨәдҫӢеҸҜеҸӮиҖғ Lysdal зӯүдәәзҡ„з ”з©¶гҖӮ
еңЁжөҒзЁӢеӣҫйЎ¶йғЁж ҮжіЁе…·дҪ“жҠҪж ·зӯ–з•ҘдҝЎжҒҜпјҢжңүеҠ©дәҺз»“еҗҲдёҙеәҠж„Ҹд№үи§ЈиҜ»иҜ•йӘҢз»“жһңгҖӮе»әи®®жҠҘе‘ҠиҜ•йӘҢжӢӣеӢҹжңҹй—ҙжҪңеңЁз¬ҰеҗҲжқЎд»¶зҡ„еҸ—иҜ•иҖ…жҖ»ж•°пјҢеҸҠе…¶дёӯжҺҘеҸ—еҗҲж јжҖ§иҜ„дј°зҡ„дәәж•°пјҢиҖҢйқһд»…жҠҘе‘ҠжҺҘеҸ—еҗҲж јжҖ§иҜ„дј°зҡ„дәәж•°гҖӮиҝҷеҸҜеё®еҠ©иҜ»иҖ…еҲӨж–ӯиҜ•йӘҢдәәзҫӨеҜ№жӢӣеӢҹдёӯеҝғиҜ•йӘҢжңҹй—ҙжүҖжңүжӮЈиҖ…зҡ„д»ЈиЎЁжҖ§пјҢиҜҘй—®йўҳдёҺеӨ–йғЁж•ҲеәҰзӣёе…іпјҢе°Өе…¶еҪ“иҜ•йӘҢз»“жһңеҜ№еҪ“еүҚдёҙеәҠе®һи·өжңүйҮҚиҰҒеҪұе“Қж—¶иҮіе…ійҮҚиҰҒгҖӮзӨәдҫӢеҸҜеҸӮиҖғ Clausen зӯүдәәзҡ„з ”з©¶пјҢе°ҶжҪңеңЁз¬ҰеҗҲжқЎд»¶еҸ—иҜ•иҖ…ж•°йҮҸзәіе…ҘиҜ•йӘҢжөҒзЁӢеӣҫпјӣд№ҹеҸҜеҸӮиҖғ FIMPACT иҜ•йӘҢзҡ„еҝ«йҖҹеӣһеә”пјҢи®Ёи®әиҜ•йӘҢз»“жһңеҜ№дёҙеәҠе®һи·өжңүйҮҚиҰҒеҪұе“Қж—¶пјҢзәіе…ҘжҪңеңЁз¬ҰеҗҲжқЎд»¶еҸ—иҜ•иҖ…ж•°йҮҸзҡ„йҮҚиҰҒжҖ§гҖӮ
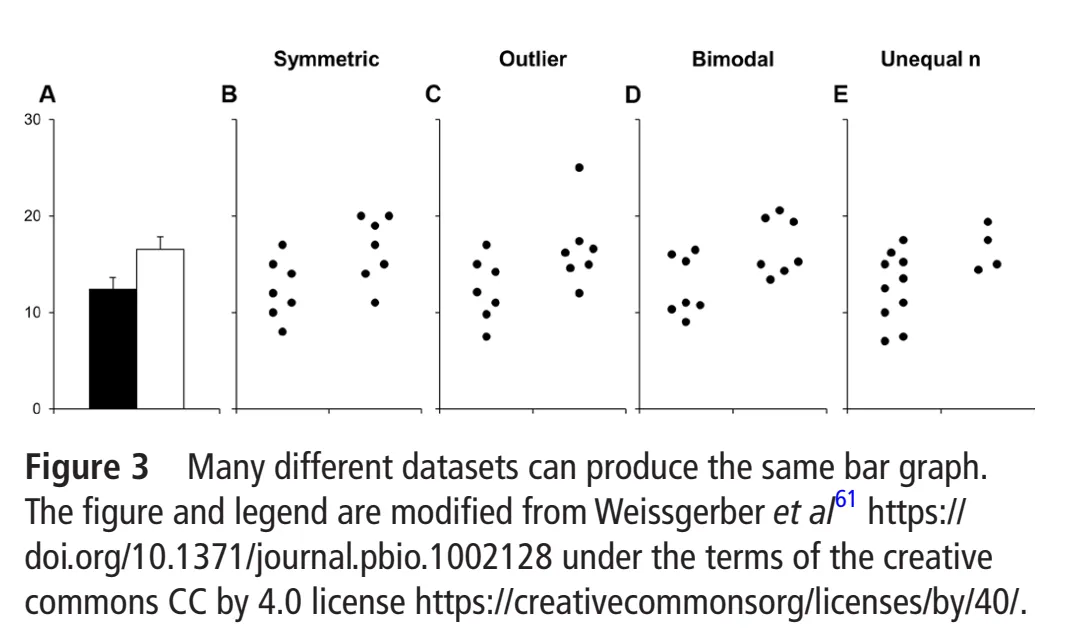
йғЁеҲҶз»“жһңйҖӮеҗҲз”ЁеӣҫеҪўеұ•зӨәгҖӮи®ёеӨҡеҹәдәҺдёҚеҗҢеҲҶеёғиҝһз»ӯж•°жҚ®зҡ„жҹұзҠ¶еӣҫжҲ–зәҝеӣҫпјҢеҸҜиғҪе‘ҲзҺ°еҮәзӣёеҗҢзҡ„и§Ҷи§үж•ҲжһңпјҲеӣҫ 3пјүгҖӮиӢҘеӣҫиЎЁдёӯжңӘзәіе…ҘеҺҹе§Ӣж•°жҚ®пјҢеӨҡж•°дҝЎжҒҜе°Ҷж— жі•иў«иҜ»иҖ…иҺ·еҸ–гҖӮе»әи®®йҮҮз”Ёж•ЈзӮ№еӣҫжӣҝд»ЈжҹұзҠ¶еӣҫпјҢдҪҝж•°жҚ®жӣҙзӣҙи§ӮгҖӮ
еӣҫ 3В еӨҡз§ҚдёҚеҗҢж•°жҚ®йӣҶеҸҜз”ҹжҲҗзӣёеҗҢзҡ„жҹұзҠ¶еӣҫгҖӮжң¬еӣҫеҸҠеӣҫдҫӢеҹәдәҺ Weissgerber зӯүдәәзҡ„з ”з©¶дҝ®ж”№пјҢйҒөеҫӘзҹҘиҜҶе…ұдә« CC BY 4.0 еҚҸи®®гҖӮ
з»“жһңпјҡдёҚиүҜдәӢ件
з ”з©¶ж–°еһӢеҢ»з–—е№Ійў„жҺӘж–Ҫж—¶пјҢз ”з©¶иҖ…еҫҖеҫҖжӣҙе…іжіЁз–—ж•ҲиҖҢйқһе®үе…ЁжҖ§гҖӮеӨҡдёӘдёҙеәҠйўҶеҹҹзҡ„иҜ•йӘҢжҠҘе‘ҠеқҮеӯҳеңЁдёҚиүҜдәӢ件жҠҘе‘ҠдёҚ规иҢғзҡ„й—®йўҳпјҢйҡҫд»ҘеҮҶзЎ®иҜ„дј°иҺ·зӣҠ - йЈҺйҷ©жҜ”гҖӮз ”з©¶дәәе‘ҳеҲ¶е®ҡдәҶ CONSORT дёҚиүҜдәӢ件жү©еұ•жқЎзӣ®пјҢд»ҘдјҳеҢ–иҜ•йӘҢдёӯдёҚиүҜдәӢ件数жҚ®зҡ„жҠҘе‘ҠгҖӮеӣ CONSORT жё…еҚ•ж ёеҝғиҒҡз„Ұз–—ж•ҲжҠҘе‘ҠпјҢе»әи®®йҮҮз”Ё CONSORT дёҚиүҜдәӢ件жү©еұ•жқЎзӣ®иЎҘе……иҜ•йӘҢжҠҘе‘ҠпјҢжҸҗеҚҮдёҚиүҜдәӢ件数жҚ®зҡ„жҠҘе‘ҠиҙЁйҮҸгҖӮ
и®Ёи®әпјҡз»“еҗҲдёҙеәҠж„Ҹд№үдёҺиҜҒе®һеҒҸеҖҡ
CONSORT жё…еҚ•жҸҗдҫӣи®Ёи®әйғЁеҲҶзҡ„ж•ҙдҪ“жЎҶжһ¶дёҺйңҖж¶өзӣ–зҡ„жқЎзӣ®пјҢ科еӯҰжңҹеҲҠеҸҜиғҪжңүйўқеӨ–иҰҒжұӮгҖӮе»әи®®йҮҮз”Ё CONSORT жё…еҚ•жҗӯе»әи®Ёи®әз»“жһ„пјҢеҝ…иҰҒж—¶иЎҘе……зӣ®ж ҮжңҹеҲҠзҡ„иҰҒжұӮгҖӮеңЁжӯӨйҮҚзӮ№ејәи°ғдёӨйЎ№е…ій”®еҶ…е®№пјҡдёҙеәҠж„Ҹд№үдёҺиҜҒе®һеҒҸеҖҡгҖӮ
е»әи®®иҒҡз„Ұдё»иҰҒеҲҶжһҗдёҺдё»иҰҒз»“еұҖгҖӮиҜ•йӘҢи®ҫи®Ўзҡ„ж ёеҝғзӣ®зҡ„жҳҜдёәиҜҘеҲҶжһҗдёҺз»“еұҖзҡ„еҒҮи®ҫжҸҗдҫӣеҸҜйқ зӯ”жЎҲгҖӮжЈҖйӘҢз»ҹи®ЎйҮҸеҸҜеҲӨж–ӯз»„й—ҙе·®ејӮжҳҜеҗҰе…·жңүз»ҹи®ЎеӯҰж„Ҹд№үгҖӮжӯӨж—¶еҲӨж–ӯ并讨и®әе…·жңүз»ҹи®ЎеӯҰж„Ҹд№үзҡ„з»„й—ҙе·®ејӮжҳҜеҗҰеҗҢж—¶е…·жңүдёҙеәҠж„Ҹд№үиҫғдёәе®№жҳ“гҖӮдҪ е·ІеңЁиҜ•йӘҢж–№жЎҲдёҺж ·жң¬йҮҸйғЁеҲҶпјҢжҳҺзЎ®йў„и®ҫе…·жңүдёҙеәҠж„Ҹд№үзҡ„жңҖе°Ҹз»„й—ҙе·®ејӮеҸҠдҫқжҚ®гҖӮиҺ·еҸ–з»„й—ҙи§ӮеҜҹе·®ејӮеҗҺпјҢж ёеҝғжҳҜеҜ№жҜ”йў„и®ҫеҖјдёҺи§ӮеҜҹеҖјпјҢи®Ёи®әи§ӮеҜҹж•Ҳеә”зҡ„еӨ§е°ҸгҖӮи§ӮеҜҹж•Ҳеә”зІҫеәҰжҳҜи®Ёи®әзҡ„йҮҚиҰҒз»ҙеәҰпјҢйҖҡеёёиҜ•йӘҢж ·жң¬йҮҸи¶ҠеӨ§пјҢи§ӮеҜҹж•Ҳеә”зІҫеәҰи¶Ҡй«ҳпјҢзІҫеәҰйҖҡиҝҮи§ӮеҜҹж•Ҳеә”зҡ„ 95% CI дҪ“зҺ°пјҢзІҫеәҰи¶Ҡй«ҳпјҢ95% CI иҢғеӣҙи¶Ҡе°ҸпјҢеҸҚд№ӢдәҰ然гҖӮе»әи®®е…Ёйқўи®Ёи®әи§ӮеҜҹж•Ҳеә”зҡ„дёҙеәҠж„Ҹд№үпјҢеҢ…жӢ¬ж•Ҳеә”еӨ§е°ҸпјҲдёҺйў„и®ҫжңҖе°ҸдёҙеәҠйҮҚиҰҒе·®ејӮеҜ№жҜ”пјүдёҺзІҫеәҰпјҢйҒҝе…Қж— ж„Ҹзҡ„иҜҒе®һеҒҸеҖҡгҖӮ
еҒҸеҖҡзұ»еһӢеӨҡж ·пјҢеҸҜеҜ№еҢ»з–—е®һи·өдә§з”ҹеӨҡж–№йқўеҪұе“ҚгҖӮдҪ еҸҜеңЁи®Ёи®әзҡ„ вҖңеұҖйҷҗжҖ§вҖқ йғЁеҲҶжҳҺзЎ®иҜҙжҳҺеҸҜиғҪеҪұе“ҚиҜ•йӘҢжөҒзЁӢжҲ–з»“еұҖзҡ„зү№е®ҡеҒҸеҖҡгҖӮе»әи®®ж’°еҶҷи®Ёи®әпјҲжҲ–ж•ҙзҜҮиҜ•йӘҢжҠҘе‘Ҡпјүж—¶пјҢе…іжіЁиҮӘиә«зҡ„ вҖңиҜҒе®һеҒҸеҖҡвҖқгҖӮеҒҸеҖҡзӣ®еҪ•еҚҸдҪңз»„е®ҡд№үпјҡвҖңиҜҒе®һеҒҸеҖҡжҢҮдёӘдҪ“дё»еҠЁеҜ»жүҫ并йҮҮз”Ёж”ҜжҢҒиҮӘиә«и§ӮзӮ№зҡ„дҝЎжҒҜпјҢеҝҪи§ҶдёҚж”ҜжҢҒиҮӘиә«и§ӮзӮ№зҡ„дҝЎжҒҜвҖқгҖӮдҪңдёәз ”з©¶иҖ…пјҢеӨҡж•°дәәдјҡж— ж„ҸжңҹжңӣиҮӘиә«е№Ійў„жҺӘж–ҪдјҳдәҺеҜ№з…§жҺӘж–ҪпјҢеҺҹеӣ еҰӮдёӢпјҡпјҲ1пјүеёҢжңӣжҺЁеҠЁйўҶеҹҹеҸ‘еұ•д»Ҙеё®еҠ©жӮЈиҖ…пјӣпјҲ2пјүи®ӨдёәиҝҷжңүеҠ©дәҺиҒҢз§°жҷӢеҚҮжҲ–иҺ·еҫ—е…¶д»–еӯҰжңҜеҘ–еҠұгҖӮдё»еҠЁж„ҸиҜҶеҲ°иҮӘиә«зҡ„иҜҒе®һеҒҸеҖҡпјҢеҸҜйҒҝе…Қж— ж„ҸиҝҮеәҰејәи°ғж¬ЎиҰҒеҲҶжһҗз»“жһңпјҲжёІжҹ“еҒҸеҖҡпјүгҖҒйҖүжӢ©жҖ§еј•з”Ёж”ҜжҢҒиҮӘиә«з»“жһңзҡ„ж–ҮзҢ®зӯүй—®йўҳгҖӮ
з»“и®әпјҡжҳҺзЎ®иҜ•йӘҢзҡ„ж ёеҝғйӘҢиҜҒзӣ®ж Ү
ж’°еҶҷиҜ•йӘҢжҠҘе‘Ҡз»“и®әж—¶пјҢе»әи®®з»“еҗҲ вҖңз ”з©¶зӣ®зҡ„вҖқвҖңеҒҮи®ҫвҖқ дёҺ вҖңиҜ•йӘҢи®ҫи®ЎвҖқ жҖқиҖғгҖӮиҜ•йӘҢж ёеҝғйӘҢиҜҒзӣ®ж ҮжҳҜд»Җд№Ҳпјҹз ”з©¶зӣ®зҡ„еҰӮдҪ•иЎЁиҝ°пјҹжҳҜиҜ„дј°е№Ійў„жҺӘж–ҪдјҳдәҺеҜ№з…§жҺӘж–ҪпјҲдјҳж•ҲжҖ§иҜ•йӘҢпјүгҖҒдёҚеҠЈдәҺеҜ№з…§жҺӘж–ҪпјҲйқһеҠЈж•ҲжҖ§иҜ•йӘҢпјүпјҢиҝҳжҳҜдёҺеҜ№з…§жҺӘж–Ҫзӯүж•ҲпјҲзӯүж•ҲжҖ§иҜ•йӘҢпјүпјҹиҝҷз§ҚжҖқиҖғж–№ејҸеҸҜејәеҢ–з ”з©¶зӣ®зҡ„гҖҒеҒҮи®ҫдёҺз»“и®әзҡ„е…іиҒ”пјҢзЎ®дҝқз»“и®әд»…еҹәдәҺиҜ•йӘҢж•°жҚ®ж”ҜжҢҒзҡ„еҶ…е®№гҖӮиӢҘдёҖйЎ№дјҳж•ҲжҖ§иҜ•йӘҢзҡ„з ”з©¶зӣ®зҡ„дёә вҖңиҜ„дј°е№Ійў„жҺӘж–Ҫ I еңЁ T ж—¶й—ҙзӮ№жҳҜеҗҰдјҳдәҺеҜ№з…§жҺӘж–Ҫ CпјҢж”№е–„ P дәәзҫӨзҡ„дё»иҰҒз»“еұҖжҢҮж Ү OвҖқпјҢдё”з»„й—ҙеә”зӯ”ж— е·®ејӮпјҢз»“и®әеҸҜејҖзҜҮиЎЁиҝ°пјҡвҖңдёҺеҜ№з…§жҺӘж–Ҫ C зӣёжҜ”пјҢе№Ійў„жҺӘж–Ҫ I еңЁ T ж—¶й—ҙзӮ№жңӘжҳҫи‘—йҷҚдҪҺ P дәәзҫӨзҡ„дё»иҰҒз»“еұҖжҢҮж Ү OвҖқгҖӮеёёи§Ғй”ҷиҜҜжҳҜе°Ҷ вҖңж— дјҳж•ҲжҖ§иҜҒжҚ®вҖқ и§ЈиҜ»дёә вҖңзӯүж•ҲжҲ–йқһеҠЈж•ҲжҖ§иҜҒжҚ®вҖқпјҢ并еҫ—еҮәе№Ійў„жҺӘж–ҪдёҺеҜ№з…§жҺӘж–Ҫж•ҲжһңзӣёеҪ“зҡ„з»“и®әгҖӮ
е®ҢжҲҗж ёеҝғеҒҮи®ҫгҖҒеҲҶжһҗдёҺз»“еұҖзҡ„з»“и®әйҷҲиҝ°еҗҺпјҢе»ә议继з»ӯжҠҘе‘Ҡжңүд»·еҖјзҡ„ж¬ЎиҰҒеҲҶжһҗз»“жһңпјҢеҗҢж—¶е‘ҠзҹҘиҜ»иҖ…жӯӨзұ»еҲҶжһҗзҡ„еҒҸеҖҡйЈҺйҷ©еҚҮй«ҳпјҡвҖңй’ҲеҜ№ж¬ЎиҰҒз»“еұҖжҢҮж Ү XгҖҒYгҖҒZпјҢз»“жһңжҳҫзӨәвҖҰвҖҰвҖқгҖӮдјҳе…Ҳеӣҙз»•дё»иҰҒеҲҶжһҗж’°еҶҷз»“и®әпјҢеҸҜйҷҚдҪҺж— ж„ҸжҠҘе‘ҠеҒҸеҖҡжҲ–жёІжҹ“еҒҸеҖҡзҡ„йЈҺйҷ©гҖӮиӢҘиҜ•йӘҢдёәжҺўзҙўжҖ§иҖҢйқһйӘҢиҜҒжҖ§пјҢжҲ–з»“еұҖжҢҮж ҮеұӮзә§е№іиЎҢгҖҒж— еҚ•дёҖдё»иҰҒз»“еұҖпјҢе»әи®®еңЁз»“и®әжң«е°ҫжҳҺзЎ®иҜҙжҳҺпјҢеҰӮ вҖңиҜҘз»“жһңйңҖеңЁжңӘжқҘиҜ•йӘҢдёӯйҮҚеӨҚйӘҢиҜҒвҖқгҖӮиҜ»иҖ…йҖҡеёёе…іжіЁиҜ•йӘҢз»“жһңзҡ„дёҙеәҠж„Ҹд№үпјҢйғЁеҲҶжңҹеҲҠе…Ғи®ёж’°еҶҷж„Ҹд№үйҷҲиҝ°пјҢйғЁеҲҶеҲҷдёҚе…Ғи®ёгҖӮиӢҘж’°еҶҷж„Ҹд№үзӣёе…іеҶ…е®№пјҢе»әи®®жҳҺзЎ®иҜҘйғЁеҲҶдёә专家жҺЁжөӢдёҺи§ӮзӮ№пјҢиЎЁиҝ°еҰӮ вҖңиҜҘз»“жһңеҸҜиғҪеҜ№вҖҰвҖҰ дә§з”ҹеҪұе“ҚпјҢеүҚжҸҗжҳҜвҖҰвҖҰвҖқгҖӮе®ҢжҲҗз»“и®әж’°еҶҷеҗҺпјҢж ёжҹҘе…¶дёҺиҜ•йӘҢзӣ®зҡ„гҖҒж‘ҳиҰҒз»“и®әзҡ„дёҖиҮҙжҖ§гҖӮ
з ”з©¶ж•°жҚ®е…ұдә«
ж №жҚ®еӣҪ家з«Ӣжі•иҰҒжұӮпјҢдҪ еҸҜиғҪеҸҜд»ҘжҲ–дёҚеҸҜд»Ҙе…ұдә«иҜ•йӘҢеҺҹе§Ӣж•°жҚ®гҖӮж•°жҚ®е…ұдә«жҳҜжҸҗеҚҮйҖҸжҳҺеәҰзҡ„ж–№ејҸпјҢйҖҡиҝҮеҗ‘дәҢж¬Ўз ”з©¶е№ҝжіӣејҖж”ҫеҸ—иҜ•иҖ…жҸҗдҫӣзҡ„ж•°жҚ®пјҢжңҖеӨ§еҢ–еҸ—иҜ•иҖ…зҡ„з§‘з ”иҙЎзҢ®гҖӮйғЁеҲҶйқһз§Ғз«Ӣиө„еҠ©жңәжһ„д№ҹиҰҒжұӮж•°жҚ®е…ұдә«гҖӮиӢҘеҸҜе…ұдә«иҜ•йӘҢж•°жҚ®пјҢйңҖиҖғиҷ‘д»ҘдёӢеҶ…е®№пјҡж•°жҚ®з®ЎзҗҶгҖҒеҢҝеҗҚеҢ–дёҺеӯҳеӮЁзҡ„е®һж“ҚжӯҘйӘӨгҖӮ
з ”з©¶дј ж’ӯзҡ„жӣҝд»ЈйҖ”еҫ„
йў„еҚ°жң¬
еҮҶеӨҮе°ҶиҜ•йӘҢжҠҘе‘ҠжҠ•зЁҝиҮіз§‘еӯҰжңҹеҲҠж—¶пјҢеҸҜиҖғиҷ‘еҸ‘еёғйў„еҚ°жң¬гҖӮйў„еҚ°жң¬жҳҜжңӘз»ҸеҗҢиЎҢиҜ„е®ЎгҖҒжңӘеңЁз§‘еӯҰжңҹеҲҠеҸ‘иЎЁзҡ„з§‘з ”жҲҗжһңпјҢйҖҡеёёдёәеҮҶеӨҮжҠ•зЁҝзҡ„зЁҝ件иҚүзЁҝпјҢд№ҹеҸҜдёәи®ЎеҲ’е…¬ејҖзҡ„ж—©жңҹзЁҝ件зүҲжң¬гҖӮеҸ‘еёғйў„еҚ°жң¬зҡ„дјҳеҠҝд№ӢдёҖжҳҜеҸҜиҺ·еҫ—ж•°еӯ—еҜ№иұЎж ҮиҜҶз¬ҰпјҲDOIпјүпјҢдҫҝдәҺж–ҮзҢ®жЈҖзҙўгҖӮеӨҡж•°еҮәзүҲе•Ҷе…Ғи®ёеҸ‘еёғйў„еҚ°жң¬пјҢдҪҶе»әи®®ж ёжҹҘзӣ®ж ҮжңҹеҲҠзҡ„йў„еҚ°жң¬ж”ҝзӯ–гҖӮзҲұжҖқе”Ҝе°”иҜҙжҳҺпјҡвҖңйў„еҚ°жң¬пјҡдҪңиҖ…еҸҜйҡҸж—¶еңЁд»»ж„Ҹе№іеҸ°еҸ‘еёғйў„еҚ°жң¬гҖӮзЁҝ件被жҺҘ收еҸ‘иЎЁеҗҺпјҢе»әи®®дҪңиҖ…йҖҡиҝҮж•°еӯ—еҜ№иұЎж ҮиҜҶз¬ҰпјҲDOIпјүе°Ҷйў„еҚ°жң¬дёҺжӯЈејҸеҸ‘иЎЁзүҲжң¬е…іиҒ”гҖӮж•°зҷҫдёҮз ”з©¶иҖ…еҸҜйҖҡиҝҮ ScienceDirect иҺ·еҸ–жӯЈејҸеҸ‘иЎЁзүҲжң¬пјҢе…іиҒ”й“ҫжҺҘеҸҜеё®еҠ©з”ЁжҲ·жҹҘжүҫгҖҒиҺ·еҸ–гҖҒеј•з”ЁдёҺдҪҝз”ЁжңҖдјҳзүҲжң¬гҖӮдҪңиҖ…еҸҜеңЁ arXiv жҲ– RePEc е№іеҸ°жӣҙж–°йў„еҚ°жң¬пјҢжӣҝжҚўдёәзЁҝ件жҺҘ收зүҲжң¬гҖӮиҜ·жіЁж„ҸпјҡйғЁеҲҶеӯҰдјҡж——дёӢжңҹеҲҠдёҺйҮҮз”ЁеҸҢзӣІеҗҢиЎҢиҜ„е®Ўзҡ„жңҹеҲҠпјҢйў„еҚ°жң¬ж”ҝзӯ–еӯҳеңЁе·®ејӮвҖқгҖӮ
йў„еҚ°жң¬е№іеҸ°жҠ•зЁҝйҖҡеёёе…Қиҙ№пјҢеҚідҫҝжңҖз»ҲеҸ‘иЎЁзҡ„иҜ•йӘҢжҠҘе‘Ҡдёәд»ҳиҙ№иҺ·еҸ–пјҢйў„еҚ°жң¬д№ҹеҸҜжҸҗдҫӣејҖж”ҫиҺ·еҸ–йҖүйЎ№гҖӮиҝҷеҸҜеңЁеҗҢиЎҢиҜ„е®Ўжңҹй—ҙиҺ·еҫ—еӨ§дј—еҸҚйҰҲпјҢ并жҸҗеүҚжҺЁе№ҝејҖж”ҫиҺ·еҸ–з ”з©¶жҲҗжһңгҖӮеҹәдәҺеҸҚйҰҲдҝ®ж”№зЁҝ件时пјҢеҸҜеҗҢжӯҘжӣҙж–°йў„еҚ°жң¬зүҲжң¬гҖӮйғЁеҲҶпјҲйқһе…ЁйғЁпјүеҮәзүҲе•Ҷе…Ғи®ёе°Ҷйў„еҚ°жң¬жӣҙж–°дёәзЁҝ件жҺҘ收пјҲжңӘжҺ’зүҲпјүзүҲжң¬пјҢ并жӯЈзЎ®еј•з”ЁжңҹеҲҠеҸ‘иЎЁдҝЎжҒҜгҖӮиҜ·жҹҘйҳ…еҮәзүҲе•Ҷйў„еҚ°жң¬ж”ҝзӯ–иҺ·еҸ–жҢҮеҜјгҖӮжң¬жҢҮеҚ—ж‘ҳиҰҒеә•йғЁж ҮжіЁдәҶејҖж”ҫиҺ·еҸ–йў„еҚ°жң¬й“ҫжҺҘпјҢиӢҘжң¬жҢҮеҚ—жңӘд»ҘејҖж”ҫиҺ·еҸ–еҪўејҸеҸ‘иЎЁпјҢж„ҹе…ҙи¶Јзҡ„иҜ»иҖ…еҸҜйҖҡиҝҮ PubMed ж‘ҳиҰҒжҹҘзңӢејҖж”ҫиҺ·еҸ–е…Ёж–ҮпјҲйў„еҚ°жң¬пјүзҡ„иҺ·еҸ–йҖ”еҫ„гҖӮ
еӘ’дҪ“дј ж’ӯ
з ”з©¶иҖ…зҶҹжӮүйҖҡиҝҮ Twitter зӯүзӨҫдәӨеӘ’дҪ“е№іеҸ°еҲҶдә«жңҖж–°з§‘з ”жҲҗжһңгҖӮзӨҫдәӨеӘ’дҪ“еҸ‘её–ж—¶пјҢйў„з•ҷз©әй—ҙж ҮжіЁпјҲ1пјүDOI дёҺпјҲ2пјүеӣҫзүҮпјҢиҝҷдёӨдёӘз®ҖеҚ•жӯҘйӘӨеҸҜжҸҗеҚҮеё–еӯҗеңЁ Altmetric зӯүе…іжіЁеәҰжҢҮж ҮиҒҡеҗҲе№іеҸ°зҡ„жӣқе…үзҺҮпјҢеҗёеј•еҸҜиғҪеҲ’иө°зҡ„иҜ»иҖ…гҖӮеҗ„з ”з©¶йўҶеҹҹдёӯпјҢAltmetric иҜ„еҲҶдёҺж–Үз« еј•з”ЁйҮҸгҖҒжңҹеҲҠеҪұе“Қеӣ еӯҗгҖҒж–°й—»зЁҝгҖҒејҖж”ҫиҺ·еҸ–зҠ¶жҖҒзӣёе…ігҖӮ
жҳҜеҗҰиҖғиҷ‘иҝҮе…¶д»–еӘ’дҪ“еҪўејҸпјҹжӢҘжҠұж•°еӯ—еӘ’дҪ“з”ҹжҖҒзҡ„з ”з©¶иҖ…пјҢеҸҜдёҺдё“дёҡдҝЎжҒҜеӣҫиЎЁи®ҫи®ЎеёҲеҗҲдҪңпјҢжҲ–дҪҝз”Ёе…Қиҙ№пјҲжҲ–е…Қиҙ№еўһеҖјпјүзҪ‘з«ҷиҮӘдё»и®ҫи®ЎгҖӮиҖғиҷ‘дёә The Conversation зӯүжқғеЁҒе№іеҸ°ж’°зЁҝ вҖ”вҖ” иҜҘж–°й—»жңәжһ„иҮҙеҠӣдәҺд»Ҙ вҖңеӯҰжңҜдёҘи°ЁжҖ§ + ж–°й—»дё“дёҡжҖ§вҖқ еҗ‘е…¬дј—дј йҖ’еӯҰжңҜз•ҢдёҺз§‘з ”з•Ңзҡ„дҝЎжҒҜгҖӮгҖҠиӢұеӣҪиҝҗеҠЁеҢ»еӯҰжқӮеҝ—гҖӢгҖҠйӘЁз§‘дёҺиҝҗеҠЁзү©зҗҶжІ»з–—жқӮеҝ—гҖӢзӯүиҝҗеҠЁеҢ»еӯҰдёҺиҝҗеҠЁзү©зҗҶжІ»з–—жңҹеҲҠпјҢи®ҫжңүйқўеҗ‘дёҙеәҠеҢ»з”ҹгҖҒжӮЈиҖ…гҖҒиҝҗеҠЁе‘ҳгҖҒж•ҷз»ғзӯүйқһеӯҰжңҜиҜ»иҖ…зҡ„еҚҡе®ўгҖӮ
еҸҜиҒ”зі»жүҖеңЁеӯҰжңҜжңәжһ„зҡ„еӘ’дҪ“дёҺдј ж’ӯйғЁй—ЁжҲ–ж–°й—»еҠһе…¬е®ӨпјҢе·ҘдҪңдәәе‘ҳйҖҡеёёж„ҝж„ҸеҚҸеҠ©ж’°еҶҷж–°й—»зЁҝгҖҒеҲҶеҸ‘иҮідё»жөҒеӘ’дҪ“жңҚеҠЎе№іеҸ°гҖҒеҜ№жҺҘеӘ’дҪ“иө„жәҗгҖӮеӘ’дҪ“дёҺдј ж’ӯйғЁй—Ёд№ҹдјҡжҸҗдҫӣжҸҗеҚҮз§‘з ”еӘ’дҪ“жӣқе…үеәҰзҡ„е®һз”ЁжҠҖе·§гҖӮ
иҜ•йӘҢжҠҘе‘ҠеҸ‘иЎЁеҗҺ
иҜ•йӘҢжҠҘе‘ҠеҸ‘иЎЁеҗҺпјҢе»әи®®е…іжіЁд»ҘдёӢеҶ…е®№пјҡпјҲ1пјүиҜ•йӘҢжіЁеҶҢеә“дёӯзҡ„ вҖңиҜ•йӘҢзҠ¶жҖҒвҖқ жҳҜеҗҰжӣҙж–°пјҹпјҲ2пјүжҳҜеҗҰйңҖиҰҒеңЁиҜ•йӘҢжіЁеҶҢеә“дёӯж·»еҠ е·ІеҸ‘иЎЁиҜ•йӘҢжҠҘе‘Ҡй“ҫжҺҘе’Ң / жҲ–е…ұдә«зҡ„еҺҹе§Ӣж•°жҚ®й“ҫжҺҘпјҹпјҲ3пјүжҳҜеҗҰйңҖиҰҒеҗ‘иө„еҠ©жңәжһ„жҠҘе‘Ҡе·Іе®ҢжҲҗзҡ„йҮҢзЁӢзў‘пјҲеҸ‘иЎЁжҲҗжһңпјүпјҹпјҲ4пјүжҳҜеҗҰжңүиҜ•йӘҢз»“жһңзҡ„е…¶д»–дј ж’ӯи®ЎеҲ’пјҹпјҲ5пјүжҳҜеҗҰжңүз¬ҰеҗҲеӣҪ家жҢҮеҚ—зҡ„йҮҚиҰҒиҜ•йӘҢж–Ү件дёҺж•°жҚ®еӯҳеӮЁеҪ’жЎЈи®ЎеҲ’пјҹ
жҖ»з»“
жҲ‘们еёҢжңӣ REPORT жҢҮеҚ—иғҪдёәдёҙеәҠиҜ•йӘҢжҠҘе‘Ҡж’°еҶҷжҸҗдҫӣе®һз”Ёеё®еҠ©пјҢдҪңдёә CONSORT зӯү вҖңйҰ–йҖүвҖқ иҜ•йӘҢжҠҘе‘Ҡе·Ҙе…·зҡ„дјҳиҙЁиЎҘе……гҖӮжң¬жҢҮеҚ—ж•ҙеҗҲдәҶжҠҘе‘Ҡзӣёе…ізҡ„йҡҗжҖ§зҹҘиҜҶпјҢж ҮжіЁдәҶжҲ‘们жӣҫйҒҮеҲ°зҡ„й—®йўҳгҖӮеҢ»з–—еҶізӯ–зҡ„иҙЁйҮҸдҫқиө–дәҺжІ»з–—ж•Ҳжһңзҡ„еҸҜйқ иҜҒжҚ®гҖӮ规иҢғзҡ„з ”з©¶жҠҘе‘Ҡж— жі•и§ЈеҶіз ”究方法еӯҰзјәйҷ·еҜјиҮҙзҡ„й—®йўҳпјҢдҪҶеҸҜеё®еҠ©иҜ»иҖ…иҜҶеҲ«зјәйҷ·гҖҒиҜ„дј°з ”з©¶иҙЁйҮҸгҖӮжІЎжңүе®ҢзҫҺзҡ„з ”з©¶пјҢжҲ‘们д№ҹдёҚе®Јз§°иғҪ 100% ејҖеұ•е№¶жҠҘе‘Ҡж— зјәйҷ·зҡ„з ”з©¶гҖӮжҲ‘们呼еҗҒжүҖжңүз ”з©¶иҖ…иҮҙеҠӣдәҺејҖеұ•пјҲ并жҠҘе‘Ҡпјүжё…жҷ°гҖҒйҖҸжҳҺзҡ„з ”з©¶гҖӮ
е·ІзҹҘдҝЎжҒҜ
вҶ’ дёҙеәҠиҜ•йӘҢз ”з©¶зҡ„жҠҘе‘ҠиҙЁйҮҸеҸӮе·®дёҚйҪҗпјҢжҷ®йҒҚиҫғе·®гҖӮ
ж–°еҸ‘зҺ°
вҶ’ REPORT иҜ•йӘҢжҢҮеҚ—жҳҜдёҖз«ҷејҸ вҖңе®һж“ҚеһӢвҖқ е®һж–ҪжҢҮеҚ—дёҺзӣ®еҪ•пјҢж•ҙеҗҲдәҶйҡҗжҖ§зҹҘиҜҶеҸҠй«ҳж•ҲгҖҒйҖҸжҳҺж’°еҶҷиҜ•йӘҢжҠҘе‘Ҡзҡ„йҰ–йҖүдҝЎжҒҜжқҘжәҗпјҲеҰӮ CONSORTпјүгҖӮ
еҺҹж–ҮдёӢиҪҪзҪ‘еқҖпјҡhttp://bjsm.bmj.com/content/56/12/683.full.pdf



