GUIDE
зј–иҖ…жҢү
гҖҖгҖҖжӯҰжұүеӨ§еӯҰдёӯеҚ—еҢ»йҷўеӨҡеӯҰ科иҜҠз–—еӣўйҳҹеҲҶдә«1дҫӢзӣҙиӮ ж·ұйғЁжөёж¶ҰеһӢеӯҗе®«еҶ…иҶңејӮдҪҚз—ҮпјҲDIEпјүжӮЈиҖ…зҡ„е®Ңж•ҙиҜҠз–—еҺҶзЁӢпјҢзӘҒеҮәдәҶд»Ҙз»“зӣҙиӮ иӮӣй—ЁеӨ–科дёәдё»еҜјгҖҒиҒ”еҗҲеҰҮ科дёҺжіҢе°ҝеӨ–科зҡ„еӨҡеӯҰ科иҜҠз–—пјҲMDTпјүеҚҸдҪңжЁЎејҸпјҢдёҚд»…е®һиҜҒдәҶEUS-FNAдҪңдёәDIEж—©жңҹиҜҠж–ӯе…ій”®е·Ҙе…·зҡ„д»·еҖјпјҢејҘиЎҘдәҶдј з»ҹеҪұеғҸдёҺжҙ»жЈҖзҡ„еұҖйҷҗжҖ§пјҢжӣҙйҖҡиҝҮMDTе®һи·өеҪ°жҳҫдәҶеӨҡеӯҰ科ж•ҙеҗҲеңЁжҸҗеҚҮжүӢжңҜж №жІ»жҖ§гҖҒдјҳеҢ–жӮЈиҖ…йў„еҗҺж–№йқўзҡ„зӨәиҢғдҪңз”ЁпјҢдёәеӨҚжқӮзӣҶи…”з–ҫз—…дёӘдҪ“еҢ–иҜҠз–—жҸҗдҫӣдәҶеүҚжІҝиҢғејҸпјҢзҙ§еҜҶеҘ‘еҗҲзІҫеҮҶеҢ»з–—дёҺи·ЁеӯҰ科еҚҸдҪңзҡ„еҪ“д»Ји¶ӢеҠҝгҖӮ


йҖҡдҝЎдҪңиҖ…пјҡжұҹд»ҺеәҶВ ж•ҷжҺҲ
пјҲжӯҰжұүеӨ§еӯҰдёӯеҚ—еҢ»йҷў з»“зӣҙиӮ иӮӣй—ЁеӨ–科пјү

дҪңиҖ…пјҡйҷҲж–ҮиұӘ

дҪңиҖ…пјҡжӣҫжө·еҲҡ
зӣҙиӮ еӯҗе®«еҶ…иҶңејӮдҪҚз—ҮеӨҡеӯҰ科иҜҠжІ»1дҫӢжҠҘе‘Ҡ并ж–ҮзҢ®еӨҚд№
йҷҲж–ҮиұӘ1пјҢжӣҫжө·еҲҡ2пјҢйғқз«Ӣж”ҝ3пјҢзҺӢз»Ҷж–Ү4пјҢиӮ–еҶӣ5пјҢжұҹд»ҺеәҶ1
[жӯҰжұүеӨ§еӯҰдёӯеҚ—еҢ»йҷў 1. з»“зӣҙиӮ иӮӣй—ЁеӨ–科пјҲжӯҰжұүеёӮдҫҝз§ҳзӣҶеә•з–ҫз—…дёҙеәҠеҢ»еӯҰз ”з©¶дёӯеҝғпјү 4. еҰҮ科 5. ж¶ҲеҢ–еҶ…科пјҢж№–еҢ— жӯҰжұү 430071пјӣ2. ж№–еҢ—зңҒиҖҒжІіеҸЈеёӮ第дёҖеҢ»йҷў жҷ®йҖҡеӨ–科пјҢж№–еҢ— иҘ„йҳі 441800пјӣ3. ж№–еҢ—зңҒжҪңжұҹеёӮдёӯеҝғеҢ»йҷў жҷ®йҖҡеӨ–科пјҢж№–еҢ— жҪңжұҹ 433100]
е…ій”®иҜҚгҖҖеӯҗе®«еҶ…иҶңејӮдҪҚз—ҮпјӣзӣҙиӮ пјӣеҶ…й•ңи¶…еЈ°еј•еҜјз»Ҷй’Ҳз©ҝеҲәпјӣзӣҙиӮ еҲҮйҷӨжңҜ
дёӯеӣҫеҲҶзұ»еҸ·пјҡR657.1
KeyВ wordsгҖҖВ Endometriosis; Rectum; Endoscopic Ultrasound-Guided Fine Needle Aspiration; Proctectomy
CLCВ number:В R657.1
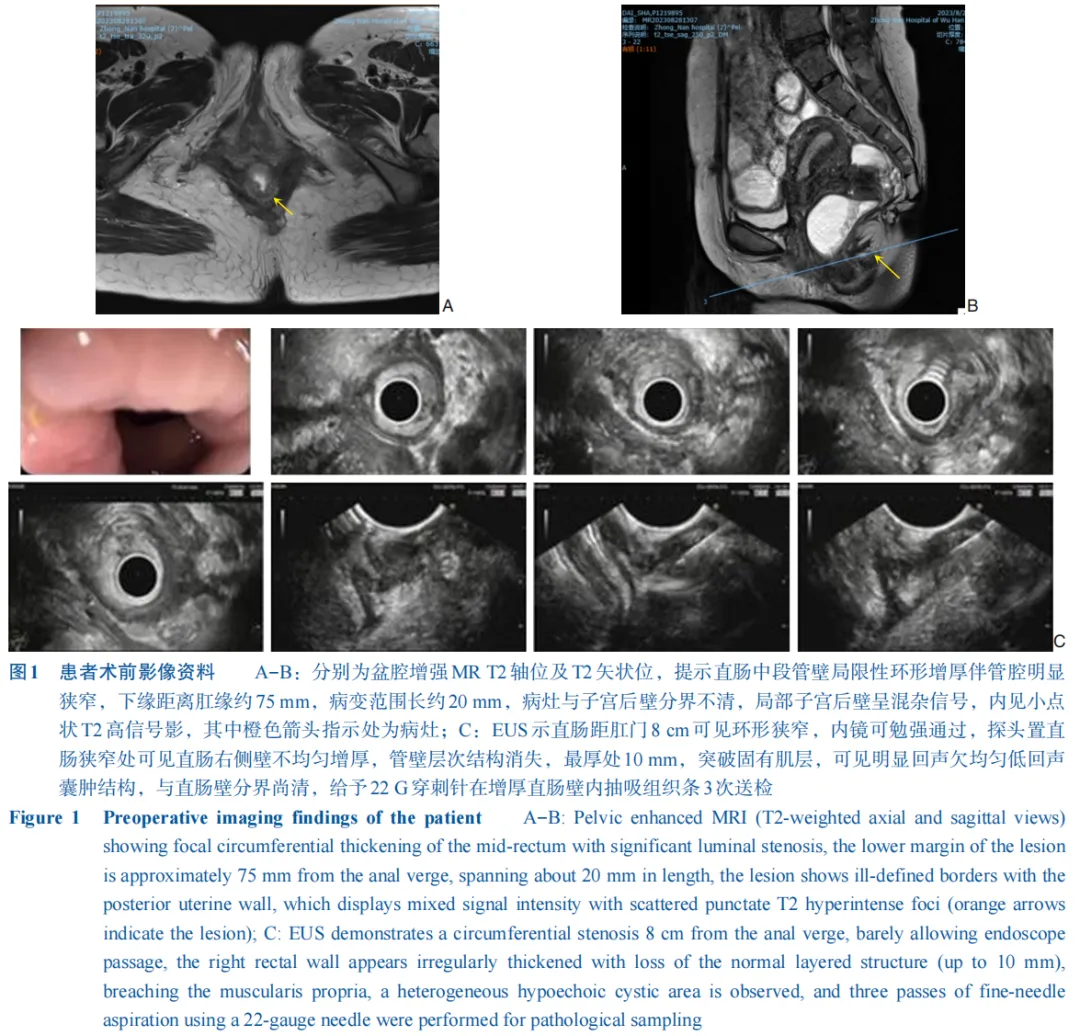
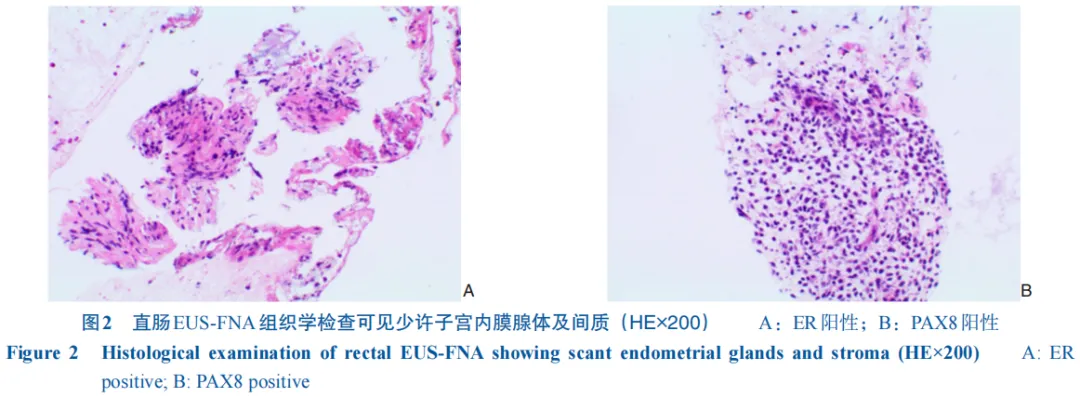
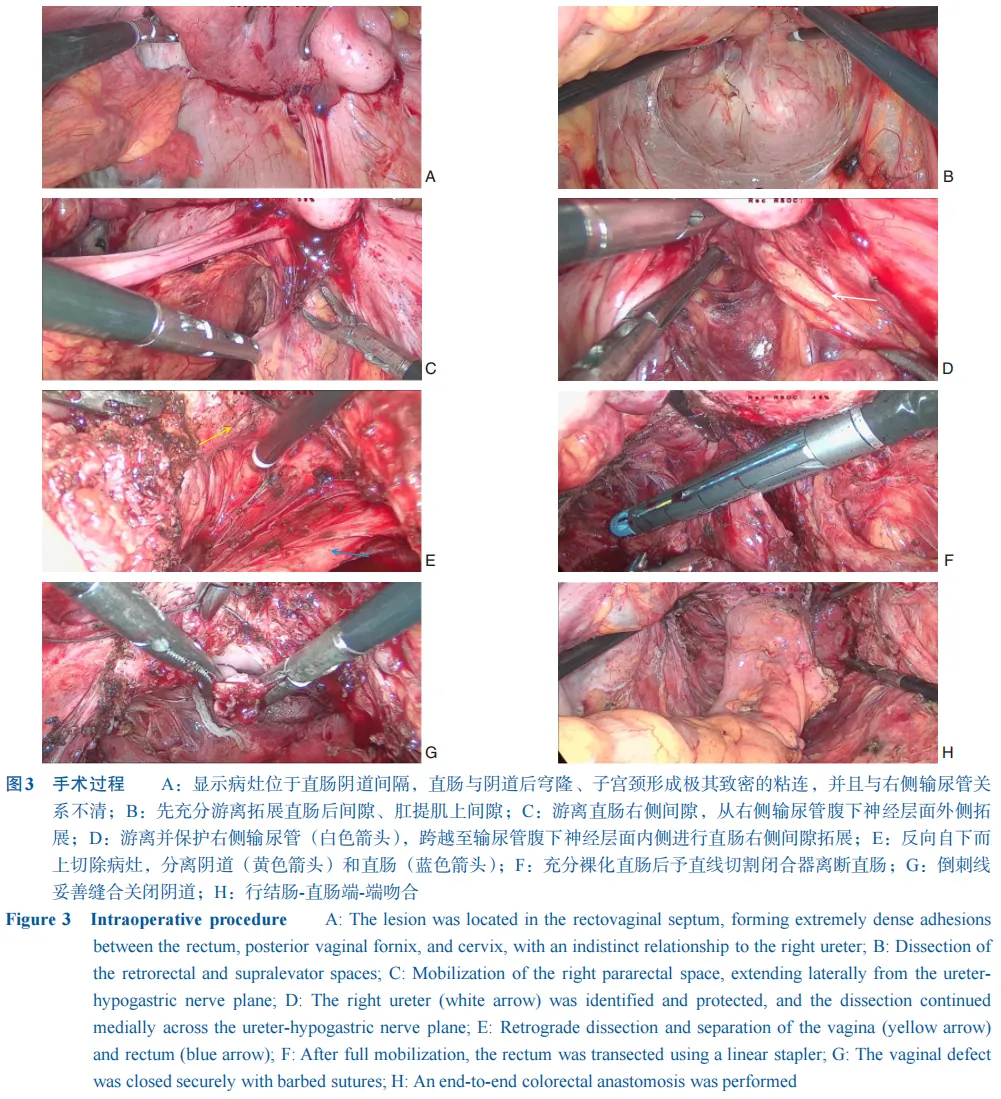
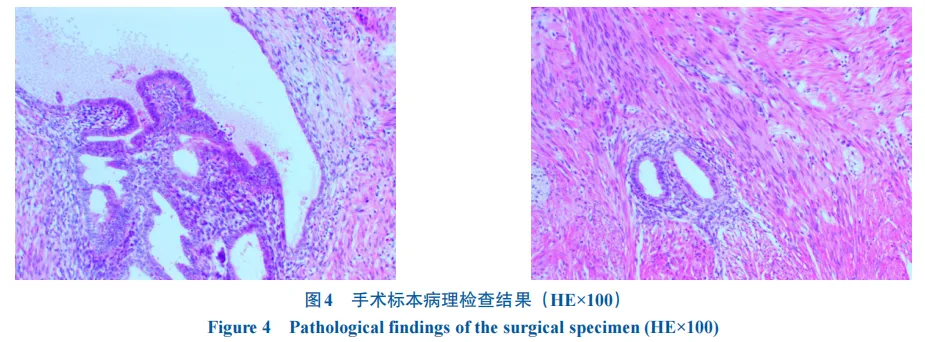
еӯҗе®«еҶ…иҶңејӮдҪҚз—ҮеҚіеӯҗе®«еҶ…иҶңзҡ„и…әдҪ“е’Ңй—ҙиҙЁеҮәзҺ°еңЁеӯҗе®«и…”д»ҘеӨ–зҡ„йғЁдҪҚпјҢеҸҜиғҪзҙҜеҸҠеӨҡеҷЁе®ҳзҡ„дёҖз§Қеёёи§ҒеҰҮ科иүҜжҖ§з–ҫз—…гҖӮзӣ®еүҚи®Өдёәеӯҗе®«еҶ…иҶңејӮдҪҚз—Үзҡ„з—…еӣ дёҚжҳҺпјҢеҸҜиғҪдёҺеӯҗе®«еҶ…иҶңж’ӯж•ЈгҖҒиЎҖз®Ўж–°з”ҹгҖҒдёҠзҡ®й—ҙиҙЁиҪ¬еҢ–гҖҒеӯ•жҝҖзҙ жҠөжҠ—гҖҒзӮҺз—ҮзӯүеӨҡз§Қеӣ зҙ еҜҶеҲҮзӣёе…ігҖӮж·ұйғЁжөёж¶ҰеһӢеӯҗе®«еҶ…иҶңејӮдҪҚз—ҮпјҲdeep infiltrating endometriosisпјҢDIEпјүжҳҜжҢҮеӯҗе®«еҶ…иҶңејӮдҪҚз—Үз—…зҒ¶жөёж¶Ұи…№иҶңдёӢзҡ„ж·ұеәҰвүҘ5 mmпјҢеҢ…жӢ¬дҪҚдәҺе®«йӘ¶йҹ§еёҰгҖҒйҳҙйҒ“зӣҙиӮ йҡ”гҖҒйҳҙйҒ“з©№йҡҶгҖҒзӣҙиӮ жҲ–иҖ…з»“иӮ еЈҒзӯүдҪҚзҪ®зҡ„з—…зҒ¶гҖӮеӯҗе®«еҶ…иҶңејӮдҪҚз—ҮжӮЈиҖ…зҙҜеҸҠз»“зӣҙиӮ зҡ„еҸ‘з”ҹзҺҮзәҰдёә8%~12%[1]пјҢе…¶дёҙеәҠиЎЁзҺ°зјәд№Ҹзү№ејӮжҖ§пјҢд»Ҙи…№з—ӣгҖҒи…№жі»гҖҒдҫҝиЎҖгҖҒжҺ’дҫҝеӣ°йҡҫзӯүж¶ҲеҢ–йҒ“з—ҮзҠ¶дёәдё»пјҲйғЁеҲҶжӮЈиҖ…зҡ„з—ҮзҠ¶еҸҜиғҪе’ҢжңҲз»Ҹе‘Ёжңҹзӣёе…іпјүгҖӮжӯӨеӨ–пјҢеӯҗе®«еҶ…иҶңејӮдҪҚз»„з»Үе…·жңүдёҖе®ҡзҡ„жөёж¶ҰжҖ§пјҢеҸҜйҖҡиҝҮеҸҚеӨҚзӮҺз—ҮгҖҒзәӨз»ҙеўһз”ҹеҜјиҮҙиӮ й»ҸиҶңзіңзғӮгҖҒжәғз–ЎгҖҒеҮәиЎҖгҖҒеҪўжҲҗиӮҝеқ—пјҢеӣ жӯӨдёҺзӮҺз—ҮжҖ§иӮ з—…гҖҒиӮ зҷҢзӯүйүҙеҲ«еӣ°йҡҫпјҢз»ҸйӘҢдёҚи¶ізҡ„ж¶ҲеҢ–еҶ…科гҖҒиғғиӮ еӨ–科еҢ»еёҲеҫҖеҫҖдјҡеҸ‘з”ҹиҜҜиҜҠжҲ–延иҝҹиҜҠж–ӯгҖӮжң¬дҫӢжӮЈиҖ…зҡ„жңҜеүҚиҜҠж–ӯгҖҒжүӢжңҜжҖқи·ҜжңүдёҖе®ҡж–°йў–жҖ§пјҢзү№дёҺеҗҢиЎҢеҲҶдә«гҖӮ
пјҲеңЁжЎҶеҶ…еҗ‘дёҠж»‘еҠЁжүӢжҢҮеҚіеҸҜжөҸи§Ҳе…ЁйғЁеҸӮиҖғж–ҮзҢ®пјү
[2]Parasar P, Ozcan P, Terry KL. Endometriosis:epidemiology, diagnosis and clinical management[J]. Curr Obstet Gynecol Rep, 2017, 6(1):34-41. doi:10.1007/s13669-017-0187-1.
[3]Meuleman C, Tomassetti C, D'Hoore A, et al. Surgical treatment of deeply infiltrating endometriosis with colorectal involvement[J]. Hum Reprod Update, 2011, 17(3):311-326. doi:10.1093/humupd/dmq057.
[4]Turocy JM, Benacerraf BR. Transvaginal sonography in the diagnosis of deep infiltrating endometriosis:a review[J]. J Clin Ultrasound, 2017, 45(6):313-318. doi:10.1002/jcu.22483.
[5]Bazot M, Malzy P, Cortez A, et al. Accuracy of transvaginal sonography and rectal endoscopic sonography in the diagnosis of deep infiltrating endometriosis[J]. Ultrasound Obstet Gynecol, 2007, 30(7):994-1001. doi:10.1002/uog.4070.
[6]ossini LG, Ribeiro PA, Rodrigues FC, et al. Transrectal ultrasound - Techniques and outcomes in the management of intestinal endometriosis[J]. Endosc Ultrasound, 2012, 1(1):23-35. doi:10.7178/eus.01.005.
[7]Noventa M, Saccardi C, Litta P, et al. Ultrasound techniques in the diagnosis of deep pelvic endometriosis:algorithm based on a systematic review and meta-analysis[J]. Fertil Steril, 2015, 104(2):366-383. doi:10.1016/j.fertnstert.2015.05.002.
[8]Bazot M, Detchev R, Cortez A, et al. Transvaginal sonography and rectal endoscopic sonography for the assessment of pelvic endometriosis:a preliminary comparison[J]. Hum Reprod, 2003, 18(8):1686-1692. doi:10.1093/humrep/deg314.
[9]Delpy R, Barthet M, Gasmi M, et al. Value of endorectal ultrasonography for diagnosing rectovaginal septal endometriosis infiltrating the rectum[J]. Endoscopy, 2005, 37(4):357-361. doi:10.1055/s-2005-861115.
[10]Desplats V, Vitte RL, du Cheyron J, et al. Preoperative rectosigmoid endoscopic ultrasonography predicts the need for bowel resection in endometriosis[J]. World J Gastroenterol, 2019, 25(6):696-706. doi:10.3748/wjg.v25.i6.696.
[11]Dunselman GJ, Vermeulen N, Becker C, et al. ESHRE guideline:management of women with endometriosis[J]. Hum Reprod, 2014, 29(3):400-412. doi:10.1093/humrep/det457.
[12]HernГЎndez GutiГ©rrez A, Spagnolo E, Hidalgo P, et al. Magnetic resonance imaging versus transvaginal ultrasound for complete survey of the pelvic compartments among patients with deep infiltrating endometriosis[J]. Int J Gynaecol Obstet, 2019, 146(3):380-385. doi:10.1002/ijgo.12894.
[13]Milone M, Mollo A, Musella M, et al. Role of colonoscopy in the diagnostic work-up of bowel endometriosis[J]. World J Gastroenterol, 2015, 21(16):4997-5001. doi:10.3748/wjg.v21.i16.4997.
[14]Keckstein J, Saridogan E, Ulrich UA, et al. The #Enzian classification:a comprehensive non-invasive and surgical description system for endometriosis[J]. Acta Obstet Gynecol Scand, 2021, 100(7):1165-1175. doi:10.1111/aogs.14099.
[15]Carvalho AC, Cardoso R, Pires F, et al. Diagnosis of bowel endometriosis using endoscopic ultrasound-guided fine needle aspiration[J]. Korean J Gastroenterol, 2023, 81(1):46-51. doi:10.4166/kjg.2022.104.
[16]Maleki Z, Erozan Y, Geddes S, et al. Endorectal ultrasound-guided fine-needle aspiration:a useful diagnostic tool for perirectal and intraluminal lesions[J]. Acta Cytol, 2013, 57(1):9-18. doi:10.1159/000342919.
[17]Miwa TK, Iwashita T, Aiba M, et al. Endoscopic ultrasound-guided fine needle aspiration for the diagnosis of bowel endometriosis:a case report[J]. Med Ultrason, 2020, 22(2):243-246. doi:10.11152/mu-2000.
[18]Cai W, Cheng G, Tao F, et al. Transrectal endoscopic ultrasound-guided fine-needle aspiration biopsy for qualitative diagnosis of pelvic space-occupying lesions:a diagnostic test[J]. Transl Cancer Res, 2022, 11(9):3267-3276. doi:10.21037/tcr-22-2057.
[19]Donnez O, Roman H. Choosing the right surgical technique for deep endometriosis:shaving, disc excision, or bowel resection?[J]. Fertil Steril, 2017, 108(6):931-942. doi:10.1016/j.fertnstert.2017.09.006.
[20]Balla A, Quaresima S, Subiela JD, et al. Outcomes after rectosigmoid resection for endometriosis:a systematic literature review[J]. Int J Colorectal Dis, 2018, 33(7):835-847. doi:10.1007/s00384-018-3082-y.
[21]Mereu L, Ruffo G, Landi S, et al. Laparoscopic treatment of deep endometriosis with segmental colorectal resection:short-term morbidity[J]. J Minim Invasive Gynecol, 2007, 14(4):463-469. doi:10.1016/j.jmig.2007.02.008.
[22]Ceccaroni M, Ceccarello M, Raimondo I, et al. вҖңA space odysseyвҖқ on laparoscopic segmental rectosigmoid resection for deep endometriosis:a seventeen-year retrospective analysis of outcomes and postoperative complications among 3050 patients treated in a referral center[J]. J Minim Invasive Gynecol, 2023, 30(8):652-664. doi:10.1016/j.jmig.2023.04.005.
[23]Ballester M, Roman H. Surgical management of deep endometriosis with colorectal involvement:CNGOF-HAS Endometriosis Guidelines[J]. Gynecol Obstet Fertil Senol, 2018, 46(3):290-295. doi:10.1016/j.gofs.2018.02.003.
[24]Ruffo G, Scopelliti F, Scioscia M, et al. Laparoscopic colorectal resection for deep infiltrating endometriosis:analysis of 436 cases[J]. Surg Endosc, 2010, 24(1):63-67. doi:10.1007/s00464-009-0517-0.
[25]Ferrero S, Camerini G, Leone Roberti Maggiore U, et al. Bowel endometriosis:Recent insights and unsolved problems[J]. World J Gastrointest Surg, 2011, 3(3):31-38. doi:10.4240/wjgs.v3.i3.31.
[26]Vercellini P, Carmignani L, Rubino T, et al. Surgery for deep endometriosis:a pathogenesis-oriented approach[J]. Gynecol Obstet Invest, 2009, 68(2):88-103. doi:10.1159/000219946.
[27]Carbone MG, Campo G, Papaleo E, et al. The importance of a multi-disciplinary approach to the endometriotic patients:the relationship between endometriosis and psychic vulnerability[J]. J Clin Med, 2021, 10(8):1616. doi:10.3390/jcm10081616.
[28]Fang QY, Campbell N, Mooney SS, et al. Evidence for the role of multidisciplinary team care in people with pelvic pain and endometriosis:a systematic review[J]. Aust N Z J Obstet Gynaecol, 2024, 64(3):181-192. doi:10.1111/ajo.13755.
[29]Karavadra B, Mawson R, Dixon S, et al. Building bridges:enhancing diagnosis and care for endometriosis across the primary-secondary care continuum[J]. Women's Reprod Health, 2025:1-9. doi:10.1080/23293691.2025.2540344.
пјҲжң¬ж–Үзј–иҫ‘гҖҖе®Ӣж¶ӣпјү
жң¬ж–Үеј•з”Ёж јејҸпјҡйҷҲж–ҮиұӘ, жӣҫжө·еҲҡ, йғқз«Ӣж”ҝ, зӯү. зӣҙиӮ еӯҗе®«еҶ…иҶңејӮдҪҚз—ҮеӨҡеӯҰ科иҜҠжІ»1дҫӢжҠҘе‘Ҡ并ж–ҮзҢ®еӨҚд№ [J]. дёӯеӣҪжҷ®йҖҡеӨ–科жқӮеҝ—, 2025, 34(10):2205-2211. doiпјҡ10.7659/j.issn.1005-6947.240427
Cite this article as:В Chen WH, Zeng HG, Hao LZ, et al. Multidisciplinary management of rectal endometriosis: a case report and literature review[J]. Chin J Gen Surg, 2025, 34(10):2205-2211. doiпјҡ10.7659/j.issn.1005-6947.240427
еҲқе®ЎВ зҶҠгҖҖжқЁ
еӨҚе®ЎВ е®ӢгҖҖж¶ӣ
з»Ҳе®Ўе§ңгҖҖжҷ–
зүҲжқғеЈ°жҳҺ



