
点击关注,一起做更好的产品
真实世界证据(Real-World Evidence, RWE)在2025-2026年迎来爆发式增长。根据多家权威机构最新数据,全球RWE解决方案市场规模在2025年达到30.3-47.4亿美元区间,预计2030-2035年将突破60-108亿美元,年复合增长率(CAGR)维持在8.4%-14.8%的高位。这一增长并非单一因素驱动,而是监管政策突破、AI技术深度融合、数据基础设施成熟、产业需求升级的四重共振结果。本文基于2025-2026年第一季度最新政策法规、权威市场数据及招聘市场实证,系统解析RWE爆火的核心逻辑。
一、监管政策层面:2025年迎来历史性突破
1、美国FDA:里程碑式政策松绑
2025年12月18日,FDA发布《使用真实世界证据支持医疗器械监管决策》最终版指南,这是自2017年以来的最重大更新,标志着RWE监管框架的质变:
核心突破:
取消个体患者数据强制提交要求:既往FDA要求RWE提交必须包含"个体患者层面的私人保密信息",导致大规模宏观数据库难以应用。2025年新规明确接受去标识化数据库,包括国家癌症登记处(SEER)、医院系统数据库、保险理赔数据库等
"适用性与可靠性"双支柱评估体系:建立结构化评估框架,涵盖数据可及性、时效性、人群代表性、数据溯源、质量保证等维度
引入因果图(Causal Diagrams)方法学:要求使用有向无环图(DAGs)识别混杂因素,提升研究设计的严谨性
政策影响量化:
2016-2025年间,仅35个药品/生物制品/疫苗申请包含RWE,而同期医疗器械领域有超过250项上市前授权使用RWE
FDA预计新规将使RWE在药品申请中的使用率提升3-5倍,显著加速肿瘤、罕见病等领域的审批进程
FDA局长Marty Makary明确表示:"我们正在消除不必要的障碍,释放强大的真实世界证据潜力,让患者更快获得改变生命的治疗"。
2、欧盟EMA:DARWIN EU网络全面运营
2025年中期报告显示,EMA的DARWIN EU网络实现关键里程碑:
| 30家 | |||
| 1.8亿人 | |||
| 显著扩容 |
2025年关键进展:
《临床试试验法规》(CTR)全面适用:2025年1月结束过渡期,超过5,000项临床试验迁移至临床试验信息系统(CTIS)
EMA-HMA联合AI工作计划发布:"2028年药品监管数据与AI"路线图,明确将RWE与AI整合为监管决策核心工具
欧洲短缺监测平台(ESMP)全面运行:2025年2月强制要求上市许可持有人使用,RWE在药物警戒中的应用成为法定要求
3、中国NMPA:从试点到制度化
2025年政策体系正式落地:
关键政策节点:
2025年上半年:NMPA正式扩大真实世界数据(RWD)应用范围,RWE支持药物上市和适应症扩展的应用指南正式落地
数据标准化强制要求:2024年7月起,RWD收集必须符合ISO 20691标准,不合规提交面临6个月审评延迟处罚
区块链溯源:2025年起,所有RWD必须实现区块链审计,单项目合规成本增加20-50万美元,但数据可信度显著提升
量化成效:
2024年:42%的新药申请包含RWD组件(较2022年的18%翻倍)
适应症分布:肿瘤和罕见病占RWD提交的67%
审批时效:RWE支持申请平均审批周期从14个月缩短至9个月,提速35%
典型案例:百济神州PD-1抑制剂替雷利珠单抗(百泽安 ®),它是国内首个依托超 5 万例真实世界数据(RWD),提前 8 个月获批新适应症的 PD-1 抑制剂。
二、市场规模与增长:2025-2026年数据实证
1、全球市场:多源数据交叉验证
基于2025-2026年第一季度发布的权威报告,全球RWE市场呈现强劲增长:
| MarketsandMarkets | 47.4亿美元 | 14.8% | ||
| Precedence Research | 33.2亿美元 | 8.39% | ||
| Straits Research | 30.3亿美元 | 8.4% | ||
| Fortune Business Insights | 20.03亿美元 | 14.4% |
关键洞察:尽管各机构统计口径存在差异(服务 vs. 软件+数据),但所有权威报告均确认8%以上的双位数增长,且2026年预测值普遍较2024年上调15%-20%。
2、细分市场结构(2025年)
按产品类型:
数据解决方案:占比55%(约16.6亿美元),包括EHR、理赔、基因组学数据
服务:占比45%(约13.6亿美元),但增速更快(CAGR 14.2%)
按应用场景:
药物开发与上市授权:占比45%(主导细分市场)
上市后监测:增速最快(CAGR 15.5%)
市场准入与报销决策:占比提升至30%,成为HTA核心依据
按治疗领域:
肿瘤学:占比30%(最大单一领域),预计2030年达35.6亿美元(CAGR 17.6%)
心血管、神经学、罕见病:合计占比40%
3、区域格局演变
| 北美 | 40-43.5% | ||
| 欧洲 | 30% | ||
| 亚太 | 20% | 增速最快 | |
| 中国 |
CAGR:复合年增长率
三、AI技术融合:2025年RWE的智能化跃迁
1、AI在RWE中的应用现状(2025年)
根据Intuition Labs 2025年11月报告,75%的制药企业已在药物开发中使用RWD,超过半数积极整合AI技术:
核心技术应用矩阵:
| 机器学习(ML) | |||
| 自然语言处理(NLP) | |||
| 大语言模型(LLM) | |||
| 深度学习 | |||
| 联邦学习 |
2、生成式AI(GenAI)的突破性应用
2025年OHDSI全球研讨会主题明确聚焦"AI、机器学习与GenAI在OHDSI中的应用",显示社区核心关切:
具体应用场景:
研究设计自动化:LLM辅助生成研究方案、统计分析计划(SAP)
医学编码智能化:自动将自由文本诊断映射至标准术语(ICD-10, SNOMED)
证据摘要生成:自动提取多数据库研究结果,生成监管提交摘要
数据质量监控:AI驱动的异常检测与数据验证
技术挑战与监管回应:
FDA 2025年草案指南:发布《考虑使用人工智能支持药品和生物制品监管决策》,要求AI应用必须具备情境特定验证、透明度和伦理保障
欧盟AI法案:EMA发布反射文件,确保AI在产品全生命周期的可信度
3、OMOP-CDM与AI的协同进化
OHDSI 2025年度回顾显示,观测医疗结果合作(OMOP)通用数据模型已成为AI驱动的RWE基础设施:
2025年关键数据:
544个数据源、54个国家、9.74亿唯一患者记录(占全球人口12%)
OHDSI标准化术语库:1,180万概念、3,784,263标准概念、145个术语集
HADES生态系统:41个R包支持标准化分析,CRAN下载量>100万次
AI增强的分布式网络:
OHDSI Evidence Network:2025年正式启动,连接15国6大洲数据伙伴,支持联邦学习架构下的多中心研究
DARWIN EU深度整合:OMOP/OHDSI成为EMA和国家监管机构生成决策级证据的核心基础设施
四、人才市场:招聘数据实证分析
1、中国RWE岗位需求井喷(2025年)
基于猎聘网、高校人才网2025年公开数据,RWE领域呈现高薪、高需求、高技能门槛特征:
海南乐城真实世界研究院2025年招聘公告(典型样本):
| 药品真研岗(统计分析) | ||||
| 数据研究岗 | ||||
| 真研医保岗 | ||||
| 生物医学新技术岗 | ||||
| 学术编辑岗 |
企业端高薪岗位(猎聘网2025年数据):
| 真实世界研究经理 | ||||
| RWE真实世界研究资深项目经理 | ||||
| 真实世界研究行业专家 | ||||
| 真实世界研究员 | ||||
| 真实世界研究医学经理 | ||||
| RWE Intern |
技能要求升级趋势:
硬性技能:Python/R/SAS(必须)、SQL(数据库查询)、OMOP-CDM(数据模型)、机器学习(加分项)
软性能力:跨部门协作、监管沟通、医学写作、AI工具应用(LLMs提示工程)
学历门槛:硕士成为标配,博士优先(尤其学术机构),海外经验加分
2、全球人才短缺与薪酬趋势
虽然具体RWE领域统计稀缺,但参照可再生能源行业(同样为数据密集型高科技领域)2025年人才报告:
68%的雇主将人才短缺列为最大增长瓶颈
48%的从业者在2025年获得加薪,21%涨幅超5%
AI专家在电网优化和预测岗位年薪达六位数美元(美国、德国、澳大利亚),年薪比通用能源岗高20%–40%
RWE领域推断:
鉴于AI+RWE的交叉特性,具备医学+数据科学+AI复合背景的人才薪酬溢价显著
CRO和药企正通过14薪、股权激励、远程办公等方式争夺顶尖人才
五、产业需求侧:制药企业的战略重构
1、研发效率危机与RWE替代
传统RCT瓶颈:
平均成本:26亿美元/新药(Tufts Center数据)
患者招募困难:80%的临床试验未能按时招募
人群代表性不足:RCT排除标准导致结果外推性差
RWE解决方案:
外部对照臂:单臂试验+RWE对照,减少样本量需求
上市后承诺:利用现有RWD满足监管对长期安全性监测要求
标签扩展:基于真实世界数据扩大适应症(如辉瑞Ibrance男性乳腺癌案例)
2、市场准入与价值证明
HTA机构要求升级:
英国NICE、德国IQWiG: increasingly 要求RWE支持报销决策
Outcome-based pricing:基于真实世界结局的定价合同需要RWE基础设施
中国医保谈判:2025年更注重临床获益和药物经济学证据,DRG/DIP支付体系全面覆盖创新药
六、爆火的核心逻辑:四重共振模型
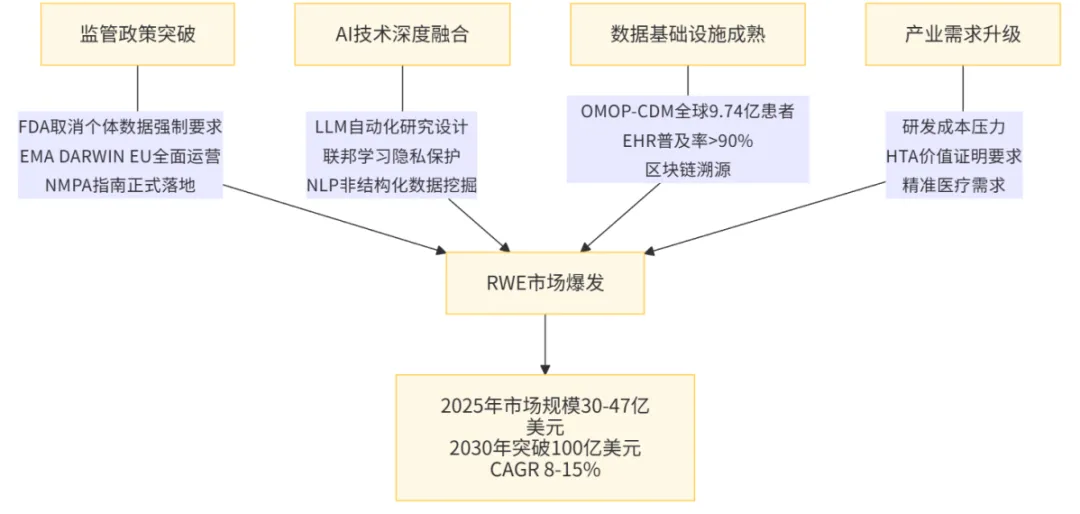
七、未来展望:2026-2030年趋势预判
1、监管科学前沿
FDA:预计2026年发布药品RWE指南更新,与医疗器械指南保持一致
EMA:DARWIN EU目标2025年开展140项研究,2026年扩容至全欧洲覆盖
中国:乐城试点经验全国推广,预计2026年50%新药申请包含RWD
2、技术融合趋势
AI Agent自主研究:从研究设计到报告生成的全流程自动化
多模态RWE:整合EHR+基因组+影像+可穿戴数据的AI分析平台
实时证据生成:基于流数据的动态安全性监测(如FDA Sentinel系统升级)
3、市场格局演变
云原生RWE平台:AWS/Azure/GCP托管的RWEaaS(证据即服务)模式普及
垂直领域深化:肿瘤RWE市场2030年达35.6亿美元,罕见病、细胞治疗成为新增长点
亚太地区崛起:中国、印度、东南亚成为CRO和数据中心建设热土
真实世界研究的爆火是政策、技术、市场、数据四重因素共振的必然结果。2025年FDA的历史性政策松绑、AI技术的深度融合、OMOP-CDM全球基础设施的成熟,以及制药企业对研发效率和准入证明的迫切需求,共同推动了这一市场的爆发式增长。
关键数据锚点:
2025年全球市场:30-47亿美元(保守/乐观估计)
2030年预测:突破100亿美元
AI渗透率:75%制药企业使用RWD,>50%整合AI
人才需求:硕士以上学历、Python/R+OMOP+AI复合技能成为标配
未来五年,RWE将从"补充证据"转变为监管决策的核心支柱,AI驱动的实时证据生成将重塑药物全生命周期管理。对于产业参与者而言,数据资产、AI能力、监管科学素养将成为核心竞争壁垒。
数据来源声明:本报告基于FDA、EMA、NMPA 2025年官方文件,MarketsandMarkets、Precedence Research、Straits Research、Fortune Business Insights等权威机构2025-2026年第一季度发布的市场报告,OHDSI 2025年度回顾,以及猎聘网、高校人才网公开招聘数据。
为什么是Meta?2025年权威期刊Meta分析论文详细解析
《生物医学新技术临床研究和临床转化应用管理条例》——监管护航下的创新与变革

实战 聚力 和合
合作共赢,打磨产品思维,传播产品理念,以成熟完善的产业链服务,助力企业与个人成长!基础研究-技术转化-产业应用闭环加速服务。科研课题设计,产品服务,技术服务,项目开发,行业咨询,产业对接 请加微信联系。



