зӮ№еҮ»и“қеӯ— е…іжіЁжҲ‘们 еёҰжӮЁдәҶи§ЈжӣҙеӨҡе№Із»ҶиғһзҹҘиҜҶ

е…ідәҺгҖҠ818еҸ·д»ӨгҖӢж ёеҝғжқЎж¬ҫзҡ„и§ЈиҜ»дёҺиЎҢдёҡеҪұе“ҚеҲҶжһҗ
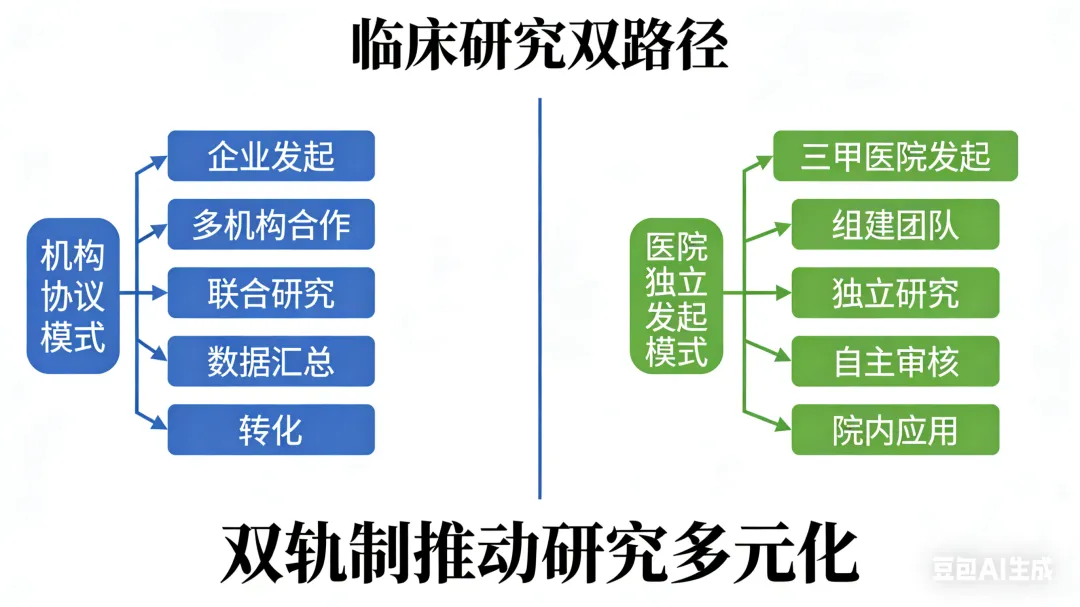
1. дёҙеәҠз ”з©¶е®һж–ҪжЁЎејҸзҡ„еҸҢиҪЁеҲ¶дёҺеёӮеңәйҖүжӢ©
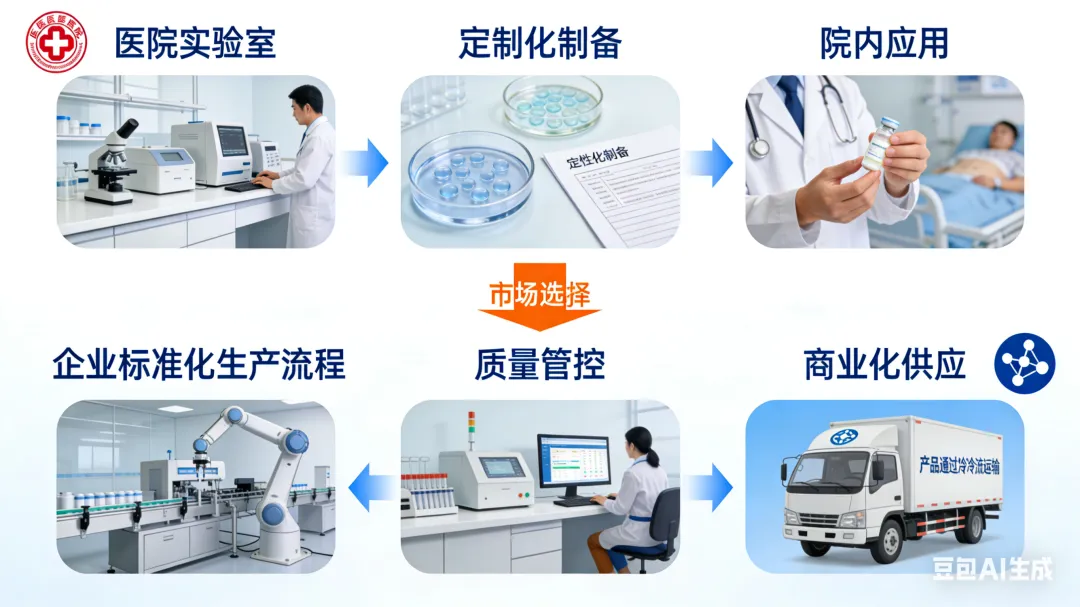
дҫқжҚ®иҜҘжі•д»Ө第еҚҒдәҢжқЎпјҢдёҙеәҠз ”з©¶еҸҜйҖҡиҝҮжңәжһ„й—ҙеҚҸи®®еҗҲдҪңејҖеұ•пјҢд№ҹе…Ғи®ёз¬ҰеҗҲиө„иҙЁзҡ„еҢ»з–—жңәжһ„зӢ¬з«ӢеҸ‘иө·гҖӮиҝҷйў„зӨәзқҖжңӘжқҘеҢ»з–—жңәжһ„еңЁз”ҹзү©еҢ»еӯҰж–°жҠҖжңҜеә”з”Ёдёӯе°ҶжӢҘжңүжӣҙеӨ§иҮӘдё»жқғгҖӮд»Ҙе№Із»ҶиғһйўҶеҹҹдёәдҫӢпјҢиӢҘеҢ»з–—жңәжһ„дҫқжҚ®и§„иҢғиҮӘиЎҢз”ҹдә§е№¶еә”з”Ёе№Із»ҶиғһеҲ¶еүӮпјҲеҚівҖңйҷўеҶ…еҲ¶еүӮвҖқпјүпјҢе…¶еёӮеңәжҺҘеҸ—еәҰе°ҶжҲҗдёәдёҖдёӘе…ій”®й—®йўҳвҖ”вҖ”жӮЈиҖ…зҫӨдҪ“жҳҜеҗҰдјҡеҖҫеҗ‘дәҺйҖүжӢ©з”ұеҢ»йҷўиҮӘдё»жҸҗдҫӣзҡ„жІ»з–—ж–№жЎҲпјҢиҝҳжҳҜжӣҙдҝЎиө–з”ұдё“дёҡз”ҹзү©еҢ»иҚҜдјҒдёҡпјҲз”іеҠһж–№пјүж ҮеҮҶеҢ–еҲ¶еӨҮзҡ„дә§е“Ғпјҹ

иҝҷдёҖи¶ӢеҠҝд№ҹеҸҜиғҪеҪұе“Қдә§дёҡзҡ„е•ҶдёҡеҢ–ж јеұҖгҖӮеҖҳиӢҘжӮЈиҖ…еҜ№еҢ»з–—жңәжһ„зӣҙжҺҘжҸҗдҫӣзҡ„жІ»з–—еҪўејҸе»әз«ӢжӣҙејәдҝЎд»»пјҢдј з»ҹиҚҜдјҒеңЁиҜҘйўҶеҹҹзҡ„е•ҶдёҡеҢ–и·Ҝеҫ„еҲҷйңҖйҮҚж–°иҜ„дј°гҖӮзӣ®еүҚпјҢд»…жңүдёӘеҲ«дјҒдёҡеҲқжӯҘе®һзҺ°дәҶе№Із»Ҷиғһдә§е“Ғзҡ„дёҠеёӮдёҺе•ҶдёҡеҢ–гҖӮжңӘжқҘеҮ е№ҙеҶ…пјҢиғҪеӨҹзңҹжӯЈзӘҒз ҙз ”еҸ‘гҖҒе®Ўжү№дёҺеёӮеңәеЈҒеһ’пјҢе®һзҺ°еҸҜжҢҒз»ӯе•ҶдёҡиҝҗиҗҘзҡ„дјҒдёҡж•°йҮҸпјҢд»Қжңүеҫ…и§ӮеҜҹгҖӮ
2. з ”з©¶жңәжһ„зҡ„еҮҶе…ҘеҹәеҮҶдёҺиЎҢдёҡжҙ—зүҢеҸҜиғҪ
иҜҘжі•д»Ө第еҚҒдёҖжқЎжҳҺзЎ®дәҶдёҙеәҠз ”з©¶жңәжһ„еҝ…йЎ»ж»Ўи¶ізҡ„дёҘж јжқЎд»¶пјҢеҢ…жӢ¬еҝ…йЎ»е…·еӨҮдёүзә§з”Ізӯүиө„иҙЁгҖҒи®ҫз«Ӣе®Ңж•ҙзҡ„еӯҰжңҜдёҺдјҰзҗҶе®ЎжҹҘдҪ“зі»гҖҒжӢҘжңүзӣёеҢ№й…Қзҡ„и®ҫж–ҪдёҺдё“дёҡеӣўйҳҹзӯүгҖӮиҝҷе®һиҙЁдёҠдёәе№Із»ҶиғһзӯүеүҚжІҝжҠҖжңҜзҡ„дёҙеәҠз ”з©¶и®ҫз«ӢдәҶжҳҺзЎ®зҡ„еҮҶе…ҘвҖңй—Ёж§ӣвҖқгҖӮ

жңӘиғҪж»Ўи¶іиҝҷдәӣеҹәжң¬жқЎд»¶зҡ„еҢ»з–—жңәжһ„е°Ҷж— жі•ејҖеұ•еҗҲи§„з ”з©¶гҖӮеӣ жӯӨпјҢи®ёеӨҡеҪ“еүҚдёҺдёҚиҫҫж Үжңәжһ„еҗҲдҪңзҡ„е№Із»Ҷиғһз ”еҸ‘дјҒдёҡпјҢе…¶йЎ№зӣ®иҝӣеәҰдёҺжҲҳз•ҘеёғеұҖеҸҜиғҪдјҡеҸ—еҲ°жҳҫи‘—еҲ¶зәҰпјҢиЎҢдёҡеҸҜиғҪйқўдёҙдёҖиҪ®еҹәдәҺеҗҲ规жҖ§зҡ„иө„жәҗж•ҙеҗҲдёҺжҙ—зүҢгҖӮ
3. еӨҡеұӮж¬Ўзӣ‘з®ЎдҪ“зі»зҡ„е»әз«ӢдёҺиҗҪең°жҢ‘жҲҳ
ж №жҚ®з¬¬е…ӯжқЎпјҢжҲ‘еӣҪе·Іе»әз«Ӣиө·д»ҺеӣҪ家еҲ°ең°ж–№зҡ„еҚ«з”ҹеҒҘеә·йғЁй—ЁеҲҶзә§зӣ‘з®ЎдҪ“зі»пјҢ并ејәи°ғеӨҡйғЁй—ЁеҚҸеҗҢз®ЎзҗҶгҖӮиҝҷдёҖжё…жҷ°зҡ„жқғиҙЈеҲ’еҲҶж—ЁеңЁе®һзҺ°е…ЁиҝҮзЁӢгҖҒж— жӯ»и§’зҡ„зӣ‘зқЈпјҢдҝқйҡңдёҙеәҠз ”з©¶дёҺиҪ¬еҢ–зҡ„е®үе…ЁдёҺиҙЁйҮҸгҖӮ
然иҖҢпјҢж–°зҡ„зӣ‘з®ЎжөҒзЁӢеңЁе®һйҷ…жү§иЎҢдёӯжүҖйңҖзҡ„еҚҸи°ғдёҺзЈЁеҗҲпјҢеҸҜиғҪдјҡеңЁзҹӯжңҹеҶ…еҪұе“Қдә§е“Ғд»Һз ”еҸ‘еҲ°жңҖз»ҲдёҠеёӮзҡ„жҺЁиҝӣж•ҲзҺҮгҖӮеҗ„зә§зӣ‘з®ЎйғЁй—ЁеҰӮдҪ•еҪўжҲҗй«ҳж•ҲеҚҸдҪңжңәеҲ¶пјҢе°ҶеҜ№е№Із»Ҷиғһзӯүдә§е“Ғзҡ„иҗҪең°йҖҹеәҰдә§з”ҹзӣҙжҺҘеҪұе“ҚпјҢе…¶е…·дҪ“еҪұе“ҚзЁӢеәҰе°ҡйңҖж—¶й—ҙйӘҢиҜҒгҖӮ
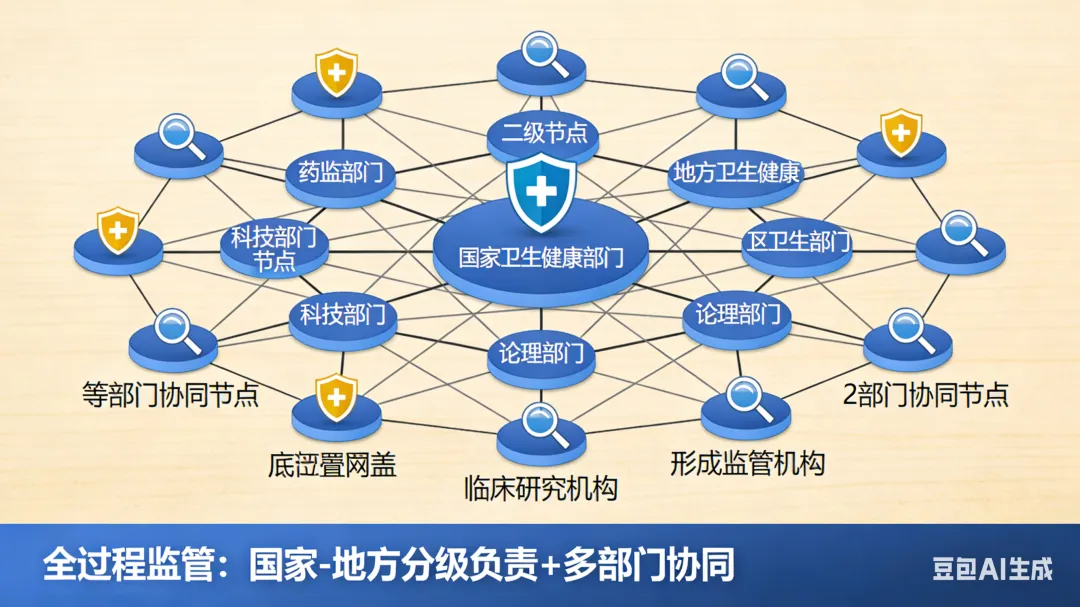
з»јеҗҲеұ•жңӣ
жҖ»иҖҢиЁҖд№ӢпјҢд»ҘгҖҠ818еҸ·д»ӨгҖӢдёәж Үеҝ—зҡ„зӣ‘з®ЎжЎҶжһ¶йҮҚеЎ‘пјҢжӯЈж·ұеҲ»еҪұе“ҚзқҖе№Із»ҶиғһиЎҢдёҡд№ғиҮіж•ҙдёӘз”ҹзү©еҢ»еӯҰж–°жҠҖжңҜйўҶеҹҹзҡ„еҸ‘еұ•иҪЁиҝ№гҖӮеҲ°2026е№ҙпјҢе№Із»ҶиғһиҚҜе“Ғзҡ„дёҠеёӮиҝӣзЁӢгҖҒдјҒдёҡзҡ„з”ҹеӯҳзҠ¶жҖҒд»ҘеҸҠж•ҙдёӘдә§дёҡзҡ„ж јеұҖжј”еҸҳпјҢйғҪе°Ҷз”ұжҠҖжңҜзӘҒз ҙгҖҒж”ҝзӯ–з»ҶеҲҷзҡ„иҗҪең°ж•ҲжһңгҖҒеёӮеңәеҸҚеә”зҡ„е…ұеҗҢдҪңз”ЁжқҘеҶіе®ҡгҖӮжңҖз»ҲеҪўжҖҒпјҢд»ҚйңҖзӯүеҫ…е®һи·өдёҺж—¶й—ҙзҡ„жЈҖйӘҢгҖӮ

гҖҗENDгҖ‘

пјҲж–Үжң«жҸҗзӨәпјҡжң¬ж–Үж—ЁеңЁз§‘жҷ®дәӨжөҒпјҢдёҚжһ„жҲҗд»»дҪ•еҢ»з–—жҢҮеҜје»әи®®гҖӮжүҖиҝ°з–—жі•йңҖеңЁжӯЈи§„еҢ»з–—жңәжһ„иҝӣиЎҢпјҢдёӘдҪ“з–—ж•ҲеӯҳеңЁе·®ејӮпјҢжІ»з–—йҖүжӢ©иҜ·йҒөеҢ»еҳұгҖӮйғЁеҲҶдҝЎжҒҜжқҘжәҗдәҺзҪ‘з»ңпјҢеҰӮеҶ…е®№ж¶үеҸҠзүҲжқғжҲ–е…¶д»–й—®йўҳпјҢиҜ·еҸҠж—¶дёҺжң¬е…¬дј—еҸ·иҒ”зі»пјҢжҲ‘们е°ҶеңЁз¬¬дёҖж—¶й—ҙеҲ йҷӨгҖӮи°ўи°ўпјҒпјүВ