1. 导言:体外脑模型血管化的战略意义与当前挑战
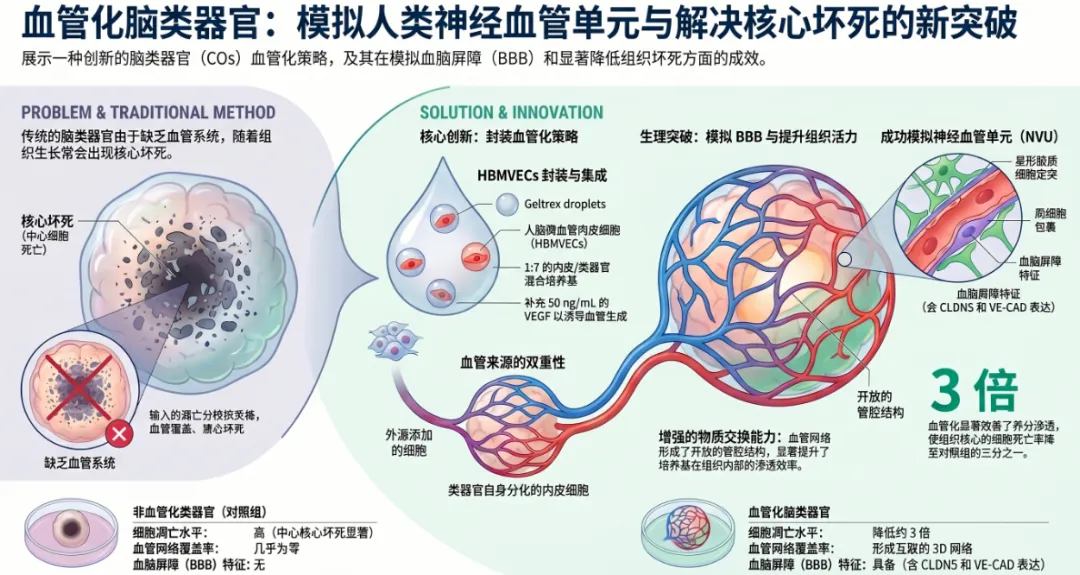
脑类器官(Cerebral Organoids, COs)作为模拟人类大脑发育与病理生理的高度自组织三维模型,在发育生物学、疾病建模及精准药物筛选领域具有不可替代的战略地位。然而,传统非血管化脑类器官由于缺乏功能性管腔灌注,其生理保真度受到严重物理约束。由于营养物质与氧气的有效扩散距离限制,当类器官生长至毫米级时,内部核心区域往往因代谢压力和缺氧触发严重的“中心坏死(Core Necrosis)”。
这种坏死不仅显著缩短了模型的实验窗口期,更通过病理性微环境干扰了神经回路的成熟与功能。因此,建立一套集成稳健内皮细胞网络并优化“新血管化动力学(Neovascularization Kinetics)”的技术方案,是当前类器官研究的攻坚核心。本报告旨在从生物物理基质、生化微环境及细胞来源多样性三个维度,阐述一套可显著降低细胞凋亡并提升组织渗透效率的最优化制备路径。
2. 血管化制备策略:封装法(Encapsulation)的优势评估
在构建集成血管网时,内皮细胞的递送策略直接决定了网络的空间深度与结构稳定性。通过严谨的对比分析评估了“表面附着法(Surface Attachment)”与“水凝胶封装法(Encapsulation Approach)”的效能差异。

战略洞察:实验证实,50,000个人脑微血管内皮细胞(HBMVECs)是维持网络连通性的最优载量。若密度过高(如 500,000 细胞以上),内皮细胞会在类器官表面形成病理性堆叠层,反而限制了管腔化发育。
3. 技术变量优化分析 I:Geltrex™ 浓度对血管形态的调控
胞外基质(ECM)的粘弹性(Viscoelastic Properties)是调节内皮细胞重塑行为的关键。通过对不同浓度的 Geltrex™ 进行定量滴定,揭示了基质物理支撑与生物学重塑之间的复杂权衡。
定量形态分析:
低浓度 (40% Geltrex): 表现出最优的生物学潜力,其血管面积百分比(Vessel Area %)最高,总血管长度最长,且空隙度(Lacunarity)最低,提供了最利于细胞迁移的环境。
高浓度 (95% Geltrex): 虽然显著加粗了血管直径(约 2.5–3 μm),但导致网络呈现严重的空缺与不连续性,且内皮覆盖率大幅下降,因此在技术选型中被排除。
战略权衡: 尽管 60% 浓度在分支能力上具有优势,但在动态培养(Agitation Control)过程中表现出严重的物理不稳定性,易导致封装液滴在收集阶段破裂。
最优设定: 最终选择 80% 浓度的 Geltrex™ 作为标准。这是一种战略性的折中方案,在确保类器官扩张所需结构支撑的前提下,维持了稳健的血管生成效率。
4. 技术变量优化分析 II:培基组成与 VEGF 投药方案
由于神经外胚层与中胚层来源的细胞对生化因子有竞争性需求,培养环境的配比必须精细平衡。
培基配比策略: 研究对比了 ECG 与成熟培养基在 1:1, 1:3, 1:7 比例下的表现。最终选定 1:7 的 ECG:CO 混合培基。
决策依据: 尽管 1:1 比例能产生密度最高的血管网,但 1:7 的低比例能最大限度降低 ECG 中 bFGF、BMP-4 及维生素 A 对神经组织发育模式(Neural Patterning)的潜在干扰。
VEGF 诱导与正反馈机制:
确立 50 ng/mL 的 VEGF 浓度为标准投药剂量,每 4 天更换一次培基。
定量证据: 在该浓度诱导下,内皮细胞通过正反馈回路使上清液中 VEGF 水平持续维持在 100 ng/mL 以上,并驱动 MMP-9 表达量在 Day 40 达到 10 ng/mL(较对照组提升约 50 倍),显著加速了 ECM 的酶解重塑与类器官的早期生长动力学。
5. 血管化类器官的结构与生理特性表征
优化后的模型不仅是简单的细胞集合,更实现了神经血管单元(NVU)的结构模拟。
形态学影响: 血管化类器官表现出显著增强的形状规整度(Circularity)。这归功于“血管网格”提供的机械支撑作用。此外,尽管组织硬度在 0.5–3 kPa 范围内波动(略高于生理脑组织的 0.1–1 kPa),但血管化过程并未导致组织进一步硬化。
BBB 关键标志物:
内皮连接: VE-CAD 和 CLDN5 在细胞交界处精准定位。
基底膜: 血管周围检测到由 IV 型胶质和 Laminin α5 构成的功能性基底膜。
细胞互作:观察到星形胶质细胞(GFAP+)足突包裹管腔及周细胞(NG2+)的缠绕。
双源镶嵌系统与 iPSC 变异:
iPSC 线特异性: 研究发现 A-iPSCs 具有较高的内源性中胚层分化潜能,而 S-iPSCs 较低。
关键证据: 在 CortiCOs(皮层类器官)实验中,证明了该模型中的血管网是由外源性 HBMVECs 与内源性 ECs 共同构成的镶嵌系统。此外,血管化组出现的 PAX6+ 表明了模型良好的背侧前脑恒常性(Dorsal Forebrain Identity)。
6. 性能评估:中心坏死(Core Necrosis)的定量缓解证据
血管化的核心效能体现在改善内部微环境并抑制程序性细胞死亡。
凋亡抑制: TUNEL 检测数据显示,血管化类器官的细胞凋亡率比非血管化对照组低 up to 3-fold(三倍)。在对照组中,坏死密集分布于致密核心(Necrotic Core),而血管化组在组织深处仍保持极高的细胞存活率。
渗透性验证: 利用 70 kDa 右旋糖苷-罗丹明 B(d-RhoB)进行渗透实验。
定量分析: 结果显示血管化组显著增强了介质内化效率。特别是在体积较小的阶段,血管化组的 d-RhoB 转移量远高于对照组;而对照组的荧光强度呈现出尺寸无关性(Size-independent),表明其内部扩散极度受限。
管腔化证据: H&E 染色证实了组织内部功能性管腔的存在,从而改善了营养物质的深层输送。
7. 结论与未来优化方向
本研究开发了一套基于商业化试剂、高可重复性的血管化脑类器官制备方案,为模拟人类神经血管单元提供了卓越的体外平台。
核心技术结论:
80% Geltrex 配合 1:7 培基比例 是平衡结构支撑、神经发育保真度与血管化效率的最佳参数。
VEGF/MMP-9正反馈循环驱动了高效的基质重塑,将类器官凋亡率显著降低了 3 倍。
血管网络通过外源性细胞封装与内源性分化的协同作用,成功缓解了中心坏死现象。
未来愿景: 尽管模型已具备 BBB 标志物,但目前仍缺乏管腔内流体剪切力。后续研究应聚焦于将预血管化类器官集成至微流控芯片中,通过实现真实流体灌注(Perfusion)进一步诱导内皮细胞成熟。
参考文献
J.Fumadó Navarro, S.Crilly, W. K.Chan, et al. “Cerebral Organoids with Integrated Endothelial Networks Emulate the Neurovascular Unit and Mitigate Core Necrosis.” Adv. Sci.12, no. 43 (2025): e07256. https://doi.org/10.1002/advs.202507256