
出品 | 陈博观察 (ID: Drchenobservation)
编辑 | Will Chan


中国已稳居全球生命科学 GenAI 发展第一梯队,2014-2023 年累计申请相关专利 3181 项,是全球专利申请头号大国,远超第二名美国的 979 项;2024 年中国在全球生命科学 GenAI 市场占比达三分之一,市场规模为 5750 万美元,2025 年市场规模已达 5.37 亿元人民币,预计未来十年将保持 20% 以上的年均复合增长率快速增长。
政策层面,2020 年以来国家多部门持续出台专项政策,形成了从标准化建设、技术创新到场景落地、监管适配的全周期支撑体系,2026 年 4 月国家药监局发布《关于 “人工智能 + 药品监管” 的实施意见》,进一步完善了药品全生命周期的数智化监管框架。投融资市场经历 2019-2021 年的快速升温后回归理性,呈现结构性分化特征,资本向具备临床验证和商业变现能力的中后期项目集中,前沿赛道创新价值兑现周期大幅缩短。
应用场景方面,AI 驱动创新药研发已实现全链条成熟落地,可将传统药物研发从靶点到临床前候选物的 4.5 年周期压缩至 12-18 个月,研发成本降低超 60%;临床试验优化、生产质控、患者管理、医学营销等场景加速渗透,GenAI 的降本增效价值已得到全行业验证。
同时,行业发展仍面临数据隐私安全、模型可解释性不足、真实环境泛化能力受限、生物安全两用风险等现实挑战,以及算力瓶颈、高质量数据供给不足、跨界人才稀缺、转化成本高企等长期发展制约。未来,GenAI 将从辅助工具向药物研发核心引擎全面演进,推动产业生态协同重构,加速前沿技术从实验室向规模化产业化落地,助力中国从医药大国向全球医药创新强国跨越。

二、生成式 AI 在生命科学行业的发展现状与全球定位
(一)技术演进历程
生命科学领域的人工智能应用已完成四轮技术迭代,进入生成式 AI 主导的全新发展阶段。1950 年代至 1970 年代,行业处于早期 AI 阶段,以基于规则和逻辑系统的人工智能初步开发为核心;1990 年代至 2000 年代初,进入基础 AI 阶段,统计模型和基本神经网络开始出现并初步应用;2012 年 - 2016 年,深度学习时代到来,人工智能被广泛用于处理生物数据和基因组分析,实现了生物信息处理的首次效率跃升;2017 年 - 2020 年,Transformer 模型与 GPT 系列模型的出现,推动行业向生成式 AI 实现范式转变;2020 年至今,生成式 AI 全面应用于生物系统建模、遗传学研究、药物研发全流程,技术生态快速成熟,成为行业创新的核心驱动力。

(二)中国的全球领先地位
在专利布局层面,中国已成为全球生命科学和医学 GenAI 应用专利的第一大国。2014-2023 年,中国相关专利申请量达 3181 项,远超美国 979 项、韩国 531 项、日本 261 项,稳居全球首位;国内申请主体中,平安集团、腾讯、百度分别以 227 项、73 项、34 项专利位列前三,展现出国内科技企业在该领域的深厚技术积累。
 来源:毕马威,生成式人工智能对中国生命科学行业的影响
来源:毕马威,生成式人工智能对中国生命科学行业的影响
在市场规模层面,中国市场增速显著高于全球平均水平。2024 年中国生命科学 GenAI 市场规模达 5750 万美元,占全球市场的三分之一;根据贝哲斯咨询数据,2025 年中国该市场规模已达 5.37 亿元人民币,预计至 2032 年将保持 20% 以上的年均复合增长率增长。全球市场方面,2025 年全球生命科学 GenAI 市场规模约 2.82 亿美元,预计 2035 年将达 17.79 亿美元,年均复合增长率 20.21%,中国已成为拉动全球市场增长的核心引擎。
(三)行业应用的核心驱动力
一是降本增效的核心价值,破解传统生命科学行业尤其是药物研发 “双十定律”(十年周期、十亿美元投入)的行业痛点。波士顿咨询数据显示,AI 生成的药物分子 I 期临床试验成功率达 80%-90%,远高于传统方法 50% 的历史平均水平,大幅提升研发成功率,降低研发成本。
二是先进的数据处理能力,生成式 AI 可高效整合分析基因组、临床、多组学、蛋白结构等海量非结构化生物数据,挖掘传统方法无法识别的生物规律与疾病机制,为生命科学基础研究与应用创新提供全新的分析工具。
三是药物开发的范式革新,实现从靶点发现、分子设计、先导化合物优化到临床前验证的全链条重构,拓展了可成药靶点的边界,为罕见病、难治性肿瘤等未被满足的临床需求提供了全新的解决方案。
四是临床试验的效率提升,通过 AI 优化试验设计、智能化患者招募、临床数据自动化管理与分析,大幅缩短临床试验周期,降低试验执行成本,提升临床数据质量与合规性。
五是患者服务的深度升级,通过生成式 AI 的智能交互能力,实现个性化患者管理、健康科普、用药指导与随访服务,提升患者治疗依从性,改善临床结局,同时扩大优质医疗服务的可及性。

三、政策驱动:中国 GenAI + 生命科学的顶层设计与落地导向
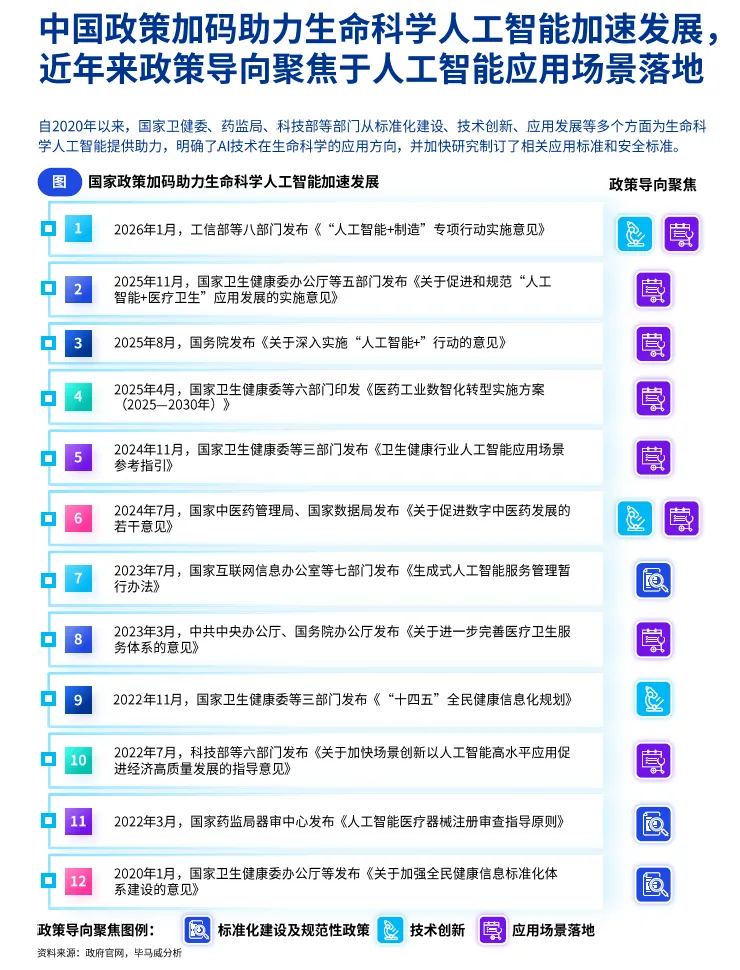
自 2020 年以来,国家卫健委、药监局、科技部、工信部等多部门持续出台专项政策,政策导向从早期的标准化体系建设,逐步转向技术创新引导,最终聚焦于应用场景的规模化落地,形成了 “基础规范 - 技术创新 - 场景落地 - 监管适配” 的全周期政策支撑体系,为行业发展划定了清晰的方向与合规边界。
(一)标准化体系建设阶段(2020-2022 年)
本阶段政策核心是搭建行业基础规范框架,为 AI 技术在生命科学领域的应用建立底层标准。2020 年 1 月,国家卫健委发布《关于加强全民健康信息标准化体系建设的意见》,首次明确推进医学人工智能在药物研发、智能临床辅助诊疗、医用机器人等领域的应用试点,提出加快研究制订人工智能技术的相关应用标准和安全标准,是行业标准化建设的纲领性文件。
2022 年 3 月,国家药监局器审中心发布《人工智能医疗器械注册审查指导原则》,为 AI 医疗器械的注册申报、技术审评与体系核查建立了明确规范,填补了 AI 医疗设备监管的空白。2022 年 11 月,国家卫健委等三部门发布《“十四五” 全民健康信息化规划》,将人工智能技术作为推动医疗健康信息化发展的核心手段,明确了技术在医疗服务、公共卫生、医药创新等领域的应用方向,为行业发展提供了中长期规划指引。
(二)技术创新与规范管理阶段(2023-2024 年)
本阶段政策核心是针对生成式 AI 的专项规范与创新引导,适配技术迭代速度,平衡创新发展与安全合规。2023 年 7 月,国家网信办等七部门发布《生成式人工智能服务管理暂行办法》,这是国内首个针对生成式 AI 产业的规范性政策,实行包容审慎和分类分级监管,为 GenAI 在生命科学领域的应用划定了基础合规底线,明确了数据安全、知识产权、内容治理等核心要求。
2024 年 7 月,国家中医药管理局、国家数据局发布《关于促进数字中医药发展的若干意见》,提出用 3-5 年时间推动大数据、人工智能融入中医药传承创新全链条,全力打造 “数智中医药”,拓展了 GenAI 的应用边界。2024 年 11 月,国家卫健委等三部门发布《卫生健康行业人工智能应用场景参考指引》,提出涵盖医疗服务管理、基层公卫服务、健康产业发展、医学教学科研四大板块、十三个类目、84 个典型应用场景,全面推动 AI 技术在医疗健康领域的场景化落地。
(三)全链条场景落地与监管完善阶段(2025 年至今)
本阶段政策核心是推动 “人工智能 +” 在生命科学全领域的深度落地,同步完善适配技术发展的监管体系,实现产业发展与监管创新的双向协同。2025 年 4 月,国家卫健委等六部门印发《医药工业数智化转型实施方案 (2025-2030 年)》,以场景化方式推进医药研发、医药生产、CXO 等全环节的数智化转型,明确了医药工业 AI 应用的核心场景与转型目标。
2025 年 8 月,国务院发布《关于深入实施 “人工智能 +” 行动的意见》,提出探索推广人人可享的高水平居民健康助手,有序推动人工智能在辅助诊疗、健康管理、新药研发、医保服务等场景的应用,是 “人工智能 +” 在生命科学领域落地的顶层设计文件。2025 年 11 月,国家卫健委等五部门发布《关于促进和规范 “人工智能 + 医疗卫生” 应用发展的实施意见》,提出 2027 年、2030 年两个阶段的发展目标,明确到 2030 年二级以上医院普遍开展医学影像智能辅助诊断、临床诊疗智能辅助决策等 AI 技术应用,“人工智能 + 医疗卫生” 应用标准规范体系基本完善。
2026 年 1 月,工信部等八部门发布《“人工智能 + 制造” 专项行动实施意见》,明确加快手术机器人、智能诊断系统等智能医疗装备创新推广,推动脑机接口等新型终端产业化,补齐了 AI 医疗装备领域的政策短板。2026 年 4 月,国家药监局发布《关于 “人工智能 + 药品监管” 的实施意见》,这是药监领域 AI 监管的顶层纲领性文件,明确到 2030 年初步构建药品监管与 AI 融合创新体系,2035 年基本形成数智驱动、智能敏捷、自主可控、生态协同的智慧化药品安全治理新格局,将 AI 应用覆盖到药品审评审批、生产流通、检验监测、风险预警等全生命周期,既为产业创新提供了清晰的监管指引,也从制度层面保障了公众用药安全。
四、中国 GenAI + 生命科学领域投融资市场特征与趋势
基于 2019-2025 年的行业全量投融资数据分析,国内生命科学人工智能领域融资市场经历了从热潮到理性的周期转变,呈现出四大核心特征,精准反映了行业从概念验证向价值兑现的发展进程。
(一)投融资周期从快速升温向理性回归,行业进入价值验证阶段
2019 至 2021 年,国内生命科学人工智能领域融资金额与项目数量均呈现加速增长态势,并于 2021 年达到近年峰值。这一时期,AI 工具在药物研发靶点发现、生物计算等核心场景实现突破性进展,大幅提升了资本市场对赛道的发展预期,大量资金涌入,行业整体活跃度与关注度达到顶峰。
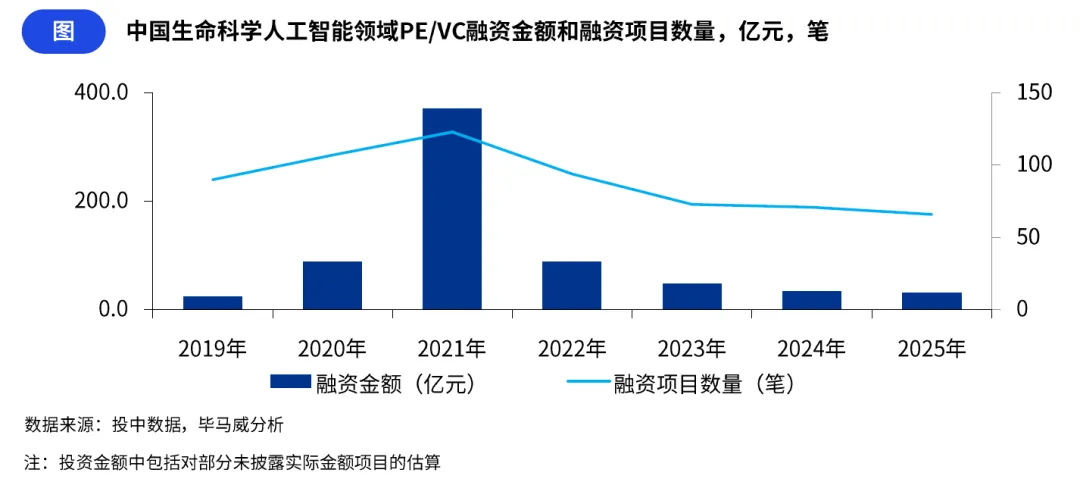
自 2021 年起,投融资市场逐步从热潮回归理性,资本偏好从关注概念炒作转向关注技术落地与商业变现能力,行业进入临床验证与价值兑现的关键阶段。2025 年国内 AI 制药领域累计融资总额超 67 亿元,同比大幅增长 130.5%,资金向头部平台型企业集中的趋势显著,市场分化持续加剧。
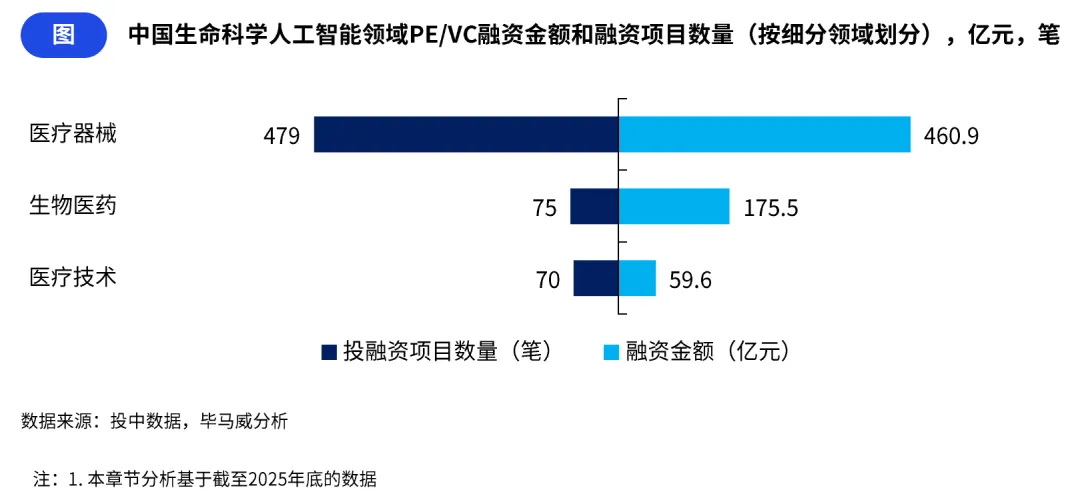
(二)细分领域呈现结构性分化,高壁垒创新赛道长期价值更受认可
从融资项目数量来看,AI 赋能医疗器械以 479 笔居首,占比远超其他细分领域,反映出医疗器械领域 AI 技术商业化落地路径更清晰,场景应用更广泛;但其单笔融资金额仅为 0.96 亿元,显著低于其他赛道。
生物医药领域融资项目数量为 75 笔,仅为医疗器械领域的 15.7%,但单笔融资金额达 2.34 亿元,是医疗器械领域的 2.44 倍,反映出资本市场对创新药研发赛道的高壁垒、长周期价值具备更强的长期认可度,愿意为具备核心技术的创新项目支付更高的估值溢价。
医疗技术领域虽有 70 笔融资,项目数量紧跟生物医药之后,但单笔融资金额仅 0.85 亿元,为所有赛道最低,凸显该领域多数技术仍处于早期验证阶段,商业化路径尚未完全清晰,资本投资态度更为谨慎。
(三)投资轮次向中后期集中,资本优先布局已验证技术的成熟项目
2019-2025 年,行业投资呈现 “早期项目减少,中后期项目集中” 的显著趋势,资本对技术变现能力的重视程度持续提升。2025 年,生命科学人工智能领域融资 B 轮及以后的项目数量占比接近五成,较 2024 年提升 10.2 个百分点,而 2019 年中后期融资阶段的项目数量占比仅为 33.3%,六年内占比提升超 16 个百分点。
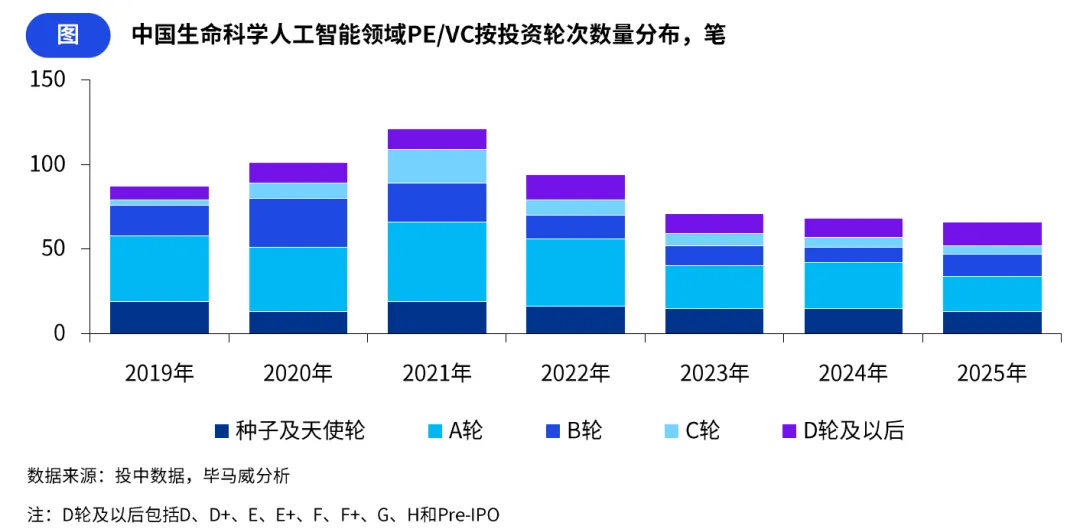
这一趋势反映出,资本市场已从早期的赛道广撒网,转向优先投资具备临床验证、政策准入和海外订单的成熟项目,更关注企业的现金流与商业化能力。进入 2026 年,尽管受资本市场整体环境影响,早期轮次投资占比出现小幅回升,但中后期项目的单笔融资金额仍保持高位,资本对已验证技术的集中度进一步提升。
(四)创新价值兑现周期大幅缩短,前沿赛道出现 “成立即融资” 新趋势
从被投企业的成立年限来看,超过五成的被投企业成立不足五年,行业创业与投资的活跃度持续保持高位。其中 2025 年全年共有 152 家企业在注册当年即获得首笔融资,尤其在 AI 制药、脑机接口、AI 智能可穿戴设备等前沿赛道,企业从创立到完成首轮融资的周期大幅压缩,部分项目实现 “成立即融资”。
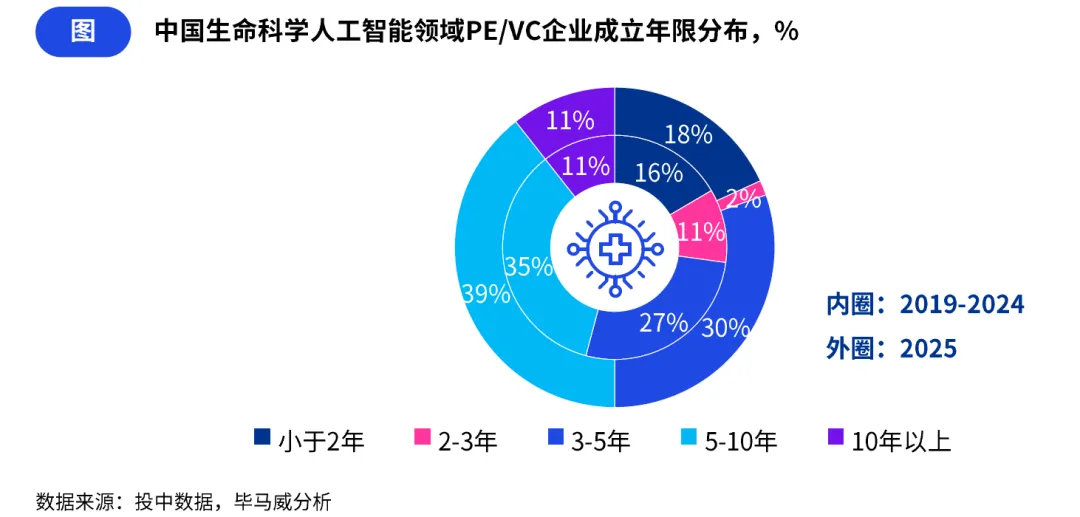
这一趋势表明,资本市场对前沿技术原型的识别与布局更加果断,前沿技术的商业化验证效率正在重塑早期投资逻辑,创新价值的兑现周期明显加快。同时,也反映出国内生命科学 AI 领域的技术创新迭代速度持续加快,产学研转化效率显著提升。
五、生成式 AI 在生命科学领域的核心应用场景与成熟实践
基于行业应用成熟度划分,生成式 AI 在生命科学领域的应用已形成 “核心场景成熟落地、新兴场景快速渗透” 的格局,其中药物研发、医学语音及图像识别应用已进入成型阶段,临床试验优化、药品营销、生产质控等场景进入扩展阶段,核心应用实践如下。
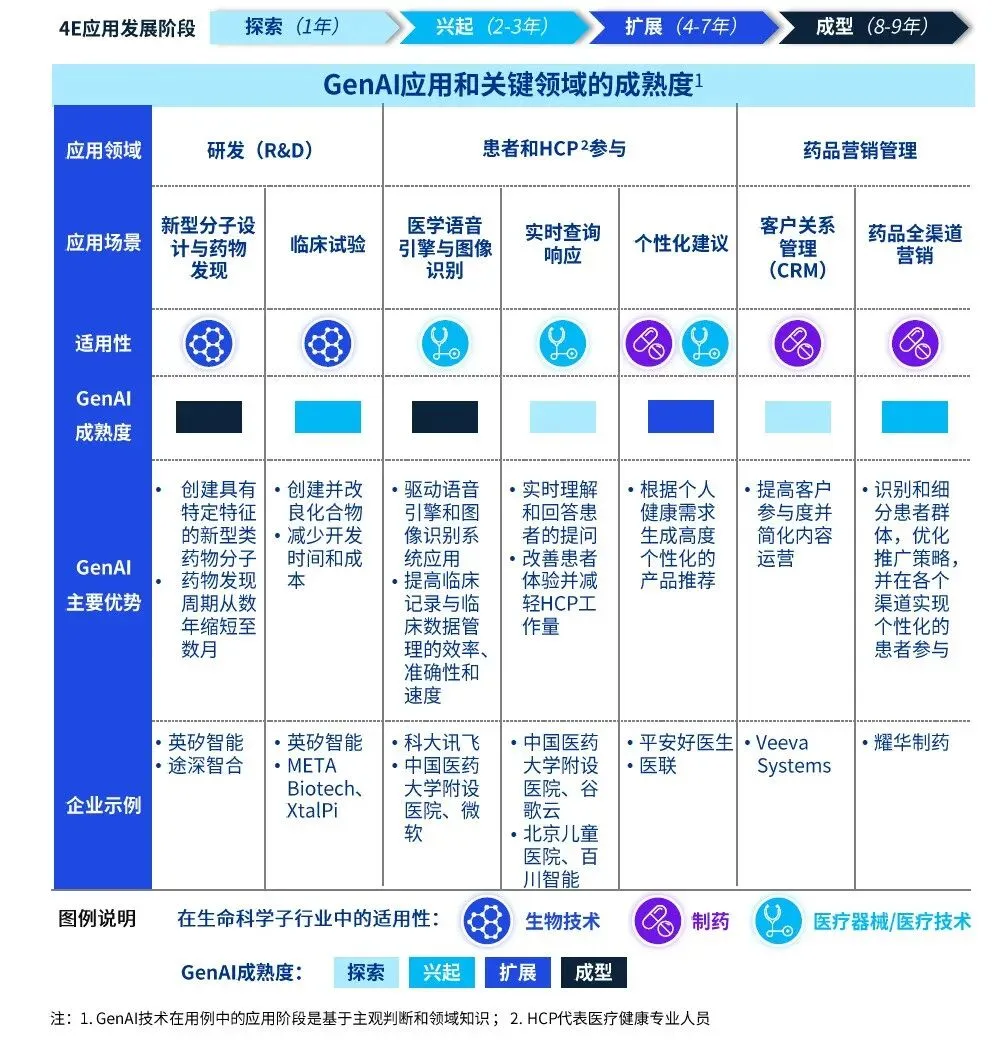
(一)AI 驱动创新药研发,实现全链条范式革新
这是目前生成式 AI 应用最成熟、价值最显著的核心场景,彻底重构了传统药物研发的流程与逻辑。国内头部生成式 AI 制药公司通过自主研发的 AI 平台,完成了全球首个全 AI 驱动的 TNIK 小分子抑制剂的研发,从靶点发现、分子设计到临床前候选物确认全程无需人工干预,将传统流程平均 4.5 年的周期大幅压缩至 12-18 个月,研发成本降低超 60%,实现了 AI 药物研发的里程碑式突破。
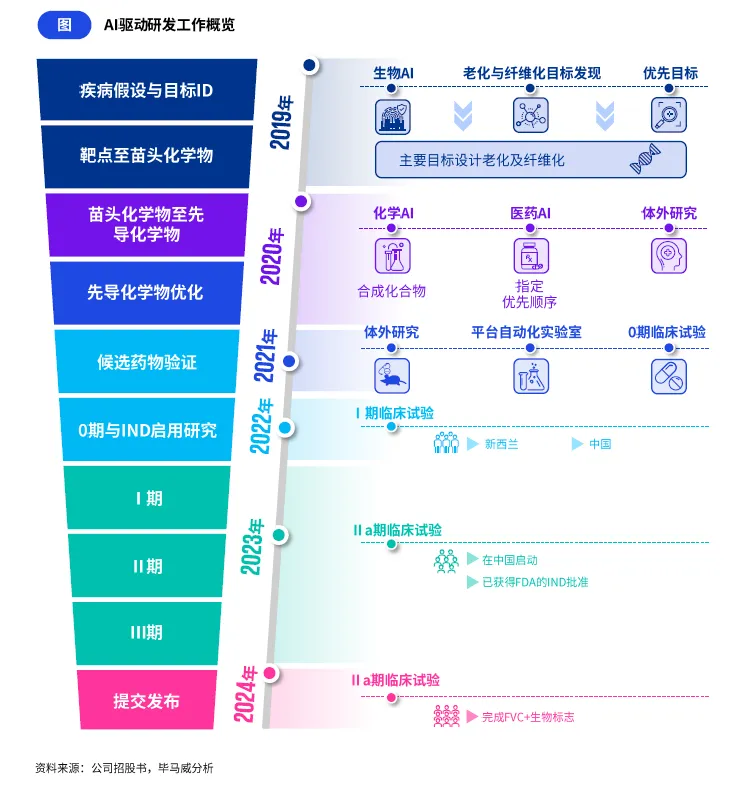
同时,国内企业创新打造了 “AI + 机器人” 的药物研发新范式,以自研 AI 为引擎,将量子物理计算、云计算、机器人实验室技术深度耦合,通过 AI 生成候选分子后,借助自动化机器人实验室快速完成合成、表达与活性测试,测试数据实时反馈至 AI 模型用于下一轮分子优化与模型迭代,形成 “计算 - 实验” 的闭环研发体系,大幅缩短了 “假设 - 验证 - 学习” 的研发周期,实现了更快的先导化合物发现、更准确的分子特性预测与更大规模的分子评估,成为国内 AI 制药企业的核心差异化优势。
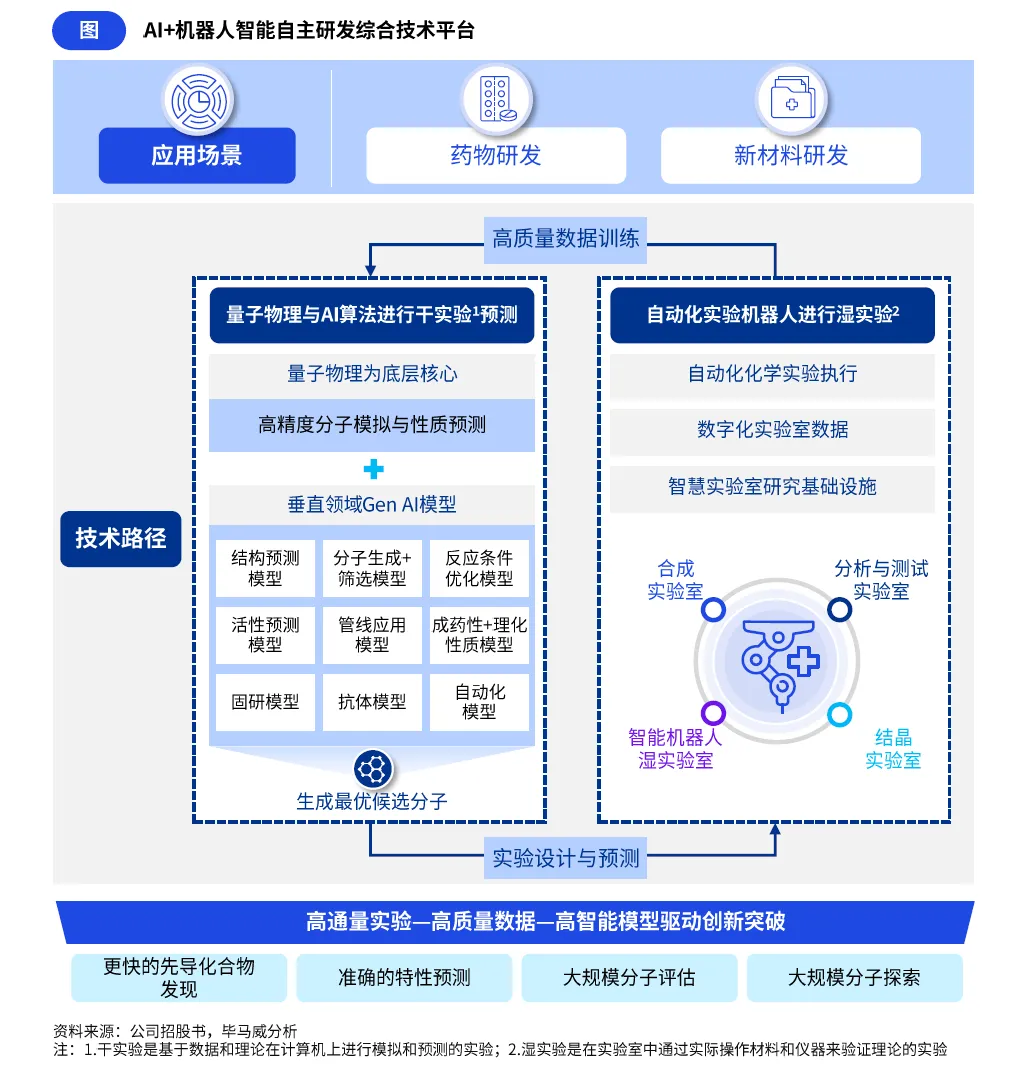
(二)全业务链规模化落地,深度嵌入制药全核心环节
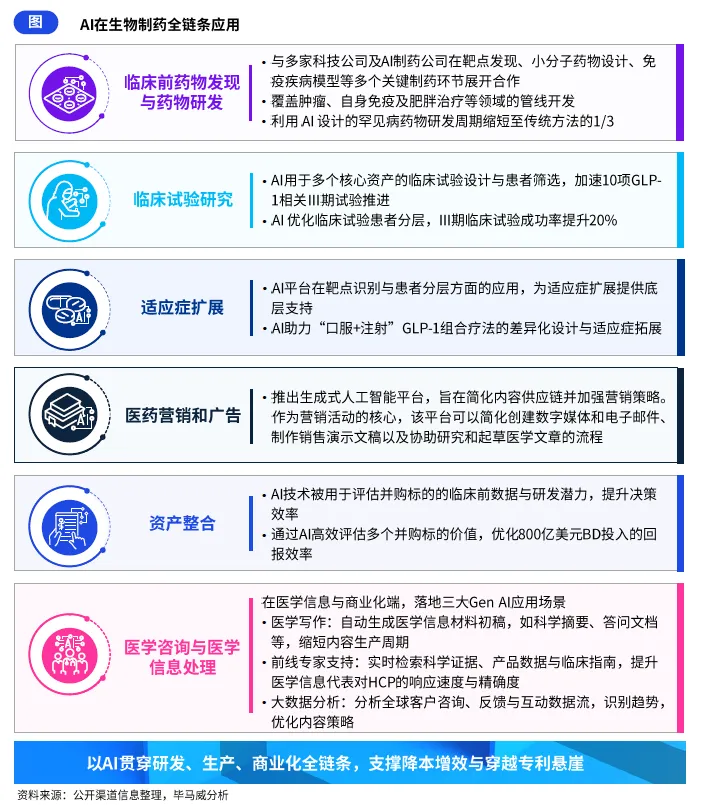
头部跨国药企已率先实现 AI 在生物制药全链条的规模化应用,将 AI 战略从研发辅助工具全面升级为驱动运营效率、成本优化与创新加速的核心引擎。在研发端,AI 深度应用于临床前药物发现、疾病模型构建、靶点验证、适应症扩展等环节,加速管线推进;在临床试验端,通过 AI 优化试验设计、患者招募与临床数据管理,提升试验执行效率;在商业化端,落地三大核心场景,包括医学内容自动化生成、医学信息代表对医疗健康专业人员的响应速度与精确度提升、营销内容策略优化,大幅缩短内容生产周期,提升营销转化效率;在生产与合规端,通过 AI 实现 CMC 申报文档自动化生成、生产流程优化与质量控制精度提升,支撑企业穿越专利悬崖,实现全生命周期的降本增效。
(三)AI 与生物技术深度融合,赋能全生命周期管理
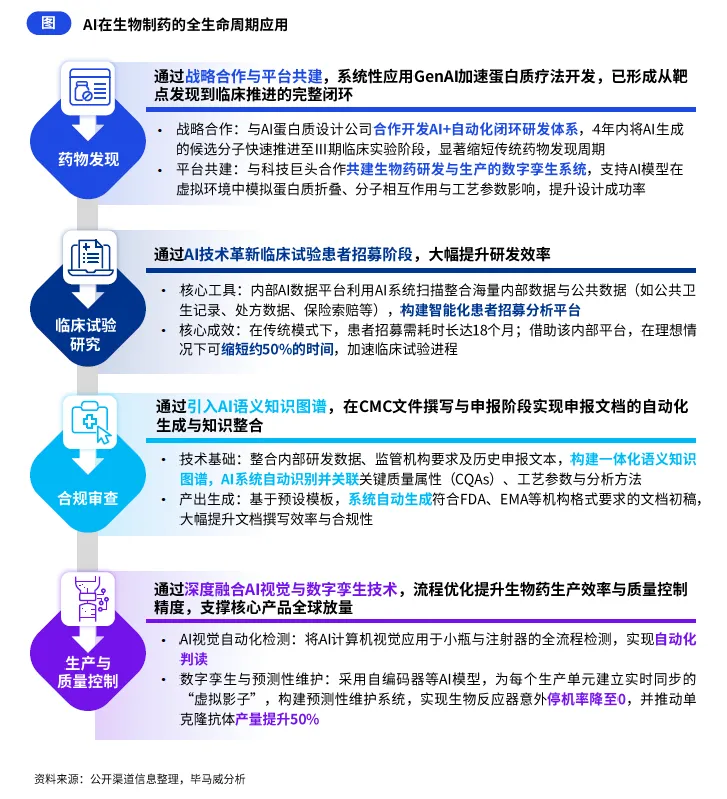
专注于生物技术药物研发的企业,通过跨界合作与 AI 工具应用,实现了从生物学洞察到生产制造的全流程赋能。在药物发现环节,与 AI 蛋白质设计公司合作开发 AI + 自动化闭环研发体系,4 年内将 AI 生成的候选分子快速推进至 II 期临床阶段,显著缩短传统药物发现周期;同时与科技巨头合作共建生物药研发与生产的数字孪生系统,支持 AI 模型在虚拟环境中模拟蛋白质折叠、分子相互作用与工艺参数影响,大幅提升分子设计成功率。
在临床试验环节,通过内部 AI 数据平台扫描整合海量内部与公共数据,构建智能化患者招募分析平台,将传统模式下长达 18 个月的患者招募周期在理想情况下缩短约 50%,大幅加速临床试验进程。在合规审查环节,引入 AI 语义知识图谱,整合内部研发数据、监管要求与历史申报文本,自动生成符合 FDA、EMA 等机构格式要求的 CMC 申报文档初稿,大幅提升文档撰写效率与合规性。
在生产与质量控制环节,将 AI 计算机视觉应用于小瓶与注射器的全流程检测,实现自动化判读;同时采用 AI 模型构建生产单元的数字孪生系统与预测性维护体系,实现生物反应器意外停机率降至 0,并推动单克隆抗体产量提升 50%,实现了生产效率与质量控制的双重突破。
(四)医疗服务与患者管理场景规模化应用,提升医疗服务可及性
在医学影像领域,AI 辅助诊断系统已在国内数千家医院落地,可实现眼底、病理、放射影像的自动化识别与辅助诊断,将基层医疗机构的诊断准确率提升 15% 以上,有效缓解了基层医疗资源不足的痛点。在临床服务领域,AI 系统可实现电子病历自动生成、病历信息结构化处理,北京阜外医院利用 AI 系统将病历首页信息准确率提升至 95% 以上,同时开发手术评估模型,对医生操作进行数据化评分,推动医疗行为标准化。在患者管理领域,生成式 AI 通过智能交互实现个性化健康科普、用药提醒、随访管理,提升患者治疗依从性,改善临床结局,扩大了优质医疗服务的覆盖范围。
六、中国创新药企与跨国药企 GenAI 实施路径的差异化分析
中国创新药企业与跨国药企在战略定位上的核心差异,导致了二者在生成式 AI 实施路径上的显著分化,这种差异既反映了中外医药研发领域不同的发展阶段与资源禀赋,也形成了差异化的竞争优势与广阔的合作空间。
 来源:毕马威,生成式人工智能对中国生命科学行业的影响
来源:毕马威,生成式人工智能对中国生命科学行业的影响
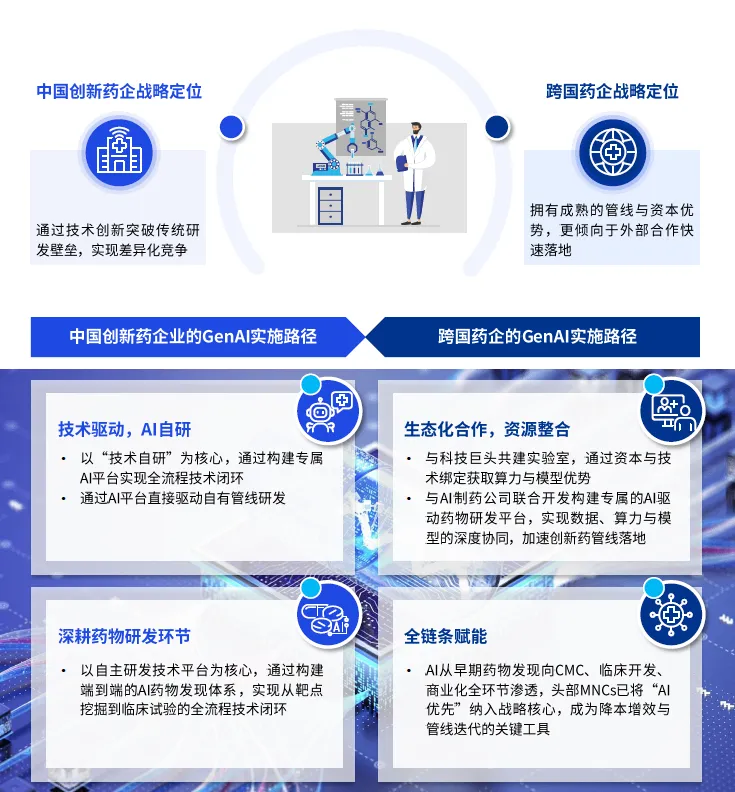
(一)战略定位的核心差异
中国创新药企的核心战略定位,是通过技术创新突破传统研发壁垒,在全球创新药赛道实现差异化竞争。国内多数创新药企成立时间较短,管线规模有限,研发资源与跨国药企存在显著差距,因此将生成式 AI 作为实现 “弯道超车” 的核心工具,聚焦于通过技术突破解决药物研发的核心痛点,快速推进创新管线落地,构建自身的核心竞争力。
跨国药企的核心战略定位,是依托成熟的管线布局、充足的资本优势与全球化的产业资源,通过生成式 AI 实现全链条效率提升与成本优化,巩固全球市场的领先地位。其 AI 战略更多是服务于现有业务体系的升级与优化,而非颠覆性的创新突破,核心目标是通过 AI 技术放大现有业务的商业价值。
(二)技术路径的核心差异
中国创新药企以 “技术自研” 为核心,聚焦于构建专属的端到端 AI 平台,实现全流程技术闭环。国内头部创新药企与 AI 制药公司,均以自研垂直大模型为核心竞争力,打造覆盖靶点挖掘、分子设计、先导化合物优化、临床试验设计的端到端 AI 药物发现体系,通过全流程的技术闭环,实现研发效率的颠覆性提升。同时,国内企业通过生态化合作补充资源短板,与科技巨头共建实验室,通过资本与技术绑定获取算力与模型优势,与 AI 制药公司联合开发专属研发平台,实现数据、算力与模型的深度协同,加速创新药管线落地。
跨国药企以 “全链条赋能” 为核心,依托外部合作实现快速规模化落地。头部跨国药企已将 “AI 优先” 纳入企业核心战略,推动 AI 从早期药物发现向 CMC、临床开发、商业化、生产质控全环节渗透,其技术路径以外部合作为主,通过与全球顶尖 AI 科技公司、AI 制药初创企业达成战略合作,快速引入成熟的 AI 技术与工具,适配自身全链条的业务需求,避免重复的底层研发投入,实现技术的快速落地与规模化应用。
(三)落地场景的核心差异
中国创新药企的 AI 应用高度聚焦于药物研发环节,尤其是早期靶点发现与分子设计。国内企业将有限的研发资源集中于药物研发的核心痛点环节,通过 AI 技术大幅缩短研发周期、降低研发成本,快速推进创新管线进入临床阶段,形成差异化的管线优势,这也是国内企业在全球 AI 制药赛道实现突围的核心方向。
跨国药企的 AI 应用实现了全业务链的全覆盖,除了研发环节的应用,还深度渗透到临床试验管理、药品生产质控、医学合规、商业化营销、患者管理等全环节,通过 AI 实现全产业链的效率优化与成本控制,最大化技术应用的商业价值,形成了全链条的 AI 应用体系。
(四)全球化布局的核心差异
中国创新药企以 AI 技术为核心抓手,推动创新药管线与技术平台的全球化出海。近年来,国内 AI 制药企业与创新药企,通过自研的 AI 技术平台开发的创新药物,接连实现海外权益的大额授权,合作对象从以往的区域授权转向全球权益合作,合作领域从传统肿瘤赛道向代谢性疾病、自身免疫疾病等蓝海市场延伸。2025 年全球制药企业从中国企业获得药品许可的数量创下历史纪录,中国 AI 制药创新已成为全球医药创新的核心供给方。
跨国药企则通过全球化的研发布局,整合全球 AI 技术资源与临床数据,推动 AI 技术在全球不同市场的适配与落地,同时通过在中国设立研发中心,与国内 AI 企业达成深度合作,布局中国市场的 AI 创新资源,实现全球化的技术与资源整合。
七、行业发展面临的核心风险与挑战
随着生成式 AI 在生命科学行业的深度应用,行业同时面临着当前可感知的现实风险,与长期发展需要突破的核心挑战,成为制约行业规模化高质量发展的核心瓶颈。

(一)当前行业面临的四大核心风险
一是数据隐私泄露风险与监管合规边界模糊。生成式 AI 模型的训练需要收集大量患者的基因组数据、临床诊疗数据等高敏感个人信息,而当前国内针对医疗健康高敏数据的个人信息保护细则仍有待完善,数据使用的责任归属、风险问责机制仍存在监管真空地带,企业在数据收集、使用、共享过程中,极易出现合规风险,同时数据泄露可能对患者隐私造成严重侵害。
二是模型可解释性不足与 AI 幻觉带来的安全风险。生成式 AI 模型普遍存在 “黑箱特性”,模型的决策逻辑透明度与可解释性不足,难以满足制药行业 “可追溯、可验证” 的核心合规要求,无法向监管机构完整解释分子设计、临床预测等决策的底层逻辑。同时,AI “幻觉” 问题会导致模型生成虚假的实验数据、临床结论与文献信息,可能造成临床数据失真、药品申报不合规,甚至引发严重的医疗安全与用药安全风险。
三是模型真实环境泛化能力受限,存在 “实验准确” 与 “临床可用” 的巨大鸿沟。多数 AI 模型在企业自有数据集上表现出优异的性能,但在真实临床环境中应用效果大幅下降,核心原因包括医学数据天然的多样性与异质性、训练数据的 “茧房” 效应导致模型适配性不足、临床环境的动态复杂性远超实验场景等,这一问题直接制约了 AI 技术从实验室向临床场景的规模化落地。
四是生物安全与两用风险。AI 驱动的生物合成工具,可能被滥用于合成病原体、设计毒性分子与生物武器,而 AI 驱动的自动化机器人实验室可实现 “无人干预” 的生物合成与筛选,进一步放大了生物安全的潜在风险,对技术的监管与风险防控提出了更高的要求。
(二)行业长期发展面临的四大核心挑战
一是基础设施不足与算力瓶颈制约。当前国内生命科学领域的数字基础设施存在 “重建设、轻共享”“强中心、弱基层” 的问题,跨机构、跨区域的数据与算力资源共享机制尚未形成。同时,生成式 AI 模型的训练与推理对算力需求激增,而国内算力资源分布不均,高端算力芯片国产化仍存在差距,构成了行业发展的双重制约,尤其对中小药企与初创企业而言,算力成本高企已成为技术应用的核心门槛。
二是高质量标准化数据供给严重不足。数据是 AI 模型训练的核心基础,而当前国内缺乏面向生物计算的高质量、标准化数据集,生物数据的标注体系尚未成熟,行业缺乏统一的数据标准与共享机制,大量医疗数据沉积于医院、科研机构的封闭平台,形成严重的 “数据孤岛”。同时,中文医疗语料、非结构化临床记录的电子化程度低,中医药古籍数据的数字化与结构化不足,进一步制约了垂直领域大模型的训练与优化。
三是跨界复合型人才严重稀缺。生成式 AI 与生命科学的深度融合,催生了对 “双栖人才” 的迫切需求,要求从业者同时具备深厚的生物医学背景与扎实的 AI 工程能力。但当前国内人工智能与生命科学领域之间存在显著的知识鸿沟,兼具两个领域专业能力的复合型人才供给严重不足,直接影响了技术的转化效率与场景落地速度,成为行业发展的核心人才瓶颈。
四是实验验证与转化成本高企,存在巨大的 “转化鸿沟”。生成式 AI 生成的候选分子、疾病模型等成果,仍需要通过大量的湿实验与临床试验进行验证,而传统的实验验证流程周期长、成本高,从模型预测到临床应用的转化成功率仍有待提升,存在巨大的 “转化鸿沟”。同时,AI 技术的应用需要企业对实验室进行自动化、数字化改造,前期投入成本高,也制约了技术在中小药企的规模化应用。
八、行业未来发展趋势与展望
随着技术的持续迭代、政策的不断完善与产业应用的持续深化,生成式 AI 将全面重构中国生命科学行业的发展格局,未来将呈现三大核心发展趋势。
(一)技术创新持续突破,从辅助工具向研发核心引擎全面演进
未来,生成式 AI 将更深度地嵌入药物研发的全生命周期,在分子设计与优化、蛋白质结构与功能预测、虚拟筛选、多尺度模拟等环节实现更具革命性的突破,从辅助研发人员的工具,转变为驱动药物研发决策的核心引擎,彻底重构药物研发的底层逻辑。
同时,生成式 AI 将与 AI Agent、自动化实验室深度融合,构建 “数据驱动 + 自主决策 + 闭环迭代” 的协同实验室体系,以生成式 AI 模型为大脑、AI Agent 为执行中枢、自动化实验室为物理载体,形成 “设计 - 实验 - 反馈 - 优化” 的全闭环研发流程,彻底重构传统实验室的研发模式。此外,量子机器学习技术将进入商业化探索阶段,与生成式 AI 结合实现生命系统的全景模拟,破解基因组、多组学、临床大数据的复杂分析难题,推动生命科学领域的基础研究实现突破性进展。
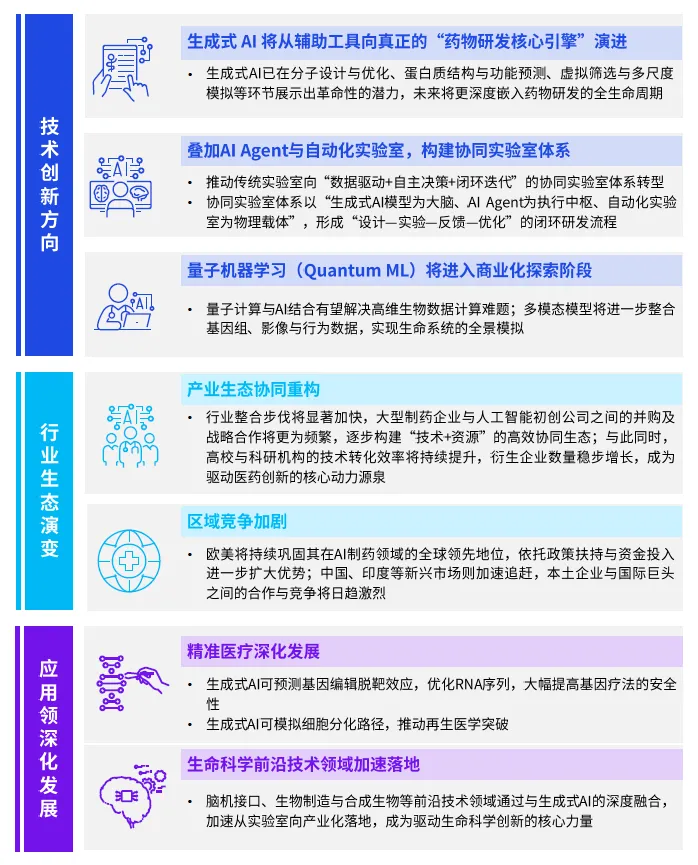
(二)产业生态协同重构,行业整合与区域竞争持续加剧
未来,中国生命科学行业的整合步伐将显著加快,大型制药企业与人工智能初创公司之间的并购、战略合作将更为频繁,逐步构建 “技术 + 资源” 的高效协同生态,头部企业将通过整合 AI 技术资源构建更高的竞争壁垒。同时,高校与科研机构的技术转化效率将持续提升,衍生企业数量稳步增长,成为驱动医药创新的核心动力源泉。
区域竞争层面,全球范围内欧美发达国家将持续扩大在底层算法、核心模型领域的先发优势,中国、印度等新兴市场将在应用创新、场景落地层面加速追赶,本土企业与国际巨头之间的合作与竞争将日趋激烈。国内市场将形成京津冀、长三角、粤港澳大湾区三大 AI 生命科学创新高地,三大区域错位发展、协同联动,推动中国在全球 AI 生命科学赛道持续扩大领先优势。
(三)应用场景持续深化,前沿技术加速产业化规模化落地
在精准医疗领域,生成式 AI 可精准预测基因编辑的脱靶效应,优化 RNA 序列设计,大幅提高基因疗法的安全性与有效性,推动个性化精准治疗的规模化落地。在再生医学领域,生成式 AI 可精准模拟细胞分化路径,推动干细胞治疗、组织工程、器官再生等领域的技术突破,为疑难疾病治疗提供新的解决方案。
在中医药领域,生成式 AI 将深度融入中医药的传承创新,实现古籍数字化、方剂优化、作用机制解析、新药研发等全链条赋能,推动中医药现代化与国际化发展。此外,脑机接口、智能医疗装备、数字疗法等前沿领域,将在生成式 AI 的赋能下加速从实验室向产业化落地,成为驱动生命科学行业创新发展的核心增长点。
九、结论
生成式人工智能正在引发中国生命科学行业的颠覆性变革,彻底重构了传统药物研发、临床诊疗、生产制造与商业化的全链条范式,为行业破解 “双十定律” 痛点、实现源头创新突破提供了核心驱动力。当前,中国已在全球生命科学生成式 AI 赛道占据领先地位,专利申请量稳居全球第一,市场规模占全球三分之一,在政策的持续加码、资本的理性加持、技术的快速迭代与产业的深度应用多重驱动下,行业正从概念验证阶段进入临床落地与价值兑现的关键时期。
同时,行业发展仍面临数据隐私、模型可解释性、算力瓶颈、人才短缺等多重风险与挑战,需要政府、企业、科研机构、医疗机构协同发力,通过完善监管政策体系、构建安全合规的数据共享机制、突破核心技术瓶颈、培养复合型跨界人才,为行业的健康可持续发展提供全方位支撑。
展望未来,生成式 AI 将从辅助工具全面升级为生命科学行业创新的核心引擎,推动行业从传统的时间密集型发展模式,向技术驱动的创新发展模式全面转型。中国生命科学行业将借助这一轮技术变革的历史性机遇,实现从医药大国向全球医药创新强国的跨越,在全球生命科学创新格局中占据更重要的地位。

