
点击蓝字

关注我们

万项临床数据
加速商业化浪潮
<<<
细胞治疗黄金时代已至
>>>
近日,华中科技大学同济医学院附属协和医院药物临床试验机构的研究团队在国际期刊《Frontiers in Pharmacology》发布了一项全球细胞治疗临床研究的系统性综述成果。

图.Global Panoramic analysis ofclinical research in cell therapy:clinical trial landscape, marketedproducts, and regulatory trends(全球细胞疗法临床研究全景分析:临床试验概况、上市产品和监管趋势)。
该研究联合哥伦比亚大学工程与应用科学学院相关学者,对截至 2025 年 10 月的全球细胞治疗临床试验、上市产品及区域监管趋势展开全面分析,勾勒出全球细胞治疗领域的发展全貌与前沿方向,为该领域的临床转化和产业发展提供了重要参考。
细胞治疗作为现代医学的核心前沿领域,凭借活细胞精准靶向病灶、修复受损组织、恢复生物功能的独特优势,已成为攻克肿瘤、免疫疾病等多种疑难病症的重要方向。相较于传统小分子药物和生物制剂,细胞治疗在临床应用中展现出不可替代的价值。本研究通过对全球顶级临床试验数据库、药监机构公告及相关文献的综合检索与分析,全面梳理了细胞治疗的全球发展格局,展现出该领域蓬勃的发展态势。
+
全球临床试验规模超万项,
中美欧成核心引领者
+
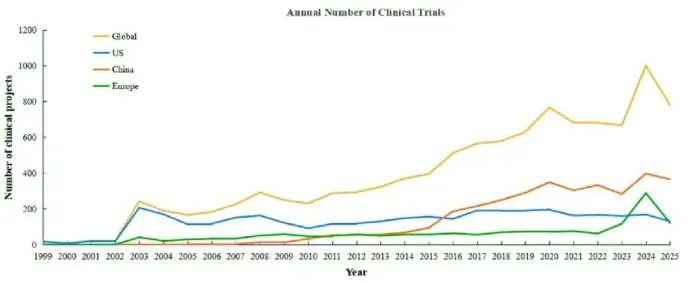
研究数据显示,全球累计已开展 10373 项细胞治疗临床试验,美国(3563 项)、中国(3365 项)、欧洲(1584 项)成为研究开展的核心区域,三者共同撑起全球细胞治疗研究的主体框架。值得关注的是,中国自 2005 年启动细胞治疗临床试验后,研究数量持续攀升,2016 年起便超越美国,成为全球细胞治疗活跃临床试验数量最多的国家,尤其在 CAR-T 疗法研究领域表现亮眼,展现出强劲的发展势头。
从研究阶段来看,全球细胞治疗研究虽以早期 I-II 期为主,但欧洲在 III 期临床试验占比上显著高于中美及全球平均水平,彰显出其在临床研究后期转化中的优势;而中美两国的在研试验占比更高,为细胞治疗的后续发展储备了大量优质研究成果。同时,中国临床试验的暂停 / 终止比例远低于美欧,研究推进的稳定性表现突出。
+
研究聚焦两大方向
肿瘤治疗成核心应用领域
+
全球细胞治疗研究主要集中在免疫细胞治疗和干细胞治疗两大方向,其中免疫细胞治疗临床试验达 5167 项,干细胞治疗 4796 项,二者受关注程度旗鼓相当。在免疫细胞治疗中,CAR-T 疗法是绝对主力,相关试验达 2409 项,占该类别近五成;干细胞治疗则以间充质干细胞(1904 项)和造血干细胞(1550 项)研究为主。
疾病应用方面,细胞治疗的研究重心高度聚焦肿瘤领域,全球超半数(56.1%)临床试验针对肿瘤开展,中美两国的肿瘤研究占比更是分别达到 61.9% 和 66.5%,远超全球平均;欧洲则在免疫疾病、循环系统疾病、肌肉骨骼疾病等领域的研究占比上形成特色优势,全球细胞治疗的应用场景正不断拓宽,覆盖多系统疾病的治疗需求。
+
各国上市产品各有特色
技术转化成果丰硕
+
随着临床研究的持续推进,全球细胞治疗的产业化转化成果斐然。各国依托自身研究优势,已获批上市多款特色鲜明的细胞治疗产品,覆盖肿瘤、血液病、自身免疫病、皮肤损伤、眼科疾病等多个领域。
其中,美国是细胞治疗产品获批数量最多的国家,拥有近30款上市产品:在造血干细胞治疗领域稳居全球领先地位;CAR-T产品获批数量达7款,居世界首位;在TIL疗法、TCR-T疗法等新兴免疫细胞治疗领域亦实现全球首次获批,多款产品在黑色素瘤、肉瘤等疾病治疗中展现出突破性疗效;此外,其体细胞治疗产品还广泛应用于糖尿病、血管损伤、角膜修复等非肿瘤领域,应用场景十分丰富。
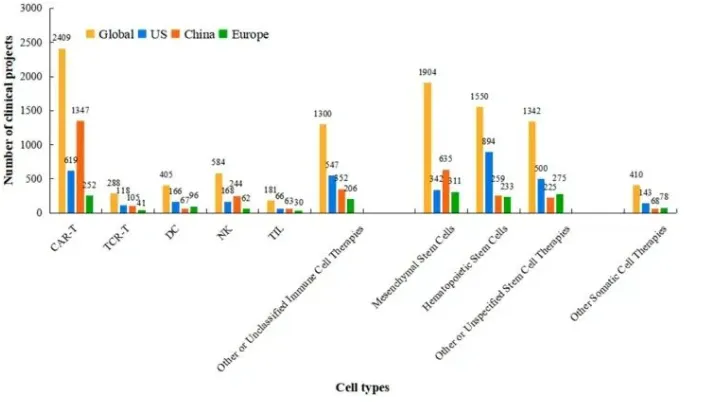
图.按细胞疗法类型划分的临床试验在主要地区的分布情况。该分组条形图比较了全球以及美国、中国和欧盟境内不同类别细胞疗法(例如,CAR-T、TCR-T、干细胞等)的注册临床试验绝对数量。数据范围和时间段(1999 年至 2025 年 10 月)与图 1相同。对于 x 轴上的每种细胞疗法类型,分组条形图(在每个分组内从左到右)分别代表全球总数、美国、中国和欧盟的试验数量。颜色方案与图 2一致:黄色(全球)、蓝色(美国)、红色(中国)和绿色(欧盟)。数据来自相同的三个注册机构(ClinicalTrials.gov、中国临床试验注册中心 (ChiCTR) 和欧盟临床试验注册中心 (EU-CTR))。
中国的细胞治疗产品研发虽起步较晚,但发展速度迅猛,目前已有 8 款产品获批上市,其中以 CAR-T 疗法为核心,多款自主研发的 CAR-T 产品在淋巴瘤、骨髓瘤、白血病等血液肿瘤治疗中表现优异,部分产品凭借高疗效、低价格纳入国家医保,大幅提升了患者的可及性;2025 年,中国首款间充质干细胞产品获批,填补了该领域的空白,为急性移植物抗宿主病等疾病的治疗提供了新方案。
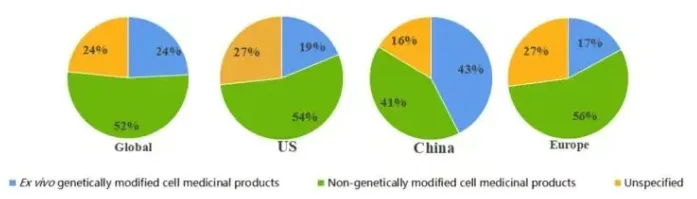
图.细胞治疗试验中基因修饰的全球和区域概况。这组由四个饼图组成的图表展示了1999年至2025年10月期间,不同地区使用基因修饰细胞产品的临床试验比例。每个饼图代表一个不同的地理范围:A,全球;B,美国;C,中国;D,欧盟。在每个饼图中,各扇形根据细胞疗法的基因修饰状态进行分类:绿色扇形代表非基因修饰细胞疗法;蓝色扇形代表体外基因修饰细胞疗法;黄色扇形代表注册信息不明确或未报告基因修饰状态的试验,因此无法进行明确分类。数据来自三个注册库(ClinicalTrials.gov、ChiCTR和EU-CTR)。
欧洲则在基因修饰自体造血干细胞治疗领域形成全球优势,多款获批产品在镰状细胞病、脑肾上腺脑白质营养不良等罕见病治疗中展现出长期疗效,同时其获批的病毒特异性 T 细胞疗法、角膜上皮干细胞疗法等,也为特定疾病患者带来了新的治疗选择。
日韩两国则在间充质干细胞治疗和体细胞治疗领域表现突出,韩国是全球间充质干细胞产品获批数量最多的国家,多款产品在心肌梗死、骨关节炎、渐冻症等疾病治疗中验证了疗效;日本的体细胞治疗产品则广泛应用于烧伤修复、软骨损伤、眼科疾病等领域,技术成熟度高,临床应用效果显著。
图示.细胞疗法
+
健区域监管体系不断完善
助力产业高质量发展
+
为推动细胞治疗技术的临床转化与产业发展,全球主要国家和地区均已构建契合自身发展特点的监管体系,并推出多项加速审批政策,为细胞治疗产品的研发与上市提供有力支撑。
美国早在1993年便搭建起细胞治疗监管框架,推出再生医学先进疗法(RMAT)等审批通道,允许依据II期临床数据进行条件性批准,兼顾审批的严谨性与灵活性。中国药监局接轨国际标准,建立“突破性治疗认定”“附条件批准”“优先审评”等加速通道,同时通过医保谈判降低产品价格,实现“创新”与“可及”的双重目标。
欧洲依托先进疗法药品法规(ATMP)建立统一的集中审批体系,推出优先药品(PRIME)计划,还允许成员国在特定条件下开展医院内先进疗法应用,提升了产品研发与应用的灵活性;日韩则推出风险分级监管、条件性限时批准等政策,大幅加快了细胞治疗产品的上市进程。
细胞治疗作为生物医药领域的创新前沿,正凭借不断突破的临床研究成果和持续完善的产业生态,从实验室走向临床应用的广阔舞台。
此次全球全景分析展现出,中美欧等核心区域在细胞治疗领域各展所长、协同发展,技术创新与监管优化的双向发力,正推动全球细胞治疗产业迈入高质量发展新阶段。
未来,随着研究的不断深入和技术的持续迭代,细胞治疗将在更多疑难疾病的治疗中发挥作用,为全球患者带来更多治愈希望,开启精准医疗的全新篇章。
鸣谢:本篇部分内容转自官方媒体/网络新闻。
声明:账号旨在分享科普知识,或传递行业前沿进展,不作为官方立场,也不作为相关医疗指导或用药建议,仅供读者参考。如本账号转载的图文视频等内容涉及版权等问题,请联系我们及时处理删除,谢谢。
END

打造人人用得起的先进的细胞技术和大健康管理平台