前言
肿瘤治疗长期面临疗效与毒性的权衡。传统化疗虽具备广谱杀伤能力,但由于缺乏肿瘤靶向性,往往在抑制肿瘤的同时带来明显的系统性毒副作用。20世纪末以来,随着单克隆抗体技术取得突破并实现临床应用,肿瘤治疗进入了靶向时代。相较传统化疗,单抗通过特异性结合肿瘤抗原,显著提升了治疗的针对性与安全性,但其作用机制更多依赖免疫介导杀伤或信号通路阻断,在部分肿瘤中仍面临杀伤能力有限、耐药性较快出现等问题。
在此背景下,抗体偶联药物(Antibody-Drug Conjugates, ADCs)应运而生。其核心思路是将肿瘤识别与杀伤相结合,通过抗体实现靶向递送,将细胞毒性药物精准输送至肿瘤细胞内部,从而在提升疗效的同时降低系统性毒性。2000年,首款ADC药物吉妥单抗奥唑米星(Mylotarg)获批上市,标志着ADC正式进入临床应用阶段。尽管早期产品在稳定性与安全性方面存在不足,但其验证了这一技术路线的可行性。近十年来,随着生物医学的持续进步,ADC已逐步从概念验证走向临床与商业化兑现。以曲妥珠单抗德鲁替康(Enhertu)为代表的新一代ADC,不仅在疗效上实现突破,还显著拓展了HER2低表达等新适应症边界,推动ADC成为当前肿瘤创新药中最具活力的细分赛道之一。
ADC药物简介
ADC药物通过特定的化学连接子(Linker),将极具杀伤力的小分子毒素载荷(Payload)偶联至单克隆抗体上,结合抗体的精准靶向以及药物的细胞毒性,从而精准且高效的消灭肿瘤细胞。以Mylotarg为例,吉妥珠单抗是作为骨架的单抗,而奥唑米星为偶联的payload。
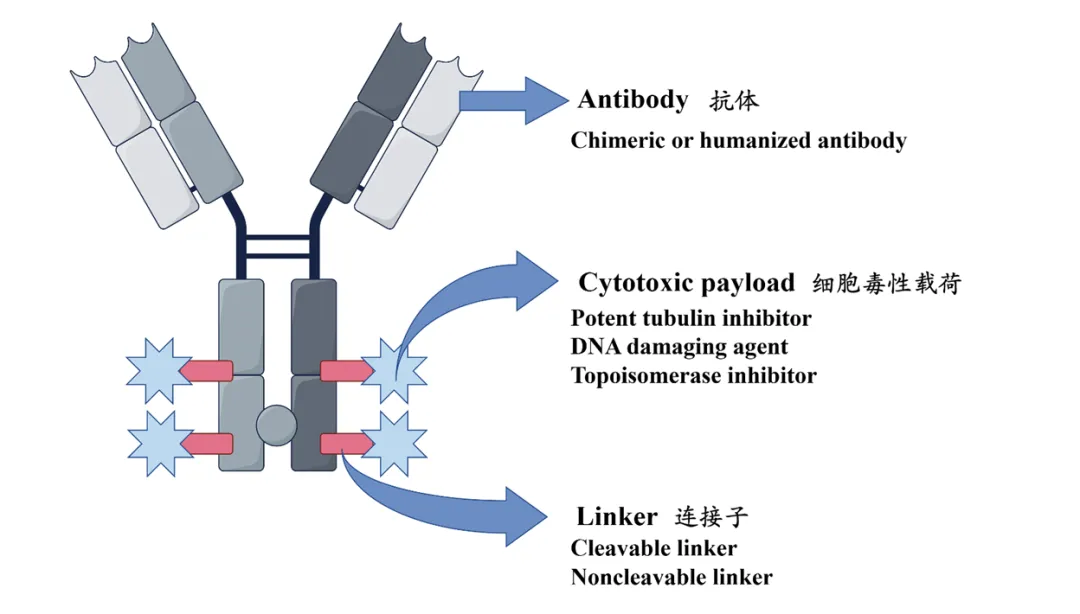
资料来源: Frontiers in Oncology, 2025
ADC药物的作用机制
ADC药物一般由静脉注射进入体内,通过其抗体部分的特异性识别并结合肿瘤细胞表面的靶抗原,形成 ADC-抗原复合物。 复合物通过受体介导的内吞作用(Receptor-Mediated Endocytosis)被摄入细胞内,形成早期内吞体(Early Endosome)。 内吞体成熟并转运至溶酶体(Lysosome)。在溶酶体的酸性环境及水解酶(如组织蛋白酶 Cathepsin)的作用下,linker发生断裂或抗体被降解。 活性小分子Payload被释放到细胞质中,并扩散至细胞核或细胞骨架。 Payload通过影响DNA或微管蛋白发挥作用,从而诱导细胞凋亡(apoptosis)或坏死(necrosis),最终对肿瘤细胞产生细胞毒性作用。
在这一过程中,部分ADC药物还具备旁观者效应(Bystander Effect):即细胞内释放的payload能够穿过细胞膜,扩散至邻近肿瘤细胞,从而杀伤那些靶抗原表达较低甚至缺失的细胞。这一机制使ADC不再依赖于高度均一的靶点表达,在肿瘤异质性较强的情况下仍能保持良好疗效。需要注意的是,并非所有ADC都具备旁观者效应,其产生取决于payload的膜通透性及linker的释放方式。当前,该效应最典型地体现在以拓扑异构酶I抑制剂为载荷的ADC中,例如德鲁替康(deruxtecan, DXd)。以此为代表的药物,如Enhertu,也因此展现出更广泛的抗肿瘤活性。
ADC药物的设计
ADC药物的发展历程
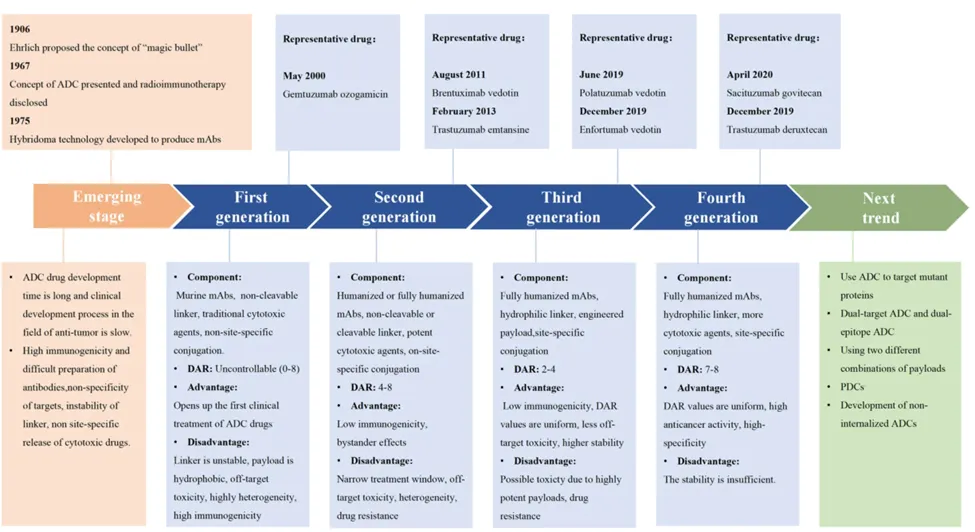
ADC药物的市场规模与竞争格局
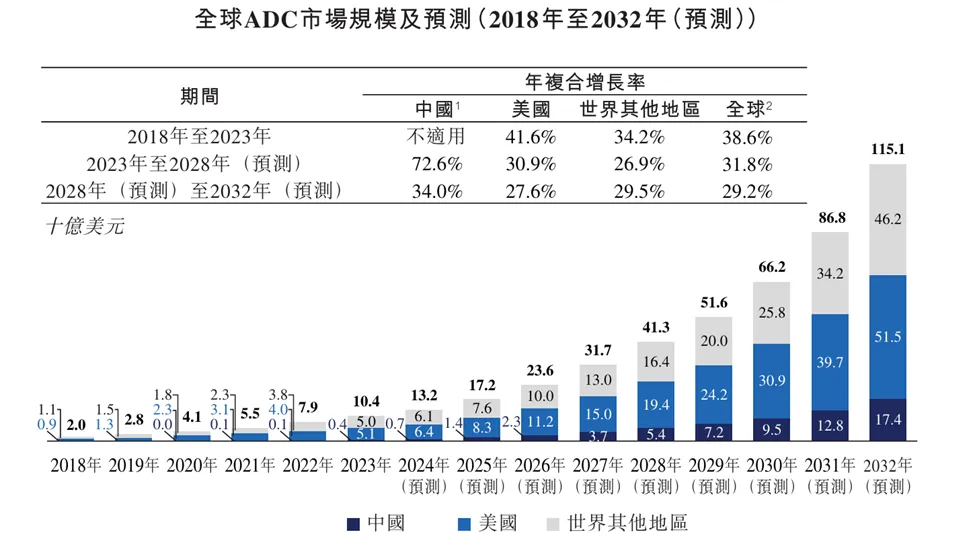
表1:目前已获批的21款ADC药物
产品 | 研发企业 | 靶点 | 适应症 | 上市时间 |
Mylotarg® | 辉瑞 | CD33 | 急性髓系白血病 | 2000.5 |
Adcetris® | Seagen | CD30 | B细胞淋巴瘤 | 2011.8 |
Kadcyla® | 罗氏/ ImmunoGen | HER2 | HER2+ 乳腺癌 | 2013.2 |
Besponsa® | 辉瑞 | CD22 | 前体B细胞急性淋巴细胞白血病 | 2017.8 |
Lumoxiti® | 阿斯利康 | CD22 | 多毛细胞白血病 | 2018.9 |
Padcev® | Seagen/安斯泰来 | Nectin-4 | 尿路上皮癌 | 2019.12 |
Enhertu® | 第一三共/阿斯利康 | HER2 | 乳腺癌,胃癌,非小细胞肺癌 | 2019.12 |
Polivy® | 罗氏 | CD79b | 弥漫性大B细胞淋巴瘤 | 2019.6 |
Trodelvy® | Immunomedics/吉利德 | TROP2 | 三阴性乳腺癌 | 2020.4 |
Blenrep® | GSK | BCMA | 多发性骨髓瘤 | 2020.8 |
Akalux® | Rakuten Medical | EGFR | 头颈部鳞状细胞癌 | 2020.9 |
Zynlonta® | ADC Therapeutics/瓴路药业 | CD19 | 弥漫性大B细胞淋巴瘤 | 2021.4 |
爱地希® | 荣昌生物/ Seagen | HER2 | 胃癌,尿路上皮癌 | 2021.6 |
Tivdak® | Genmab/Seagen/再鼎医药 | TF | 宫颈癌 | 2021.9 |
Elahere® | 艾伯维/ Immunomedics/华东医药 | FRα | 铂耐药卵巢癌 | 2022.11 |
佳泰莱® | 科伦博泰/默沙东 | TROP2 | 三阴性乳腺癌,非小细胞肺癌 | 2024.11 |
Datroway® | 第一三共/阿斯利康 | TROP2 | 乳腺癌 | 2024.3 |
Emrelis® | 艾伯维/华东医药 | c-Met | 非小细胞肺癌 | 2025.5 |
艾维达® | 恒瑞医药 | HER2 | 非小细胞肺癌 | 2025.5 |
舒泰莱® | 科伦博泰 | HER2 | 乳腺癌 | 2025.10. |
美佑恒® | 乐普生物 | EGFR | 鼻咽癌 | 2025.10. |
注:Blenrep® 于2020年在美国通过 FDA Accelerated Approval 途径获得加速批准,但后续在确证性III期临床试验中未能证明其临床获益显著优于现有治疗方案,未能满足加速审批的验证性要求。因此,Blenrep于2022年撤出美国市场。但最终于2025年以联合治疗方案形式重新获得美国监管机构批准上市
从市场格局看,ADC行业虽然已有一定数量产品获批上市,但商业价值仍高度集中于少数头部品种。据表1,目前全球已有21款ADC药物获批上市,靶点覆盖HER2、TROP2、Nectin-4、CD79b等多个方向。2025年全球ADC市场总销售额约为168亿美元,其中前三大产品Enhertu、Kadcyla和Padcev合计实现销售额99.97亿美元,占总市场约60%;前七大产品合计贡献159.92亿美元,占比约95%,头部集中趋势十分明显。
表2:ADC药物销售额前十名
排名 | 药物名称 | 公司 | 靶点 | 2025年销售额(亿美元) | 同比增长 |
1 | Enhertu® | 第一三共/阿斯利康 | HER2 | 49.82 | 33% |
2 | Kadcyla® | 罗氏/ ImmunoGen | HER2 | 27.09 | 17% |
3 | Padcev® | Seagen/安斯泰来 | Nectin-4 | 23.06 | 45% |
4 | Polivy® | 罗氏 | CD79b | 21.29 | 46% |
5 | Adcetris® | Seagen | CD30 | 17.79 | -7% |
6 | Trodelvy® | Immunomedics/吉利德 | TROP2 | 13.97 | 6% |
7 | Elahere® | 艾伯维/ Immunomedics/华东医药 | FRα | 6.9 | 44% |
8-10 | - | - | - | 4.38 | - |
合计 | 164.3 | - |
在这一格局下,Enhertu无疑是当前ADC市场最具代表性的龙头产品。2025年,Enhertu由第一三共和阿斯利康合计实现销售额49.82亿美元,占整个ADC市场约30%,单品销售规模已显著领先其他已上市ADC。同时,Enhertu还在通过增加新的适应症以获取更大市场。2025年12月,FDA批准Enhertu联合pertuzumab用于不可切除或转移性HER2阳性乳腺癌的一线治疗,进一步强化了其在HER2赛道中的领先地位。根据多方机构预测,2026年Enhertu将继续维持销量增速,并向90亿美元的峰值销售目标迈进。整体来看,当前ADC市场的增长并不均衡,主要由少数临床优势明确、扩适应症能力强的核心品种驱动。
Enhertu的成功并非偶然。作为第三一共DXd平台最具代表性的产品之一,其优势并不来自单一参数领先,而是来自DAR、linker与payload三者协同优化后形成的整体产品力。
1.首先,Enhertu具有较高的平均DAR(约7.8)明显高于早期HER2 ADC。较高且相对可控的DAR意味着单个抗体分子能够递送更多payload,从而提升单位结合事件的杀伤效率。需要指出的是,高DAR本身并不必然带来更优疗效,关键在于在提高载药量的同时,仍能维持可接受的体内稳定性与安全性,而Enhertu正是在这一点上实现了较好的平衡。
2.其次,Enhertu具备较强的旁观者效应。其采用可切割四肽linker(Gly-Gly-Phe-Gly),在肿瘤细胞内经溶酶体蛋白酶裂解释放DXd。释放后的DXd不受linker干扰,具有较高膜通透性,其细胞毒性作用可扩散至邻近肿瘤细胞,从而形成显著的旁观者效应。这使Enhertu不仅能够有效杀伤HER2高表达肿瘤细胞,也更有机会覆盖邻近的HER2低表达或表达异质性肿瘤细胞,这一点对于HER2-low人群的治疗意义尤为重要。临床上,DESTINY-Breast04奠定了Enhertu在HER2-low晚期乳腺癌治疗中的地位,而基于DESTINY-Breast06,FDA又于2025年1月将其适应症进一步扩展至HR阳性、HER2-low或HER2-ultralow转移性乳腺癌患者,显著拓宽了受益人群。
3.第三,Enhertu所采用的DXd payload本身也是其成功的重要基础。DXd属于高效拓扑异构酶I抑制剂,能够通过干扰DNA复制相关过程诱导肿瘤细胞死亡,同时自身具备较好的膜通透性,拥有强旁观者效应。与稳定的linker设计配合后,Enhertu能够在提升肿瘤内有效递送的同时,尽量控制非靶向暴露。不过,这并不意味着其毒性可以忽略,间质性肺病/肺炎等不良反应仍是临床使用中的关键安全性关注点。
总体来看,Enhertu的成功本质上来源于抗体,linker,payload三者协同设计的全面优化。高DAR提升了有效递送密度,可裂解四肽linker保证了肿瘤内释放效率以及旁观者效应,而具备膜通透性的DXd则放大了旁观者效应。对于当下ADC行业而言,真正决定产品上限的是能否通过体系化设计做出在疗效、安全性和适应症拓展上都更优的ADC,而Enhertu正是此类产品的代表。
中国市场以及中国公司
从行业发展阶段看,中国ADC赛道正逐步从参与研发走向商业化起步。当前已上市的ADC中,中国企业主导的产品共有5款,且多数产品是在2024-2025年间陆续获批,整体仍处于商业化早期。需要指出的是,国产ADC的意义并不只在于上市产品数量增加,更在于中国企业已经在HER2、TROP2、EGFR等成熟靶点上形成一定的管线密度,并开始尝试通过适应症选择、平台设计优化等方式来建立差异化竞争力。
沿用上文提到的ADC代际划分框架,国内较早上市的爱地希可以大致归入二代ADC,而后续其他产品在偶联工艺、linker与payload设计上则更接近三代ADC。这意味着,中国企业当前的核心逻辑已经不再只是能否做出ADC,而是能否做出在特定适应症中更具竞争力的ADC。
在已上市国产ADC中,恒瑞医药的瑞康曲妥珠单抗(艾维达)是一个值得关注的案例。该产品于2025年5月获国家药监局(NMPA)附条件批准上市,用于既往接受过至少一种系统治疗的HER2突变晚期或转移性非小细胞肺癌(NSCLC),并成为国内首个获批用于HER2突变NSCLC的中国自主研发ADC。根据HORIZON-Lung临床研究披露的数据,瑞康曲妥珠单抗在既往经治HER2突变晚期NSCLC患者中实现了74.5%的客观缓解率(Objective Response Rate, ORR)、11.5个月的中位无进展生存期(Progression-Free Survival, PFS)以及48.6%的12个月PFS率,显示出较强的临床活性。对比Enhertu在DESTINY-Lung02中的结果,Enhertu的ORR为57.7%,中位持续缓解时间(Duration of Response,DoR)为8.7个月。艾维达在缓解率和无进展生存期上表现出较强潜力,但由于两者来自不同试验,且终点口径、入组特征和随访背景并不完全一致,现阶段仍无法据此得出明确优劣判断。不过,现有证据可以说明艾维达已显示出成为国内HER2 ADC重要竞争者的潜力,但其能否真正挑战Enhertu的领先地位,还取决于后续适应症拓展、更多临床数据积累以及商业化执行能力。
另外,艾维达的潜力并不只体现在已获批的NSCLC适应症。根据恒瑞公开资料,该产品已在乳腺癌、胃癌/胃食管结合部腺癌、结直肠癌、胆道癌及妇科恶性肿瘤等多个方向开展临床布局,并已获得多项突破性治疗认定。这也反映出当前中国ADC企业的共同思路:在成熟靶点上先实现局部突破,再通过扩适应症与平台化开发逐步放大产品价值。总体来看,中国ADC企业已经从模仿者变成有竞争力的参与者,但未来真正决定竞争格局的,仍将是差异化产品力、适应症拓展效率以及商业化兑现能力。
小结
总体来看,ADC行业已经走过了早期概念验证的阶段,正加速迈入产品集中上市与商业化兑现的新周期。过去决定行业方向的是技术可行性,而未来决定竞争格局的,将是产品能否在疗效、安全性、适应症拓展和商业化落地之间形成真正均衡的综合优势。当前市场高度向头部品种集中,Enhertu的成功也表明,ADC的核心竞争力并不来自某一个单点参数领先,而是抗体、linker与payload协同优化后形成的体系化产品力。
从更长维度看,随着同靶点管线持续增加,ADC行业将不可避免地进入更激烈的结构性竞争阶段。届时,能够做出一款ADC已不足以支撑价值,真正能够胜出的企业,需要在临床定位、差异化设计、适应症扩张效率以及商业化能力上持续建立壁垒。对于中国企业而言,当前的意义也已不只是实现从0到1的上市突破,而是在成熟靶点拥挤、竞争加剧的环境中,逐步证明自己具备做出优质ADC并兑现产品价值的能力。整体而言,ADC仍是肿瘤创新药中最具确定性的高景气赛道之一,但未来行业红利将更多属于少数真正具备差异化产品力的平台型企业。
免责声明:本文仅为行业研究与信息分享之用,不构成任何投资建议或买卖依据。文中内容主要基于公开信息整理,作者力求客观准确,但不对其完整性、准确性和时效性作任何保证。市场有风险,决策需谨慎。