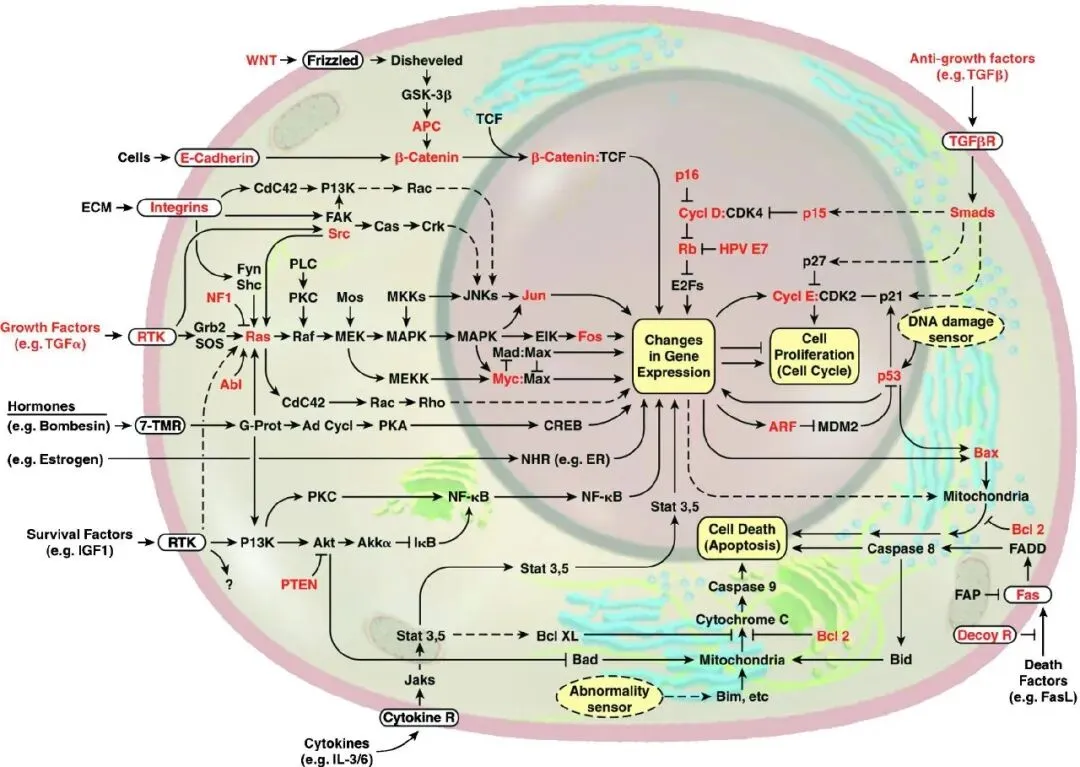
2009年美国国家科学院发布的《21世纪的新生物学》白皮书,旨在回应生物学领域的范式转变,提出“新生物学”(New Biology)作为国家战略核心。报告指出,生物学正从传统还原论研究转向跨学科整合,通过融合生物学子领域(如基因组学、生态学)与物理、计算、工程等学科,构建系统性理解生命的能力。
核心理念是:生物学不再是孤立探索,而是以解决社会重大挑战为驱动,实现从分子到生态系统的预测性控制,类似20世纪初物理学革命构建的标准模型。报告强调,美国必须引领这一变革,以确保科技竞争优势并应对食物安全、环境可持续、清洁能源和个性化医疗等全球性危机。
白皮书框架以“问题驱动”为核心,围绕四大社会挑战展开:食物(如设计气候适应性作物)、环境(如监测生态系统服务)、能源(如开发可持续生物燃料)和健康(如实现个体化医疗)。为实现目标,报告提出四大支柱性建议:其一,启动国家新生物学倡议,通过多机构(如NIH、NSF、DOE)长期协作,避免资源碎片化;其二,优先发展信息技术,构建统一数据基础设施,以处理海量生物数据;其三,推动跨机构合作机制,打破行政壁垒,优化资源配置;其四,改革教育体系,培养“新生物学家”——具备深度学科知识及多学科“工作流利度”的人才。整体框架强调,投资需聚焦交叉技术(如合成生物学、AI分析)和基础科学,以催化创新链条从实验室到社会应用。
报告主张通过10年以上国家倡议,将新生物学打造为“基础设施式”科学,其成功依赖于三大要素:跨部门合作(政府、学界、产业)、数据民主化(如共享数据库)和教育重构(如 interdisciplinary 课程)。这一框架不仅旨在短期突破,更着眼于培育新生物经济生态,使美国在21世纪生物革命中保持领导地位。白皮书的远见在于,它将生物学定位为整合性平台科学,其进展将辐射至农业、医药和环保等领域,最终实现可持续社会解决方案。
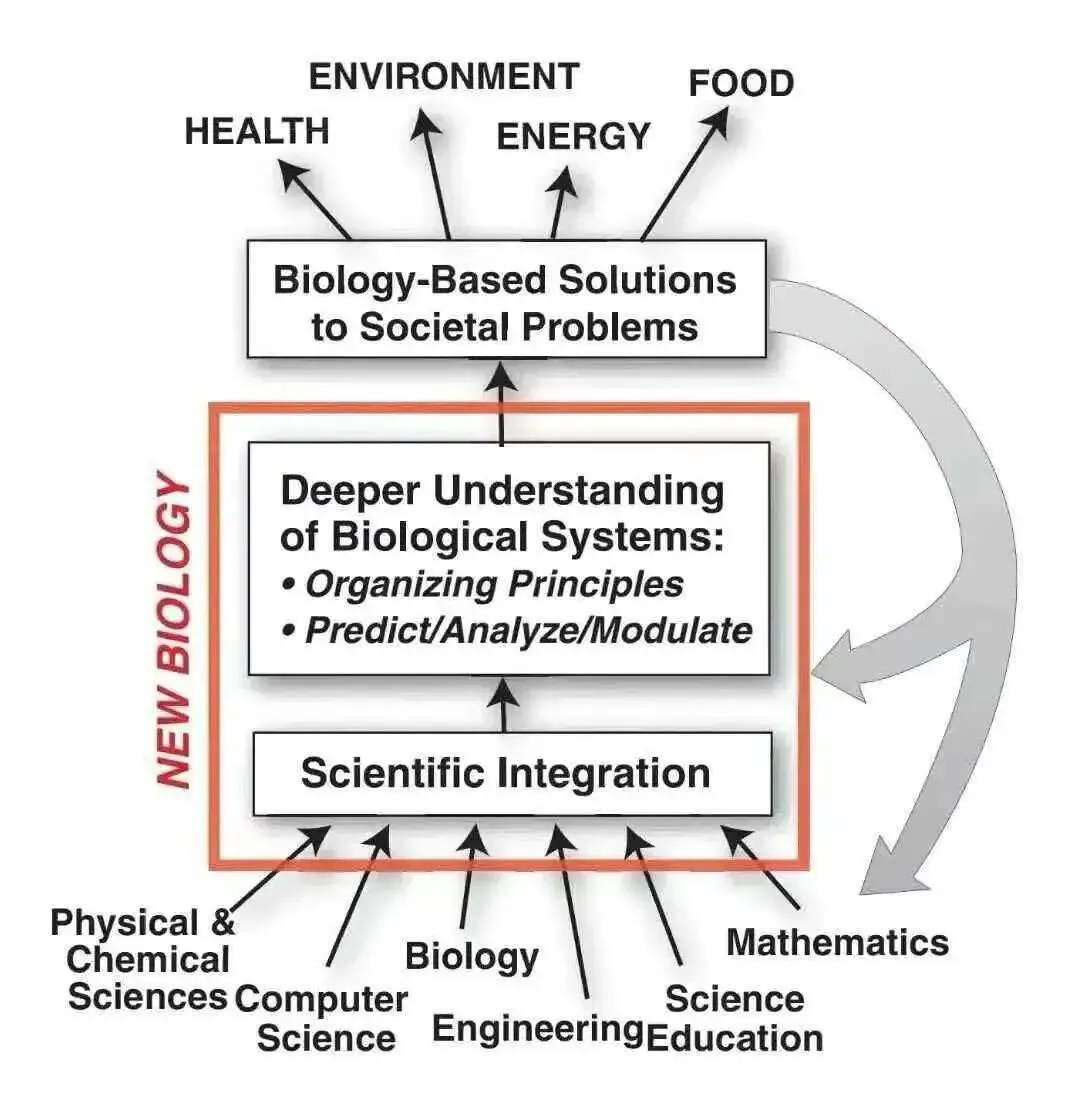
报告背景与核心愿景
2009年,美国国家科学院发布《21世纪的新生物学:确保美国引领即将到来的生物学革命》报告,旨在回应生物学领域的范式转变。报告指出,生物学正从分散的、还原论的研究转向整合的、系统性的“新生物学”(New Biology),其核心是通过跨学科融合(整合生物学子领域、物理、计算、工程和数学)来解决社会重大挑战。这一愿景的提出,源于当时生物学领域的三大趋势:
技术爆炸:基因组学、高通量技术等进步使大规模数据生成成为可能。
学科融合:生物学与物理、计算科学等的交叉催生了系统生物学、合成生物学等新领域。
社会需求:食物安全、环境可持续性、能源转型和健康医疗等全球性问题亟待生物学驱动解决方案。
报告框架基于一个核心论点:生物学正处于类似20世纪初物理学的“拐点”,通过整合与交叉,有望构建类似物理学“标准模型”的生物学统一框架,从而实现对生命系统的预测性理解和精准干预。
物理学发展史(如标准模型)和DNA解析的突破,正是这一愿景的历史参照——报告希望生物学能复制物理学的成功,通过整合实现范式革命。
2009年报告的整体框架分析
报告框架以“问题驱动”为核心,围绕目标、方法和实施路径展开:
终极目标:通过新生物学解决四大社会挑战
报告明确将新生物学定位为“社会解决方案的引擎”,聚焦四个关键领域:
食物挑战:设计可持续适应气候变化的作物(如通过基因编辑和系统生物学优化作物生长)。
环境挑战:监测和恢复生态系统功能(如利用遥感技术和生态建模)。
能源挑战:开发可持续生物燃料(如优化微生物合成途径)。
健康挑战:实现个性化医疗(如整合基因组学、蛋白质组学和临床数据)。
这些目标并非孤立,而是强调跨尺度整合——从分子到生态系统,类似物理学中从粒子到宇宙的统一框架。
方法论:跨学科融合与技术驱动
报告提出新生物学的本质是“整合”,具体体现为:
学科交叉:打破生物学内部壁垒(如生态学与分子生物学结合),并引入物理、计算、工程等领域的工具(如数学模型、微流体芯片、AI分析)。
技术基石:优先发展信息技术(大数据存储、共享平台)、成像技术(实时细胞观测)、高通量技术(单细胞测序)和合成生物学(工程化生命系统)。
系统思维:强调从“部件清单”(如基因序列)转向“系统预测”(如网络动态模型),这与物理学中从粒子行为预测宏观现象的逻辑一致。
实施路径:国家倡议与系统变革
报告提出四大核心建议,构建了完整的行动框架:
建议1:启动国家新生物学倡议
通过多机构合作(NIH、NSF、DOE等)推动长期(≥10年)项目,资金独立于现有预算,避免零散化投入。
建议2:跨机构协作机制
设立专门机构协调资源,避免重复建设,类似人类基因组计划的成功模式。
建议3:优先发展信息技术
信息被视为“新生物学货币”,需构建统一数据基础设施(如生物云平台),解决数据异构性和共享难题。
建议4:教育改革培养“新生物学家”
“新生物学家”需具备深度学科知识+多学科“工作流利度”,推动课程改革(如哈佛大学将生物学与艾滋病治疗结合的教学案例)。
报告特别指出,成功需依赖三大支柱:跨部门合作(政府-学界-产业)、数据基础设施投入、教育体系重构。这一框架与用户提到的AI制药公司(如Recursion Pharmaceuticals和Xaira Therapeutics)的虚拟细胞研发理念高度契合——它们正是报告预言的“整合性研究”的当代实践者。
2009—2026年:17年发展评价
17年来,生物学领域部分实现了报告的愿景,但在整合深度和社会影响上仍存差距。以下结合AI制药崛起进行分析:
1. 成就:技术突破与部分整合实现
技术爆炸超预期:
基因组学:测序成本下降超万倍(从30亿美元到100美元),单细胞测序、CRISPR基因编辑普及,实现了报告预言的“部件清单”完善。
数据驱动:AI和机器学习已广泛应用于药物发现(如Recursion Pharmaceuticals用计算机视觉筛选细胞表型),部分实现了报告强调的“预测生物学”。
跨学科萌芽:合成生物学(如工程化微生物生产药物)、生物医学工程(如器官芯片)等领域已初步融合生物学与工程学。
社会应用初见成效:
健康领域:个性化医疗进展显著,如免疫治疗(用户提到的PD-1抑制剂)和mRNA疫苗(COVID-19中验证),体现了“从基因型到表型”的整合研究。
能源与环境:合成生物学生产生物燃料(如Amyris公司的工程酵母)、生态监测网络(如NASA的卫星遥感)已落地。
2. 不足:整合深度与系统瓶颈
数据孤岛仍存:
报告愿景的“统一信息基础设施”未完全实现。尽管有GenBank等数据库,但数据标准不一、共享机制缺乏(如临床医疗数据难以对接科研),限制了AI模型的泛化能力。用户提到的Xaira Therapeutics依赖专有数据集,正反映了数据割裂的现实。
学科壁垒未彻底打破:
教育滞后:大多数高校仍以传统学科划分院系,“新生物学家”培养缓慢。报告呼吁的跨学科课程(如哈佛案例)未成主流。
研究碎片化:多数AI制药公司(如Recursion)仍聚焦垂直领域(如细胞图像分析),而非报告设想的“全系统模拟”。虚拟细胞模型尚处早期,离“虚拟人体”基础设施差距甚远。
社会挑战应对不足:
食物与能源:作物抗逆设计、生物燃料经济性仍未突破,气候变化压力加剧了这些挑战。
健康医疗:个性化药物成本高昂,全球可及性低(如CAR-T疗法),未完全实现“普惠性健康”愿景。
3. 原因分析:执行偏差与外部环境
资金与协作不足:报告建议的“跨机构倡议”未能规模化落地。美国科研资金仍以单一机构主导(如NIH主导生物医学),跨部门项目(如DOE与NIH合作)有限。
技术成熟度时间差:AI在2010年后才爆发(如深度学习革命),而报告撰写时AI技术尚未成熟,导致早期资源更偏向传统生物学。
商业化与科研脱节:尽管AI制药公司兴起,但多数追求短期商业回报(如靶点发现),而非报告倡导的“基础性系统理解”。
结论:前瞻性与未来展望
2009年报告具有显著前瞻性:它精准预言了生物学向数据驱动、跨学科整合的转型方向,尤其是对AI和信息技术核心地位的强调,已由当前AI制药浪潮验证。
然而,报告低估了系统变革的复杂性——整合需打破学术、制度和商业惯性。
未来方向应延续报告框架,但需强化三点:
数据民主化:建立国家级生物数据联盟,推动数据标准化与开源。
跨界人才培养:仿照物理学中的理论-实验-计算三角结构,设计生物学交叉学位。
公共-私营合作:将AI制药公司的工程化经验(如Xaira的虚拟细胞平台)反向输入基础研究,加速“虚拟生物系统”落地。